基于学科核心素养的初中化学教学设计
2018-03-26胡巢生

摘要: 尝试基于高中化学“核心素养”视角,对比、分析并整合3个版本教科书的内容,设计了“质量守恒定律”教学活动,从解读质量守恒定律发现史、创新实验设计、评价实验体系,分析实验结果、三重表征与定性定量相结合等方面培育并落实学生发展核心素养的目标。
关键词: 核心素养; 初中化学; 质量守恒定律; 实验探究; 教学设计
文章编号: 10056629(2018)2004505中图分类号: G633.8文献标识码: B
1问题的提出
高中化学核心素养包括宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学精神与社会责任。是学生在接受相应学段的教育过程中,逐步形成的适应个人终生发展和社会发展需要的必备品格和关键能力[1]。这些核心素养,既适合高中化学,又涵盖初中化学。质量守恒定律基于元素守恒,原子种类、数目不变,能定量计算参加反应的各物质间的质量比,在生产实践中,能有意识地控制投料、产出;是化学反应中质量关系问题解决的理论依据,也是培养学生化学学科核心素养的重要载体。
针对质量守恒定律主题,已有一些相关研究,如钱海如、赵华归纳了初中阶段5个层次的“进阶模型”,提出教学中注意的4个问题[2]。郭建虹将对比教学法运用于史料知识、实验探究、数据分析中,构建物质变化观[3]。还有老师从不同的角度进行了不同的教学设计,不过,较少从发展学生化学学科核心素養的角度进行思考。
笔者对比、分析3个版本教科书[4][5][6]中“质量守恒定律”的内容设计,尝试基于高中化学“核心素养”视角,借助化学史料、科技发展、实验设计等情境和真实问题的解决,通过小组讨论、合作探究,实现学生对宏微结合、定性与定量结合、以实验为基础等化学学科思想的理解和知识的意义建构,设计出以“问题链、环节、探究”为抓手,化学史资源为支撑的教学设计,以充分挖掘质量守恒定律内容中包含的基本观念和方法,着力探索学生在初中化学课程学习中形成的关键能力和必备品格(图1)。
2教学流程与情境设计
[师]在一定条件下,反应物之间发生化学反应生成新物质,如镁条燃烧生成氧化镁,乙醇燃烧生成二氧化碳和水,等等。参加反应的各物质质量总和与反应生成的各物质质量总和相比较,是否发生了变化?你的猜想是什么?
[生]可能不变、可能偏大、可能偏小。
2.1解读质量守恒定律发现史——提升“科学精神与社会责任”等学科核心素养
“科学精神与社会责任”是化学学科实践能力,是对化学学科价值很好的诠释。化学史是让学生切实体验严谨的科学态度、科学精神的一种很好的形式。宋心琦教授指出,“以史为鉴”的应有之意不应该仅限于励志,更应当着眼于科学素质的培育和提高。
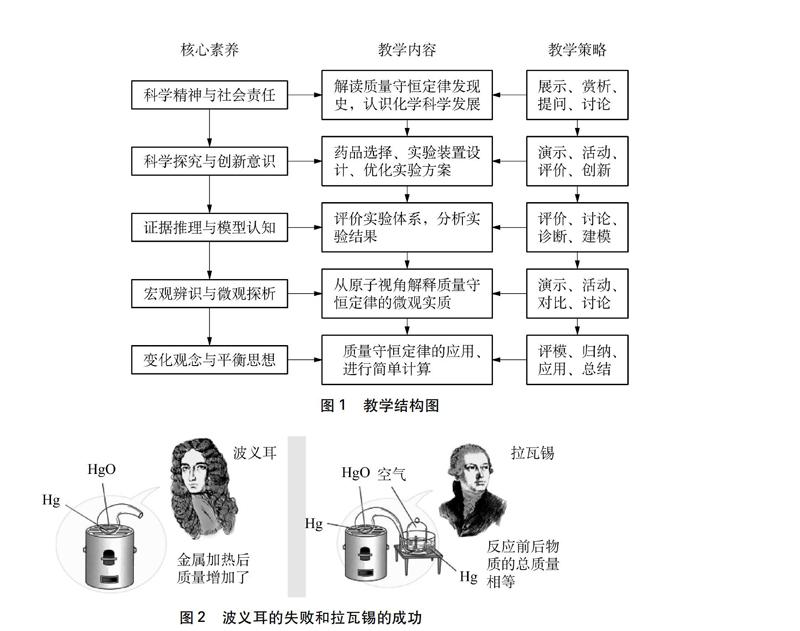
[师]好的,让我们先来了解一下质量守恒定律的发现史: 两位科学家的实验貌似相同(图2),但实验结论却截然不同: 波义耳在一个敞口的容器中加热金属,结果发现反应后容器中物质的质量增加了。
而拉瓦锡用较精确的定量实验法,在密封容器中研究氧化汞的分解与生成中各物质质量之间的关系。
[师]没有标准答案的科学家是怎么看待这一问题的?你对此有什么想法?你能得到什么结论?你的依据是什么?
[生]……
[师]让我们来共同赏析拉瓦锡的经典实验!1776年,拉瓦锡采用常温下呈液态的汞作为药品,除用作反应物,还可以通过连通器直接用于测定反应器(曲颈甑)内空气体积的变化。
步骤1: 2Hg+O2△2HgO(加热条件下,汞汽化,与氧气发生气相反应,氧气可以完全耗尽,还可以通过连通器测量反应器内气体体积的变化)。
步骤2: 他把制得的浮在汞液面上的“红色沉淀”加热至500℃左右,2HgO△2Hg+O2↑,得到等质量的汞。他收集这些失而复得的气体,发现与之前曲颈甑里消失的空气一样多,他将此气体称为“纯粹空气”或“真实空气”。
步骤3: 将步骤2得到的O2和步骤1剩余的气体混合,得到“原来”的空气。
随后,拉瓦锡继续进行相关实验: 氧化汞的分解,分解后再化合……实现了氧气的吸收与生成——氧的循环,使氧气的形态更加清楚了。可以看到这个实验设计的完美,可谓是一箭三雕: 证明了质量守恒定律;提出了“氧化学说”;验证了空气是混合物[7]。
拉瓦锡能够通过实验证明质量守恒定律,并提出“氧化学说”,最重要的原因在于他明确了反应体系,并在密闭体系中测量体系在反应前后的质量变化。因此,教学重心是如何让学生通过对不同类型实验的分析,感受、认识到明确“体系”与“环境”这一对重要的化学概念,对于化学研究具有重要的意义。从而明确,研究化学变化时需要有“体系”意识。
值得一提的是,波义耳和拉瓦锡都是化学史上的“教父级”人物,绝不能因为波义耳与质量守恒定律的失之交臂,而认为其对化学科学的贡献远比拉瓦锡小。在“燃素说”理论根深蒂固的影响下,波义耳认为金属焙烧增重是由于燃烧时产生的“火粒子”(火素)穿过玻璃后被金属吸收所致[8]。其结论的错误,应是对理论框架的突破和实验手段(化学体系的选择、实验装置的设计等)的选择问题。
[生]学生沉浸于科学发现的过程,形成强调证据推理的严谨求真的科学态度。
[师]以上我们赏析了拉瓦锡的实验,我们将重温“质量守恒定律”的科学发现之旅,你将如何设计实验呢?
[生]设计的核心思想就是要形成密闭体系。
设计意图: 利用“波义耳的失误,拉瓦锡的成功”的真实史料,让学生了解、感受科学家的科学发现的过程,学习科学家敢于质疑、严谨求实的科学态度,并从中挖掘出实验验证质量守恒定律的思路和方法,形成通过证据和推理进行证实或证伪来建立观念。从而,培养学生“科学精神与社会责任”和证据推理等化学学科核心素养。
2.2创新实验设计——提升“科学探究与创新意识”等学科核心素养
用实验验证“质量守恒定律”是《义务教育化学课程标准(2011版)》规定的重要探究活动[9]。3个版本教科书都注重利用实验探究来帮助学生理解质量守恒定律,但实验内容的选择及开放性等的差异明显(表1)。
不同的实验呈现方式蕴含不同的学科教育价值。设计实验时,应引导学生明确研究的目标与对象,寻找影响因素最少的化学体系,以确定实验原理、步骤,并选取适当的仪器。从而,有计划、有步骤、有针对性地挖掘实验在培养学生实验探究与创新意识方面的功能。因此,笔者借鉴3个版本教科书的实验设计,尝试改进并设计两大类探究实验: 有气体参与(或生成)的反应;没有气体参与(或生成),只涉及液态、固态物质的反应,以实现从教材实验到探究实验的转变。值得一提的是,对于有气体产生的实验,一般不宜采用气球形成密封装置[10]。
[视频]2013年我国宇航员王亚萍在太空实验室称量质量。
[师]王亚萍在太空实验室里称量物质质量的方法与地球实验室相同吗?
[生]不同,无法通过重力来称物体的质量了。
[师]因此,我们设计实验时,应充分考虑科学实验的环境因素。接下来我们来设计实验加以验证(图3)。
[学生实验1]硫酸铜溶液和氢氧化钠溶液反应前后质量的测定。
仪器及药品: 锥形瓶(盛放氢氧化钠溶液)、试剂瓶(盛放硫酸铜溶液)、胶头滴管、电子天平(精度0.01g)
[学生实验2]石灰石与稀盐酸反应前后质量的测定。
仪器及药品: 锥形瓶(少量石灰石)、试剂瓶(盐酸)、注射器、电子天平(精度0.01g)
[视频实验3]红磷燃烧前后质量的测定
仪器及药品: 锥形瓶(底部铺有细沙)、红磷、玻璃管、酒精灯、电子天平(精度0.1g、 0.01g)各一台、气球
[提问]敞口装置有大量白烟冲出,精度0.1g的电子天平称量后仍然相等,为什么?
[讨论]引出仪器精度问题。
[提问]换用精度0.01g的电子天平,天平示数先减小,待锥形瓶冷却后示数又增大,为什么?
设计意图: 通过“等”与“不等”的实验设计,让学生明确设计适当的密闭体系、选取合适精度的仪器设备对定量实验的重要性,以帮助学生建立解决化学问题的基本框架。从而,培养学生基于证据分析做出推理判断和解决实际化学问题的能力,提升学生的“科学探究与创新意识”等化学学科核心素养。
2.3评价实验体系,分析实验结果——提升“证据推理与模型认知”等学科核心素养
“证据推理与模型认知”是运用证据推理和模型化思想解决相关化学问题的能力和品质。是化学科学探究形成结论的思维方法,是化学特征的思维方法[11]。因此,笔者利用“思维框架图”对实验结果进行分析。从而,提升学生建立模型并学会用模型思想认识物质及其变化的一般规律。
[师]通过以上几个实验,你认为实验探究质量守恒定律成功的关键有哪些?
[生]是否采用“封闭装置”,使实验装置封闭的方法有很多,如使用注射器、塞子等。
[师]请小组讨论,你认为在化学反应过程中,反应物和生成物的质量是如何变化的呢?
[生]反应前后,反应物和生成物的质量相等。
[师]原因是什么?
[生]反应前后天平示数仍然相等。
[师]同学们只看到了实验的表面,而未看请化学反应的实质。事实上,我们看到的只是“m(仪器)+m(剩余物)+m(反应物)=m(仪器)+m(剩余物)+m(生成物)”。因此,需对称得的质量进行去伪存真的分析。下面,我们以硫酸铜溶液和氢氧化钠溶液反应为例,分析“整个体系”内物质质量,思维框架如图4。
[板书]质量守恒定律: 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
设计意图: 利用“整个体系”内物质质量的思维框架图,对实验结果进行了去伪存真的分析,突出对“参加化学反应”内涵的理解,实现了从“整个体系”到“具体反应”的思维转换。从而,厘清了“证据”与“结论”的关系。
2.4三重表征与定性定量相结合——提升“宏观辨识与微观探析”、“变化观念与平衡思想”等学科核心素养
铜片在空气中灼烧后固体质量的变化、电解水实验及其微观解释是课程标准新增的情景素材[12],为充分发展学生的“三重表征”思想和能力,人教版、沪教版和鲁教版教科书分别以氢气燃烧、镁条燃烧和过氧化氢分解为例,从微观视角分析质量守恒定律的实质。这些素材既能培养学生通过辨识宏观现象预测物质的微观结构,又能从分子、原子层次分析宏观现象,还能培养学生用动态的视角看待纷繁复杂的化学变化,从化学变化中元素守恒和质量转化守恒的视角考察分析化学反应和解决化学问题。从而,有效提升学生“宏观辨识与微观探析”、“变化观念与平衡思想”等化学学科核心素养。
[师]分析电解水的示意图(图5),谈谈你对物质的化学变化的认识?
[生]化学反应中,参加反应的各物质的原子,重新组合而生成其他物质。
[生]参加反应的H2O与反应后生成的H2、 O2的分子数目比为2∶1∶2,反應前后氢、氧原子的种类和数目都不变。
[师]很好。接下来,请同学们通过计算分析反应物和生成物的相对质量的变化情况。
[生]反应前为: 2×(2+16)=36,反应后为: 2×1×2+2×16=36,故质量相等。
[师]参加反应的水和生成的氢气、氧气的质量比是多少呢?若要得到16g氧气,需要电解多少水?
[生]学生计算得出: 9∶1∶8,需要电解16g水。
[师]由此可以得出,质量守恒定律的实质是: 在化学变化中,反应前后原子种类和数目不变、原子的质量不变。
[练习]略。
设计意图: 学生化学核心素养的形成过程与化学基本观念的形成过程密不可分。探析电解水的微观本质,从定性、定量两个视角分析化学反应的本质,既发展了学生的“三重表征”思
想,又帮助学生构建并形成了化学变化中物质的质量比恒定的观念和质量守恒定律的一般理论模型。为解释“水不能变成油”等原本未知的问题、化学方程式和利用化學方程式的定量计算等奠定基础。从而逐步建立起物质变化观、微粒观、元素观等化学基本观念,最终形成“宏观辨识与微观探析”“变化观念与平衡思想”等化学学科核心素养。
3教学反思
质量守恒定律是学生从对化学反应定性认识开始到定量认识化学变化的转折点,蕴含着丰富的发展学生核心素养的素材。可在教学过程中结合情境的设置、问题的设计、教学资源的开发、评价方式的选择等潜移默化地引导学生去积极建构,但应注意各教学环节都应与学生的认识进阶、认知结构相适应,精心设计教学内容,努力帮助学生解决好相关的思维转换,组织有效的学习活动。既要培养学生对宏观守恒的微观解释,又要培养学生从微观的角度认识、解释宏观现象的思维方式,形成“化学变化过程中元素不变”的观念。
参考文献:
[1]周业虹.基于发展化学学科核心素养的教学设计案例分析[J].化学教学, 2016,(8): 36~39.
[2]钱海如,赵华.初中阶段守恒观的“进阶模型”研究[J].化学教学, 2017,(8): 25~29.
[3]郭建虹.基于建构化学基本观念的对比教学法[J].化学教育, 2016,37(1): 30~33.
[4]王晶,郑长龙.全日制义务教育教科书·化学(九年级上册)[M].北京: 人民教育出版社, 2012: 92~98.
[5]王祖浩,王磊.全日制义务教育教科书·化学(九年级上册)[M].上海: 上海教育出版社, 2012: 100~103.
[6]毕华林,卢巍.全日制义务教育教科书·化学(九年级上册)[M].济南: 山东教育出版社, 2013: 100~104.
[7]胡巢生.“测定空气中氧气的含量”实验探究[J].化学教育, 2013, 35(11): 77~78,80.
[8]刘瑞,郑长龙,白玉琴.燃烧问题——波义耳与燃素学说[J].化学教育, 2009, 31(10): 77.
[9][12]中华人民共和国教育部制定.义务教育化学课程标准[S].北京: 北京师范大学出版社, 2012: 15~16,27.
[10]胡巢生.例谈气球在化学实验中的使用[J].化学教学, 2017,(4): 71~73.
[11]吴星.对高中化学核心素养的认识[J].化学教学, 2017,(5): 3~7.
