131I联合甲巯咪唑治疗Graves病患者疗效及发生甲状腺功能减低的影响因素研究
2018-03-22刘少正胡杰群张庆陈庆杰阳正亚张青
刘少正,胡杰群,张庆,陈庆杰,阳正亚,张青*
Graves病是自身免疫性甲状腺疾病,是由甲状腺滤泡上皮细胞分泌过多甲状腺激素进入血液循环而导致的甲状腺毒症。对我国10个城市甲状腺疾病的流行病学调查显示,甲状腺功能亢进患病率为3.7%,其中80%是由Graves病引起[1]。Graves病的治疗方法主要有抗甲状腺药物、131I治疗以及手术治疗。其中,放射性131I治疗Graves病是简单有益的治疗方法,但可引起甲状腺功能减低的发生。本研究评价131I联合甲巯咪唑治疗Graves病患者的效果,并探讨发生甲状腺功能减低的影响因素,为患者治疗方法的选择提供依据。
1 对象与方法
1.1 研究对象 选取2009—2015年南昌大学第一附属医院与南昌市第三医院经甲状腺功能检测结合临床表现等确诊为Graves病患者2 428例为研究对象,其中男600例,女1 828例;年龄10~74岁,平均年龄(34.3±12.5)岁。患者均符合《中国甲状腺疾病诊治指南》[2]中Graves病的诊断标准,符合131I治疗适应证且无禁忌证;排除随访期间发生甲巯咪唑过敏、肝功能及血常规异常等患者,妊娠及哺乳期患者,临床资料不完整且失访患者。患者均签署知情同意书,并通过南昌大学第一附属医院伦理委员会审查。
1.2 方法
1.2.1 治疗方法 有甲巯咪唑禁忌证患者仅使用131I治疗(A组,1 201例),无甲巯咪唑禁忌证患者使用131I联合甲巯咪唑治疗(B组,1 227例)。
治疗前,患者禁食含碘食物2周以上,对正接受甲巯咪唑治疗的患者,若无甲巯咪唑禁忌证,无需停用。治疗期间常规使用对症治疗的药物(如β-受体阻滞剂等),对合并浸润性突眼和较重的良性突眼患者,在治疗后第3天加用泼尼松30 mg予以控制,疗程2个月。
两组患者均接受131I治疗(碘化钠口服液,成都中核高通同位素股份有限公司),治疗剂量(MBq)=每克甲状腺组织剂量(MBq/g)×甲状腺质量(g)/24 h摄碘率。其中,甲状腺质量由3名核医学医师触诊估计甲状腺质量及质地,同时参考甲状腺静态显像结果进行评价;每克甲状腺组织剂量2.22~4.44 MBq/g,根据患者年龄、病程、摄碘率(用转换率来表示:转换率=2 h摄碘率/24 h摄碘率)、甲状腺质地、抗甲状腺抗体等因素决定。根据患者复诊结果,重复治疗间隔时间在6个月以上。
B组患者于131I治疗3 d后常规给予甲巯咪唑(德国默克公司)10 mg/次,1次/d。2个月后复查,并根据复查结果调整剂量。甲状腺功能正常后,甲巯咪唑低剂量(5 mg/d,隔日1次)维持3~6个月,超声显示甲状腺大小恢复正常,或促甲状腺素受体抗体(TRAb)正常后停用。
1.2.2 疗效评价 患者131I治疗后2个月复诊,之后可适当延长复诊间隔,至少随访12个月后进行效果评价。游离三碘甲腺原氨酸(FT3)、游离甲状腺素(FT4)水平降低且促甲状腺激素(TSH)水平升高,诊断为甲状腺功能减低,并使用甲状腺素替代治疗;FT3、FT4水平升高,TSH水平降低,需再次进行131I治疗或使用甲巯咪唑控制,为部分缓解;甲状腺功能亢进临床症状、体征消失,FT3、FT4均在参考范围内(包含亚临床甲状腺功能亢进或减低,但TSH<10 μU/ml),且未服用抗甲状腺功能亢进或减低药物,为完全缓解。
1.3 统计学方法 采用SPSS 17.0进行统计学分析,正态分布的计量资料以(x±s)表示,多组间比较采用单因素方差分析,多重比较采用LSD-t检验;非正态分布的计量资料以M(P25,P75)表示,组间比较采用非参数检验;计数资料以百分数表示,无序资料的比较采用t检验,等级资料的比较采用Wilcoxon秩和检验;采用多因素Logistic回归分析治疗结局的影响因素。以P<0.05为差异有统计学意义。
2 结果
2.1 疗效评价 患者均获得>12个月随访,平均随访时间(33±30)个月。2 428例Graves患者治疗后,甲状腺功能减低838例(34.51%),部分缓解180例(7.41%),完全缓解1 410例(58.08%)。B组疗效优于A组,差异有统计学意义(u=-5.770,P<0.05,见表1)。

表1 不同治疗方法的Graves病患者疗效情况〔n(%)〕Table 1 Outcome of patients with Graves disease between different treatment
2.2131I联合甲巯咪唑治疗不同疗效的Graves病患者临床资料比较131I联合甲巯咪唑治疗不同疗效的Graves病患者性别、年龄、病程、治疗前服用甲巯咪唑比例、131I剂量、甲状腺质量、转换率、抗甲状腺过氧化物酶(TPO)、重复治疗比例比较,差异均有统计学意义(P<0.05)。其中,部分缓解者男性比例、甲状腺质量、重复治疗比例大于完全缓解者,年龄、131I剂量、转换率、TPO低于完全缓解者,男性比例高于甲状腺功能减低者,年龄低于甲状腺功能减低者;甲状腺功能减低者病程短于完全缓解、部分缓解者,治疗前服用甲巯咪唑比例低于完全缓解者,131I剂量、TPO、重复治疗比例高于完全缓解、部分缓解者,甲状腺质量低于完全缓解、部分缓解者,转换率低于完全缓解者、高于部分缓解者,差异均有统计学意义(P<0.05,见表2)。
2.3 Logistic回归分析 以性别、年龄、病程、治疗前服用甲巯咪唑、131I剂量、甲状腺质量、转换率、TPO、重复治疗为自变量,是否出现甲状腺功能减低为因变量进行多因素Logistic回归分析,变量赋值见表3。多因素Logistic回归分析显示,131I剂量、甲状腺质量、转换率、TPO是131I联合甲巯咪唑治疗的Graves病患者发生甲状腺功能减低的影响因素(P<0.05,见表4)。

表3 131I联合甲巯咪唑治疗的Graves病患者发生甲状腺功能减低影响因素的Logistic回归分析变量赋值Table 3 Variables and their assignment associated with hypothyroidism in Graves disease patients treated by 131I combined with methimazole analyzed with Logistic regression
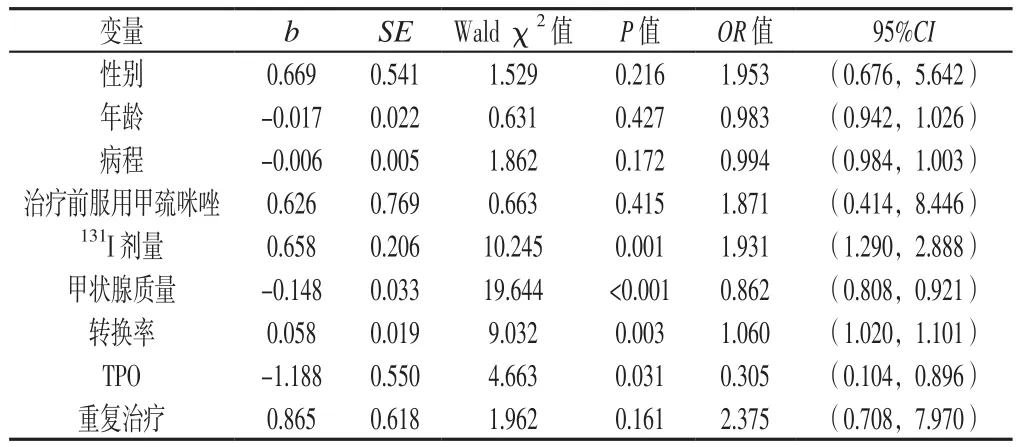
表4 131I联合甲巯咪唑治疗的Graves病患者发生甲状腺功能减低的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis of the associated factors for hypothyroidism among Graves disease patients treated by 131I combined with methimazole
3 讨论
131I治疗Graves病的机制是利用131I的β射线照射甲状腺,破坏甲状腺滤泡细胞,减少甲状腺素分泌,具有费用低、简单、安全、疗效好的优点,但也存在发生甲状腺功能减低的风险。部分甲状腺功能减低患者不能遵照医嘱终身规律甲状腺素替代治疗,未能够及时得到控制及纠正,尤其是中老年患者。甲状腺功能减低表现为食欲减退、腹胀、恶心、胃酸分泌减少、便秘、贫血,同时影响神经系统,表现为记忆力减退、意力不能集中、理解和计算能力降低、表情淡漠、抑郁不语等,而妊娠期甲状腺减低患者可损害后代神经发育,增加早产、流产、低体质量儿、死胎和妊娠期其他疾病的发生风险,需及时给予治疗。
本研究显示,131I联合甲巯咪唑治疗的患者甲状腺功能减低发生率为24.45%,低于单用131I治疗的患者,同样低于METSO等[3]、AHMAD等[4]单用131I治疗患者甲状腺功能减低的发生率(分别为55.8%、59%)。本研究根据患者病情,在治疗期间并不追求大剂量131I一次性治愈Graves病,以降低发生甲状腺功能减低的风险,建议给予适量的131I剂量,使肿大的甲状腺尽可能缩小,后联合甲巯咪唑治疗,但治疗时间会一定程度延长。有研究证实,使用抗甲状腺药物是Graves病患者治疗失败的原因,其具有较高的停药后复发率,另外,甲状腺大小也是该病药物治疗后复发的相关因素之一[5]。Graves病是一种自身免疫性疾病,其主要机制是由人体自身抗体TRAb直接作用于甲状腺细胞表面的受体,导致甲状腺功能亢进的发生,甲状腺细胞程序性死亡(即凋亡)是其主要的病理改变,是Bcl-2与白介素促甲状腺素受体抗体活性氧簇等细胞因子相互作用的结果[6]。抗甲状腺药物可阻止并抑制甲状腺素合成,主要机制是通过抑制甲状腺过氧化物酶,阻断甲状腺素的合成和释放,并参与了机体自身免疫调节。因此,131I联合抗甲状腺药物治疗可提高患者治愈率,同时降低甲状腺功能减低的发生风险。
前期研究显示,131I剂量、131I转换率、甲状腺过氧化物酶抗体及甲状腺质量是Graves病患者131I治疗后发生甲状腺功能减低的影响因素,而未发现抗甲状腺药物与甲状腺功能减低之间的关系[7],本研究结果与之不同。本研究患者在选用131I治疗前并未要求停服甲巯咪唑,而前期研究均需停服甲巯咪唑2周或2周以上。本研究重点关注131I治疗的最优剂量,以降低甲状腺功能减低的发生风险和提高甲状腺功能恢复正常率。研究认为,患者在吸收低剂量131I之后服用若干个月甲状腺素替代治疗,能够促进甲状腺功能恢复正常,可能是由于未坏死的细胞功能得以恢复,而若干年后晚发甲状腺功能减低可能与131I剂量无关,而且绝大多数患者难以恢复甲状腺功能正常[8]。笔者观察到,部分仅采用甲巯咪唑治疗的Graves病患者,在自然进程中仍可自发发生甲状腺功能减低。本研究发现,131I作为一线治疗,如果患者仍然是甲状腺功能亢进,可继续服用甲巯咪唑,但药物治疗周期比指南[2]推荐的抗甲状腺药物一线治疗周期更短。CHEN等[8]同样认为,低剂量131I联合抗甲状腺药物的治疗方案能有效地治疗甲状腺功能亢进,显著降低甲状腺功能减低发生率,可能是较有意治成永久甲状腺功能减低更好的治疗方式。

表2 131I联合甲巯咪唑治疗不同疗效的Graves病患者临床资料比较Table 2 Comparison of clinical data of Graves disease patients treated by 131I combined with methimazole among different outcome
此外,临床对使用131I治疗的安全性一直存在疑虑,认为可导致癌症或遗传性疾病的风险增加。有研究对107例3~19岁Graves病患者进行131I治疗,随访时间为26~36年,未发现有发生甲状腺癌或白血病患者[9]。本研究在全部随访期间也并未发现1例恶性疾病发生。前期研究显示,131I治疗育龄期Graves病患者安全、简便,对妊娠期及子代TSH水平无不良影响[10],值得在育龄期Graves病患者中推广。
综上所述,131I联合抗甲状腺药物治疗可降低Graves病患者甲状腺功能减低发生风险,提高完全缓解率。131I治疗是Graves病主要的治疗方式,具有疗效高、安全、费用低廉、方法简便、不良反应少等优点,而甲状腺功能减低是131I治疗后最主要的并发症,其发生受多个因素影响,具体机制尚不明确,一定程度制约了131I治疗的应用。如能建立131I治疗Graves病的规范化方案,最大限度延缓永久性甲状腺功能减低的发生,则会提高131I在临床治疗甲状腺功能亢进中的应用。
作者贡献:刘少正、张青进行文章的构思与设计,对文章整体负责,监督管理;刘少正、张庆进行研究的实施与可行性分析;陈庆杰、阳正亚进行数据收集;刘少正、胡杰群进行数据整理、统计学处理;张庆、张青进行结果的分析与解释,负责文章的质量控制及审校;刘少正撰写论文及论文修订。
本文无利益冲突。
[1]滕卫平,邢小平,童南伟,等.中国十城市甲状腺疾病流行病学调查[C]//中华医学会第九次全国内分泌学学术会议论文汇编.北京:中华医学会,2010:11.TENG W P,XING X P,TONG N W,et al.Epidemiological survey of thyroid diseases in ten cities,China[C]//The Ninth National Conference on Endocrinology of the Chinese Medical Association.Beijing:Chinese Medical Association,2010:11.
[2]单忠艳.《中国甲状腺疾病诊治指南》导读[J].中国实用内科杂志,2008,28(4):260-261.SHAN Z Y.Guide to diagnosis and treatment of thyroid disease in China[J].Chinese Journal of Practice Internal Medicine,2008,28(4):260-261.
[3]METSO S,JAATINEN P,HUHTALA H,et al.Long-term followup study of radioiodine treatment of hyperthyroidism[J].Clin Endocrinol (Oxf),2004,61(5):641-648.DOI:10.1111/j.1365-2265.2004.02152.x.
[4]AHMAD A M,AHMAD M,YOUNG E T.Objective estimates of the probability of developing hypothyroidism following radioactive iodine treatment of thyrotoxieosis[J].Eur J Endocrinol,2002,146(6):767-775.
[5]任汉强,沈小波.Graves病抗甲状腺药物治疗后复发的相关因素分析[J].西南军医,2012,14(2):263-265.REN H Q,SHEN X B.Analysis of the related factors of recurrence of Graves's disease after antithyroid drug treatment[J].Journal of Military Surgeon in Southwest China,2012,14(2):263-265.
[6]石英,黄国良.Fas/FasL途径在Graves病发病机制中的作用[J].国外医学(内分泌学分册),2005,25(1):48-50.DOI:10.3760/cma.j.issn.1673-4157.2005.01.018.SHI Y,HUANG G L.The role of Fas/FasL pathway in the pathogenesis of Graves disease[J].Section of Endocrinology Foreign Medical Sciences,2005,25(1):48-50.DOI:10.3760/cma.j.issn.1673-4157.2005.01.018.
[7]刘少正.Graves甲亢131I治疗后甲状腺功能减退的因子分析[D].南昌:南昌大学,2013.LIU S Z.Factor analysis of hypothyroidism after131I treatment in the patients with Graves hyperthyroidism[D].Nanchang:Nanchang University,2013.
[8]CHEN D Y,SCHNEIDER P F,ZHANG X S,et al.Striving for euthyroidism in radioiodine therapy of Graves' disease: a 12-year prospective,randomized,open-label blinded end point study[J].Thyroid,2011,21(6):647-654.DOI:10.1089/thy.2010.0348.
[9]READ C H Jr,TANSEY M J,MENDA Y.A 36 year retrospective analysis of the efficacy and safety of radioactive iodine in treating young Graves'patients[J].J Clin Endocrinol Metab,2004,89(9):4229-4233.DOI:10.1210/jc.2003-031223.
[10]刘少正,张青,张庆.女性Graves病131I治疗后的生育情况与子代健康初步分析[J].中国妇幼保健,2015,30(26):4506-4508.DOI:10.7620/zgfybj.j.issn.1001-4411.2015.26.36.LIU S Z,ZHANG Q,ZHANG Q.A preliminary analysis of the fertility condition and offspring health of women with Graves's disease after131I treatment[J].Maternal & Child Health Care of China,2015,30(26):4506-4508.DOI:10.7620/zgfybj.j.issn.1001-4411.2015.26.36.
