电针对魏一凯二氏大鼠抑郁模型大鼠海马CA1区突触可塑性及5-羟色胺转运体蛋白的影响*
2018-03-19韩栩珂武上雯徐世芬
韩栩珂,尹 平,殷 萱,武上雯,徐世芬
(上海中医药大学附属市中医医院 上海 200071)
抑郁症是一种以持久而明显的心境低落为主要临床特征的常见情感障碍,重度抑郁症可因自杀而导致死亡,严重危害人类身心健康且终生患病率高达15%-17%[1]。据WHO统计,全球约有3.5亿人患有抑郁症[2],预计到2020年抑郁症将会成为仅次于心脏病的第二大危害性疾病[3]。抑郁症不仅影响神经系统,还涉及消化系统、免疫系统等方面的病变[4]。近年来,突触可塑性与抑郁症的关系越来越受到关注。突触可塑性作为脑可塑性的主要表现,是指突触在神经细胞连续活动影响下发生的特异性突触传递效能、突触形态结构和突触发育的可塑性[5]。突触传递效能的变化可因性质不同,分为长时程增强(Long-term potentiation,LTP)和长时程抑制(Long-term depression,LTD)两方面[6]。神经递质介导的突触传递效能的持续改变可以引起抑郁情绪状态的发生。抑郁症患者的LTP样可塑性与健康人相比显着受损,且这种突触可塑性衰减在抑郁状态缓解后恢复[7]。因此,LTP可能是形成学习记忆的重要分子基础[8]。有研究证明,选择性5-HT再摄取抑制剂(SSRIs)的抗抑郁作用与突触可塑性的改善密切相关[9]。5-HT又称血清素,是一种单胺类神经递质,在睡眠,摄食,性行为,温度调节,疼痛和认知等生理功能以及情感障碍,焦虑症,精神病等病理状态中起重要作用[10]。而5-HTT(5-羟色胺转运体)是一种跨膜转运蛋白,先和突触间隙中的5-HT结合,后将其转运至神经元的轴突末稍,对调节5-HT代谢及功能起着关键作用[11]。抑郁和焦虑的发生与5-HTT的活动变化相关[12]。研究发现,在受5-HTT基因型影响的抑郁症患者中,大脑5-HT周转率显著增加,而在接受SSRI治疗12周后,血清素周转率下降[13]。
前期研究表明,电针百会、印堂后可以明显改善抑郁大鼠的抑郁样行为,改善海马的突触可塑性,增强LTP[14]。但电针的具体的作用途径不明确,是否和5-HTT有关,还有待进一步研究。因此,本实验以电针百会、印堂穴,选取WKY鼠为抑郁动物模型,采用以上指标来观察电针治疗对抑郁模型大鼠抑郁样行为、海马CA1脑区突触可塑性以及5-HTT蛋白表达的影响。
1 材料与方法
1.1 实验动物
本实验采用从北京维通利华实验动物技术有限公司购买的雄性4周龄WKY大鼠30只和Wistar大鼠10只,均为SPF级,合格证编号:SCXK(京)2012-0001。大鼠购入后均进行一周适应性喂养,自由摄食饮水,明暗光照12/12小时昼夜交替,室内相对湿度为50%-60%,室温约(22±2)℃。
1.2 药物与试剂
氯化钠(NaCl)、碳酸氢钠(NaHCO3)、硫酸镁(MgSO4)、磷酸二氢钠(NaH2PO4)、无水氯化钙(CaCl2)、氯化钾(KCl)、D-葡萄糖(D-Glucose)、氯化胆碱(Choline choloride)、丙酮酸钠(Na pyruvate)、抗坏血酸钠(Sodium ascorbate)、葡萄糖酸钾(K-gluconate),Sigma公司。
内参 GAPDH,Kang Chen公司,1∶20000;一抗5-HTT,Abcam公司,1∶1000;抗兔二抗,Millipore公司,GB23303,1∶4 000。BCA蛋白定量试剂盒购于上海生工生物工程股份有限公司;蛋白提取试剂盒购于上海碧云天生物技术有限公司;戊巴比妥钠,购于上海敏锐有限公司。
1.3 仪器
ADZ-Ⅱ华佗电针治疗仪,苏州医疗用品有限公司;ANY maze视频分析系统,Stoelting公司;旷场实验、强迫游泳实验系统,上海移数信息科技有限公司;pClamp 10.2记录分析软件、AxoClamp-2B放大器、Digidata 1322A数模转换器,Axon公司;垂直电泳槽、转印电泳仪、ECL发光成像系统,Bio-rad公司。
1.4 分组与干预
30只WKY大鼠随机分至电针组(EA)、假针组(Sham EA)和模型组(Model),每组10只;Wistar大鼠10只设为正常组(Control)。电针组:参照《实验动物针灸穴位图谱》定位大鼠“百会”和“印堂”穴,将电针治疗仪导线的正负极两端露出铜丝并缠绕于0.2 mm×13 mm一次性不锈钢毫针上,用胶布固定。钻3个直径约1 cm的小孔于透明储物盒底端,附有毫针的导线通过其中一个孔,剩余两孔作为换气孔。将大鼠置于实验台上,毫针刺入百会穴约5 mm,印堂穴约2 mm,医用胶布固定针灸针。用透明储物盒扣住大鼠,启动电针仪,给予2 Hz连续波,从0.1 mA开始逐渐加大强度,电流依据大鼠的耐受情况以头部颤动且不嘶叫为度。电针治疗每次15 min,每日一次,连续治疗3周。电针过程中,注意观察大鼠是否抓挠针灸针,若出现该情况,可轻微敲击储物盒以转移大鼠注意力。治疗期间,保持安静,尽量避免对大鼠产生情绪影响。
假针组:抓取方法与电针组相同,将同规格的毫针浅刺入与电针组相同的体表位置,但不刺入穴位,以避免针刺的非特异性效应。针灸针与电针仪导线相连,但不通电。留针和治疗时间均与电针组相同。
正常组、模型组均常规饲养,不予治疗。
1.5 检测指标
1.5.1 糖水偏好实验(Sucrose preference test,SPT)
壶天晓伸手将镜心羽衣护在身后,侧过头低声叮嘱镜心羽衣下一步要采取的行动。镜心羽衣听后,眼睛瞪得溜圆,连连摇头。壶天晓举起左手,示意她照计划行事。镜心羽衣一步一回头地离开他,向定在一旁的丁达走去。
正式实验操作前的48 h被分为两个阶段,第一阶段的24 h训练大鼠适应饮用蔗糖水,每个鼠笼放置1%蔗糖水150 mL和纯水150 mL各一瓶,供大鼠自由饮用。第二个阶段的24 h,所有大鼠禁食禁水。正式实验(即电针干预3周)时,给予大鼠1%蔗糖水和纯水各150 mL,12 h后调换两瓶水的位置,24 h后测量每只大鼠蔗糖水和纯水的消耗量,并计算糖水偏好百分比。糖水偏好比计算公式为:[(蔗糖水饮用量)/(蔗糖水饮用量)+ (纯水饮用量)]× 100%。
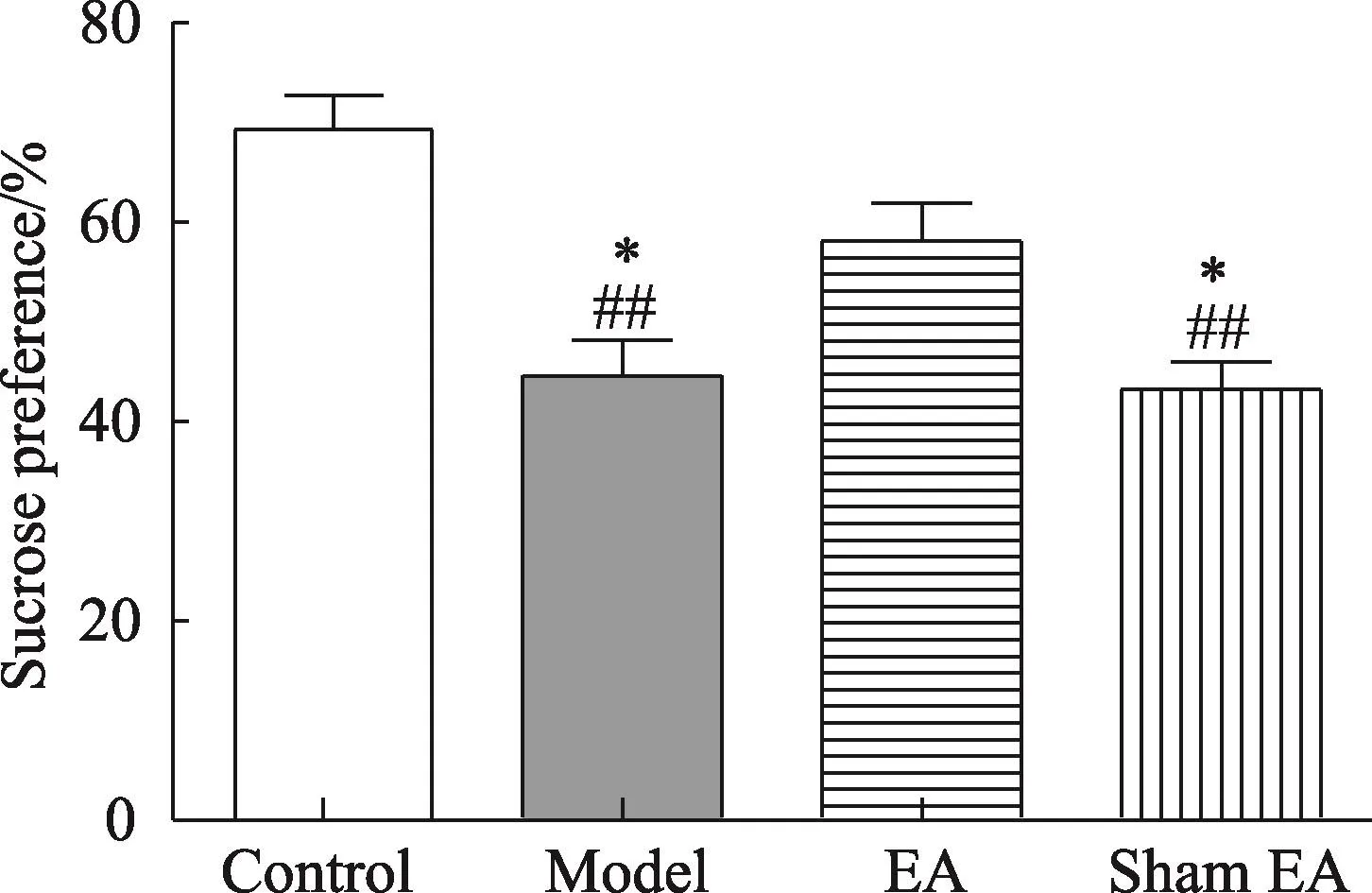
图1 各组大鼠糖水偏好百分比
1.5.2 旷场试验(Open filed test,OFT)
旷场实验箱为四周和底面均为黑色的立方体敞箱(80 cm×80 cm×40 cm),其中底座被分成16×16 cm的等宽方格25个。将单只大鼠放置于箱底中央格,箱顶摄像头记录其自由活动5 min内的运动情况,主要包括大鼠的中央运动时间和距离,水平运动总时间和总距离,垂直和站立次数。并实时连接电脑,对实验数据储存分析。每只大鼠测定结束后,立即清理实验箱中排泄物,并使用75%酒精消毒去除气味,方可进行下一只大鼠的实验检测。
1.5.3 强迫游泳实验(Force swimming test,FST)
强迫游泳实验在一个高40 cm、底面直径30 cm的透明圆柱形有机玻璃容器中进行。在容器中注入约32 cm的自来水,水温23-25℃。实验分为两天,第一天对所有大鼠进行15min的预游泳训练,结束后擦干放回笼中,常规饲养。24 h后开始正式实验,每只大鼠逐个倾斜、头部向上放入水中进行强迫游泳测试5 min,采用ANY maze软件记录分析大鼠在此期间内的静止不动时间,静止不动包括暂停大部分运动、停止挣扎、仅有轻微前爪移动以维持平衡等状态[15]。为避免干扰实验结果,在每只大鼠测试结束后,都应清洁容器并更换用水。
1.5.4 场电位实验
行为学实验结束后第二天,配制人工脑脊液(ACSF)和改良的人工脑脊液(mACSF)。大鼠麻醉后断头取脑,沿中缝将大脑切成两半,其中一半于-80℃超低温冰箱储存,待Western blotting使用。剩余一半于切片槽内连续切取包含完整海马脑区的冠状切片370 μm。将切好的脑片移至31℃的ACSF中热激1 h,室温孵育1 h。将脑片移至记录槽中,刺激电极(钨电极)置于CA1区Schaffer侧枝上,玻璃记录电极置于CA1区辐射层。将刺激大小调整至能诱发fEPSP斜率达到最大反应的1/2-2/3的刺激强度,刺激方波的波宽设为0.05 ms,刺激间隔为30 s,并稳定记录15 min以上作为基线。随后连续给予2 s的100 Hz高频电刺激(high frequency stimulation,HFS),诱导LTP。然后将刺激间隔改回30 s,并记录45 min以上。
1.5.5 Western blotting
取海马CA1脑区并称重BCA法测定浓度后,配平浓度,100℃水浴7 min后4℃冷却上样。电泳参数设置为恒压80 V,30 min后转为110 V。恒流150 mA转膜90 min,后使用5%脱脂牛奶封闭1h。一抗于4℃孵育过夜后,用TBST洗膜10 min/3次,然后二抗孵育2 h,再TBST洗10 min/3次,显影进行统计。
1.6 统计学方法
所有实验数据均采用GraphPad Prism 5.0进行统计分析并绘图,以均数±标准差(x±s)表示。各样本组间两两比较采用单因素方差分析(One-Way ANOVA),Post-hoc检测采用Tukey法,P<0.05为差异有统计学意义。
2 结果
2.1 蔗糖水偏好实验结果
与Control组相比较,Model及Sham EA组糖水偏好比显著降低(P<0.01)。经过3周的电针治疗后,EA组的糖水喜好比明显高于Sham EA组(P<0.05)。与Model组相比,EA组的糖水喜好比也升高(P<0.05)。Sham EA组与Model组相比,差异无统计学意义(图1)。
2.2 旷场实验结果
与Control组相比,Model组中央运动时间明显减少(P<0.001)。而经过电针治疗3周后,EA组的中央运动时间增多(P<0.05)(图2-A)。与Control组相比,Model组总运动时间明显减少(P<0.01)。与Model组相比,EA组的总运动时间明显增加(P<0.05)(图2-B)。与Control组相比,Sham EA及Model组的中央运动距离明显缩短(P<0.01)。电针治疗3周后,EA组大鼠中央运动距离有增加的趋势,且高于Sham EA、Model组,但差异无统计学意义(图2-C)。与Control组相比,Model组的总运动距离缩短(P<0.05)。与Sham EA组相比,Control组的总运动距离明显增加(P<0.01)。电针治疗后,抑郁模型大鼠的总运动距离并无明显变化,其余各组间比较无统计学差异(图2-D)。与Control组相比,Sham EA和Model组大鼠垂直站立次数显著减少,且差异有统计学意义(P<0.001,P<0.01)。而3周电针治疗后,WKY大鼠的垂直站立次数增多,高于Sham EA和Model组,但各组间比较无明显统计学差异(图2-E)。
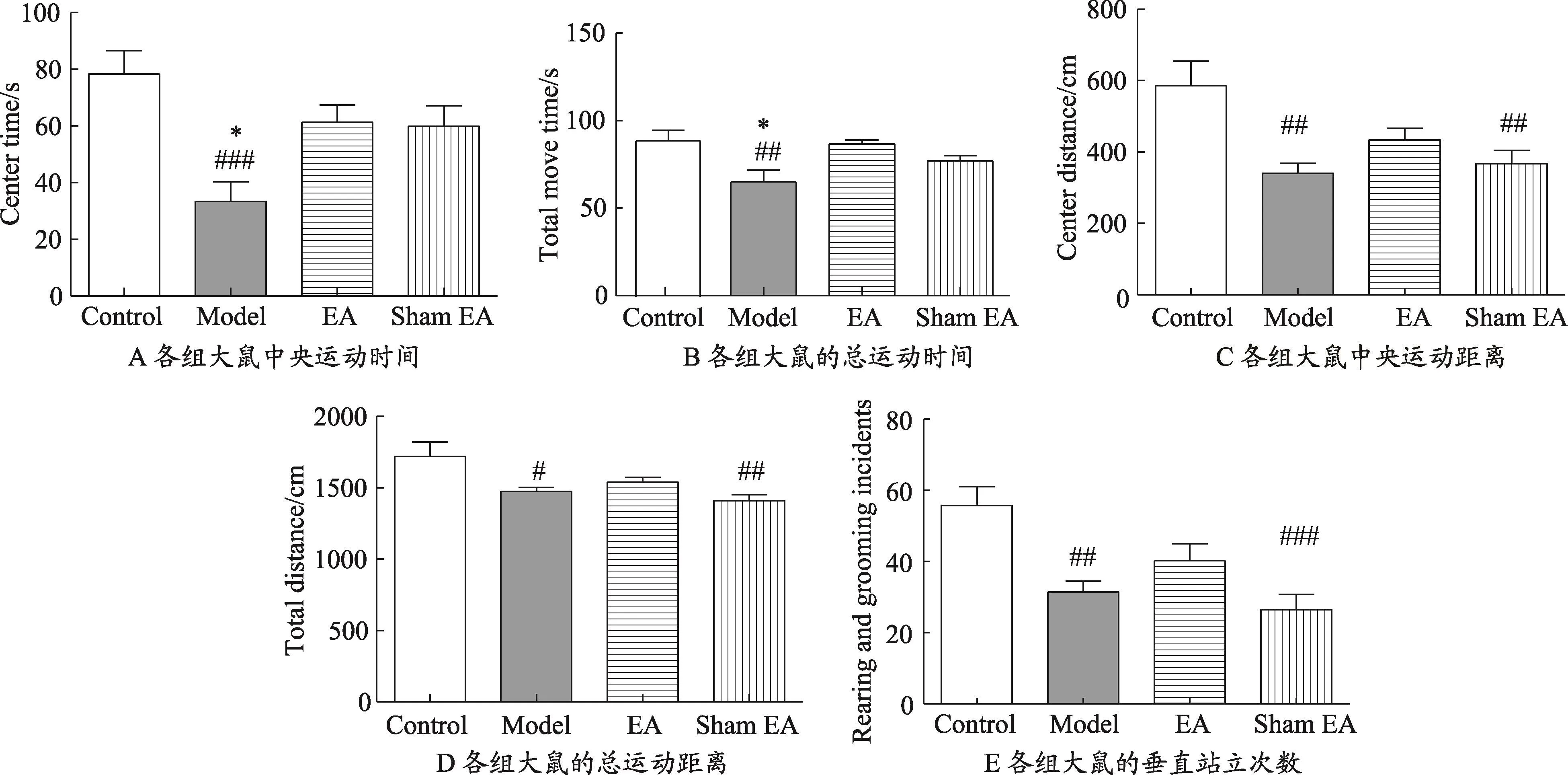
图2
2.3 强迫游泳实验结果
与Control相比,Model组和Sham EA组大鼠在强迫游泳实验中的不动时间明显增多(P<0.05)。3周的电针治疗能明显减少抑郁模型大鼠的不动时间,与Sham EA组相比,EA组大鼠的不动时间减少(P<0.05)。Model组与Sham EA组比较,差异无统计学意义(图3)。
2.4 海马CA1区Schaffer通路LTP诱导情况
Control组及EA组均能成功诱导出LTP,而Model组和Sham EA组LTP诱导失败。Control组和EA组的fEPSP斜率值为(192.0±1.13%,135.1±1.22%),Model组和Sham EA组fEPSP斜率值为(105.2±0.51%,107.4±0.50%)。Control组、EA组与Model组、Sham EA组相比,有显著性差异(P<0.001)(图4)。
2.5 海马CA1区5-HTT蛋白表达结果
结果显示,EA组与Sham EA组相比较,海马CA1区5-HTT蛋白表达减少(P<0.05);Model组与Control组比较,其表达增加(P<0.01)。表示WKY大鼠海马CA1区5-HTT蛋白表达明显高于正常大鼠,过度的5-HTT表达可导致抑郁症,电针可显著降低抑郁模型大鼠海马CA1区5-HTT的表达(图4)。
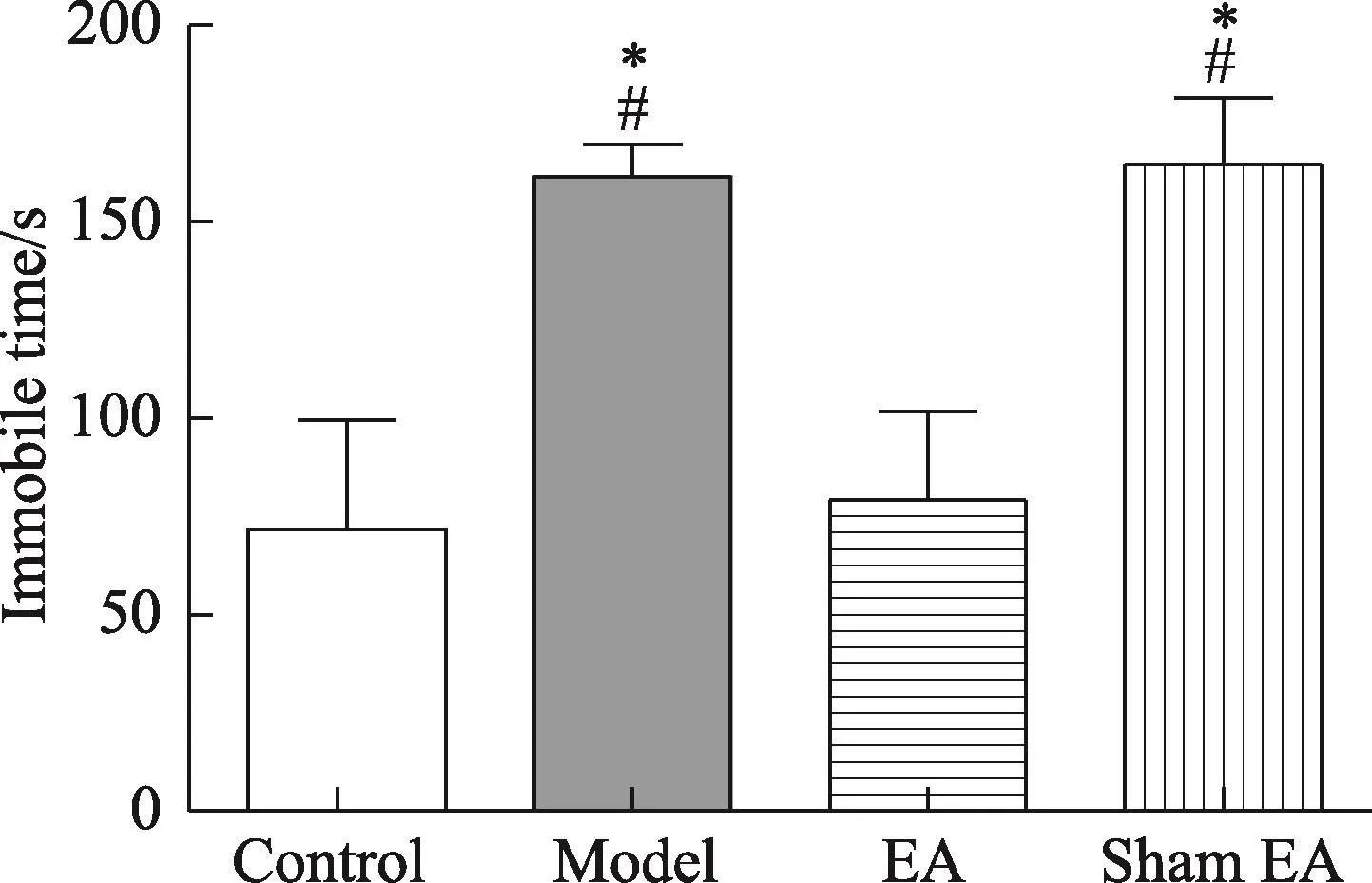
图3 各组大鼠的不动时间
3 讨论
中医认为,抑郁症属于“郁证”范畴,也称作“脏躁”、“百合病”等。病位以脑为主,涉及心、肝、脾、肾等脏腑。本病由于情志内伤,久而郁结,心神不交,逐步发展为脑腑气机紊乱、脏腑阴阳气血失调。心神失养,七情失制,灵台不清,故出现心境低落、沉默寡言、失眠健忘等一系列情志症状。气机升降失司,脏腑功能紊乱,水谷精微运化失常,故出现不思饮食、消化不良、喜静恶动、肌肉酸痛等一系列躯体症状。《本草纲目》曰:“脑为元神之府”。故抑郁症这种病位以脑为主,心神失养的情志疾病,治疗应以调神醒脑、安神益智、疏肝解郁为主。督脉上通于脑,下通于肾,贯于心,是“精髓升降之道路”,在百会穴处与手足三阳经和足厥阴肝经交汇,与脑、心、肾、肝都有直接的联系。百会穴位于巅顶,统领一身之气,是统摄阳气,醒脑开窍,定惊益智之要穴。印堂穴虽为经外奇穴,但为督脉循行于前额所经之穴,是健脑宁心、解郁安神之要穴。百会与印堂配伍,可达到“督脉通,则诸经通,脑窍聪,气机畅”的效果。因此,本实验选择“百会”、“印堂”为针刺主穴。
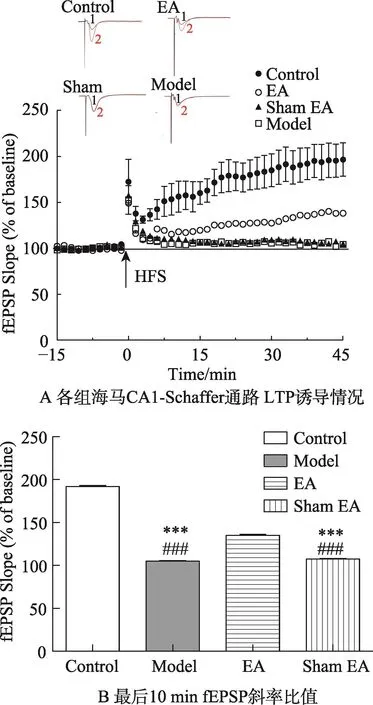
图4
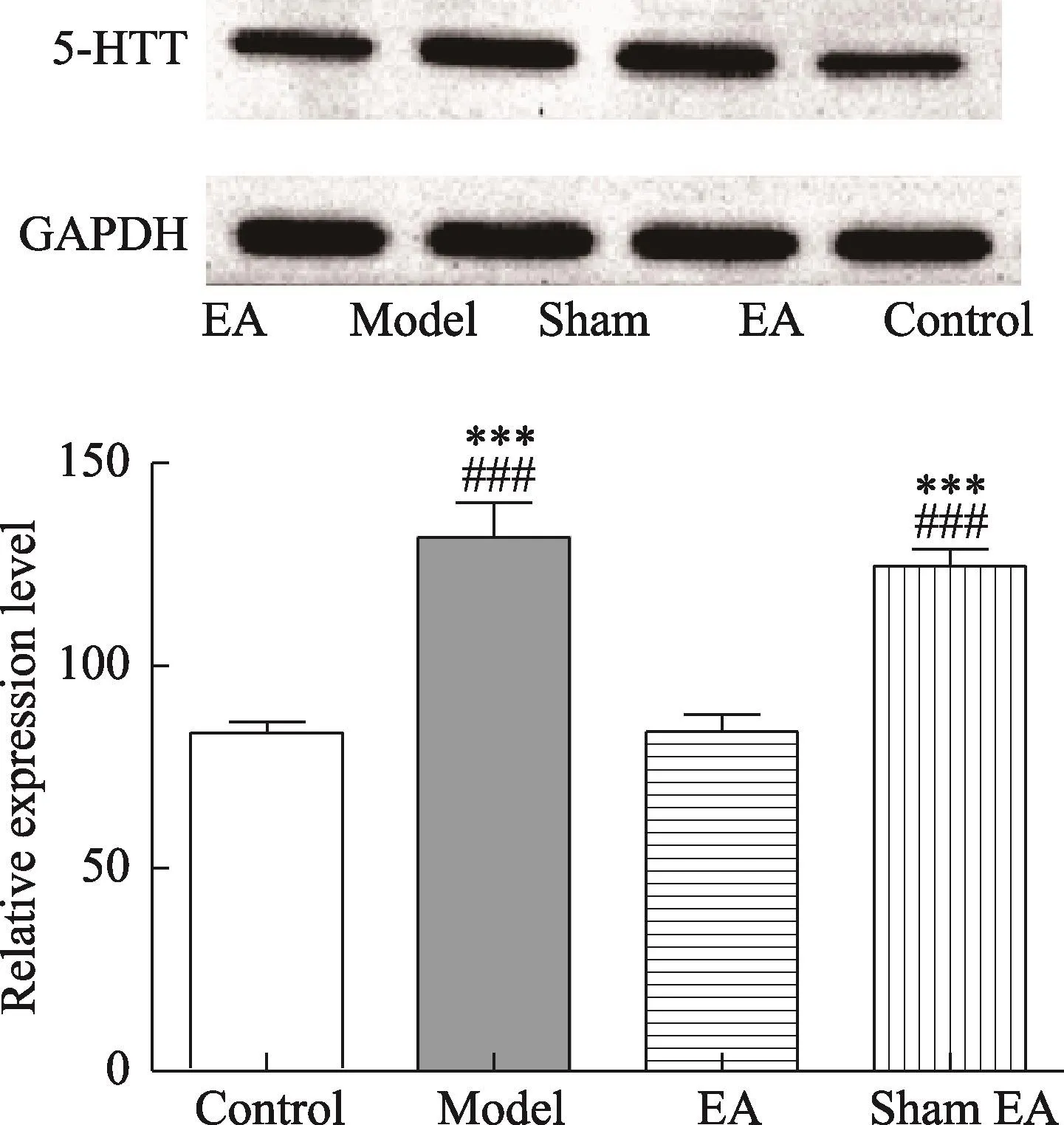
图5 CA1区5-HTT表达情况
本研究应用电针百会、印堂进行干预后发现抑郁大鼠的抑郁样行为发生了明显的改善,包括糖水偏好性、旷场行为和强迫游泳等。糖水偏好实验是根据动物对甜味的偏好而设计检测方法,糖水偏好量可以反映动物快感缺失的程度[16]。快感缺失是指体验快乐的能力降低,是抑郁症的重要特征[17]。因此,糖水偏好实验常被用来评估大鼠的抑郁样行为。旷场实验,可以用来衡量大鼠在新奇环境中的自发探索行为和紧张度。在陌生环境中,抑郁动物会表现出紧张焦虑,选择在区域周边活动,很少进行中心区域探索。而当抑郁状态缓解时,由于其自身的好奇探索天性,会逐渐增多在中心区域的行动时间,因此是评价抑郁样行为的常用检测方法。强迫游泳实验是模拟一个不可逃避的应激环境,动物从试图挣扎到放弃逃脱,随后处于行为绝望的状态,是用来反映大鼠求生欲望及绝望行为的经典行为学评价方法[18]。目前认为,这种行为绝望类似于人类抑郁症的表现[19]。
抑郁大鼠模型,我们选择Wistar Kyoto(WKY)大鼠,该鼠为转基因抑郁大鼠,所表现出的昼夜节律紊乱、血浆ACTH和皮质酮水平增高、对HPA轴应激失调的高反应性,都与临床抑郁症患者相同[20]。相关研究也报道WKY大鼠糖水摄入量减少,快感缺失[21],强迫游泳实验的不动时间增多,求生欲望减弱[22],且对压力具有极度敏感性和稳定遗传性,该大鼠所表现的抑郁行为稳定,在国内外实验中常被作为抑郁症的动物模型进行研究[23-25]。
有关抑郁症的具体发病机制尚未完全明确,但近些年已被人们普遍接受的抑郁症单胺类神经递质受体假说认为,抑郁症与5-HT受体的数量及敏感性密切相关[26]。5-HTT是一种跨膜转运蛋白,主要存在于中枢神经系统的突触前膜,它在5-HT重摄入神经元轴突末端的过程中起重要作用[27]。5-HTT活性的改变与抑郁风险增加相关[12]。5-HTT也是终止5-羟色胺能神经传递的主要手段,是许多抗抑郁治疗的关键作用点[28],研究认为下调海马CA1区5-HTT的过表达,从而修复受损的海马突触可塑性,可以缓解抑郁模型大鼠的抑郁样行为。先前的研究还报道,5-羟色胺能机制参与了大鼠海马CA1脑区心理应激诱发的突触可塑性改变[29]。因此,这些数据表明,不平衡的5-HT受体水平与突触可塑性变化是抑郁症的关键病理生理机制。
本实验的结果与目前的证据相一致,即过度的5-HTT表达可导致抑郁症。Western blot结果显示电针可显著降低抑郁模型大鼠海马CA1区5-HTT蛋白的表达。我们的研究表明电针治疗可以降低海马CA1区5-HTT蛋白的表达,从而促进突触可塑性和缓解抑郁样行为。
4 结论
电针可明显改善抑郁模型大鼠的行为学症状,提示电针的抗抑郁机制可能与下调海马CA1区5-HTT的过表达有关,从而起到修复受损的海马突触可塑性,进而缓解其抑郁症状的效果。本研究揭示了电针抗抑郁的作用途径及部分机制,为电针治疗抑郁症的机理阐释提供了新的实验依据。
