巧用“类价二维图”,构建思维模型
2018-03-19傅新军山东省威海市第三中学山东威海
傅新军(山东省威海市第三中学,山东 威海)
一、认识“类价二维图”
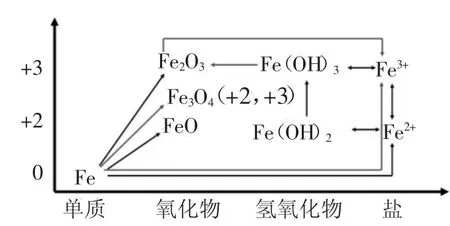
“类价二维图”是以元素为核心,从类别和价态两个角度来认识物质性质和转化的一种二维坐标图。它能够引导学生从分类的角度分析元素及化合物,把物质分为氢化物、单质、氧化物、酸、碱、盐等,能帮助学生根据物质的类别,推测物质可能具有的性质;还可以引导学生从氧化还原的角度,分析物质的氧化性和还原性,进而分析物质所发生的氧化还原反应,最终形成多角度认识物质转化的思维模型。例如铁元素的“类价二维图”如下所示。
二、“类价二维图”的应用
在教学中如何深入挖掘“类价二维图”的功能价值,引导学生通过“类价二维图”来认识元素化合物,下面跟大家分享一下北京工业大学附属中学的马炜老师运用“类价二维图”所设计的硫元素的复习课,本节课的课题为《NaHSO3的性质探究》。
1.课题设计背景
这节课设计的背景是学生在课前已经对硫单质、二氧化硫、硫酸、硫酸根等相关知识做了比较系统的梳理,这节课实际上是对以上知识的一个总结和提升。对于学生来说,NaHSO3相对于SO2和Na2SO3更为陌生一些,从物质类别上说属于多元弱酸的酸式盐,既能与酸反应又能与碱反应,能够了解学生对离子反应的掌握情况,同时NaHSO3在水溶液中既有电离又有水解,能够帮助学生回顾电离平衡和水解平衡的相关知识;从化合价角度来说,它既有氧化性又有还原性,能够引导学生去深入理解氧化还原反应的相关知识,因此,这个素材的选取有利于培养学生多角度分析问题的能力。
2.课堂设计思路
环节一:给学生3分钟在学案上画出硫元素的“类价二维图”,并找学生代表展示二维图,介绍二维图中各物质之间的相互转化关系。
环节二:小组内展开讨论,依据硫元素的“类价二维图”预测NaHSO3的化学性质,小组代表进行陈述,教师进行点评,学生自我整理。师生共同得出结论,NaHSO3的化学性质主要有以下几点:(1)多元弱酸的酸式盐:电离、水解;(2)与酸反应;(3)与碱反应;(4)具有还原性:与高锰酸钾、溴水反应;(5)具有氧化性:与硫化钠反应。
环节三:实验验证:小组内通过交流合作,根据所预测的NaHSO3的化学性质,结合老师所提供的实验仪器和药品,设计合理的实验方案对预测结果进行验证。由小组代表进行陈述,教师进行点评,学生自我整理。最后小组内开展实验,分工明确,操作规范,记录实验现象,得出实验结论。
【实验1】测定NaHSO3的pH
问题探究:(1)如何测溶液的pH?(2)为什么NaHSO3溶液显酸性?(3)分析NaHSO3的水溶液中离子的浓度大小?
【实验2】把盐酸滴入NaHSO3溶液中观察反应现象。
问题探究:有同学认为NaHSO3溶液中加入BaCl2溶液,会发生反应NaHSO3+BaCl2=NaCl+HCl+BaSO3↓,这样的考虑对不对?
【实验3】与高锰酸钾的反应
【实验4】与碘水的反应
【实验5】与硫化钠溶液的反应
……
环节四:课堂小结
以NaHSO3为核心,从物质类别角度得出它属于多元弱酸的酸式盐,既可以电离又可以水解,进而得出它既可以与酸反应,也可以与碱反应,还可以与某些盐反应;从化合价角度分析,它既可以做氧化剂也可以做还原剂,进而引出可以与氧化剂和还原剂的反应。
3.教学效果评价
本节课在素材的选择上能够充分研究考试纲要,深入把握学生的学情,了解学生的已知点、障碍点和发展点,从硫元素的“类价二维图”出发,以NaHSO3这种相对陌生的物质作为载体,引导学生预测性质,设计实验来验证性质,最终将物质分类、氧化还原、离子反应、电离平衡、水解平衡、离子浓度大小比较以及离子检验等相关知识整合起来,帮助学生从多个角度去认识NaHSO3的性质,从而引导学生突破思维界限,提升学生的学科思维能力。教师能够通过小组合作、实验设计等活动,培养学生良好的实验探究能力和交流合作能力,以复习元素化合物来带动化学实验的复习,以化学实验的复习来整合元素化合物的复习,相互融合,相互促进。
