铁氰化钾分光光度法测定头孢氨苄
2018-03-18吴珊
吴 珊
(新乡学院 化学化工学院,河南 新乡 453003)
头孢氨苄(cefalexin,CEX)是一种β-内酰胺类抗生素[1],具有抗菌谱广、无交叉耐药性、低残留、毒副作用小等特点,广泛用于临床医学、兽医界[2]。因此,对头孢氨苄的测定研究具有重要的意义。目前,已报道的头孢氨苄的测定方法有:微生物检测法[3]、高效液相色谱法[4]、光化学荧光分析法[5]、旋光法[6]等。本文以铁氰化钾为探针利用分光光度法测定头孢氨苄,并通过正交实验优化测定条件。
1 实验部分
1.1 实验方法
分别移取1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]和3.00mL、1.5×10-2mol/L的FeCl3及3.00mL、1.096g/L的头孢氨苄于50mL比色管中,用新煮沸冷却的蒸馏水稀释至刻度,摇匀于50℃下反应40min,以试剂空白为参比,于700nm处测定吸光度A。
1.2 吸收光谱
通过测定吸收光谱可以得出,Fe(III)在420nm时有较大吸收,而在700nm处无明显吸收;普鲁士蓝的最大吸收波长为700nm;空白试剂在700nm处有比较小的吸收,而头孢氨苄在500~800nm范围内没有吸收。为了消除其他试剂对吸光度的干扰,本实验以试剂空白为参比,测定700nm处生成物普鲁士蓝的吸光度而确定头孢氨苄的含量。
2 结果与讨论
2.1 不同条件对吸光度的影响
2.1.1 三氯化铁的量对吸光度的影响
固定其它条件不变:反应温度:20℃;反应时间:30min;总体积:25mL。向七组比色管中均加入3.00mL、1.096g/L的头孢氨苄,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]。
分别向七组比色管中加入不同量的1.5×10-2mol/L的FeCl3,用蒸馏水定容至25mL。在20°C下反应40min,测得相应的吸光度。通过检测得出,吸光度随着FeCl3用量的增加先增大而后减小。头孢氨苄溶液和K3[Fe(CN)6]溶液中加入1.00mL的FeCl3(1.5×10-2mol/L)溶液时,吸光度达到最大为0.130。
2.1.2 铁氰化钾的量对吸光度的影响
固定其它条件不变:头孢氨苄(1.096g/L) 3.00mL;FeCl3(0.015mol/L) 1.00mL;温度:20℃;反应时间:30 min;总体积:25mL,向九组比色管中均加入等量的头孢氨苄, FeCl3溶液,再分别向九组比色管分别加入不同量的K3[Fe(CN)6],用蒸馏水定容至25mL。结果表明,相应的吸光度随着K3[Fe(CN)6]的用量的增加先增大后减小。
2.1.3 温度对吸光度的影响
固定其它条件不变,向八组比色管中均加入3.00mL、1.096mol/L的头孢氨苄,1.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]。将八组比色管分别置于20~90℃的水浴锅中40min,结果表明,吸光度随着温度的增大而增大。
2.1.4 时间对吸光度的影响
固定其它条件不变,向九组比色管中均加入3.00mL、1.096g/L的头孢氨苄,1.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],用蒸馏水定容至25mL。检测后发现在20℃下,随着时间的推移,吸光度逐渐增大。
2.2 正交实验
根据以上实验结果,选择三氯化铁的量、铁氰化钾的量、反应时间、温度这四个因素为研究对象进行正交实验。

表1 因素水平
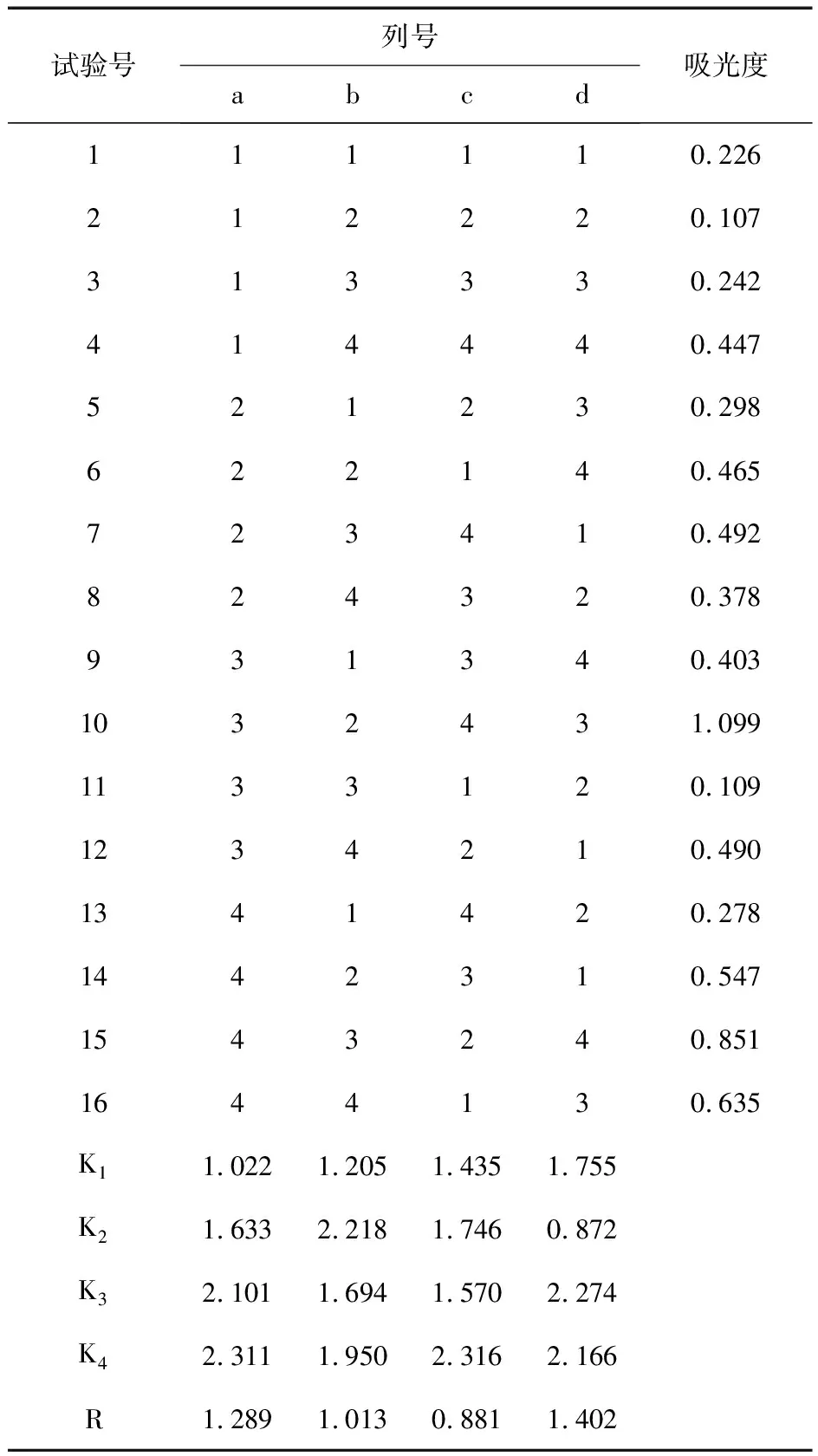
表2 正交实验数据
极差的大小顺序为:Rd>Ra>Rb>Rc,最优方案为:A4B2C4D3。 从表中可以看出影响因素最大的是温度,取加和最大的水平作为最佳条件。得出的最优方案:3.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],反应时间40min、温度为50℃。在最优方案下,利用分光光度法对头孢氨苄进行测定。
2.3 标准曲线
配制一系列头孢氨苄的标准溶液,以吸光度A与相应的c进行线性回归。头孢氨苄在80~160μg/mL范围内与A呈现良好线性关系。线性回归方程为A=0.03281+0.00749c(μg/mL),线性相关系数R=0.9982。

图1 头孢氨苄溶液的标准曲线
2.4 精密度检测
平行测定12份试液,其吸光度A分别为0.708、0.708、0.710、0.710、0.711、0.710、0.710、0.710、0.711、0.710、0.709、0.710,由测得的A值得到其相对标准偏差为:δ = 9.57×10-4。
2.5 检出限的测定
平行测定12份试剂空白试液:在比色管加入3.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],用蒸馏水定容至25mL,测得A值分别为:0.643、0.643、0.642、0.642、0.642、0.643、0.643、0.642、0.642、0.642、0.642、0.641,标准偏差σ=5.95×10-4,计算检出限为0.2384μg/mL。
2.6 样品的制备与分析
2.6.1 头孢氨苄样品的分析
分别移取2.28 mL、2.74 mL、3.65 mL的头孢氨苄溶液(1.096g/L)于3支25mL比色管中,依次向每支比色管加入3.00 mL FeCl3溶液、1.00 mL K3[Fe(CN)6]溶液,用蒸馏水定容后在50°C恒温水浴中加热40 min,然后对同一浓度的样品平行测定3次,进行加标回收实验(参比为不含药品的空白试剂),如表3。
2.6.2 牛奶样品的制备及牛奶中头孢氨苄的测定
分别移取1.00mL新鲜纯牛奶至4个小烧杯中,再移取1.84mL、1.096g/L的头孢氨苄溶液至1、2、3号烧杯,移取1.00mL、pH值=4.6的HAc-NaAc缓冲溶液至4个小烧杯,混合均匀后静置10min。
对混合溶液进行抽滤,将抽滤后的清液倒入25mL比色管中,再用缓冲液冲洗抽滤瓶,将冲洗液也倒入比色管中,分别移取0.46mL、0.86 mL、1.76mL的头孢氨苄溶液(1.096g/L)于1、2、3号管中,再依次加入3.00mLFeCl3、1.00mLK3[Fe(CN)6],用蒸馏水定容后在50°C恒温水浴中加热40min,以4号比色管为参比,对同一浓度的样品平行测定3次,进行加标回收实验,测定结果如表4。

表3 样品及回收率的测定

表4 牛奶中样品及回收率的测定
本文采用分光光度实验对头孢氨苄进行分析,在铁氰化钾存在条件下,头孢氨苄可将三氯化铁中的Fe(III)还原为Fe(II),生成的Fe(II)与铁氰化钾反应生成可溶性的普鲁士蓝。实验结果表明此法可直接用于片剂头孢氨苄含量的测定;同时,也可应用于对牛奶中头孢氨苄残留的检测,该方法的建立对实现牛奶质量的监测具有重要现实意义。
