苹果渣氧化纤维素的制备及表征
2018-03-16李列琴陈雪峰刘宁孙玉姣屈兵练
李列琴,陈雪峰*,刘宁,孙玉姣,屈兵练
1(陕西科技大学 食品与生物工程学院,陕西 西安,710021)2(陕西海升集团,陕西 西安,710100)
陕西省作为我国重要的苹果种植及加工基地,每年因浓缩苹果汁加工产生约60 万t苹果渣,其富含膳食纤维、维生素、矿物质等,具有较高的营养价值[1]及良好的功能特性[2-3]。现阶段苹果渣主要用作动物饲料,利用价值低,有必要对其开展综合利用技术研究实现梯次高值利用。
纤维素作为一种不溶性膳食纤维,占苹果渣含量的35%左右[4],它在调节人体胃肠道消化、改善食品品质等方面具有重要的作用,极具开发前景。研究发现,对纤维素进行适当改性可改善其物理性质及结构,如氧化可增加纤维素的持水性、分散性等[5],也可使纤维素葡萄糖单元产生新的活性位点,成为制备各种新品的中间体。目前纤维素的氧化方法有多种,如次氯酸盐氧化体系法、高碘酸钠氧化体系法、卤酸盐氧化体系法等[6]。本研究选用高碘酸钠氧化体系法对苹果渣纤维素进行氧化,以醛基含量及样品保留率为评价标准,通过单因素、正交试验对其工艺进行优化,利用扫描电镜、红外光谱、X-射线衍射及持水力测定进行表征,以期探索适合工业化制备苹果渣纤维素衍生物的新途径,为其更广泛应用提供技术支撑,也为提高苹果渣综合利用价值提供新思路。
1 材料与方法
1.1 材料与试剂
苹果渣(已去除水溶性多糖),安徽省宿州市砀山县安徽砀山海升果业有限责任公司;固体NaOH、浓HCl、无水乙醇、丙酮、冰乙酸、高碘酸钠、乙二醇、百里香酚兰、盐酸羟胺、甲醇(分析纯),天津市天力化学试剂有限公司;亚氯酸钠(分析纯),郑州派尼化学试剂厂;KBr(光谱纯),天津市科密欧化学试剂有限公司。
1.2 仪器与设备
HH-4恒温水浴锅,金坛市宏华仪器厂;101-1AB型电热鼓风干燥箱,天津市泰斯特仪器有限公司;电子天平,赛多利斯科学仪器(北京)有限公司;SHB-Ⅲ循环水多用真空泵,西安太康生物科技有限公司;H-1850R湘仪台式高速冷冻离心机,长沙湘仪离心机仪器有限公司;THZ-C-1全温振荡器,太仓市实验设备厂;FEI Q45+EDAX Octane Prime环境扫描电子显微镜+能谱仪,美国FEI和EDAX;VECTOR-22傅立叶红外光谱仪、D8 Advance型X-射线衍射仪,德国布鲁克Bruker公司。
1.3 试验方法
1.3.1 苹果渣不溶性膳食纤维制备
称取一定量去除水溶性多糖的苹果渣(过80目筛),按料液比1∶20(g∶mL)加入4% NaOH溶液,于45 ℃保温1.5 h,水洗至中性,弃去滤液;向滤渣中加入相同比例的2%盐酸溶液,60 ℃保温1.5 h,水洗至中性;滤渣用无水乙醇和丙酮各洗涤2次,水洗至中性,滤渣于60 ℃烘干即得苹果渣不溶性膳食纤维。
1.3.2 苹果渣纤维素提取
称取一定量苹果渣不溶性膳食纤维(过20目筛),以料液比1∶20(g∶mL)加入14% NaOH溶液,于35 ℃、160 r/min条件下反应20 h,水洗至中性,弃去滤液,滤渣于60 ℃烘干即得苹果渣纤维素。重复上述步骤,对纤维素进行纯化。利用亚氯酸钠与冰乙酸对其进行脱色[7-8]。
1.3.3 苹果渣氧化纤维素制备单因素试验
向苹果渣纤维素中加入一定浓度高碘酸钠溶液,于一定温度、160 r/min条件下避光反应特定时间,滤渣用0.2 mol/L乙二醇溶液浸泡0.5 h,水洗,60 ℃烘干即得苹果渣氧化纤维素。称重,计算样品保留率;采用盐酸羟胺法[9]测定醛基含量。
样品保留率计算公式(1):

(1)
式中:m0,苹果渣纤维素质量,g;m1,苹果渣氧化纤维素质量,g。
(1)料液比对氧化纤维素醛基含量及保留率影响:向苹果渣纤维素中分别加入料液比为1∶10、1∶15、1∶20、1∶25、1∶30、1∶35(g∶mL)的0.5 mol/L高碘酸钠溶液,设定反应时间4 h,温度40 ℃,测定干燥样品的醛基含量及保留率。
(2)高碘酸钠浓度对氧化纤维素醛基含量及保留率影响:向苹果渣纤维素中分别加入浓度为0.2、0.3、0.4、0.5、0.6 mol/L的高碘酸钠溶液,设定料液比为1∶20(g∶mL),反应时间4 h,温度40 ℃,测定干燥样品的醛基含量及保留率。
(3)时间对氧化纤维素醛基含量及保留率影响:向苹果渣纤维素中加入浓度为0.6 mol/L的高碘酸钠溶液,料液比1∶20(g∶mL),温度40 ℃,设定反应时间分别为2、4、6、8、10 h,测定干燥样品的醛基含量及保留率。
(4)温度对氧化纤维素醛基含量及保留率影响:控制试验的反应温度分别为:30、35、40、45、50 ℃,高碘酸钠浓度0.6 mol/L,料液比1∶20(g∶mL),反应时间4 h,测定干燥样品的醛基含量及保留率。
1.3.4 苹果渣氧化纤维素制备正交试验
在单因素试验基础上,选取料液比、高碘酸钠浓度、时间、温度为因素,醛基含量及样品保留率为评价标准(其中,醛基含量为首要评价标准),设计4因素3水平正交试验,试验因素水平表如表1所示。

表1 氧化纤维素正交试验因素水平表Table 1 Orthogonal test factors and levels of oxidizedcellulose
1.3.5 扫描电镜(SEM)分析
分别将纤维素、低氧化程度纤维素(醛基含量为2.58 mmol/g,下同)、高氧化程度纤维素(醛基含量为6.02 mmol/g,下同),固定在载物盘中,喷金处理。观察样品颗粒的形貌,拍摄相应倍数的电镜照片,进行分析。
1.3.6 傅立叶红外光谱(FTIR)分析
称取氧化前后苹果渣纤维素3 mg,与300 mg干燥的KBr粉末均匀混合进行研磨压片,于4 000~400 cm-1波长下进行上机测试,分析扫描光谱图。
1.3.7 X-射线衍射(XRD)分析
称取氧化前后苹果渣纤维素1 g,于载物台上进行扫描,设置参数为:管电压40 kV,管电流40 mA,铜靶,旋转2θ角:5~60°,步长0.02°[10]。
1.3.8 持水力(WHC)测定
称取氧化前后苹果渣纤维素0.5 g,放入称重后的离心管中,加蒸馏水75 mL,于25 ℃下保温24 h,4 000 r/min下离心0.5 h,倾去上清液,滤纸吸干水分,称重,计算持水力(WHC)[公式(2)]:

(2)
式中:m0,样品干重,g;m1,样品湿重,g。
1.3.9 数据分析
所有数据均采用SPSS 16.0(SPSS,Chicago,IL,USA)统计分析软件进行分析。
2 结果与分析
2.1 高碘酸钠氧化条件对氧化纤维素醛基含量及样品保留率的影响
2.1.1 料液比对氧化纤维素醛基含量及保留率影响
由图1可知,随料液比增加,氧化纤维素醛基含量呈先增后降趋势。在料液比分别为1∶10、1∶15、1∶20时醛基含量差异显著(p<0.05)。当料液比为1∶20时,醛基含量出现最大值,为4.65 mmol/g。料液比大于1∶30时,醛基含量显著下降。样品保留率始终持续显著下降(p<0.05)。其原因可能是开始阶段随着料液比的增加,纤维素氧化程度加深,醛基含量增加;料液比大于1∶20时,纤维素更多地接触到氧化剂,氧化后纤维素单元结构上的醛基被再度氧化,生成醇、酮、羧基等复杂体系物质[11],导致醛基含量减少。有研究表明,随着深度氧化的进行,纤维素葡萄糖单元上对应位置的碳碳键断裂,结晶度降低[12],因此其溶解性增加,样品保留率减少。在该试验范围内样品保留率均大于80%,综合考虑,确定反应料液比为1∶20。

图1 料液比对氧化纤维素醛基含量及保留率影响Fig.1 Effect of the solid-liquid ratio on the aldehyde group content and retention rate of oxidized cellulose
2.1.2 高碘酸钠浓度对氧化纤维素醛基含量及保留率影响
由图2可知,氧化纤维素醛基含量随高碘酸钠浓度的增加而增加,相反地,样品保留率随高碘酸钠浓度增加持续显著降低。高碘酸钠浓度小于0.5 mol/L时,醛基含量显著增加。浓度大于0.5 mol/L时,醛基含量增加明显趋于缓慢,说明此时醛基含量已接近最大值。这可能是由于样品保留率降低,部分纤维素还未被氧化就溶解,造成了醛基含量增加的局限性。考虑到高碘酸钠的溶解度,本试验最终选择的高碘酸钠浓度为0.6 mol/L。
2.1.3 时间对氧化纤维素醛基含量及保留率影响

图2 高碘酸钠浓度对氧化纤维素醛基含量及保留率影响Fig.2 Effect of the concentration of sodium periodate on the aldehyde group content and retention rate of oxidized cellulose
由图3可知,氧化纤维素醛基含量随反应时间的增加呈先增后降趋势,样品保留率持续显著降低。前4 h内,醛基含量显著增加。超过4 h后,氧化效果达到最大,氧化剂开始与生成的醛基反应使其进一步氧化从而降低了该氧化的效果,也说明该试验过程反应速率较高。综合考虑,确定反应时间为4 h。

图3 时间对氧化纤维素醛基含量及保留率影响Fig.3 Effect of the time on the aldehyde group content and retention rate of oxidized cellulose
2.1.4 温度对氧化纤维素醛基含量及保留率影响
由图4可知,氧化纤维素醛基含量随温度增加不断增加,40 ℃时醛基含量达到最大值4.75 mmol/g。温度大于40 ℃时,醛基含量显著下降。与此同时,样品保留率也显著降低,可能是因为该反应对温度较为敏感,温度上升至一定程度时,氧化剂被高温分解,氧化作用急剧降低,整体反应减缓。较高温度时样品保留率较大幅度降低,可能是因为此时反应体系比较复杂,温度的增加加大了样品在该条件下溶液中的溶解度。综合考虑,确定反应温度为40 ℃。
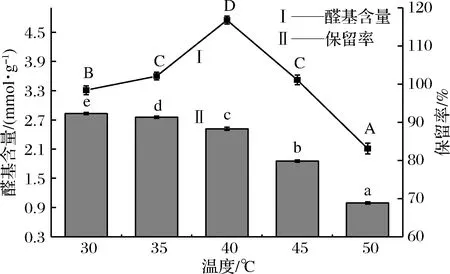
图4 温度对氧化纤维素醛基含量及保留率的影响Fig.4 Effect of the temperature on the aldehyde group content and retention rate of oxidized cellulose
2.1.5 正交试验优化结果分析
根据单因素试验结果,设计L9(34)正交试验如表2所示。此过程旨在优化氧化工艺,确保样品保留率的同时达到最佳氧化效果。由表2可知,影响苹果渣纤维素氧化程度的因素主次顺序为:高碘酸钠浓度>料液比>时间>温度;影响氧化纤维素样品保留率的因素主次顺序为:温度>高碘酸钠浓度>时间>料液比。制备氧化纤维素的最优组合为A3B3C2D3,即料液比1∶25(g∶mL),高碘酸钠浓度0.6 mol/L,时间4 h,温度45 ℃。对主要评价指标醛基含量进行了方差分析,结果表明:高碘酸钠浓度的F比为10.11,大于F临界值,因此,该因素显著。由此得出,适宜浓度的高碘酸钠可使纤维素葡萄糖单元上对应位置的碳碳键断裂,充分释放羟基,达到高度氧化的效果。对正交试验的最优组合进行重复试验,结果为:醛基含量6.02 mmol/g,样品保留率81.33%,此时醛基含量较优化之前升高。因此,该正交试验较为成功,也进一步说明正交试验具有一定的预见性。
本试验探讨样品保留率的目的是使纤维素氧化程度最高的同时,保证样品得率,以便应用于实际生产中。由表2及最优组合结果可知,在该试验范围内,样品保留率均大于80%,说明该条件下氧化纤维素样品保留效果良好。

表2 氧化纤维素正交试验结果Table 2 Orthogonal test results of oxidized cellulose
2.2 氧化前后纤维素SEM分析
图5为1 500倍下氧化前后苹果渣纤维素扫描电镜图。氧化前后整体纤维素条状结构并未发生明显改变。观察其细微变化可看出,图Ⅱ和Ⅲ中氧化纤维素表面出现一些较小的颗粒状、片状物质,这可能是因为氧化试剂冲击纤维素表面,造成了其部分表皮脱落。图Ⅲ高氧化程度纤维素出现条状断裂现象,可能是由于纤维素氧化过程中打断了其葡萄糖单元结构上的碳碳键,内部结构改变引起了外部形态的变化。综上,高碘酸钠氧化对于纤维素外部整体结构的破坏较小,这在一定程度上保证了物质本身的完整度,对于后续深入研究具有很大帮助。

Ⅰ-纤维素;Ⅱ-低氧化程度纤维素;Ⅲ-高氧化程度纤维素图5 氧化前后纤维素扫描电镜图(×1 500)Fig.5 Scanning electron microscopes of cellulose before and after oxidation(×1 500)
2.3 氧化前后纤维素FTIR分析


图6 氧化前后纤维素红外谱图Fig.6 Infrared spectra of cellulose before and after oxidation

2.4 氧化前后纤维素XRD分析
如图7所示为氧化前后苹果渣纤维素X-射线衍射谱图。氧化前后纤维素衍射曲线差别明显。氧化前纤维素分别在12°及20°附近有纤维素Ⅱ的特征衍射峰[16],氧化后纤维素在12°特征峰消失。说明氧化后纤维素晶体类型发生了改变,这可能是由于氧化过程中纤维素葡萄糖单元发生了主键断裂及醛基转化造成的。氧化前后纤维素的衍射峰峰型起伏较大,不平滑,可能是样品处理过程中的酸碱腐蚀引起的。对比氧化前后衍射峰强度可知,氧化后纤维素衍射峰峰位明显降低,且氧化程度越高,峰位越低。说明该氧化过程具有降低纤维素结晶度的作用,氧化程度越高,作用越明显,这对于纤维素的物性改善及其更广泛应用具有很大帮助。
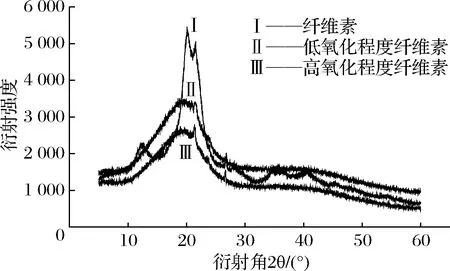
图7 氧化前后纤维素X-射线衍射谱图Fig.7 X-ray diffraction spectra of cellulose before and after oxidation
2.5 氧化前后纤维素WHC分析
表3为氧化前后苹果渣纤维素持水力测定结果。氧化后纤维素持水力显著增加(p<0.05),且氧化程度越高,持水力越大。具体地,两种不同氧化程度纤维素持水力分别增加了59.88%和77.62%。可能的原因有两种,一是氧化打开了纤维素环状结构,使其分散性增加,增大了与水的接触面积;二是结构方面,氧化过程中纤维素葡萄糖单元上的羟基逐步被醛基取代,醛基相对羟基亲水性更大,因此持水力增加。氧化纤维素持水力的增加是纤维素物性改善的重要体现,这对于其日后进一步开发作为保鲜剂类产品在食品保鲜领域的广泛应用具有现实意义。

表3 氧化前后纤维素的持水力 单位:g/g
注:同一行不同字母表示差异显著(p<0.05)。
3 讨论
利用高碘酸钠在非均相体系中氧化苹果渣纤维素,在单因素试验基础上设计L9(34)正交试验对氧化工艺进行优化。优化结果为:料液比1∶25(g∶mL),高碘酸钠浓度0.6 mol/L,时间4 h,温度45 ℃;此时氧化纤维素醛基含量最高为6.02 mmol/g,样品保留率81.33%。经扫描电镜及红外光谱表征,该衍生物具有明显的氧化纤维素形态和醛基结构。赵斌等[17]对椰衣纤维进行高碘酸钠氧化,氧化纤维素醛基含量为3.85 mmol/g。杨扬等[18]对阔叶木浆进行高碘酸钠氧化,氧化纤维素醛基含量为1.43 mmol/g。本试验制备的苹果渣氧化纤维素与其他类似研究相比,醛基含量更高,样品保留率也较高,这对其日后工业化生产十分有利。
本试验成功制备了苹果渣氧化纤维素,因其具有较高的持水力,有望进一步开发作为保鲜剂类产品广泛应用于食品行业;还因其具有醛基的活性位点及较低的结晶度,可作为进一步改性纤维素的中间体。这是探索新型苹果渣纤维素衍生物制备的有效途径,氧化后纤维素更深层次的物性及结构探讨今后进将一步研究。
[1] MADRERA R R, BEDRINANA R P, VALLES B S. Enhancement of the nutritional properties of apple pomace by fermentation with autochthonous yeasts[J]. LWT-Food Science and Technology, 2017, 79:27-33.
[2] RANA S, GUPTA S, RANA A, et al. Functional properties, phenolic constituents and antioxidant potential of industrial apple pomace for utilization as active food ingredient[J]. Food Science and Human Wellness, 2015, 4(4):180-187.
[3] LOHANI U C, MUTHUKUMARAPPAN K, MELETHA-RAYIL G H, et al. Application of hydrodynamic cavitation to improve antioxidant activity in sorghum flour and apple pomace[J]. Food and Bioproducts Processing, 2016, 100:335-343.
[4] 谢碧霞, 李安平. 膳食纤维[M]. 北京:科学出版社, 2006:12-16.
[5] 许云辉, 陈宇岳, 林红. 氧化纤维素的研究进展及发展趋势[J]. 苏州大学学报, 2006, 26(2):16-21.
[6] 熊俊军. 纤维素的选择性氧化及阳离子化[D]. 广州:华南理工大学, 2013.
[7] 李丽, 罗仓学, 王白鸥, 等. 苹果渣中纤维素、半纤维素的提取分离[J]. 食品科技, 2008(1):132-136.
[8] MORTADA W I, KENAWY I M M, ABOU E1-REASH Y G, et al. Microwave assisted modification of cellulose by gallic acid and its application for removal of aluminium from real samples[J]. International Journal of Biological Macromolecules, 2017, 101:490-501.
[9] 王琴梅, 廖燕红, 滕伟, 等. 盐酸羟胺-电位滴定法测定氧化海藻酸钠上的醛基浓度[J]. 分析试验室, 2008, 27(S1):83-86.
[10] 党子建, 黄恵华. 改性菠萝皮渣纤维素染料吸附剂的性质研究[J]. 现代食品科技, 2011, 27(7):747-750.
[11] 戴磊. TEMPO氧化法纳米纤维素及其复合膜的制备和性能研究[D]. 无锡:江南大学, 2015.
[12] 刘乐, 张国耀, 范嘉骐. 纤维素结晶变体的x-射线衍射法的定量测定[J]. 纺织科学研究, 1988(2):52-54.
[13] 刘羽, 邵国强, 许炯. 竹纤维与其它天然纤维素纤维的红外光谱分析与比较[J]. 竹子研究汇刊, 2010, 29(3):42-46.
[14] 袁艳丽, 朱春山, 张晓渊. 从糠醛渣中提取纤维素的工艺[J]. 化工进展, 2013, 32(2):466-469.
[15] 王献玲, 方桂珍, 戴晓峰, 等. 二醛基纤维素的制备及其对尿素的吸附性能[J]. 林业科学, 2011, 47(4):141-146.
[16] 杨淑敏, 江泽慧, 任海青, 等. 利用X-射线衍射法测定竹材纤维素结晶度[J]. 东北林业大学学报, 2010, 38(8):75-77.
[17] 赵斌, 黄广民, 王政. 利用高碘酸钠氧化制备椰衣醛基纤维[J]. 天然产物研究与开发, 2016, 28(8):1 244-1 250.
[18] 杨扬, 刘金刚, 苏艳群. 利用高碘酸钠选择性氧化阔叶木浆[J]. 中国造纸, 2015, 34(4):16-21.
