1946例肿瘤患者化疗及相关药品不良反应临床分析
2018-03-13王睿晴张艳华北京大学肿瘤医院暨北京市肿瘤防治研究所药剂科恶性肿瘤发病机制及转化研究教育部重点实验室北京0042北京大学医学部药学院临床药学与药事管理系北京009
王睿晴,张艳华,刘 红(.北京大学肿瘤医院暨北京市肿瘤防治研究所药剂科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京 0042;2.北京大学医学部药学院临床药学与药事管理系,北京 009)
药品不良反应(adverse drug reaction,ADR)是指合格药品在正常用法用量情况下出现的与用药目的无关的有害反应。药品不良反应报告是开展不良反应监测的基础,我国已经建立了以药品生产、经营、使用单位为主体的监测和报告体系,在药品监管领域发挥了积极作用[1]。化疗是当前在对肿瘤患者实施临床治疗时最常见的方法,临床疗效显著。但因化疗无靶向性,在杀灭肿瘤细胞同时也会对正常细胞造成伤害,导致患者出现诸多不良反应和并发症,严重影响治疗效果与患者健康[2]。笔者对北京大学肿瘤医院2011–2016年肿瘤患者临床用药过程中,发生的ADR进行数据统计。重点关注易引起ADR的药品及药品所属类别,ADR多发年龄,不同给药途径引起ADR对比以及ADR种类。旨在重视肿瘤治疗过程中相关药物引起的ADR,定期监测与报告,减少ADR的发生。
1 资料与方法
1.1 资料来源
下载2011–2016年度国家药品不良反应监测系统接收的北京大学肿瘤医院肿瘤患者药品不良反应报告,对资料所含的1946例患者所使用的2835个ADR报告进行统计分析。
1.2 方法
笔者依据《新编药物学》进行药物分类,分别从患者年龄分布、给药途径分布、引起ADR的药品分类、引起ADR的药品排名顺序、ADR累及系统/器官及临床表现等方面进行描述性、回顾性分析。利用Excel进行数据统计与分析。
2 结果
2.1 性别与年龄分布
6年间的数据综合情况分析结果显示,男女比例为1 : 1.02,数量相近。结果显示:51~70岁肿瘤患者发生ADR概率较高,应注重防范。详见表1。

表1 2011–2016年引起ADR患者性别与年龄分布Tab 1 The gender and age distribution of ADR patients from 2011 to 2016
2.2 药品分类及排名
依据《新编药物学》分类将药品分为二十二类,详见表2。6年间,引起ADR药品排名前10位及构成比见表3。
2.3 给药途径分布
肿瘤医院2011–2016年发生ADR患者的给药途径主要集中在静脉滴注2338例次(82.47%),口服给药252例次(8.89%),静脉注射55例次(1.94%),皮下注射48例次(1.69%),肌肉注射42例次(1.47%),动脉给药29例次(1.02%),泵内注射24例次(0.85%)等。
2.4 ADR累及系统/器官损害及主要临床表现
2011–2016年患者发生ADR累及系统/器官损害及主要临床表现详见表4。
3 讨论
3.1 ADR与性别、年龄的关系
6年数据显示,药品引发ADR的患者中男女比例基本持平,无明显特征性分布。51~60岁组占最多比例,其次为61~70岁组。导致中老年人ADR发生率较高水平的原因有多种,其中生理机能退行性变化引起的药动学改变是最主要原因。主要包括[3]:1)中老年人代偿反应机制下降、神经系统功能退化,中枢抑制药物敏感度上升,药物进入机体后易刺激神经系统产生不良反应症状;2)中老年人内分泌功能降低,体内负责药物承载和运输的蛋白酶数量减少,导致药物代谢减慢、吸收率降低,使药物长期在体内堆积;3)中老年人体液量少,机体中不能与血浆蛋白结合的游离型药物量大,导致药物总体活性增强,加大不良反应风险。因此,建议临床在中老年患者治疗过程中采取一定措施,例如:优选副作用较少的药物;尽量用口服或外用代替静脉注射;联合用药时应间隔用药,避免药物间相互作用;用药期间应忌口,同时鼓励患者运动,增强体质,以此代替滋补药物,避免长期使用抗菌药物,降低中老年患者不良反应发生率[4]。
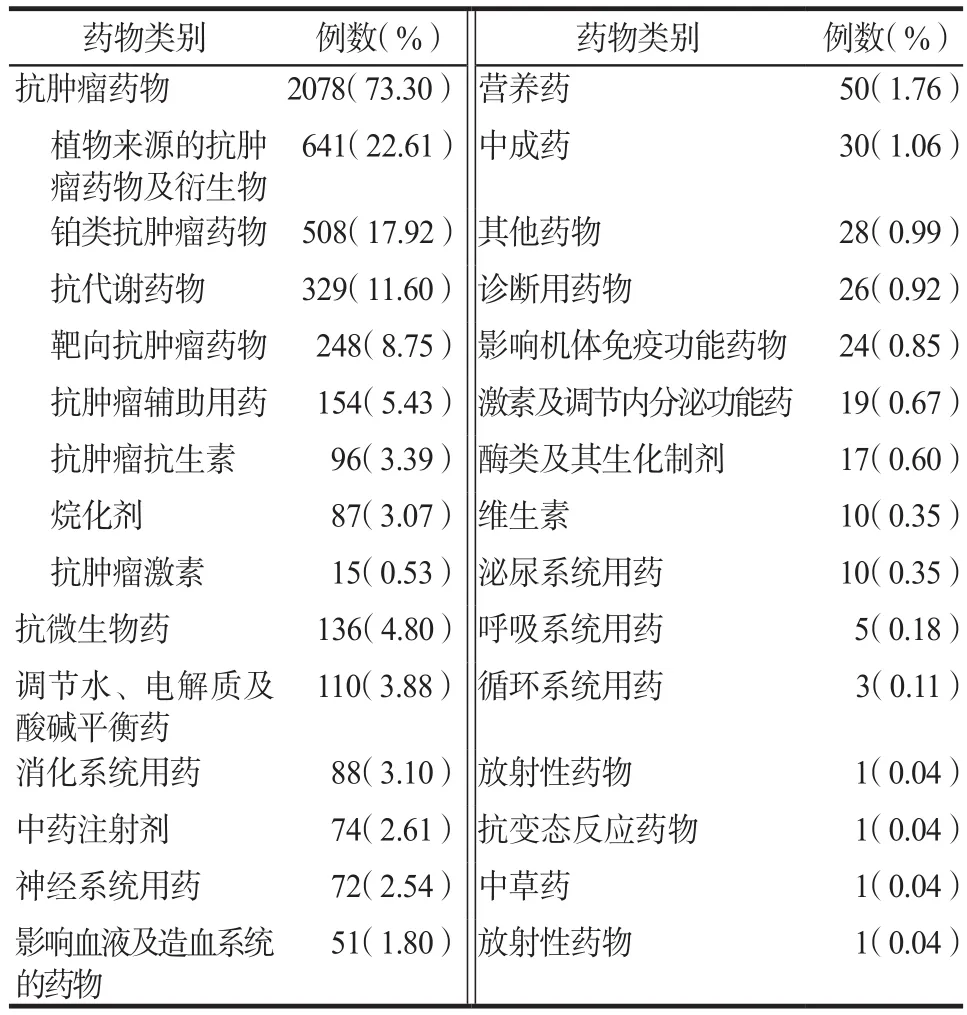
表2 2011–2016年引起ADRs药品分类Tab 2 Classification of drugs causing ADRs from 2011 to 2016
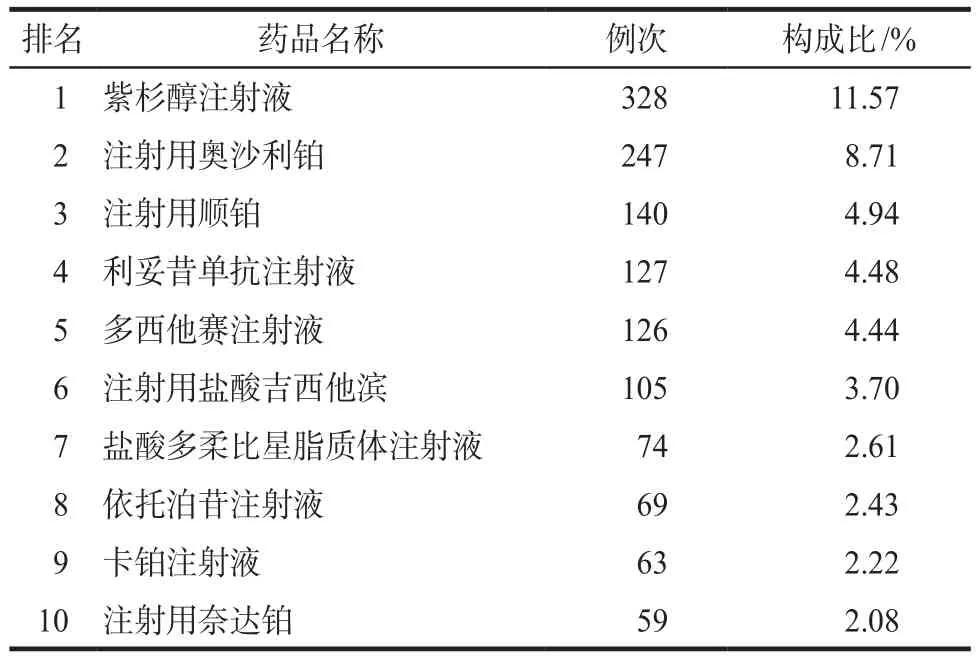
表3 2011–2016年引起ADR排名前10位药品名称Tab 3 Top 10 drugs causing ADR from 2011 to 2016
3.2 ADR与药物种类的关系
由表2可见,我院ADR共涉及二十二类药品,植物来源的抗肿瘤药物及衍生物所致ADR病例数居首位,有2078例(73.30%),其次为铂类抗肿瘤药物。引发ADR病例数最多的药品分别为紫杉醇、奥沙利铂、顺铂。紫杉醇类化合物是已有的最优秀的高效低毒广谱抗癌药之一,是第一种在临床试验中被认可,并通过化疗手段治疗多种肿瘤疾病的紫杉烷类化合物,被称为“晚期癌症的最后一道防线”[5]。紫杉醇属于剂量限制性药物,大部分患者在达到某剂量时,会出现较为严重的骨髓抑制反应[6]。本文数据显示由紫杉醇引发的ADR共计328例次(11.57%)。建议临床缓慢滴注,询问患者过敏史,前提允许时提前使用苯海拉明等抗组胺类和地塞米松等激素类药物,最大程度降低过敏反应[7]。对于紫杉醇引起的骨髓抑制反应,可针对性使用激素类药物及粒细胞集落刺激因子等,控制脊髓毒性的延伸,增加患者的耐受性。对于心血管毒性患者,应及时供氧并静卧。对于神经毒性患者,可给予镇定剂、神经生长因子、维生素B1等缓解症状[8]。对于紫杉醇引起的胃肠道反应,主要原因是其抑制了中枢5-HT的水平,进而引发恶心、呕吐等,可预先准备5-HT3受体拮抗剂[9],以减轻症状。联合用药需注意滴注顺序。

表4 ADR累及的系统/器官、主要临床表现Tab 4 Systems/organs involved in ADR and the clinical manifestations
3.3 ADR与给药途径的关系
1964例ADR报告中,静脉滴注给药引发ADR次数最多,共2338例次(82.47%)。静脉滴注给药后,药物直接进入血液,不经肝脏代谢,且药物的pH、渗透压、微粒等也可能引发ADR[10]。同时抗肿瘤药物的生物利用度较低,且静脉给药对胃肠道造成较大刺激。由静脉滴注引发的ADR,例如:依托泊苷浓度不超过0.25 mg·mL-1,临床使用时经常减少输液量,可能导致患者严重骨髓抑制[11],筛查我院数据时,使用依托泊苷的患者,曾出现过白细胞急剧下降等ADR。紫杉醇注射液浓度超过1.2 mg·mL-1,导致骨髓抑制、外周神经毒性及黏膜炎。盐酸多柔比星浓度超过2 mg·mL-1,主要副作用为骨髓抑制。多西他赛稀释后的最终浓度不超过0.9 mg·mL-1,超浓度可致严重中性粒细胞减少,皮肤反应等[12]。由于肿瘤患者体质问题,ADR发生率更高,引发后果更加严重。因此,临床应严格控制静脉滴速及合理规范药物浓度等来减轻由于静脉滴注导致的ADR。
3.4 ADR累及系统/器官及主要临床表现
我院药物使用主要以抗肿瘤药物为主,抗肿瘤药物进入人体后易引起发热,这可能与抗肿瘤药物激活内源性致热源,使其释放进入血液有关;另外,此类药物引起肿瘤细胞大量坏死脱落也是造成发热等症状的重要原因。发热通常于输注过程中发生,停药后体温迅速恢复正常,继续用药则持续发热,停药后再次用药则再次发热。全身性损害及血液系统损害最为常见,其中以过敏反应(564例次)及骨髓抑制(446例次)为主。药物过敏反应和药物的药理作用、用药剂量的关系较小, 当患者为过敏体质时,更易出现过敏反应,发生过敏反应的症状与药物的给药方式有关[13]。相关研究表明,所有药物都有引发过敏反应的可能性,出现皮疹、发热等症状,较为严重的可能出现神经血管性水肿、哮喘,甚至发生过敏性休克导致患者死亡。因此,加强对药物过敏反应的预防以及进行优质的护理措施极其重要。
综上所述,为最大幅度减少ADR发生,用药前医师要严格遵循循证医学,用药后要严密观察。尤其在输注开始30 min内,发现问题立即处理。ADR监测是一项长期的工作,需要加强对医药护人员的ADR知识培训,加强临床各科室ADR监测员之间的信息交流,切实做好ADR监测工作。
[1] 王成岗,王东芳,许莉莉,等.我国药品不良反应公众报告的需求调研及思考[J].中国药物警戒,2017,14(7):402-406.
[2] 康艳霞,闵婕,张东伟,等.阿瑞匹坦联合托烷司琼预防高致吐化疗药物引起恶心呕吐的临床研究[J].现代肿瘤医学,2016,24(12):1946-1948.
[3] 张凌林.对老年人常见药物不良反应的分析[J].当代医药论丛,2016,14(20):35-36.
[4] 陈希.老年人常见的西药不良反应和对策[J].微量元素与健康研究,2017,34(5):87-88.
[5] 刘先芳,梁敬钰,孙建博.紫杉醇:具有里程碑意义的天然抗癌药物[J].世界科学技术-中医药现代化,2017,19(6):941-949.
[6] 谢艾维.紫杉醇的不良反应及其合理应用[J].中国药物经济学,2015,(1):34-36.
[7] 江彦,傅彦妍,宋洪涛.我院105例多西紫杉醇不良反应报告分析[J].中国药房,2016,27(26):3646-3649.
[8] 周艳.抗肿瘤药紫杉醇的不良反应及临床合理用药分析[J].中国现代药物应用,2017,11(9):138-139.
[9] 钱生勇,冯平,徐艳艳.某院24例紫杉醇脂质体不良反应分析[J].中南药学,2012,10(10):796-797.
[10] 任淑娟,吉金燕,解娟,等.我院304例药品不良反应报告分析[J].西北药学杂志,2014,29(1):93-96.
[11] 李孟芬.静脉输液滴注速度对药物不良反应的影响[J].医学信息,2015,28(42):281.
[12] 赵方允,丁莉,王丽,等.275种常用静脉滴注药物浓度与滴速分析[J].中国医院药学杂志,2017,37(14):1405-1408.
[13] 马婷.增强CT造影剂外渗及过敏反应的预防护理[J].内蒙古中医药,2013,32(19):174-175.
