经肛全直肠系膜切除术与腹腔镜TME治疗直肠癌的临床疗效比较
2018-03-09彭方兴周航宇
陈 进 彭方兴 周航宇 吴 宸
(四川绵阳四〇四医院普通外科 四川绵阳 621000)
直肠癌是消化道常见恶性肿瘤,随着微创技术的进步,腹腔镜全直肠系膜切除术 (total mesorectalexcision,TME)已成为直肠癌患者外科主要术式。近年来随着微创技术的不断革新,经肛门微创术和TME有融合趋势,在此背景下,经肛门全直肠系膜切除术(transanal total mesorectal excision,taTME)逐渐被用于临床[1],有报道显示taTME在直肠癌外科手术治疗中可能具有显著优势[2-3]。但临床对taTME与常规腹腔镜TME的对比研究却较少。为此,本研究纳入60例直肠癌患者,比较两种手术方案的应用价值,现报告如下。

表1 两组手术情况比较
1 资料与方法
1.1 一般资料 纳入2015年1月至2016年5月本院60例直肠癌患者作为研究对象,随机分为两组,每组各30例。观察组中男性13例,女性17例;年龄41~58岁,平均 (50.35±7.81)岁;体重指数(BMI)20~23 kg/m2,平均(21.56±1.07) kg/m2;肿瘤距肛缘距离 4.5~7.5 cm,平均(6.06±1.41) cm;分期:Ⅰ期12例,Ⅱ期 10例,Ⅲ期8例;肿瘤直径 1.5~3.5 cm,平均(2.37±0.86)cm。 对照组中男性16例,女性14 例;年龄 42~60 岁,平均(51.48±8.22)岁;BMI:19~22 kg/m2,平均(20.98±1.36) kg/m2;肿瘤距肛缘距离4~8 cm;(6.15±1.38) cm;分期:Ⅰ期 11 例,Ⅱ期 13例,Ⅲ期 6 例;肿瘤直径 1~2.5 cm,平均(2.46±0.93)cm。两组患者性别、年龄、BMI、肿瘤距肛缘距离、肿瘤分期、直径等基本资料差异均无统计学意义(均P>0.05)。患者均对治疗知情同意。
1.2 纳入标准 (1)所有患者均经病理活检确诊;(2)未发生远处转移。
1.3 排除标准 (1)肝肾功能严重不全者;(2)凝血功能障碍者;(3)因肠梗阻或出血需急诊手术者;(4)因依从性差不能有效配合手术者。
1.4 手术方法
1.4.1 观察组 行全身麻醉,患者取截石位,扩肛,在直视下用盘式拉钩撑开肛门,于肿瘤下缘1 cm和2 cm处分别行荷包缝合,封闭肠腔,保留荷包线残端。置入穿刺器,使CO2压力维持12 mmHg。用超声刀切开直肠后壁,参照尾骨,沿直肠后方和尾骨前方向近端游离,沿直肠系膜后壁锐性分离直肠骶骨韧带和筋膜,进入直肠后间隙。游离前方时以前列腺或阴道、子宫颈为指引,沿Denonvilliers筋膜游离,经右侧间隙进入腹腔,将盆腔小肠推入腹腔,翻转游离直肠使之进入腹腔,继续沿直肠固有筋膜向近端游离,至能看到肠系膜下动脉(IMA)根部时,用超声刀切断IMA血管,清扫周围淋巴结,游离乙状结肠系膜,将游离肠管经肛门拖出,移除标本。在直肠近端置入吻合器钉砧,荷包缝合,远端残端行贯穿全层荷包缝合,留置引流管至骶前,再行肠管端—端吻合。
1.4.2 对照组 行全身麻醉,患者取膀胱截石位,分别在脐上、左右麦氏点及脐两侧置入Trocar,建立人工气腹,维持10~12 mmHg。切开乙状结肠和腹膜的粘连,沿Toldt’s筋膜向头侧切开外侧腹膜,延长至腹膜返折处。另将肠管向左侧牵拉,在骶岬前方肠系膜右侧切开腹膜,向IMA根部延长,在乙状结肠系膜后方向左侧锐性分离,使之与左侧平面汇合,形成系膜后窗口。继续游离乙状结肠系膜至IMA根部,清扫周围淋巴结,并在距腹主动脉1 cm处和胰腺下缘1 cm处切断IMA和肠系膜下静脉根部。用超声刀切开骶骨直肠筋膜,并向左右两侧游离,在前方切开腹膜返折,沿腹会阴筋膜向下锐性游离,至完全游离直肠及其周围系膜。采用一次性使用腹腔镜下切割吻合器于肿瘤远端下2~4 cm处切断肠管,近端15 cm切断肠管,移除标本。近端置入吻合器抵顶,回纳腹腔。缝合切口,建立气腹后,经肛门置入吻合器行端—端吻合。
1.5 观察指标 (1)记录两组手术情况:两组手术时间、术中出血量及输血比例、淋巴结清扫数目及中转开腹情况。(2)记录两组术后恢复情况:两组术后肛门首次排气时间、进流质饮食时间、首次下床活动时间、拔管时间、住院时间及镇痛药物(曲马多)使用情况。(2)比较两组患者住院期间术后并发症发生情况。(4)随访1年,以电话和入院复诊进行随访,每月通过电话随访2次,每3~6月入院复诊1次,记录两组无进展生存率和总生存率。
1.6 统计学方法 选用SPSS 19.0统计学软件对数据进行处理。计量资料以()表示,两组间比较行t检验;计数资料以[n(%)]表示,两组间比较行χ2或Fisher确切概率检验;预后情况采用Kaplan-Meier法进行描述,生存时间采用Log Rank检验比较。以P<0.05为差异有统计学意义。
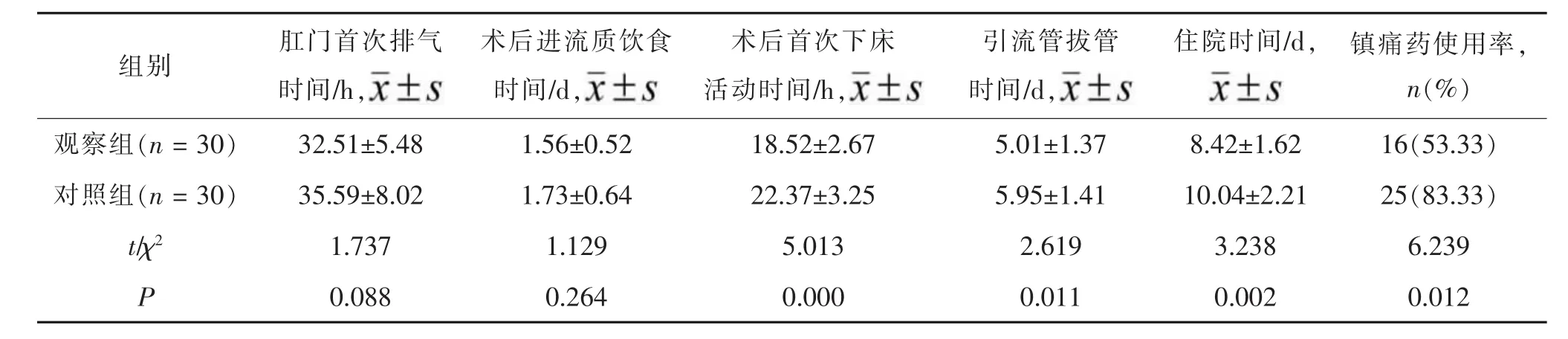
表2 两组术后恢复情况比较
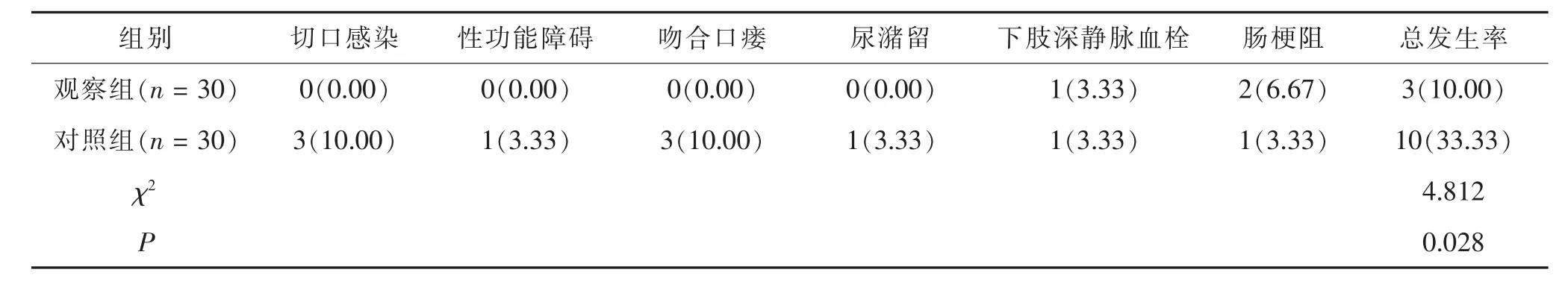
表3 两组术后并发症比较[n(%)]
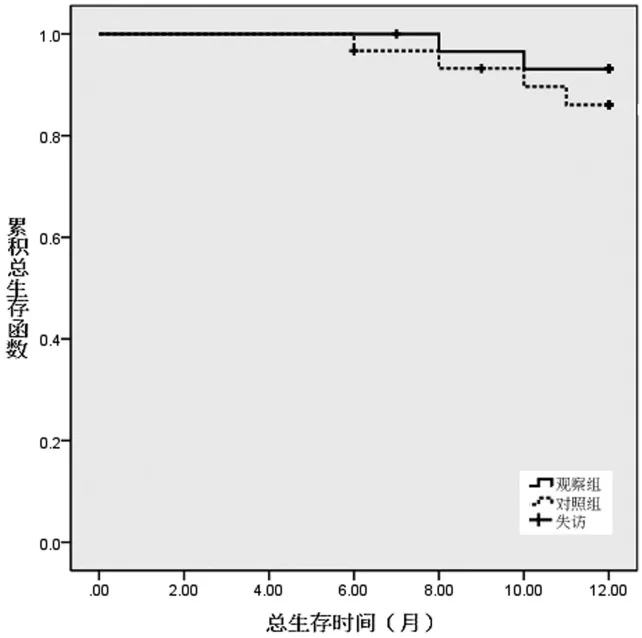
图1 两组术后1年总生存率比较
2 结 果
2.1 两组手术情况比较 两组术中均无中转开腹病例,观察组术中出血量显著低于对照组 (P<0.05),两组手术时间、术中输血比例及淋巴结清扫数目差异均无统计学意义(均P>0.05)。见表1。
2.2 两组术后恢复情况比较 两组术后肛门首次排气时间和进流质饮食时间差异均无统计学意义(均P>0.05),观察组术后首次下床活动时间、引流管拔管时间、住院时间及镇痛药使用率均显著少于对照组(均P<0.05)。见表2。
2.3 两组术后并发症比较 观察组术后并发症总发生率显著低于对照组,差异有统计学意义(P<0.05)。 见表 3。
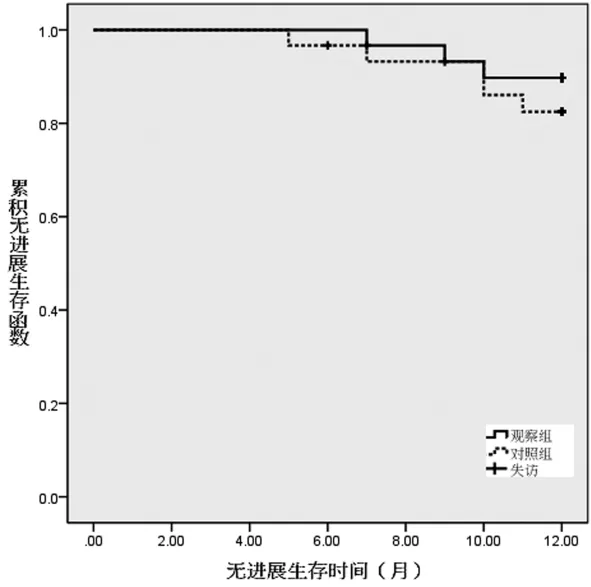
图2 两组术后1年无进展生存率比较
2.4 两组预后比较 随访1年,观察组无进展生存26例、总生存27例、失访1例,对照组无进展生存23例、总生存24例、失访2例。两组总生存率和无进展生存率差异均无统计学意义 (Log rank χ2=0.779、0.608,P=0.377、0.436)。 见图 1 及图 2。
3 讨 论
taTME经肛门处理病变肠段,无需腹部切口,符合经自然孔道内镜外科手术理念。自2013年临床报道首例完全行taTME术的直肠癌患者以来,taTME迅速引起临床重视[4],该术式从肿瘤远端进行,由下而上逆行操作,能获得满意的操作角度,降低了游离远端直肠的难度,同时保证了肿瘤充足的远端切缘,改进了常规腹腔TME术的不足,这也可能是患者术后复发率较低的重要原因。另外,taTME与常规腹腔镜TME相比,逆行路径解决了后者对中下段直肠周围系膜暴露不佳的局限,能清晰显露终末神经丛,减少对盆腔神经的损伤,因而术后具有较低的尿潴留和性功能障碍发生率。杨盈赤等[5]也指出taTME避免了多次击发直线切割器和腹部切口对机体的损伤,能显著降低术后感染和吻合口瘘风险。本研究对比taTME与腹腔镜TME术,发现前者并发症总发生率显著低于对照组,与既往报道相符[6]。观察组术后下床活动时间和住院时间亦显著少于对照组,提示taTME较腹腔镜TME更有利于术后早期康复。赵日升等[7]认为taTME较腹腔镜TME能显著减少手术时间和术中出血量,本研究中观察组无输血病例,仅对照组有2例因肿瘤浸润深度较深、肿瘤位置低、手术视野不清,造成术中操作创伤较大造成出血量增加所致。但本文显示,两种术式手术时间和输血例数并无显著性差异,这可能与本研究样本量小、本院开展taTME时间不长、对该技术欠熟练及经验不足有关。taTME与常规腹腔镜手术不同,要求术者熟悉盆腔解剖结构层次,康亮等[8]研究认为taTME存在学习曲线,需要通过充分前期准备才能进入技术稳定期,充分发挥taTME的优势。
本研究中在进行直肠后方间隙游离时以尾骨为参照,并经肛门暂时置入吸引器,这有利于降低手术难度,顺利进入后方疏松间隙。而在游离前方时则以阴道或子宫颈、前列腺为指引,遵循先后方再两侧的原则。临床也有研究者指出taTME存在的技术难度,认为器具长度和弯曲度的限制使游离肠系膜下血管和脾曲较为困难[9-11]。本研究还发现,观察组术后发生2例肠梗阻,这可能是因taTME不能进行盆底腹膜重建而使小肠进入腹腔所致。因此,虽然taTME较传统腹腔镜具有显著优势,但其仍处于发展探索阶段,有待于进一步完善。有研究者提出单孔腹腔辅助taTME具有较高的可行性和安全性,可作为常规腹腔镜向完全 taTME 过渡的术式[12]。 Dumont等[13]证实单孔腹腔镜辅助taTME对伴骨盆狭窄的男性直肠癌患者具有显著优势,但该研究样本量少,其对患者的远期疗效还有待于扩大样本量的前瞻性研究。另外,本研究对两组患者术后1年预后进行随访,发现taTME组总生存率和无进展生存率差异均无统计学意义,这可能与样本量少和随访时间短有关,因而对于taTME对患者远期生存率的影响有待于进一步研究。
综上所述,taTME较常规腹腔镜TME具有更高的安全性,有助于术后患者早期康复,改善患者预后,但该术式技术水平要求高,需充分的术前准备,其对患者远期预后的影响有待于进一步验证。
[1]ZHANG H,ZHANG Y S,JIN X W,et al.Transanal singleport laparoscopic total mesorectal excision in the treatment of rectal cancer[J].Techniques in Coloproctology,2013,17(1):117-123.
[2]宋明东,周活动,谢伟,等.腹腔镜全直肠系膜切除术治疗低位直肠癌的疗效观察[J]. 结直肠肛门外科,2014,20(2):136-138.
[3]申占龙,叶颖江,SAM A,等.直肠癌经肛门全直肠系膜切除解剖层面及盆腔神经保护[J].中国实用外科杂志,2015,35(8):847-849.
[4]甄亚男,肖瑞雪,石会勇,等.腹腔镜辅助经肛门全直肠系膜切除与传统腹腔镜手术治疗直肠癌疗效比较的Meta分析[J].中华胃肠外科杂志,2016,19(6):702-707.
[5]杨盈赤,金岚,张忠涛.完全经肛门TME腹腔镜直肠癌手术的实践与技巧[J].中华普外科手术学杂志电子版,2016,10(2):97-100.
[6]李会晨,付文政,张锡朋.经肛门全直肠系膜切除术治疗低位直肠癌[J].中华结直肠疾病电子杂志,2014,13(2):61-62.
[7]赵日升,汪挺.经肛与腹腔镜全直肠系膜切除术治疗直肠癌的短期疗效比较[J].中华胃肠外科杂志,2015,10(5):486-486.
[8]康亮,罗双灵,陈文豪,等.经肛门全直肠系膜切除术的学习曲线[J].中华胃肠外科杂志,2016,19(8):917-922.
[9]练磊,汪建平.经肛门全直肠系膜切除术的应用前景[J].中华胃肠外科杂志,2014,12(6):616-619.
[10]张忠涛.完全经肛门全直肠系膜切除—腹腔镜直肠癌手术未来的方向[J].中国实用外科杂志,2015,35(8):844-846.
[11]张明庆,李会晨,张锡朋.直肠癌经肛门全直肠系膜切除术的临床应用[J].中国中西医结合外科杂志,2016,22(5):517-519.
[12]张浩,张云生,金雄伟,等.完全经肛单孔腹腔镜全直肠系膜切除术治疗直肠癌[J].中国内镜杂志,2012,18(4):379-383.
[13]DUMONT F, GO R D, HONOR C, et al.Transanal endoscopic total mesorectal excision combined with singleportlaparoscopy[J].Diseases of the Colon&Rectum,2012,55(9):996.
