输油管道腐蚀垢样中硫酸盐还原菌对Q235钢腐蚀行为的影响
2018-03-02,,,
, ,,
(1. 西南石油大学 油气藏地质及开发工程国家重点实验室,成都 610500; 2. 油气消防四川省重点实验室,成都 610000;3. 塔里木油田,塔里木 841000)
微生物腐蚀(MIC)是威胁管线安全运行的重要因素[1]。从1910年盖恩斯发现微生物腐蚀(MIC)到1934年荷兰学者屈尔等提出硫酸盐还原菌(SRB)参与金属腐蚀中阴极氢去极化的理论之后,人们对微生物腐蚀逐渐重视[2]。研究表明,SRB引起的微生物腐蚀是钢铁加速腐蚀破坏的主要原因之一[3-4]。
管道在输送原油过程中造成的内腐蚀,主要是由原油中的腐蚀性介质引起的。原油本身具有极小的腐蚀性,有研究显示,管线即使在亲油条件下腐蚀速率也是微不足道(≤0.025 um/a)的[5]。然而实践经验表明,输油管线内腐蚀常常出现在油品运输过程中管线容易产生沉积的局部区域。输油管线在正常操作条件下,悬浮在油相中的水滴不可避免,在管线低洼处,油相中重质组分或水滴等可能会沉积下来,而沉积物的存在将会为细菌菌落的形成创造有利条件。原油运输过程中随着沉积物中含水量的不断增加,可能导致输油管道表面由亲油性转变为亲水性,从而有益于MIC发生[6-7]。目前,石油工业中的微生物腐蚀问题已经引起了相关从业人员的高度重视,多数研究都集中在油田注水系统中的SRB腐蚀问题上,而有关输油管线中的SRB对钢材腐蚀行为影响的研究却相对较少。因此,研究输油管道中存在积水与腐蚀管垢低洼处的微生物腐蚀行为,对全面认识和控制输油管道的腐蚀与防护具有重要的现实意义。
据相关调查,目前世界总腐蚀穿孔量的90%都来自管线内壁腐蚀[8],微生物亦是造成管线腐蚀的主要因素之一。我国油田大多已进入高含水期,二次采油注水系统中,SRB的大量繁殖将导致地面及地下设施腐蚀及硫化物污染,造成油田巨大的经济损失。大量试验表明,在油田注水系统中,SRB成群悬浮在水体中或成群附着在管壁上,对金属表面的去极化作用使管道和设备的腐蚀速率增加15倍[9]。PUEKORIUS等指出,一个壁厚约400 μm的钢管在细菌腐蚀下,60 d即穿孔,腐蚀速率为2.4 mm/a,腐蚀深度有时可达10 mm以上[10]。王凤平等[11]认为当输油管线流速较慢时,细菌腐蚀或沉积物下的腐蚀会更加突出。
塔里木某输油管线中原油流量较低,难以将微量游离水带走而聚积在管道低洼处,致使局部内腐蚀较为严重。管输原油本身含微量硫,但其现场所取管线低洼处腐蚀管垢中总硫含量却明显升高,试验前对所取管输原油及腐蚀管垢进行气相色谱(GC)测试,其结果显示原油中主要成分为各种烷烃,未检测到含硫化合物,而管垢中检测到有机酸的存在,有机酸的出现为生物代谢提供了能源及所需的营养物质,在一定程度上促进了细菌的繁殖。本工作通过对输油管道腐蚀垢样进行SRB富集和H2S含量测定,为SRB在管线内的生长代谢导致输油管线腐蚀管垢总硫含量增加提供理论依据,并结合Q235钢在接菌和灭菌(溶液中不接种SRB)条件下的电化学和腐蚀挂片试验及相应腐蚀形貌和产物表征结果,研究了SRB对Q235钢腐蚀行为的影响。
1 试验
采用Var10EL-III元素分析仪对原油及清管物中的C、N、H、S元素含量进行测定。采用Q235钢作为SRB腐蚀研究的目标材料,其化学成分如下:wC0.15%,wMn0.35%,wSi≤0.3%,wS≤0.050%,wP≤0.045%。电化学试验及挂片腐蚀试验用试样的尺寸分别为φ10 mm×10 mm(A试样)和5 mm×3 mm×2 mm(B试样)。将A试样一端与有绝缘外皮的铜导线连接,并用环氧树脂包覆其非工作面,仅露出圆柱形的工作面,用水磨砂纸逐级打磨工作面至5 000号,再用去离子水冲洗、酒精清洗,吹干后备用。B试样用砂纸逐级打磨后,在丙酮溶液中浸泡1 h除去表面油污,接着依次在体积分数分别为25%、50%、75%、100%的无水乙醇中脱水15 min,吹干后备用。
试验所用SRB取自塔里木某输油管道的腐蚀管垢,将密封保存的腐蚀管垢1.5 g注入150 mL已除氧灭菌的培养基(试验溶液)中。每升培养基成分为:0.5 g Na2SO4,1.0 g NH4Cl,1.0 g CaCl2,0.5 g K2HPO4,2.0 g MgSO4·7H2O,5.8 g 60%(质量分数)乳酸钠,1.0 g酵母粉,0.5 g半胱氨酸盐酸盐[12]。采用最大或然数法(MPN)对SRB进行生长周期内菌量变化的计数试验,为增加试验的准确性,细菌计数采用三个平行试验。参考HJ/T 60-2000《水质硫化物的测定 碘量法》标准,取5 mL富集菌液于灭菌的250 mL培养基中采用二级吸收法测试其在一个生长周期内的H2S气体含量变化趋势,用PHS-3酸度计测试生长周期内的pH变化趋势。
电化学测量采用三电极体系,工作电极为A试样,参比电极为饱和甘汞电极(SCE),使用饱和氯化钾盐桥补偿电压降,将参比电极和电解质连接,辅助电极为铂片。电化学试验在CS310电化学工作站上完成,自腐蚀电位采样频率为0.02 Hz,电化学阻抗谱测试采用振幅为10 mV的正弦波交流信号进行扰动,测试的频率为10-2~105Hz。分别测量试样在接菌溶液和灭菌溶液中浸泡不同时间后的电化学阻抗谱。
挂片灭菌后分别放入接有SRB和灭菌的培养基中,密封培养基,26 d后取出挂片,用除锈液(500 mL HCl+500 mL去离子水+3.5 g六次甲基四胺)去除试样表面腐蚀产物后称量。采用JSM-7500F型电子扫描显微镜(SEM)观察腐蚀挂片的表面形貌,并用SEM自带的能谱仪(EDS)对腐蚀产物进行元素表征。
2 结果与讨论
2.1 腐蚀管垢形貌及成分
试验所富集的SRB均取自图1(a)中所示的管线低洼处输油管道的腐蚀管垢,由图1(b)可见,管道内部壁面出现了明显的坑蚀,输油管道管垢SRB富集结果如图1(c)。
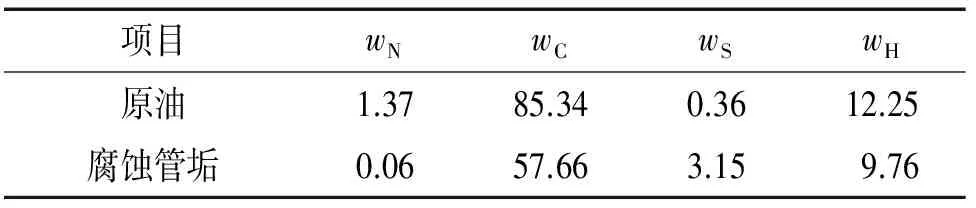
由表1可见:管输原油及腐蚀管垢中的主要元素为C、H、S、N。其中,腐蚀管垢中S的质量分数高达3.15%,约是原油中S含量的9.58倍。为了找出管线中S的来源,对输油管道腐蚀管垢进行了SRB富集,以验证SRB代谢过程产生了硫化物是腐蚀垢样中S含量上升的原因。

(a) 取样位置 (b) 管内壁形貌 (c) SRB富集瓶图1 现场管样形貌Fig. 1 Morphology of the tube sample:(a) sampling position (b) internal corrosion morphology of oil pipeline (c) SRB enrichment bottle
2.2 SRB富集、计数及H2S含量测定
腐蚀管垢中SRB的富集结果如图1(c)所示。14 d后富集瓶变为黑色,证明了管线SY/T 0532-2012中存在着SRB的生长代谢。 SRB为厌氧菌,可采用《油田注入水细菌分析方法——绝迹稀释法》进行细菌分析。同时利用MPN对SRB一个生长周期内含量变化进行计数。由图2可见:SRB生长经历了指数期、稳定期和衰亡期三个阶段,在第6天时细菌数量达到最大,约108 个/mL,此后由于营养物质的消耗殆尽细菌数量迅速下降。

图2 SRB在一个周期内的生长曲线Fig. 2 Growth curve of SRB in one growth cycle
SRB造成管线腐蚀主要是因为在代谢过程中产生了H2S气体,可加速钢的腐蚀。MA等[13]研究认为H2S对阳极溶解和阴极氢的析出都具有强烈的促进作用,SRB代谢过程中产生的H2S可增加管线钢硫化物应力腐蚀开裂(SSCC)的可能性。硫化物应力腐蚀开裂的机理主要包括氢脆理论,该理论认为腐蚀的阴极反应产生氢,氢原子进入金属内部,并扩散到裂缝尖端,使这一区域变脆,在拉伸应力作用下发生脆断。SRB的代谢产物H2S将促进渗氢过程,有学者认为H2S的存在使Fe-H键能降低,氢原子很容易从金属表面转移到深处从而进入金属内部导致氢脆。采用二级吸收法测试一个生长周期内H2S气体含量及pH的变化趋势,结果如图3所示。
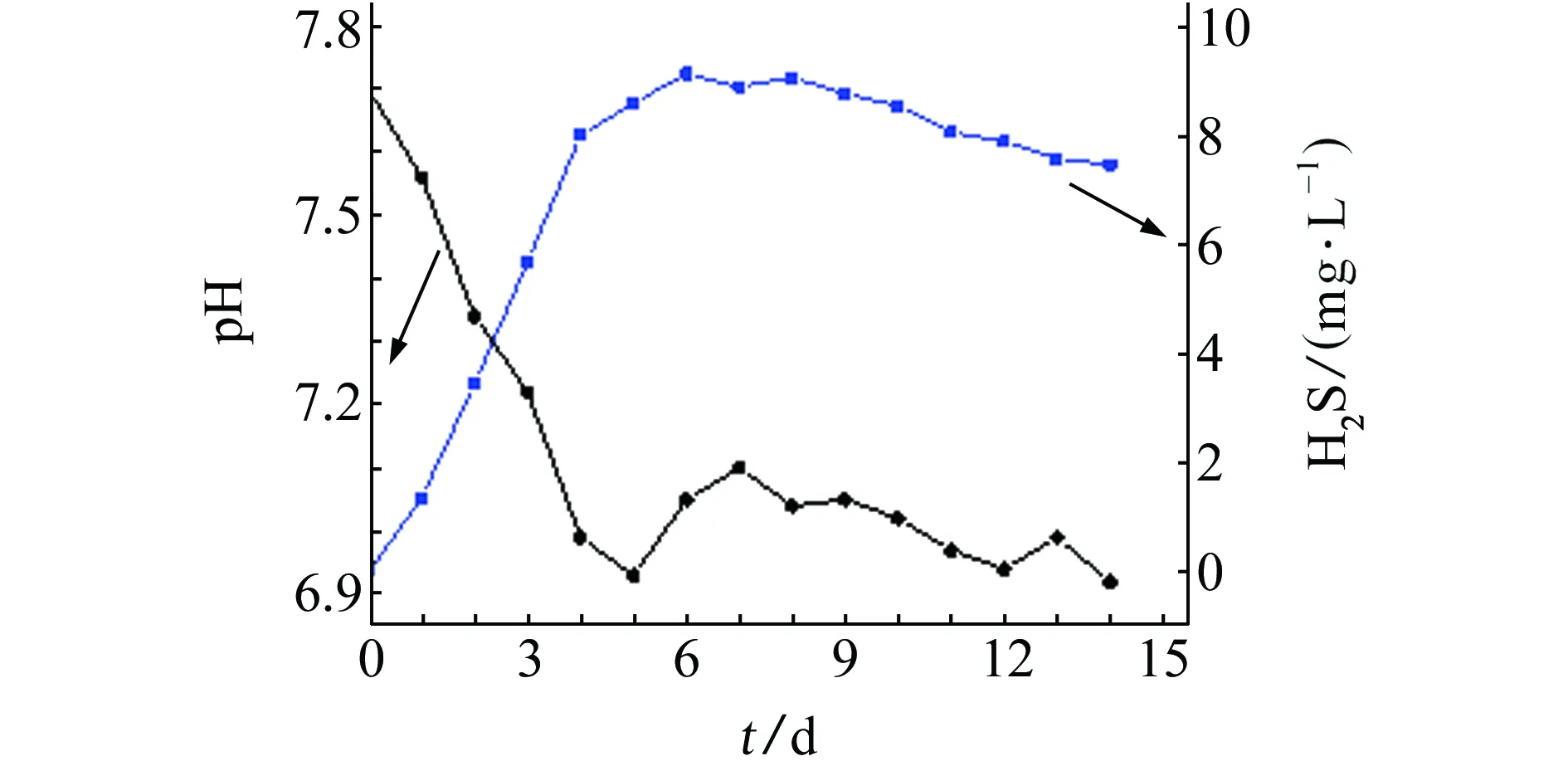
图3 SRB生长周期内H2S及pH变化曲线Fig. 3 Change curves of H2S and pH in the growth cycle of SRB
二级吸收硫化物含量(mg·L-1)计算公式见式(1)。
(1)
式中:V0为空白试验硫代硫酸钠标准溶液用量;Vi为一、二级吸收时硫代硫酸钠标准溶液用量;V为试样体积;16.03为硫离子(1/2 S2-)摩尔质量;c为硫代硫酸钠标准溶液浓度。
试样中硫化物含量c(mg·L-1)计算公式见式(2)。
c=c1+c2
(2)
式中:c1为一级吸收硫化物含量;c2为二级吸收硫化物含量。
SRB代谢是管线中S元素的来源,由图3可见:当细菌处于生长对数期时,溶液中含菌量迅速增加,H2S含量快速上升,pH变小,到第6天时体系中H2S的质量浓度达到最大,为9.12 mg/L。此后细菌处于稳定生长期,pH和H2S含量的变化幅度不大,也基本处于稳定状态。约到第10 天,随着体系中营养物质的消耗,细菌含量快速下降,代谢过程中产生的H2S也随之减少。输油管线内部一般为厌氧环境,管线中SRB在输送过程中,随着原油中的游离水沉降到管道低洼处,在代谢过程中产生H2S等物质,将会加速管线的腐蚀。
2.3 电化学性能
由图4可见:试样在含SRB的溶液中浸泡6 d后,阻抗半径明显小于浸泡1 d时的,即随着浸泡时间的延长,工作电极的腐蚀速率变大[14],这是因为在对数生长期细菌快速繁殖代谢产生H2S气体,其具有较高的导电性,加速试样的腐蚀。当浸泡时间为14 d时,阻抗半径又再次变大,这是因为随着SRB生长进入稳定期,生物膜及腐蚀产物覆盖在金属表面,抑制了金属腐蚀,腐蚀速率下降。根据YU等[15]的研究,对碳钢的SRB腐蚀而言,生物膜和腐蚀产物的贡献是不能分离的,所以在膜或腐蚀产物的影响下,阻抗半径再次变大。在无SRB溶液中,试样浸泡6 d的阻抗半径大于浸泡1 d的,这是因为在工作电极表面形成了一层氧化膜或腐蚀产物膜,阻碍了腐蚀进行。
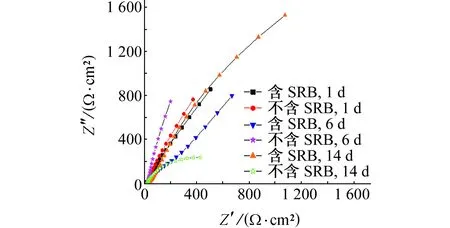
图4 Q235钢试样在不含和含有SRB的试验溶液中浸泡不同时间后的电化学阻抗谱Fig. 4 EIS of Q235 steel in the soulutions without and with SRB for different times
在灭菌条件下,电容性半圆出现在Nyquist图高频区,原因可能是金属氧化物的形成和腐蚀产物的形成,低频区的容抗出现则是因为电化学的动力学因素。而在接菌环境中,高频区出现电容性弧则与细菌吸附、表面氧化膜形成和腐蚀产物沉淀有关[16-17]。美国一些学者在研究厌氧菌生物膜下细菌腐蚀时发现,随着生物膜的积累,钢片表面会发生点蚀[18]。
2.4 挂片试验
表2为试样在含有和不含SRB的试验溶液中经过26 d浸泡试验后的腐蚀速率。腐蚀速率(mm·a-1)计算公式见式(3)。
(3)
式中:mt为试验前挂片质量;m0为试验后挂片质量,g;S为挂片表面积;t为腐蚀时间。

表2 试样在含有和不含SRB的试验溶液中经过26 d浸泡试验后的腐蚀速率Tab. 2 Corrosion rate of samples in the solutions with and without SRB for 26 d mm·a-1
由表2可见:试验溶液中含有SRB,试样的腐蚀速率达到0.101 mm/a,这表明SRB的存在加速了Q235钢的腐蚀。由图5可见:在不含SRB的溶液中,经过26 d浸泡后,试样表面不均匀腐蚀轻微;而在含有SRB的溶液中,经过26 d浸泡后,试样表面腐蚀明显,点蚀坑布满试样整个表面,并已连成片状。这表明,SRB的存在使得试样表面腐蚀形式由轻微不均匀腐蚀向严重局部腐蚀转变。
SRB会加速试样发生局部点蚀,而塔里木某输油管线内部腐蚀情况如图1(b)所示,可知管线内部局部坑蚀现象比较严重。SRB促进钢片局部点蚀发生的原因,是因为在一定溶解氧及pH条件下,SRB的存在会促进阴极和阳极表面去极化作用,促使反应加快,钢管腐蚀加剧。KUHR提出了阴极去极化理论,认为SRB促进了阴极氢去极化,其代谢过程中产生的S2-进一步反应形成FeS等腐蚀产物,沉积于金属管壁并呈锈垢状,而锈垢的存在一方面为SRB提供了厌氧环境,促进了SRB在锈垢下的生长繁殖,同时锈垢本身也可作为金属阴极,从而诱发钢片产生局部腐蚀[19-20]。在适宜的条件下SRB生长代谢,在管道表面尤其是低洼处形成点蚀坑,伴随着蚀孔内阳极的溶解,Fe2+聚集,为维持蚀坑内电中性,Cl-将渗透入蚀坑内,使Fe2+发生水解,酸化蚀坑底部环境,最终导致点蚀坑迅速发展造成钢管穿孔失效。

(a) 含SRB (b) 不含SRB图5 去除腐蚀产物后Q235钢表面形貌Fig. 5 Corrosion morphology of Q235 steel after removing corrosion products(a) in SRB medium (b) in sterile medium
由表3可见:试样表面主要成分为C、O、Fe、P、S和Ca。在不含SRB的溶液中腐蚀产物以铁的氧化物为主,有微量铁的硫化物生成,可能是因为试验溶液中存在含硫物质。而在含SRB的溶液中,硫化物含量明显上升,且试样表面腐蚀产物为黑色,这说明在接菌溶液中,发生了微生物腐蚀,生成了黑色的FeS等腐蚀产物[21],这可能是诱发钢片产生局部腐蚀的主要原因。
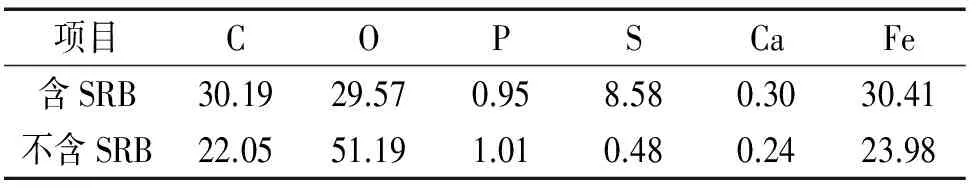
表3 有无SRB条件下试样表面成分分析结果(原子分数)Tab. 3 Surface component analysis of samples in SRB and sterile mediums (atom fraction) %
3 结论
(1) 塔里木某输油管线中存在SRB的生长代谢,微生物代谢过程中产生的硫化氢可能是导致管线中硫元素上升的因素,增加了管线钢硫化物应力腐蚀开裂的可能性。
(2) SRB导致Q235钢局部腐蚀严重,使得钢片表面腐蚀形式由轻微不均匀腐蚀向严重局部腐蚀转变。
(3) SRB代谢产物主要为含硫化合物,这可能是诱发钢片产生局部腐蚀的主要原因。
[1] BEECH I B,GAYLARDE C C. Recent advances in the study of biocorrosion[J]. Rev Microbiol,1999,30(3):177-190.
[2] DAUMAS S,MASSIANI Y J,CROUSIER J. Microbiological battery induced by sulphate-reducing bacteria[J]. Corrosion Science,1988,28:1041-1050.
[3] BORENSTEIN S W. Microbiologically influenced corrosion of austenitic stainless steel weldments[J]. Mater Perform,1991,30(1):52-54.
[4] JAVAHERDASHTI R. A review of some characteristics of MIC caused by sulphate-reducing bacteria:past,present and future[J]. Anti-Corros Method M,1999,46(3):173-180.
[5] FRIESEN W,PETROVIC S,DONINI J C,et al. Relative corrosivities of crude oils from oil transmission pipelines[C]//NACE Northern Area Eastern Conference,[S.l.]:[s.n.],2012.
[6] BEEN J,HOLM M. Evaluating corrosion and inhibition under sludge deposits in large diameter crude oil pipelines[J]. Journal of the Electrochemical Society,2010,162(10):D491-D496.
[7] BRENDAN C. Long term evaluation of microbial induced corrosion contribution to underdeposit sludge corrosivity in a heavy crude oil pipeline[C]//Corrosion,[S.l.]:[s.n.],2013.
[8] 曹然伟. 管线钢腐蚀的材料因素与环境因素关联性研究[D]. 成都:西南石油大学,2011.
[9] SUICKLAND L N. A case history of microbiologically influenced corrosion in the lost hills oilfield[J]. Corrosion,1996(12):297.
[10] 邱学青,肖锦. 硫酸盐还原菌的腐蚀性与杀菌处理的缓蚀效果研究[J]. 油田化学,1991,2(8):149-152.
[11] 王凤平,康万利,敬和民. 腐蚀电化学原理、方法及应用[M]. 北京:化学工业出版社,2008.
[12] LIU F L,ZHANG J,SUN C X,et al. The corrosion of two aluminium sacrificial anode alloys in SRB containing sea mud[J]. Corrosion Science,2014,83:375-381.
[13] MA H Y,CHENG X L,LI G Q,et al. The influence of hydrogensulfide on corrosion of iron under different conditions[J]. Corrosion Science,2000(10):1669-1683.
[14] 曹楚南. 腐蚀电化学原理[M]. 第3版. 北京:化学工业出版社,2008.
[15] YU L,DUANG J Z,DU X Q,et al. Accelerated anaerobic corrosion of electroactive sulfate-reducing bacteria by electrochemical impedance spectroscopy and chronoamperometry[J]. Electrochemistry Communications,2013,26:101-104.
[16] COTE C,ROSAS O,SZTYER M,et al. Corrosion of low carbon steel by microorganisms from the ‘pigging’ operation debris in water injection pipelines[J]. Bioelectrochemistry,2014,97:97-109.
[17] AlABBAS F M,WILLIAMSON C,BHOLA S M,et al. Influence of sulfate reducing bacterial biofilm on corrosion behavior of low-alloy,high-strength steel (API-5L X80)[J]. Int Biodeterior Biodegrad,2013,78:34-42.
[18] 刘宏芳,徐立铭. 硫酸盐还原菌生物膜下钢铁腐蚀研究概况[J]. 油田化学,2000,17(1):94-96.
[19] CHEN S Q,WANG P,ZHANG D. Corrosion behavior of copper under biofilm of sulfate-reducing bacteria[J]. Corrosion Science,2014,87:407-415.
[20] SUL B G H,TILLER A K. Cathodic characteristics of mild steel in suspensions of phate-recteria bacteria[J]. Corrosion Science,1968(8):583-585.
[21] CHEN Y J,TANG C Q,JOHN M,et al. Long-term survival of desulfovibrio vulgaris on carbon steel and associated pitting corrosion[J]. Corrosion Science,2015,90:89-100.
