低酰基结冷胶-乳清蛋白混合凝胶的凝胶特性
2018-03-01李荣马慧婷姚兰英陈青
李荣,马慧婷,姚兰英,陈青
(浙江工商大学食品与生物工程学院,浙江杭州 310018)
蛋白质因为具有卓越的营养价值、生物活性和功能特性,广泛应用于食品、化工和医药等领域,乳清蛋白则因具有良好的加工特性和营养价值而备受食品工业的重视[1~3]。乳清蛋白可以形成凝胶,故而其经常作为增稠剂、微胶囊壁材和食用膜等在食品工业中应用[4~6]。多糖是食品中另一种常见的大分子组分,多糖的存在会影响乳清蛋白凝胶的形成过程,从而影响食品的质构、色泽等特性。因而多糖和乳清蛋白相互作用研究一直是食品领域的研究热点[7~9]。目前关于乳清蛋白和多糖的相互作用研究主要集中在乳清蛋白和果胶、黄原胶、卡拉胶等胶体上,Wagoner等[10]发现乳清蛋白和果胶在pH为5且在85 ℃加热25 min可形成蛋白质-果胶可溶性复合物,复合物的粒径随着乳清蛋白浓度的增加而增大,可溶性复合物可以在乳清蛋白降解温度之上进行热定形,热定形处理可以提高复合物的热稳定性及减小粒径分布。Lam等[11]研究发现,卡拉胶和乳清蛋白混合体系会通过静电作用形成网络结构,混合体系的流变特性取决于卡拉胶的种类,κ-和i-卡拉胶形成的混合凝胶储能模量相差不大,但λ-卡拉胶形成的混合凝胶储能模量很小,卡拉胶的添加会降低混合体系的表面张力。Le等[12]发现β-乳球蛋白/黄原胶复合凝胶的力学性能主要取决于黄原胶,β-乳球蛋白/黄原胶复配比例越小、浓度越低,孔径越小,保水性越好。结冷胶是另一种可用于食品工业中的微生物胞外多糖,其因为具有使用量少、香味释放性好、耐热及复配性好等优点,使用越来越广泛[13~15],迄今为止,关于乳清蛋白和结冷胶的相互作用研究还非常匮乏。有鉴于此,本研究以乳清蛋白和结冷胶作为研究对象,考察离子种类、离子浓度和基体浓度对结冷胶-乳清蛋白混合凝胶凝胶特性的影响,以期为我国的乳品工业和新型食品的开发提供理论指导。
1 材料与方法
1.1 材料与试剂
低酰基结冷胶(Low acyl gellan,LA),美国CP Kelco公司;乳清蛋白(Whey protein concentrated,WP,其中蛋白质含量≥80%,灰分≤6.0%,乳脂≤7.5%),新西兰恒天然公司;叠氮化钠,分析纯,东阳市天宇化工有限公司;KCl、NaCl、CaCl2、MgCl2,分析纯,四川成都科龙化工试剂厂。
1.2 仪器与设备
JZ78-1磁力搅拌器,杭州通用电子仪表厂;电子天平,北京赛多利斯仪器系统有限公司;D-37520 osterode台式高速冷冻离心机,美国Thermo公司;TA-XT 2i物性分析仪,英国SMS公司;CR-400色差计,日本Konica Minolta公司。
1.3 实验方法
1.3.1 低酰基结冷胶-乳清蛋白混合凝胶的制备
乳清蛋白溶液的制备:室温下将一定量的乳清蛋白粉末加入到去离子水中,磁力搅拌5 h直至乳清蛋白全部溶解,添加质量分数为0.02%的叠氮化钠作为抑菌剂。
低酰基结冷胶溶液的制备:将适量结冷胶粉末加入到去离子水中,室温下溶胀24 h,于90 ℃下进行磁力搅拌,直至结冷胶粉末完全溶解形成澄清透明的溶液,并用90 ℃去离子水补偿由于蒸发而损失质量。
低酰基结冷胶-乳清蛋白混合凝胶的制备:将制备好的乳清蛋白溶液与低酰基结冷胶溶液在60 ℃下磁力搅拌5 min进行混合,并加入一定数量的NaCl和CaCl2溶液混合均匀,趁热分装在Φ30 mm×20 mm的模具中,用15 ℃的冷水浴冷却10 min,在4 ℃冰箱中放置24 h凝胶。将凝胶脱模后进行单轴应力压缩、保水性及不透光性测试。在进行相关性能测试前,凝胶试样均在室温下稳定0.5 h。
本研究中所用低酰基结冷胶的最终质量浓度分别为:0.1、0.2、0.3%,乳清蛋白的质量浓度分别为7.5、10.0、12.5、17.5%。钠离子的浓度为30、60、90和120.0 mmol/L,钙离子的浓度为10、20和30 mmol/L。
1.3.2 不透明指数(Opacity Index,OI)测定
将按照方法1.3.1制备的混合凝胶用实验室自制的切割工具切成厚度为2 mm的薄片,用色差计测定混合凝胶的明亮度L。L=0表示黑色,L=100表示白色。样品放在白色背景下测得的明亮度记为Lw;黑色背景下测得的明亮度记为Lb。不透明指数(OI)为:
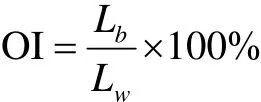
1.3.3 单轴应力压缩
力学性质采用单轴应力压缩法进行测试,选用直径为45 mm的圆柱形夹具,测试模式为compression。具体的测试参数为:测试速度为1 mm/s,压缩应变为80%直至凝胶破碎。根据得到的力-时间关系曲线,计算出相应参数。本研究中用于混合凝胶凝胶特性分析的参数主要有断裂应变、断裂应力和杨氏模量。因为在压缩测试中试样横截面积会发生改变,故而我们把测得的力和变形分别根据公式(1)和(2)进行了校正,将它们分别转化成Hencky应力(σH)和Hencky应变(εH):

式中:F(t),t时刻的应力,N;H(t),t时刻时试样的高度,mm;A0,试样的初始横截面积,mm2;H0,试样的初始高度,mm。
断裂应力和断裂应变分别是σH-εH曲线最高点所对应的应力和应变。杨氏模量则是σH-εH曲线初期呈直线变化部分的斜率(本研究中应变<0.05)。
1.3.4 保水性(WHC)测试
将按照1.3.1方法制备好的混合凝胶脱模,从其中部切出尺寸为20 mm×20 mm×15 mm的样品。在空离心管中加入切好的凝胶,在12000 g下离心15 min,去除水,并记录剩余凝胶的质量,根据下式计算保水性:
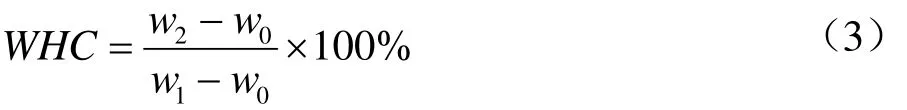
式中:w0是空离心管质量,g;w1是离心前凝胶和离心管的总质量,g;w2则是离心后凝胶和离心管的总质量,g。
1.3.5 数据统计分析
文中所有数据均利用origin 8.0和SPSS 17.0进行数据处理和分析。在实验中为了减少实验误差,提高数据的可信度,不透光指数检测重复三次,保水性和力学性质重复五次。
2 结果与分析
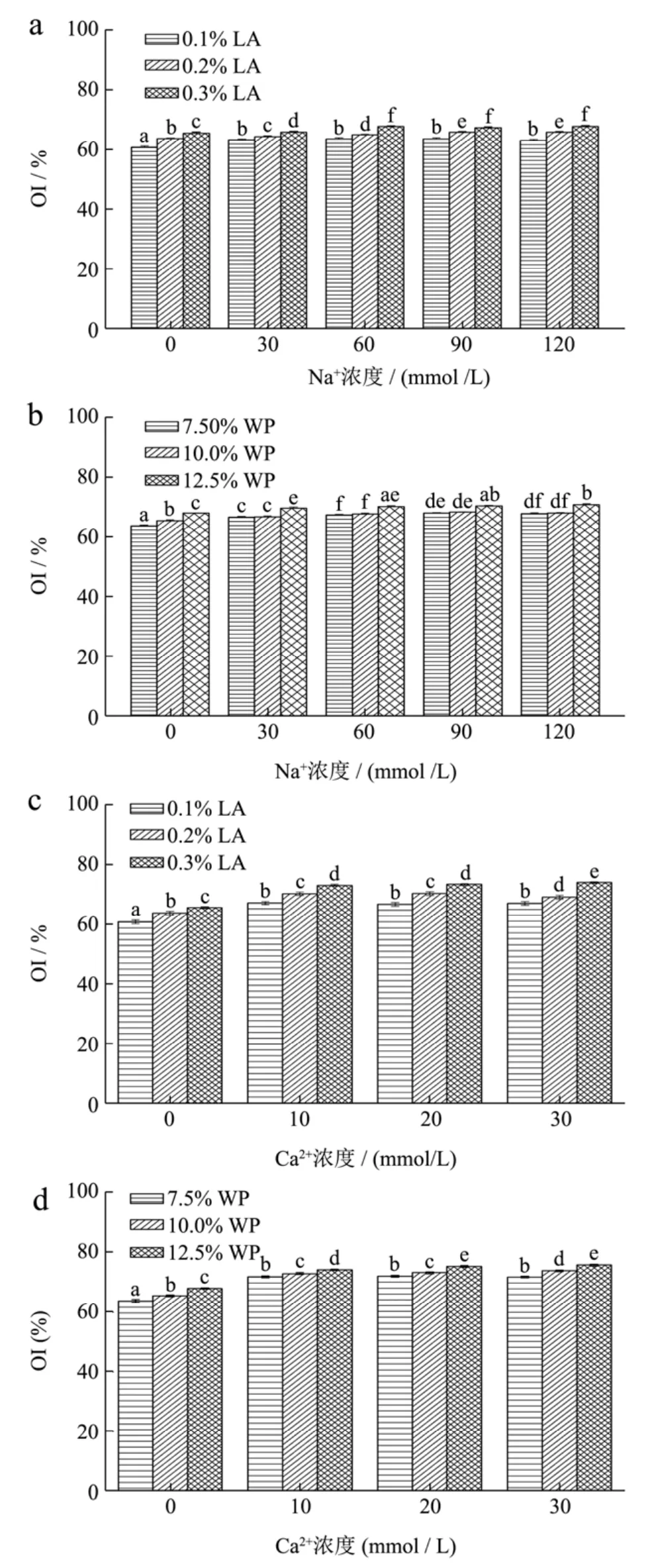
图1 离子和浓度对低酰基结冷胶/乳清蛋白混合凝胶不透明性的影响Fig.1 Effects of ion and concentrations on the opacity index of LA/WP mixed gels
图1给出了离子和浓度对低酰基结冷胶-乳清蛋白混合凝胶不透明指数的影响。不难发现,在所研究的浓度范围内,乳清蛋白和结冷胶均形成了不透明混合凝胶。随着离子浓度的增大,混合凝胶的不透明指数也随之增大,空白组的不透明指数与加入离子的其他组差异显著(p<0.05),当离子浓度超过一定值之后,混合凝胶的不透明指数则基本保持恒定。混合体系内低酰基结冷胶和乳清蛋白浓度越高,混合凝胶的不透明指数越大。与钠离子相比,钙离子浓度对混合凝胶不透明指数的影响更为显著(p<0.05),和对混合凝胶宏观形貌的研究结果一致。在对低酰基结冷胶-乳清蛋白混合凝胶宏观形貌观察时发现,混合凝胶是不透明凝胶。当体系内低酰基结冷胶浓度固定不变时,乳清蛋白浓度较低的混合凝胶呈现乳白色,表面光滑且质地均匀。随着乳清蛋白浓度的增加,混合凝胶会呈现出乳清蛋白的黄色,凝胶成型性减弱且质地变得粗糙。当乳清蛋白含量固定不变时,体系内结冷胶浓度较小时,形成的凝胶较软;结冷胶浓度增大,混合凝胶则变得坚实且尺寸稳定性越好。这是因为低酰基结冷胶形成的凝胶硬而脆,故而当体系内低酰基结冷胶浓度增大,形成的混合凝胶就更坚实。
2.2 混合凝胶的力学性质
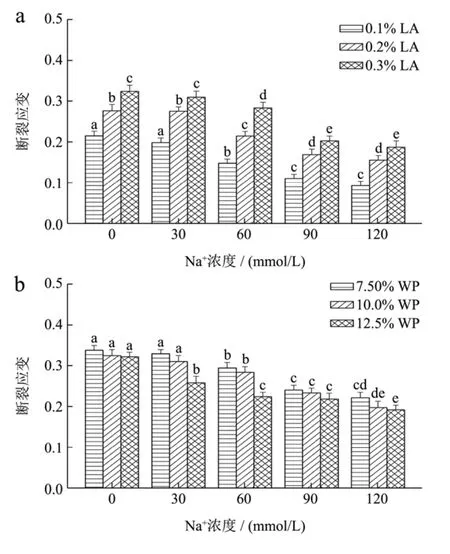
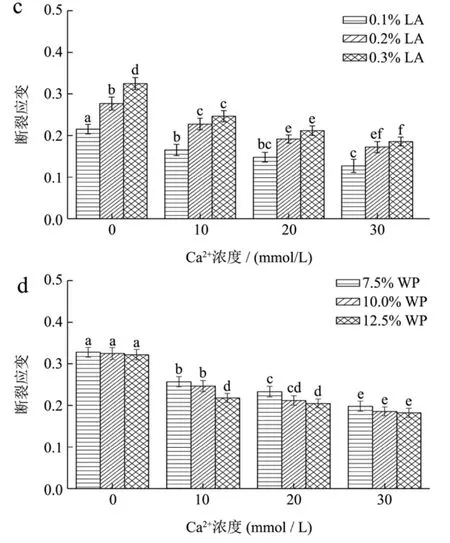
图2 离子和浓度对低酰基结冷胶/乳清蛋白混合凝胶断裂应变的影响Fig.2 Effects of ion and concentrations on the fracture strain of LA/WP mixed gels
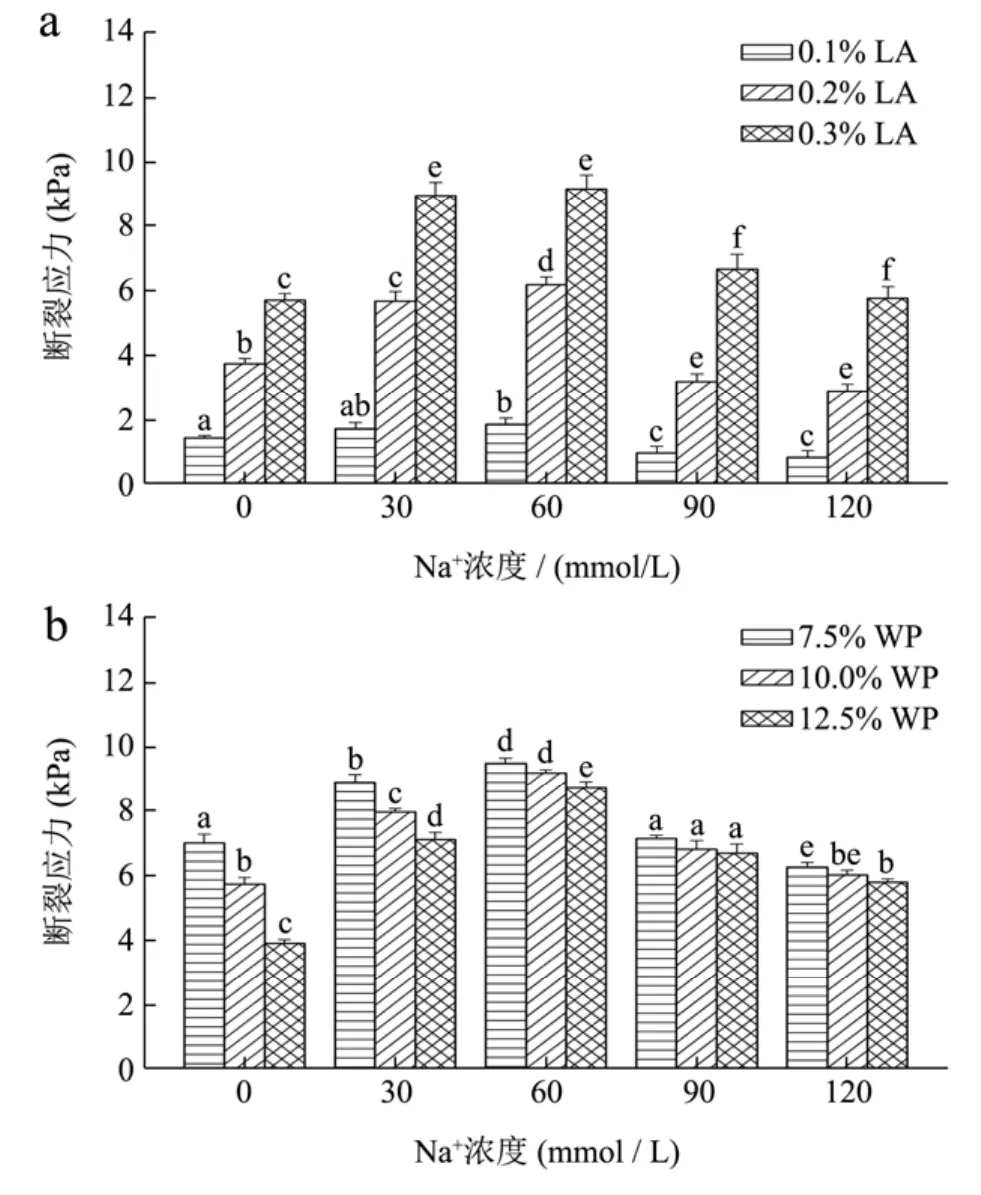
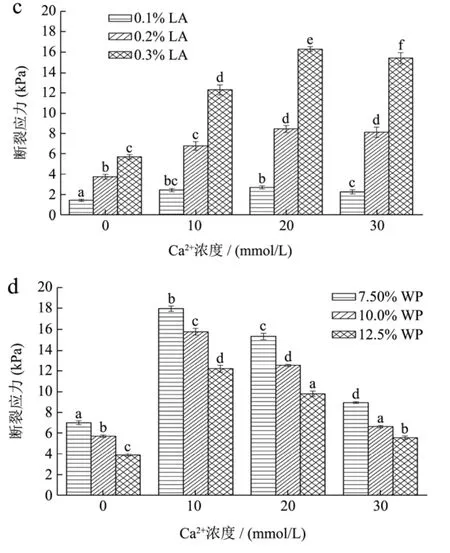
图3 离子和浓度对低酰基结冷胶/乳清蛋白混合凝胶断裂应力的影响Fig.3 Effects of ion and concentrations on the fracture stress of LA/WP mixed gels
图2给出了离子种类及其浓度对低酰基结冷胶-乳清蛋白混合凝胶断裂应变的影响。由图可见,无论是添加钠离子还是钙离子,混合凝胶的断裂应变均随着离子浓度的增大而略有减小,这两种离子的区别并不明显。体系内低酰基结冷胶浓度越大,乳清蛋白浓度越低,混合凝胶的断裂应变则越大。相对于乳清蛋白而言,结冷胶浓度的增大对混合凝胶断裂应变的影响程度更显著(p<0.05),这是因为混合凝胶形成的网络结构骨架主要是由低酰基结冷胶提供的,而乳清蛋白主要是以聚集体的形式填充在结冷胶形成的网络结构中,因此低酰基结冷胶浓度越高,形成的网络结构越致密,混合凝胶的结构越强。Spotti等[16]考察了乳清分离蛋白-紫穗槐状皂荚木胶(ECG)混合凝胶的力学性能和微观结构,发现不凝胶的ECG多糖对混合凝胶断裂应变影响很小,这和我们的研究结果类似。
凝胶强度可用断裂应力进行表征,断裂应力越大,说明凝胶越强。混合凝胶断裂应力的变化曲线见图3。随着离子浓度的升高,混合凝胶的断裂应力出现了先增大后减小的变化趋势,当钠离子和钙离子浓度分别为60 mM和10或20 mM时,混合凝胶的断裂应力存在最大值。获得相同凝胶强度时需要的二价离子浓度比一价离子更低。阳离子诱导凝胶理论认为[17],阳离子的添加可以减小低酰基结冷胶分子链上羧基(负电荷)之间的静电排斥,促使结冷胶双螺旋结构的聚集,增强凝胶强度;但过多的阳离子又会增大分子链间的排斥作用,因而离子浓度存在一个最佳值。钠离子可以通过水分子与结冷胶分子形成羧基-钠离子-水分子-钠离子-羧基的链接,而二价钙离子则形成羧基-钙离子-羧基的链接方式,故而达到相同凝胶强度时钙离子所需的浓度更低。
2.3 混合凝胶网络孔径
凝胶的宏观性质和微观结构密切相关,Spotti认为乳清蛋白凝胶网络孔径可用公式(4)进行计算[16]:
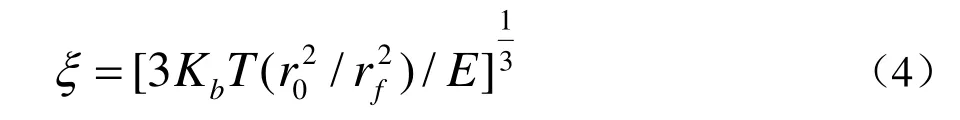
式中,ξ是孔径,Kb是波兹曼常数,T是绝对温度,E是力学性能测试中得到的杨氏模量,
低酰基结冷胶-乳清蛋白混合凝胶网络孔径的变化规律如图4所示。可见,当乳清蛋白浓度维持恒定时,低酰基结冷胶浓度越大,混合凝胶的孔径越小。当结冷胶浓度是0.1%时,凝胶孔径约为280~320 nm,但当结冷胶浓度增大至0.3%时,孔径减小到200~280 nm,说明结冷胶浓度越大,形成的网络结构越致密。当结冷胶浓度保持恒定时,凝胶的网络孔径则随着乳清蛋白含量的增加而略有增大。
对比低酰基结冷胶和乳清蛋白浓度的影响,不难发现,低酰基结冷胶浓度对混合凝胶网络孔径的影响更加明显,这可能是因为局部浓度增加所致。对于本研究中使用的乳清蛋白而言,其未经过热处理,自身不能形成有效的网络结构,混合凝胶的网络骨架是由低酰基结冷胶形成的,低酰基结冷胶浓度越大,分子间的作用越强,形成的网络结构越致密。而乳清蛋白不是网络的主要形成物质,因而其对孔径的影响较小。离子种类和离子浓度对混合凝胶孔径也有影响,随着离子浓度的增加,混合凝胶的孔径先减小而后增大,即存在一个最佳离子浓度,在此浓度下,混合凝胶的孔径最小。钙离子诱导得到的混合凝胶网络孔径均小于钠离子诱导凝胶,表明钙离子更利于形成致密结构的混合凝胶。这部分的研究结果和混合凝胶力学性质的研究结果一致。
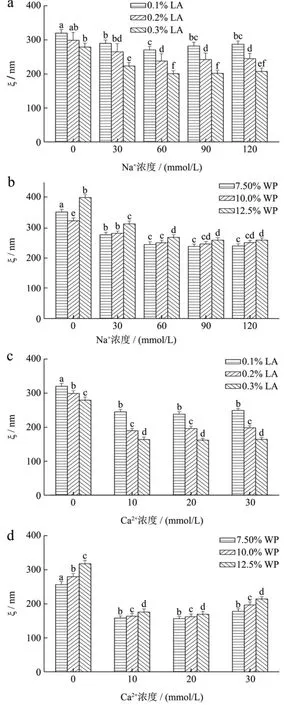
图4 离子和浓度对低酰基结冷胶/乳清蛋白混合凝胶网络孔径的影响Fig.4 Effects of ion and concentrations on the pore size of LA/WP mixed gels
2.4 混合凝胶的保水性
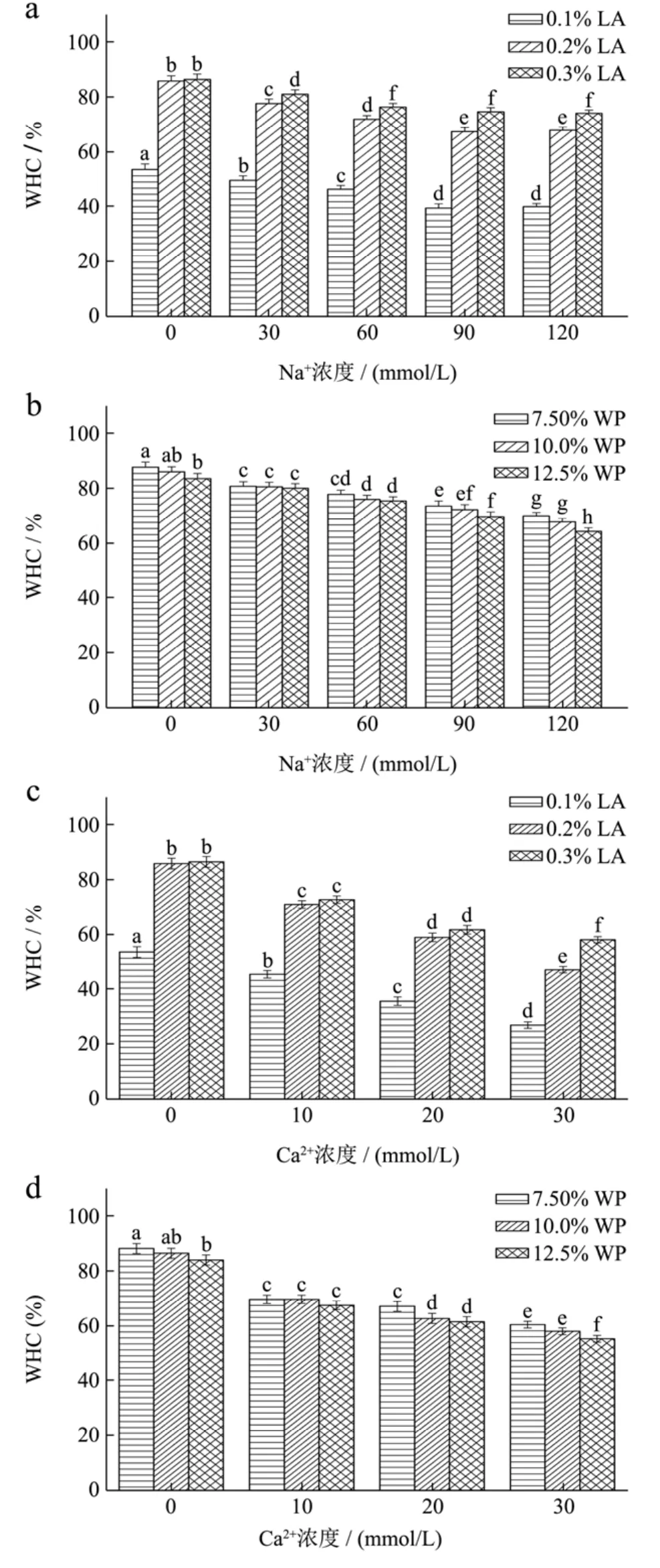
图5 离子和浓度对低酰基结冷胶-乳清蛋白混合凝胶保水性的影响Fig.5 Effects of ion and concentrations on the WHC of LA/WP mixed gels
保水性是凝胶一个非常重要的性质,有研究者发现,低酰基结冷胶具有优异的保水性,但其受离子的影响显著。图5给出了混合凝胶保水性的变化规律,可见,混合凝胶的保水性会随着离子浓度的增大而略有降低。体系内低酰基结冷胶浓度越大、乳清蛋白浓度越小,混合凝胶的保水性则越好。结冷胶凝胶会形成含有大量孔隙的海绵状网络结构[18],低酰基结冷胶浓度越高,形成的网络结构越致密,故而保水性越好。与低酰基结冷胶相比,乳清蛋白对凝胶保水性的影响更为微弱。这和我们对混合凝胶孔径以及力学性质的研究结果一致。
2.5 钠离子和钙离子的协同效应
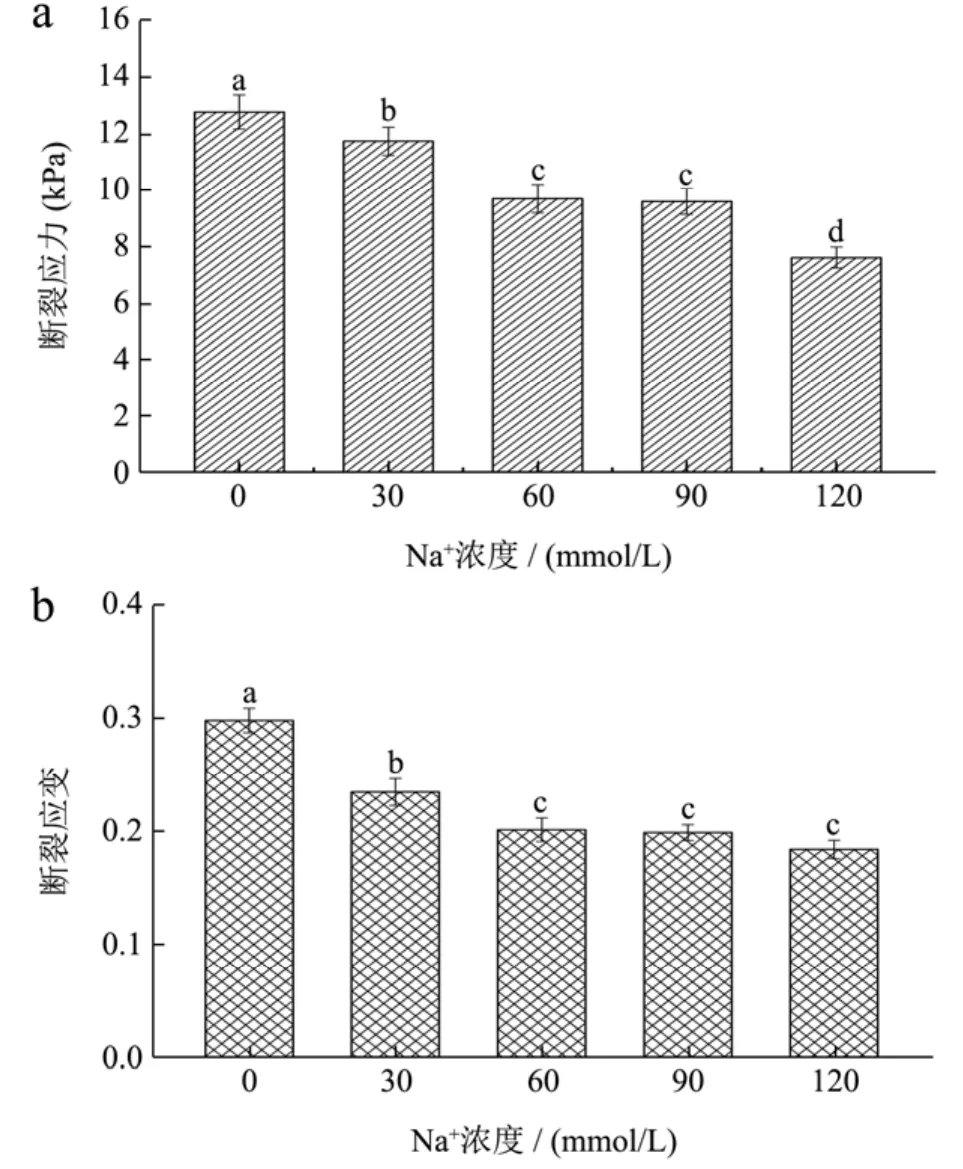
图6 Ca2+(5 mmol/L)和Na+协同作用对低酰基结冷胶/乳清蛋白混合凝胶力学性能的影响Fig.6 Effects of Na+ concentration on the mechanical properties of LA/WP mixed gels containing 5 mmol/L Ca2+
一价和二价阳离子都有促进基体高分子聚集的作用,当两者共存时,一方面可能由于离子的相互竞争从而阻碍结冷胶的双螺旋构型聚集,表现为凝胶弱化;另一方面,可能产生协同作用,使得混合凝胶增强。图6给出了钠离子和5 mmol/L的钙离子对混合凝胶力学性质的影响。显然,当体系中没有钠离子加入时,混合凝胶的断裂应力和断裂应变均为最大,断裂应力约为13 kPa,随着钠离子浓度的升高,混合凝胶的断裂应力和断裂应变逐渐降低,这要归因于钠离子浓度较低时,结冷胶上的羧基和钠离子的链接不能形成足够多的氢键,并减弱了钙离子在羧基间形成的链接,故而随着钠离子浓度的升高,凝胶会弱化。同时,在钙离子存在的情况下,二者之间无法形成有序的双螺旋构型,因此可以认为钙离子和钠离子在促进混合凝胶形成上不存在协同效应。
3 结论
本文研究了低酰基结冷胶-乳清蛋白混合凝胶的凝胶特性,考察了离子种类、离子浓度和基体浓度对混合凝胶光学特性、力学性质、网络孔径以及保水性质的影响。结果表明,混合凝胶的保水性和断裂应变随着离子浓度的增加逐渐减小,而断裂应力和凝胶孔径则随着离子浓度的增加出现了先增大后减小的变化趋势。钙离子形成的凝胶强度更大。相对于乳清蛋白而言,低酰基结冷胶的添加对混合凝胶性质影响更为显著。钙离子和钠离子在促进凝胶形成上无协同效应。
[1] Nguyen B T, Nicolai T, Chassenieux C, et al. Heat-induced gelation of mixtures of whey protein isolate and sodium caseinate between pH 5.8 and pH 6.6 [J]. Food Hydrocolloids,2016, 61: 433-441
[2] Qi P X, Onwulata C I. Physical properties, molecular structures, and protein quality of texturized whey protein isolate: effect of extrusion moisture content [J]. Journal of Dairy Science, 2011, 94(5): 2231-2244
[3] Fan M C, Hu T, Zhao S M, et al. Gel characteristics and microstructure of fish myofibrillar protein/cassava starch composites [J]. Food Chemistry, 2017, 218: 221-230
[4] 卢晓明,王静波,任发政,等.乳清蛋白在食品工业中的应用[J].食品科学,2010,31(1):262-267
LU Xiao-ming, WANG Jing-bo, REN Fa-zheng, et al.Applicstion of whey protein in food industry: a review [J].Food Science, 2010, 31(1): 262-267
[5] Jiang S, Zhang X, Ma Y, et al. Characterization of whey protein-carboxymethylated chitosancomposite films with and without transglutaminase treatment [J]. Carbohydrate Polymers, 2016, 153: 153-159
[6] 马中苏,隋思瑶,张宁,等.肉桂醛浓度对浓缩乳清蛋白/壳聚糖复合膜性能的影响[J].现代食品科技,2015,31(2):113-118
MA Zhong-su, SUI Si-yao, ZHANG Ning, et al. Effects of cinnamaldehyde concentrations on the performance of whey protein concentrate-chitosan composite film [J]. Modern Food Science and Technology, 2015, 31(2): 113-118
[7] Qi P X, Xiao Y P, Wickham E D. Stabilization of whey protein isolate (WPI) through interactions with sugar beet pectin (SBP) induced by controlled dry-heating [J]. Food Hydrocolloids, 2017, 67: 1-13
[8] Spotti M J, Martinez M J, A M R Pilosof, et al. Influence of maillard conjugation on structural characteristics and rheological properties of whey protein/dextran systems [J].Food Hydrocolloids, 2014, 39(39): 223-230
[9] 许晶,齐宝坤,赵青山,等.乳清蛋白-β-葡聚糖美拉德产物热凝胶流变性的研究[J].现代食品科技,2016,32(1):111-115,209
XU Jing, QI Bao-kun, ZHAO Qing-shan, et al. Rheological properties of thermal gels prepared from whey protein-β-glucan maillard products [J]. Modern Food Science and Technology, 2016, 32(1): 111-115, 209
[10] Wagoner T B, Foegeding E A. Whey protein epectin soluble complexes for beverage applications [J]. Food Hydrocolloids,2017, 63: 130-138
[11] Lam R S H, Nickerson M T. The properties of whey protein-carrageenan mixtures during the formation of electrostatic coupled biopolymer and emulsion gels [J]. Food Research International, 2014, 66: 140-149
[12] Le X T, Turgeon S L. Textural and waterbinding behaviors of beta-lactoglobulin-xanthan gum electrostatic hydrogels in relation to their microstructure [J]. Food Hydrocolloids, 2015,49(30): 216-223
[13] Mahdi M H, Conway B R, Mills T, et al. Gellan gum fluid gels for topical administration of diclofenac [J]. International Journal of Pharmaceutics, 2016, 515: 535-542
[14] Zhang N, Xu J C, Gao X, et al. Factors affecting water resistance of alginate/gellan blend films on paper cups for hot drinks [J]. Carbohydrate Polymers, 2017, 156: 435-442
[15] Buldo P, Benfeldt C, Carey J P, et al. Interactions of milk proteins with low and high acyl gellan: Effect on microstructure and textural properties of acidified milk [J].Food Hydrocolloids, 2016, 60: 225-231
[16] Spotti M J, Santiago L G, Rubiolo A C, et al. Mechanical and microstructural properties of milk whey protein/espina corona gum mixed gels [J]. LWT-Food Science and Technology, 2012, 48: 69-74
[17] Morris E R, Nishinari K, Rinaudo M. Gelation of gellan-A review [J]. Food Hydrocolloids, 2012, 28(2): 373-411
[18] Fuchigami M, Teramoto A. Texture and structure of high-pressure-frozen gellan gum gel [J]. Food Hydrocolloids,2003, 17(6): 895-899
