新型生物医用钛合金的设计及应用进展
2018-02-22麻西群于振涛牛金龙刘少辉贺新杰
麻西群,于振涛,牛金龙,余 森,刘少辉,贺新杰
(西北有色金属研究院陕西省医用金属材料重点实验室,陕西 西安 710016)
材料的力学性能和生物相容性是外科植入钛材设计的关键指标,传统的外科植入钛材的选材标准只包括2个基本因素:材料的强度和弹性模量。随着生物医用钛及钛合金植入物在临床领域的不断应用,生物相容性和安全性、生物力学相容性与人体骨匹配概念的提出,材料设计标准要求也随之提高、增加,并强调4个新的主要设计因素:(1)在追求低成本的同时,继续降低弹性模量,达到与人体骨(约 30 GPa)弹性模量的最佳匹配;(2)提高钛合金的生物相容性,选择无毒型的Al和V等合金元素;(3)继续提高钛合金的抗拉强度和疲劳强度,使之不低于传统 Ti−6Al−4V 合金;(4)个性化设计,即针对不同年龄人群设计出适合长期和短期植入的植入体,尤其是对儿童及年轻人,要设计出骨长入较差的新型钛合金,以避免植入物被拆除时造成新的损伤。这些因素已经成为新一代生物医用钛合金材料设计的基本要求。
1 国内外新型医用钛合金的设计方法
作为钛合金体内植入材料,目前的研究主要集中在β型钛合金上。而对于新型医用低弹性模量β型钛合金的设计理论而言,大多采用Mo当量、Kβ稳定化系数、d电子合金设计理论、平均电子浓度e/a、第一性原理和分子轨道理论等方法进行合金成分的设计和组织性能的预测。此外,还有团簇连接原子模型、神经网络技术、模糊逻辑等方法,这些钛合金成分设计的方法,经试验验证均取得了较理想的效果[1-4]。
合金元素主要通过影响Mo当量来影响合金的组织与性能,当Mo当量在0~9时,随Mo当量的增加,强度增加。因此,Mo当量设计是获得高强度钛材最简便的途径之一。在医用钛合金Mo当量法设计的同时,一般还根据所添加的β稳定元素含量的不同,将其细分为近β型钛合金、亚稳β型钛合金和稳定β型钛合金,常见的β稳定元素及相关设计参数如表1所示。

表1 常用β稳定化元素的临界浓度βc对合金相变温度的影响Tab.1 Effects of βc values of common β stabilizing elements on phase transformation temperature
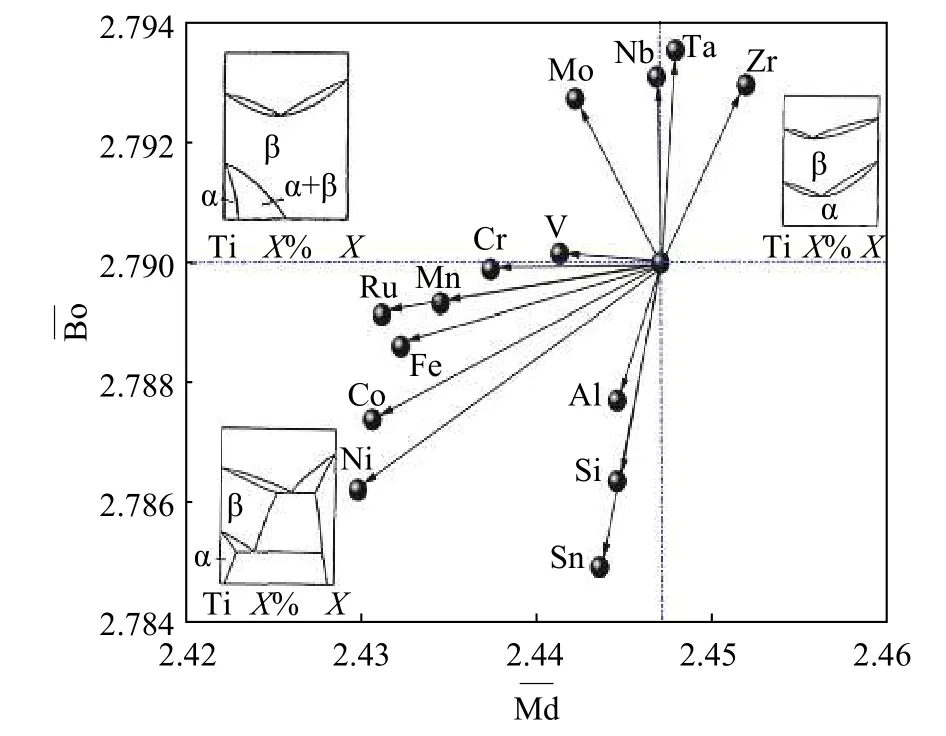
图1 Ti-M二元合金的Bo-Md图Fig. 1 Bo-Md diagram for various Ti-M binary alloys
对于多元钛合金系统,其合金成分较多,从而造成复杂的多相显微结构和宽泛的力学性能。目前使用较多的是d电子合金设计理论,一般设计准则是先确定合金具有低弹性模量的电子轨道参数范围或数值,然后根据不同合金元素的电子轨道参数及d电子合金设计理论,计算出合金的平均电子轨道参数,使之符合设定的目标,如图1所示。图1中绘出了不同电子轨道参数对应的合金元素与钛的二元合金相图。目前,大多数成功开发的新型医用低弹性模量β型钛合金都是采用该法设计研究的,如图2所示。此类钛合金的弹性模量均低于医用纯钛和Ti−6Al−4V 钛合金,与人体骨的弹性模量接近[5]。
根据平均价电子数与弹性模量的相关曲线规律,当平均价电子数为4.20~4.25时,合金的弹性模量较低,日本学者采用此法率先开发出了基本成分为 Ti(Nb,Ta,V)+(Zr,Hf)+O 的低弹性模量 β 型钛合金—橡胶金属,该合金的平均价电子数约为4.24,其弹性模量与人体骨更为接近,但强度等性能较低,无法作为外科植入材料[6]。郝玉琳等[7]发明的新型Ti2448钛合金的平均价电子数只有4.15(如图3所示),理论上该值并不在低弹性模量区间,但实际弹性模量最低可达40 GPa[2]。因此,该法并不适于大多数新型医用钛合金的设计。
模糊逻辑和神经网络技术的合金设计法都需要大量的合金成分及相应的性能数据。使用模糊逻辑推理软件或神经网络软件建立合金成分与性能的数学模型,再利用其他数据进行修正,从而进行性能预测及合金成分优化,该类设计方法目前尚不完善[1]。

图2 常见医用低弹性模量钛合金在Bo-Md相稳定图中的位置Fig. 2 Position of the common low modulus titanium alloys in Bo-Md Phase stability diagram

图3 橡胶金属及相近成分钛合金的弹性模量、弹性应变和加工硬化率Fig. 3 Elasticity modulus, elastic strain and work hardening rate of gum metal and other Ti alloys with similar composition
综上所述,新型低弹性模量β型钛合金的设计要点主要是成分上的创新和性能的预测。常用的具有优良生物相容性的合金元素主要有Nb,Mo,Ta,Zr,Sn,Fe等,而对于低成本合金来说,Ta价格昂贵,熔点较高,不适于低成本设计的标准。而Fe会对射线造成阻碍,不利于患者术后进行CT或MRI检查。
2 新型医用钛合金的设计研究最新进展
截止到目前,国际上已设计成功的低弹性模量β型钛合金共20余种,已被纳入标准的新型医用β型钛合金有Ti−13Nb−13Zr,Ti−12Mo−6Zr−2Fe,Ti−15Mo,Ti−15Mo−5Zr−3Al和 Ti−45Nb。其中前 3 种是为了降低应力屏蔽效应,降低合金的弹性模量和提高其生物相容性的要求,由美国设计开发的[8-9]。Ti−15Mo−5Zr−3Al合金是日本神户制钢在Ti−15Mo合金的基础上按照提高耐蚀性和抗拉强度的要求进行设计的。Ti−45Nb合金的设计起初由美国按航空航天用紧固件等零部件的要求进行设计,随后由于其具有高强度,低弹性模量和耐蚀性好等综合性能而被引入医用领域[10]。随着低弹性模量β型钛合金的不断应用,日本开展了大量的研究,日本大同特殊钢公司基于DV−Xα理论,采用d电子合金设计理论设计开发出了弹性模量最低为55 GPa的Ti−29Nb−13Ta−4.6Zr(TNTZ)亚稳β型钛合金。为了降低TNTZ亚稳β型钛合金的成本和弹性模量,提高其强度及疲劳性能,Mitsuo分别通过添加不同含量的O和Cr、大塑性变形、累积冷轧、变形诱发相变、热机械处理等方法来优化合金的强度、弹性模量、塑性和超弹性等综合力学性能,揭示了TNTZ亚稳β型钛合金的弹性模量随高压扭转次数或织构的增加而降低,及单晶TNTZ亚稳β型钛合金对晶体取向的依赖性,并通过提高O含量来抑制无热ω相的生成,提高Cr含量,合金冷变形前后弹性模量从64 GPa升高至77 GPa,因此提出了脊柱固定器用自调节弹性模量类钛合金的设计方法[11-16]。目前,能够达到自调节的新型钛合金有Ti−Cr系合金,随后发展 了 Ti−17Mo,Ti−30Zr−5Cr,Ti−30Zr−7Mo 和 Ti−30Zr−3Mo−3Cr合金。日本科研人员设计的低弹性模量钛合金都是基于TNTZ亚稳β型钛合金,通过改变合金元素及成分进行设计和研究的[17-18]。
近年来,生物材料学界对新型医用钛合金提出了新的设计准则,在钛合金设计初期,首先必须了解植入体的类型。对于长期植入人体无需取出的植入体而言,植入体与骨的吸收越快,结合度越高则越好。对于术后需要拆卸的植入体而言,即针对植入骨髓的一类植入体,例如股骨柄、胫骨、肱骨、用于接骨板固定的螺钉和用于儿童的植入体,为了防止钙磷沉淀使植入体长入骨头,日本学者开发了一系列具有高强度、低弹性模量和优异生物相容性的Ti−Zr系合金,如 Ti−Zr−Nb,Ti−Zr−Nb−Ta,Ti−Zr−Al−V合金。其中,Ti−30Zr−xMo 合金已经被充分发展为适用于可取出植入体的最佳材料[19-20]。之后,还开发出了具有自调节弹性模量的Ti−30Zr−7Mo和Ti−30Zr−3Mo−3Cr合金。这主要是由于Zr一方面是骨头的成分之一,另一方面Zr的质量分数达到25%以上时,能够抑制钙磷沉淀。
国内,郝玉琳等[7,21]在低弹性模量钛合金领域取得了较好的研究成果,该团队研发的多功能Ti2448低弹性模量钛合金已先后获得美国和中国专利授权,2006年建立材料企业标准1项,采用该合金制作的骨科用接骨板和脊柱固定系统两类植入器件已完成临床试验。
西北有色金属研究院生物材料研究所自20世纪70年代就致力于各类医用金属材料的设计、研发及产业化应用,尤其是在相关钛合金材料的研发和产业化应用方面均走在世界前列。自1999年,已先后开发出 Ti−2.5Al−2.5Mo−2.5Zr(TAMZ)(第一个具有我国自主知识产权的医用钛合金)、Ti −25Nb−3Zr−2Sn−3Mo(TLM)、Ti−15Nb−5Zr−3Mo(TLE)、Ti−10Mo−6Zr−4Sn−3Nb(TB12)医用钛合金板、棒、管、丝、箔材及超细晶块体材料等外科植入加工材。其中,TLM钛合金不仅剔除了传统医用钛材中含有的Al,V等毒性或过敏性元素,其相组成也非常多样化(α″,ω,α,β),不同组织下的力学性能可调范围大:抗拉强度为 645~1 270 MPa,弹性模量为40~90 GPa,疲劳强度为450~720 MPa。此类合金宽泛的性能不仅能够满足目前传统外科植入用钛材所要求的性能指标,而且具有一定的可调性和超弹性[9-10],非常适应用于今后理想外科植入物随人体骨力学参数的自适应调整。
图4为TLM钛合金髓内针及牙种植体以及相关的力学性能数据。目前,围绕TLM钛合金的研究已取得多项国家发明专利[22-24]。低弹性模量的TLM钛合金的设计准则是:

图4 TLM钛合金相关医疗器械及性能数据Fig.4 Medical devices made of TLM titanium alloy and the mechanical properties
(1)选择低成本、无毒性合金元素,并确定以Ti−Nb合金系作为合金设计的基础体系;
(2)采用d电子理论、Mo当量经验公式及Kβ稳定系数相结合的方法,根据钛合金二元相图及d电子轨道相图,选择低弹性模量和能够产生多种亚稳态相变及马氏体的区间,以便获得更加宽泛的性能区间;同时,根据Mo当量及Kβ稳定系数与相变温度曲线图确定钛合金处于介稳状态的参数,依据第一性原理计算Sn,Zr,Mo对钛合金强度、弹性模量及马氏体转变温度的影响;
(3)考虑钛合金难加工的工艺性特点,优化、计算并反复预测合金元素及其含量对TLM钛合金生物力学性能的影响,并通过试验检测和进一步优化获得稳定的具有宽泛性能的新型低弹性模量的医用钛合金。
目前,TLM钛合金和TB12钛合金外科植入加工材已分别于2005年、2016年建立了西北有色金属研究院企业标准3项、工艺规程3项。TLM钛合金被制作为各类接骨板、接骨螺钉、颅骨修复网板、牙种植体、血管支架及心脏壳形件等器械。TB12钛合金牙弓丝也已被国内某知名公司用于牙弓丝的生产和销售。
3 生物医用钛合金材料的未来发展方向
近年来,钛合金在生物医用领域的应用呈快速发展的趋势,这也将对钛合金的性能提出更高的要求。结合国内外当前的研究现状,得出生物医用钛合金材料未来发展的方向如下:
(1)单晶生物医用钛合金,沿某一方向生长获得的单晶材料可获得接近人体骨的弹性模量,用这种单晶制作植入体具有更好的弹性模量匹配;
(2)超细晶低弹性模量、高强度钛合金的生物力学相容性及产业化技术研究;
(3)超弹性和形状记忆功能医用低弹性模量钛合金的组织性能调控;
(4)通过调节孔隙率的大小来降低生物医用多孔钛合金材料弹性模量的同时,如何提升其力学性能。
