微纳结构硅在锂离子电池中的研究现状
2018-02-22刘旭燕吴晓龙朱新杰
刘旭燕,吴晓龙,杨 敏,朱新杰
(1.上海理工大学机械工程学院,上海200093;2.上海理工大学材料科学与工程学院,上海200093)
随着当今世界对能量需求的日益扩大,发展寿命长、环保、低成本的储能电池显得尤为重要。自1991年索尼锂离子电池商业化以来,锂离子电池在各领域的应用与日俱增[1]。现如今,锂离子电池在手机、笔记本电脑和其他许多便携式电子设备方面得到了广泛的应用。除此之外,锂离子电池也越来越多地被应用在电动汽车领域[2]。主要原因是,锂离子电池具有高的比容量、可快速充放电以及高库仑效率等优点。而在众多电化学电源的研究中,锂离子电池也被认为是最有可能实现大规模应用的储能电源。因此,针对锂离子电池的研究一直都专注于提高其容量及充放电效率等方面。
一般来说,锂离子电池是由两个独立的集流器构成的正、负电极组成的。除此之外,电解液可以保证锂离子在两电极间的迁移,隔离膜可以避免正、负两极的直接接触[3]。正极通常由锂的化合物(LiCoO2,LiNiO2或LiMn2O4)组成,而负极通常采用的是锂−碳层间化合物LixC6。锂离子电池充放电过程中的嵌锂和脱锂过程是通过电化学反应完成的。这一过程中,锂离子通过正负极之间的电解质扩散来实现迁移。
近年来,关于大容量锂离子二次电池的研究进展缓慢。其主要原因是,作为锂离子电池常用的正极材料钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)和它们的衍生物,以及已经商业化的石墨类负极材料的实际应用容量已经接近理论容量,难以有所提升。因此,为满足社会对高容量锂离子二次电池的需求,发展高容量低成本的新型电极材料成为近年来的研究热点。
石墨,是目前商业用锂离子电池中主要的正极材料,其理论比容量为 372 mA·h·g−1[4]。其具有低的放电电压平台(0.1~0.2 V),并且其低廉的价格使得石墨在商业化的锂离子电池中有着广泛的应用[5]。除此之外,在电池的循环过程中,石墨也表现出良好的稳定性和高的比容量。然而,石墨除了理论比容量较低之外,还容易与部分电解质发生溶剂共嵌入现象。例如,碳酸乙烯酯和碳酸丙烯酯是锂离子电池电解液中常用的溶剂,然而碳酸丙烯酯基电解液与石墨阳极不兼容,主要原因是碳酸丙烯酯可在石墨表面发生分解,从而使得石墨电极容易从集流器上剥离脱落[6]。这些原因均限制了石墨在锂离子电池领域中的应用。
硅在自然界中的储量非常丰富,在地壳中的质量分数为24.6%,仅次于氧。目前,硅因具有高的理论比容量(4 200 mA·h·g−1),是潜在的最佳替代石墨的电极材料。如此高的理论比容量是由于电极反应中1个硅原子最高可以形成约4个锂离子键(只针对Li4.4Si/Li22Si5的化学计算),而对于石墨电极材料来说,至少6个碳原子才可形成1个锂离子键[7]。除此之外,在合金材料中,硅的堆积密度与锂接近,所以硅具有高的体积比容量。因此,硅负极材料与电解液不会发生溶剂共嵌入现象,其适用的电解液范围更广。另外,相对于石墨材料,硅有更高的脱嵌锂电位,可以有效避免大倍率充放电过程中锂的析出,因此电池的安全性更高。
1 硅电极现在面临的问题
充放电过程中巨大的体积效应(400%)[8],成为硅在锂离子电池方面应用的最大障碍。然而硅并不是唯一存在体积膨胀问题的材料,其他高理论容量的材料,如锡(Sn),锗(Ge),锑(Sb)都有相似的体积膨胀问题[9]。这种体积膨胀产生的应力,使得硅颗粒容易产生裂缝,从而导致破裂、粉碎。由于粉碎的发生,碎片之间无法正常接触,而使得活性物质与活性物质、活性物质与集流体之间失去电接触。同时由于新的表面不断暴露出来,使得固相电解质层(SEI膜)不能稳定形成,最终导致电池的可逆容量降低、循环稳定性和倍率性能变差。图 1(a)和图 1(b)[10]正是对体积膨胀所导致电极失效的解释。
SEI膜是由电解液中有机溶剂的分解产物和盐的分解产物组成的。由于SEI膜是锂离子的优良导体、是电子的绝缘体,因此SEI膜的形成在一定程度上能够阻止锂离子电池循环性能的下降。同时,电池的可逆电荷损失、倍率性能和循环性能均依赖于SEI膜的质量。其中电解液中不可逆电荷的损失与SEI膜形成过程中锂离子的丢失有关。第1个循环周期过后不可逆电荷的损失将导致容量下降,这就是初始库仑效率较低的原因。另外,SEI膜的形成量与电极材料的表面积有关。由于体积膨胀每个循环周期过后,硅电极碎片数量增多,其表面积也随之增加,从而使得SEI膜在每个循环周期的嵌锂过程中不断形成。在SEI膜的形成过程中,比表面积越大消耗电解质中锂离子的数量越多,随之SEI膜也越厚,最终导致电池的循环能力不断下降。图1(c)显示了由于更多新表面的不断暴露,SEI膜随着循环周期的增加而逐渐增厚的过程。为了克服体积膨胀这一难题,近年来,研究者们进行了大量的探索及尝试,试图通过构筑不同结构的硅电极来缓解体积膨胀,以达到提高硅电极锂离子电池性能的目的。下面,本文将对微纳结构硅电极材料的研究进展及其性能进行综述。
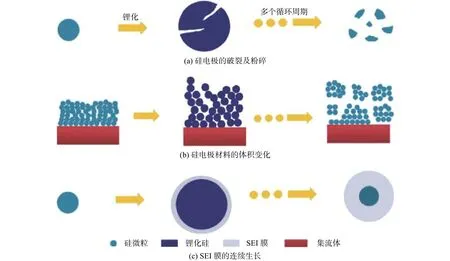
图1 硅电极充放电过程的失效示意图[10]Fig.1 Failure mechanism in charge-discharge process of silicon electrode[10]
2 硅的纳米结构
商业用硅通常选用粒径为微米或纳米尺度的粉末。市售的硅粉表面通常包覆一层氧化层。另外,在实验室的合成过程,即便是有微量的氧和水存在,氧化层也很容易形成。因此,在使用硅微纳米粉体前,通常需要进行预处理来除去表面的氧化物钝化层。硅在锂离子电池方面应用时,面临的最大难题是其本身的体积膨胀而使实际性能变差,基于此,可以通过改变其结构来解决这一问题。例如:介孔硅利用不同孔径的孔来减缓体积膨胀,来减缓由体积剧烈膨胀引起的颗粒粉碎。除此之外,薄膜是硅材料最常用的结构,但硅不易形成厚膜,这限制了硅薄膜的实际应用。核壳结构,对于硅来说,常采用刚性骨架支撑Si/B4C复合体以减缓体积膨胀。硅纳米线和硅纳米管通过圆柱形结构利用径向膨胀应变和应变驰豫来减小压力。近年来,越来越多的研究人员将关注的焦点转移到通过控制纳米结构来提高硅负极材料的性能上来。这里,我们将讨论这些结构的性能优点以及存在的问题。
2.1 硅纳米颗粒
硅颗粒尺寸的大小对电池性能下降的速度有着巨大的影响。一般来说,与粒径较大的颗粒相比,粒径较小的颗粒的电化学性能更加稳定。同时,随着颗粒尺寸的增大,其初始容量会增大,但是也会伴随着快速的容量衰退。纳米颗粒的尺寸越小,其结构越稳定,这是因为体积膨胀过程中的机械应力减小。有研究表明,一定尺寸范围内的硅纳米颗粒在充放电过程中不会发生粉碎。即当颗粒尺寸小于150 nm时,颗粒不会出现裂缝或者发生破裂。图2[19]显示了由50和100 nm的硅颗粒制成的电极的性能差异。图 2(a)~图 2(f)分别为硅颗粒的TEM、能量过滤(EF)TEM 和高分辨率(HR)TEM 图像。图 2(g)~图 2(h)显示了在 30 个循环周期内,它们的锂化比容量均高于 1 000 mA·h·g−1,并且颗粒尺寸越小其电池容量越大。

表1 不同结构的硅电极锂离子电池的性能比较Tab.1 Comparison of the performance of silicon electrodes with different structures for the lithium ion battery
2.2 硅纳米线
硅纳米线是由Chan等[20]通过水汽−液−固(VLS)的过程在不锈钢集流器上生长得到的。硅纳米线的主要优点有3个:存在可膨胀空间、电接触能力强、无需粘合剂。另外,硅纳米线电极可以承受一定的由体积膨胀所带来的压力,从而避免粉化。这是因为硅纳米线具有应变弛豫的特性,能够允许一定范围内的线径膨胀。此外,在集流器上生长的硅纳米线具有强的电接触性能,并且每条纳米线都存在连续高效的电子传输。这确保了硅纳米线结构电极具有高的容量,并且体积膨胀不会轻易导致硅纳米线的碎裂。图3[20]进一步总结了Chan等针对硅纳米线所做的工作,其中图 3(a)和图 3(b)阐示了硅薄膜和硅颗粒电极在应用中的粉化问题。
2.3 硅纳米管
硅纳米管具有类似硅纳米线的结构,近年来也受到了广泛的关注。就像硅纳米线一样,硅纳米管的体积膨胀也是从中心开始的,但硅纳米管不是一个坚实的圆柱体,而是一个中空的管状结构。管形的目的主要是为了增加与电解质接触的面积。Wu等[21]针对硅纳米管使用了双壁法,即利用硅氧化物(SiOx)作为硅纳米管外壁的限制层。他们制备的双层硅纳米管(DWSiNT)可以允许锂离子通过硅氧化物层,同时也可防止电解质接触除硅氧化层以外的其他电池结构。由于限制层SiOx是刚性的,因此锂化过程中硅纳米管只能向内部扩张。有了这一限制,SEI膜便可以保持完整性,解决了SEI膜不能稳定形成的问题。这里的SEI膜会不断形成直到形成的膜足够厚而不会受到膨胀的影响为止。在充电过程中,体积膨胀在内部发生而不会破坏外部的SEI膜。另外,硅氧化物限制层也可以被碳涂层取代。利用碳涂层作限制层来缓冲体积膨胀也是一种常用的方法,而利用SiOx作为限制层主要与SiOx的刚性特征有关。另外,体积膨胀时可能会发生碳涂层不能完全包覆的现象,导致电极破裂解体。
2.4 多孔硅
对于锂离子电池硅电极来说,合适的孔结构不仅可以促进锂离子的快速脱嵌,提高材料的倍率性能,还可以缓释材料在充放电过程中的体积膨胀,提高循环稳定性。另外,若在制备多孔硅材料时加入碳材料,还可以有效改善其导电性能,进一步改善材料的电化学性能。制备多孔硅的常用方法有模板法、刻蚀法和镁热还原法,其中最常用的方法是模板法。模板法按照模板的形态可分为软模板法和硬模板法。一般来说,软模板法成本较高,且合成条件苛刻,原料的储存也很困难;硬模板法的成本较低,制备方法也更简单。Kim等[22]在900 ℃氩气中,对丁基硅凝胶和SiO2颗粒的复合材料进行了退火处理,得到具有碳包覆结构的介孔(40 nm)碳硅复合材料。此种纳米硅材料能够适应较大的应力变化。并且在1C的电流密度下,100个充放电循环周期后其比容量仍可以达到 2 800 mA·h·g−1。

图2 不同颗粒尺寸硅电极的微观结构图、不同颗粒尺寸硅电极材料制备的锂离子电池的嵌锂容量-循环次数曲线[19]Fig.2 Microstructure of the silicon particles with different size, Lithiation (discharge) capacity as a function of cycle number for electrodes prepared from the silicon electrodes with different size particles[19]
刻蚀也是制备多孔硅材料的常用方法之一,包括电化学刻蚀法和金属催化刻蚀法。Ge等[23]针对硼掺杂的硅,利用银作为催化剂,在HF溶液(含有Ag+)中进行了刻蚀,得到具有多孔结构的纳米硅。然后利用化学气相沉积(CVD)法在多孔硅表面沉积一层无定形碳,最后再与石墨烯进行复合。所制得的材料在1/4 C和1/2 C的电流密度下经过200次循环后,其比容量分别为 1 400 和 1 000 mA·h·g−1,表现出良好的循环稳定性和倍率性能。
近年来,镁热法还原氧化硅制备硅基材料的方法也得到了广泛的关注。由于硅的导电性差,镁热还原后还需在多孔硅的表面包覆一层无定形碳。Casimir等[24]通过镁热还原法制得了含有微晶硅的多孔硅,最后利用CVD法在其表面沉积了一层无定形碳。该材料在1 C的电流密度下经100次循环后,其可逆比容量高达 1 500 mA·h·g−1。

图3 充放电过程中硅颗粒和硅纳米线形态变化的示意图[20]Fig. 3 Schematic of morphological changes that occur in Si and Si nanowires during electrochemical cycling[20]
3 结论与展望
自锂离子电池诞生以来,其在诸多领域中都得到了应用。从目前市场对锂离子电池的需求来看,可快速充放电型的锂离子电池是重要的发展方向。硅电极虽具有高的理论比容量,但是阻碍其性能发展的最大问题是其锂化过程中巨大的体积膨胀效应。根据上文中硅纳米颗粒、硅纳米线、硅纳米管、多孔和空心结构硅的研究,不难发现,通过改变结构可以有效地缓解体积效应。通过硅纳米颗粒与硅纳米管(线)的性能比较发现,减小维度可以提高硅电极材料的电化学性能,但即使是硅纳米颗粒、硅纳米管(线)或是硅纳米纤维都无法避免与电解质直接接触,从而容易获得较大的不可逆容量。同时,由于硅的导电性能较差,使得硅电极锂离子电池的内阻过大,限制了锂离子及电子的传导,致使电化学动力学性能和倍率性能变差。然而,若单纯地掺杂其他元素并不能使这一状况有明显的改善,因此需要具有特殊结构的硅基复合材料,如多孔结构或空心结构。比较看来,目前已研究的不同结构的硅电极材料中,核壳结构及多壁纳米管结构既可以解决硅与电解液的直接接触问题,又可以通过包覆外壳来提高硅电极材料的导电性。
锂离子电池作为储能设备具有较高的能量密度,但是其功率密度与超级电容器相比却相差甚远。因此,保持循环稳定性、提高硅基材料的可逆比容量、提高倍率性能是硅基负极锂离子电池在研究过程中需要解决的问题。另外,实验室制备电极材料的过程中常使用特殊的制备方法,如CVD法等,虽然可以获得具有特殊结构及性能优良的材料,但是制备成本往往较高,很难实现商业化。因此,如何降低硅基材料的制备成本,寻找简易、可工业化的制备方法是硅基电极材料实现工业化过程中急需解决的问题。
综上所述,在今后的研究工作中应尽可能根据实用化原则设计、制备具有高体积能量密度和质量能量密度的硅基锂离子电池负极材料,进而逐步实现硅基负极材料从试验向实际生产方向的转变。
