3-(5-苄叉基噻唑并均三唑酮)氟喹诺酮类化合物的合成及其抗肿瘤活性
2018-02-15姜亚玲黄文龙胡国强
姜亚玲,李 珂,黄文龙,胡国强
(1郑州工业应用技术学院药物化学教研室,郑州 451150;2中国药科大学新药研究中心,南京 2100091;3河南大学药学院,开封 475001)
药物研发起源于先导物的发现和优化,而基于机制或(和)结构的药效团和骨架迁越的药物分子设计是发现新先导物的有效途径[1]。拓扑异构酶不仅是抗菌氟喹诺酮药物的作用靶标,也是抗肿瘤药物的重要作用靶点[2],同时,鉴于喹啉环也是药物分子的优势药效团骨架,由此可通过结构修饰的策略将氟喹诺酮的抗菌活性转化为抗肿瘤活性[3]。由均三唑杂环构建的噻唑并均三唑稠杂环[4]及N-苄叉基绕丹宁修饰的酰胺结构[5]作为C-3羧基的生物等排体均可提高其抗肿瘤活性,这为C-3羧基等排体的结构优化提供了新思路。基于α,β-不饱和酮结构单元不但是构建药物分子的重要有机合成子,也是靶向抗肿瘤药物,如小分子靶向酪氨酸激酶抑制剂舒尼替尼[6]和许多天然有效成分,如查耳酮和黄酮类的核心骨架[7]。因此,用α,β-不饱和酮结构作为C-3位均三唑环的修饰基团值得关注。考虑到均三唑及噻唑杂环作为基本的药效团骨架在构建结构多样的候选药物分子的重要性[8],为实现均三唑、噻唑、α,β-不饱和酮三者的有效拼合,本研究用α,β-不饱和酮对均三唑环进行稠合修饰,进而构建了“苄叉基的含噻唑并均三唑酮”骨架,以此作为培氟沙星C-3羧基的等排体,设计合成了3-苄叉基噻二唑并均三唑酮的氟喹诺酮化合物(6a~6l),并评价了其体外的抗肿瘤活性。
1 合成路线
目标化合物6a~6l的合成见路线(1)。培氟沙星酰肼2与硫氰化钾缩合生成C-3酰氨基硫脲3,接着在氢氧化钠水溶液中发生分子内闭环反应得到C-3均三唑硫醇4,它与氯乙腈发生亲核取代反应得到C-3均三唑硫乙腈5。中间体5与取代的苯甲醛在HOAc-H2SO4体系中经环合、水解、Claisen-Schmidt缩合三步一锅反应制得相应的C-3噻唑并均三唑不饱和酮化合物6a~6l。
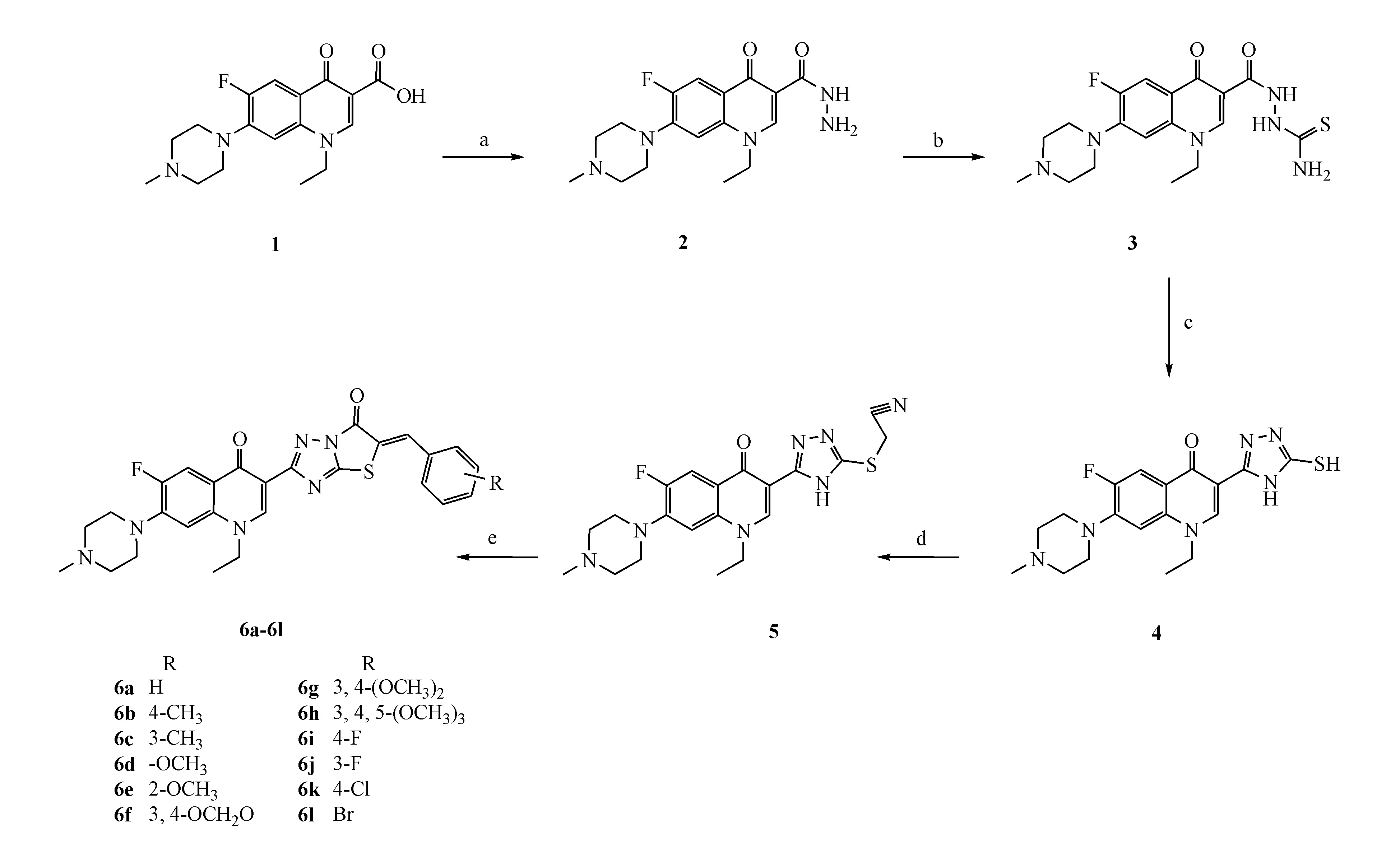
Scheme1 Synthetic route of the title compounds (6a-6l)
a:N2H4H2O,reflux;b:KSCN,HCl,reflux;c:NaOH,reflux;d:ClCH2CN,KOH,EtOH,rt;e:Ar-CHO,HOAc,H2SO4,reflux
2 实验部分
2.1 材 料
WK-1B数字熔点仪(上海申光仪器有限公司);AM-400型核磁共振仪、Esquire LC型质谱仪(德国Bruker公司);PE2400-Ⅱ元素分析仪(美国PE公司)。中间体培氟沙星C-3均三唑硫醇4按文献[4]的方法制备,其他试剂均为市售分析纯。实验所用人肝癌细胞株SMMC-7721、人胰腺癌细胞株Capan-1和人白血病细胞株HL60均购于中科院上海细胞生物研究所。
2.2 化学合成
中间体1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-(5-氰甲硫基-4H-1,2,4-三唑-3-基)-喹啉-4(1H)-酮(5)的合成
培氟沙星C-3均三唑硫醇4(20.0 g,51.5 mmol)悬浮于氢氧化钾(3.5 g,62.5 mmol)无水乙醇溶液(1 000 mL)中,加热溶解物料,冰浴下滴加氯乙腈(4.7 g,62.5 mmol),常温搅拌反应10 h,然后搅拌回流3 h,放置过夜。过滤,固体用水洗至中性,干燥。用无水乙醇重结晶,干燥,得18.0 g淡黄色结晶物5,收率82%,mp:225~227 ℃;1H NMR:11.37(1H,s,NH),8.87(1H,s,2-H),7.82(1H,d,J=13.0 Hz,5-H),7.26(1H,d,J=7.4 Hz,8-H),4.36(2H,J=7.0 Hz,CH2),4.18(2H,s,CH2CN),3.35(4H,m,piperazine-H),2.52(4H,m,piperazine-H),2.34(3H,s,N-CH3),1.38(3H,J=7.0 Hz,CH2);MS(m/z):428[M+H]+。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-芳甲叉基-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6a~6l)的合成通法
中间体5(2.0 g,4.7 mmol)和取代的苯甲醛(5.0 mmol)加入到冰乙酸(50 mL)中,滴加浓硫酸(1.0 mL),混合反应物搅拌回流反应24 h。减压蒸除溶剂,加去离子水50 mL和适量的活性炭,回流脱色1 h。热过滤,用氨水碱化pH 9.0~10.0。放置析出固体,过滤,用去离子水洗涤,干燥。无水乙醇-DMF混合溶剂重结晶,得目标化合物6a~6l。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-苯甲叉基-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6a) 收率72.5%,mp:232~234 ℃;1H NMR:8.84(1H,s,2-H),8.16(1H,s,Ar-CH),7.84(1H,d,J=13.0 Hz,5-H),7.76~7.24(6H,m,Ph-H and 8-H),4.42(2H,J=7.0 Hz,CH2),3.36(4H,m,piperazine-H),2.54(4H,m,piperazine-H),2.32(3H,s,N-CH3),1.37(3H,J=7.0 Hz,CH2);MS(m/z):517[M+H]+;Anal.Calcd.for C27H25FN6O2S:C 62.78,H 4.88,N 16.27;Found:C 63.04,H 4.65,N 16.42。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(4-甲基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6b) 收率68.3%,mp:216~218 ℃;1H NMR:8.82(1H,s,2-H),8.13(1H,s,Ar-CH),7.85(1H,d,J=13.0 Hz,5-H),7.74~7.23(5H,m,Ph-H and 8-H),4.40(2H,J=7.0 Hz,CH2),3.35(4H,m,piperazine-H),2.52(4H,m,piperazine-H),2.32,2.26(3H,2s,N-CH3and Ph-CH3),1.35(3H,J=7.0 Hz,CH2);MS(m/z):531[M+H]+;Anal.Calcd.for C28H27FN6O2S:C 63.38,H 5.13,N 15.84;Found:C 63.62,H 4.87,N 16.10。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(3-甲基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6c) 收率54.7%,mp:204~206 ℃;1H NMR:8.85(1H,s,2-H),8.14(1H,s,Ar-CH),7.86(1H,d,J=13.0 Hz,5-H),7.73~7.26(5H,m,Ph-H and 8-H),4.38(2H,J=7.0 Hz,CH2),3.35(4H,m,piperazine-H),2.54(4H,m,piperazine-H),2.36,2.24(3H,2s,N-CH3and Ph-CH3),1.37(3H,J=7.0 Hz,CH2);MS(m/z):531[M+H]+;Anal.Calcd.for C28H27FN6O2S:C 63.38,H 5.13,N 15.84;Found:C 63.55,H 4.92,N 16.07。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(4-甲氧基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6d) 收率75.2%,mp:235~237 ℃;1H NMR:8.92(1H,s,2-H),8.18(1H,s,Ar-CH),7.86(1H,d,J=13.0 Hz,5-H),7.76~7.25(5H,m,Ph-H and 8-H),4.45(2H,J=7.0 Hz,CH2),3.87(3H,s,OCH3),3.37(4H,m,piperazine-H),2.54(4H,m,piperazine-H),2.34(3H,s,N-CH3),1.41(3H,J=7.0 Hz,CH2);MS(m/z):547[M+H]+;Anal.Calcd.for C28H27FN6O3S:C 61.52,H 4.98,N 15.37;Found:C 61.77,H 4.76,N 15.62。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(2-甲氧基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6e) 收率52.3%,mp:204~206 ℃;1H NMR:8.87(1H,s,2-H),8.16(1H,s,Ar-CH),7.87(1H,d,J=13.0 Hz,5-H),7.72~7.32(5H,m,Ph-H and 8-H),4.46(2H,J=7.0 Hz,CH2),3.88(3H,s,OCH3),3.36(4H,m,piperazine-H),2.53(4H,m,piperazine-H),2.35(3H,s,N-CH3),1.42(3H,J=7.0 Hz,CH2);MS(m/z):547[M+H]+;Anal.Calcd.for C28H27FN6O3S:C 61.52,H 4.98,N 15.37;Found:C 61.70,H 4.82,N 15.56。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(3,4-二氧亚甲基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6f) 收率81.5%,mp:242~244 ℃;1H NMR:8.93(1H,s,2-H),8.22(1H,s,Ar-CH),7.92(1H,d,J=13.0 Hz,5-H),7.83~7.36(4H,m,Ph-H and 8-H),6.25(2H,s,OCH2O),4.48(2H,J=7.0 Hz,CH2),3.37(4H,m,piperazine-H),2.56(4H,m,piperazine-H),2.36(3H,s,N-CH3),1.45(3H,J=7.0 Hz,CH2);MS(m/z):561[M+H]+;Anal.Calcd.for C28H25FN6O4S:C 59.99,H 4.49,N 14.99;Found:C 60.24,H 4.21,N 15.26。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(3,4-二甲氧基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6g) 收率68.2%,mp:226~228 ℃;1H NMR:8.91(1H,s,2-H),8.23(1H,s,Ar-CH),7.83~7.36(5H,m,Ph-H,5-H and 8-H),3.86(6H,2s,2OCH3),4.46(2H,J=7.0 Hz,CH2),3.35(4H,m,piperazine-H),2.54(4H,m,piperazine-H),2.35(3H,s,N-CH3),1.43(3H,J=7.0 Hz,CH2);MS(m/z):577[M+H]+;Anal.Calcd.for C29H29FN6O4S:C 60.40,H 5.07,N 14.57;Found:C 60.58,H 4.31,N 14.82。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(3,4,5-三甲氧基苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6h) 收率66.4%,mp:228~230 ℃;1H NMR:8.92(1H,s,2-H),8.24(1H,s,Ar-CH),7.96(1H,d,J=13.0 Hz,5-H),7.82(2H,s,Ph-H),7.32(1H,d,J=7.4 Hz,8-H),3.87(9H,2s,3OCH3),4.53(2H,J=7.0 Hz,CH2),3.45(4H,m,piperazine-H),2.57(4H,m,piperazine-H),2.37(3H,s,N-CH3),1.48(3H,J=7.0 Hz,CH2);MS(m/z):607[M+H]+;Anal.Calcd.for C30H31FN6O5S:C 59.39,H 5.15,N 13.85;Found:C 59.62,H 5.34,N 14.11。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(4-氟苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6i) 收率76.6%,mp:234~236 ℃;1H NMR:8.93(1H,s,2-H),8.25(1H,s,Ar-CH),8.04(1H,d,J=13.0 Hz,5-H),7.86~7.38(5H,m,Ph-H and 8-H),4.54(2H,J=7.0 Hz,CH2),3.46(4H,m,piperazine-H),2.55(4H,m,piperazine-H),2.36(3H,s,N-CH3),1.52(3H,J=7.0 Hz,CH2);MS(m/z):535[M+H]+;Anal.Calcd.for C27H24F2N6O2S:C 60.66,H 4.53,N 15.72;Found:C 60.87,H 4.32,N 15.92。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(3-氟苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6j) 收率63.2%,mp:227~229 ℃;1H NMR:8.95(1H,s,2-H),8.23(1H,s,Ar-CH),8.02(1H,d,J=13.0 Hz,5-H),7.87~7.42(5H,m,Ph-H and 8-H),4.52(2H,J=7.0 Hz,CH2),3.47(4H,m,piperazine-H),2.56(4H,m,piperazine-H),2.35(3H,s,N-CH3),1.48(3H,J=7.0 Hz,CH2);MS(m/z):535[M+H]+;Anal.Calcd.for C27H24F2N6O2S:C 60.66,H 4.53,N 15.72;Found:C 60.42,H 4.76,N 15.53。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(4-氯苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6k) 收率60.3%,mp:218~220 ℃;1H NMR:8.90(1H,s,2-H),8.23(1H,s,Ar-CH),7.96(1H,d,J=13.0 Hz,5-H),7.82~7.35(5H,m,Ph-H and 8-H),4.52(2H,J=7.0 Hz,CH2),3.45(4H,m,piperazine-H),2.53(4H,m,piperazine-H),2.34(3H,s,N-CH3),1.48(3H,J=7.0 Hz,CH2);MS(m/z):551,553[M+H]+(35Cl,37Cl,);Anal.Calcd.for C27H24ClFN6O2S:C 58.85,H 4.39,N 15.25;Found:C 59.13,H 4.14,N 15.52。
1-乙基-6-氟-7-(4-甲基-哌嗪-1-基)-3-[5-(4-溴苯甲叉基)-噻唑[3,2-b][1,2,4]三唑-6(5H)-酮-2-基]-喹啉-4(1H)-酮(6l) 收率57.4%,mp:206~208 ℃;1H NMR:8.89(1H,s,2-H),8.21(1H,s,Ar-CH),7.94(1H,d,J=13.0 Hz,5-H),7.78~7.32(5H,m,Ph-H and 8-H),4.50(2H,J=7.0 Hz,CH2),3.43(4H,m,piperazine-H),2.52(4H,m,piperazine-H),2.33(3H,s,N-CH3),1.46(3H,J=7.0 Hz,CH2);MS(m/z):595,597[M+H]+(79Br,81Br,);Anal.Calcd.for C27H24BrFN6O2S:C 54.46,H 4.06,N 14.11;Found:C 54.68,H 4.32,N 14.33。
2.3 抗肿瘤活性评价
对合成的12个新目标化合物(6a~6l)和对照蒽醌类抗肿瘤药阿霉素(DOX)及母体培氟沙星(1)用DMSO配成0.01 mol/L浓度的储备液,按文献[5]的方法测定其对人肝癌细胞株SMMC-7721、人胰腺癌细胞株Capan-1和人白血病细胞株HL60的半数抑制浓度(IC50),结果见表1。
Table1 Antiproliferative activity of the title compounds (6a-6l) against SMMC-7721,Capan-1 and HL60 tumor cells
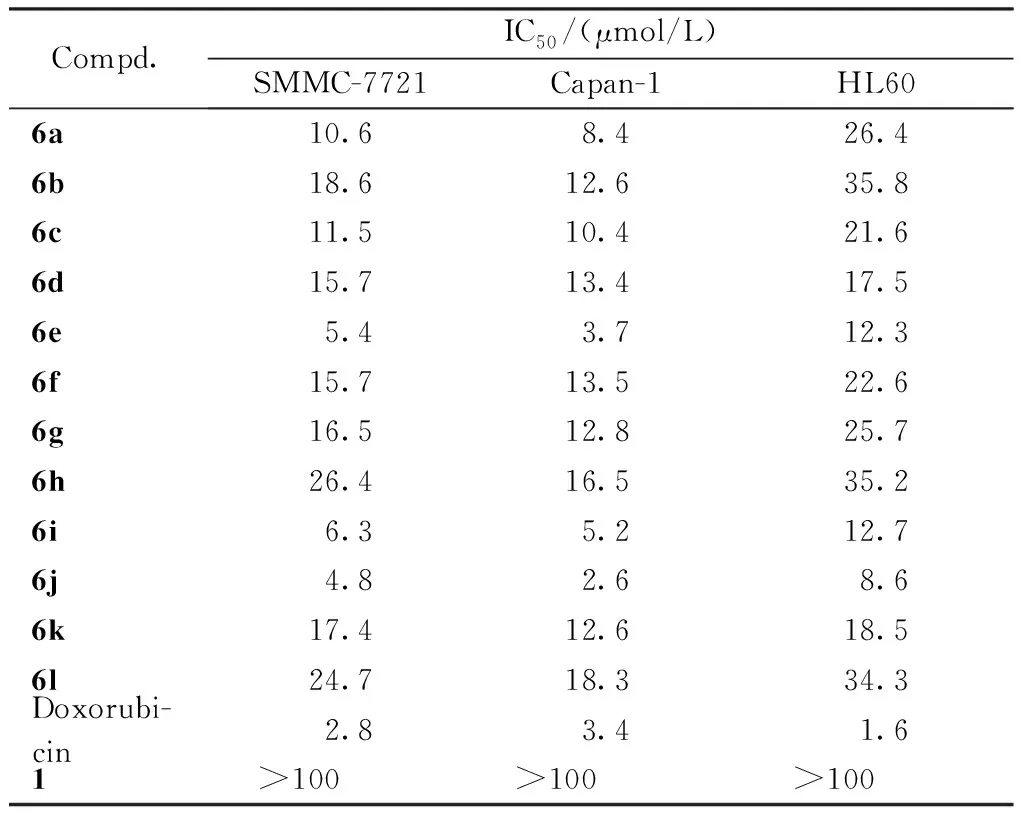
Compd.IC50/(μmol/L)SMMC-7721Capan-1HL606a10.68.426.46b18.612.635.86c11.510.421.66d15.713.417.56e5.43.712.36f15.713.522.66g16.512.825.76h26.416.535.26i6.35.212.76j4.82.68.66k17.412.618.56l24.718.334.3Doxorubi-cin2.83.41.61>100>100>100
体外抗增殖活性结果表明,12个目标化合物对3种试验肿瘤细胞株的IC50均低于35.0 mol/L,显著强于对照母体培氟沙星(100 mol/L)的活性。同时,构效关系表明,构建的稠杂环不饱和酮双键的芳香苯环的取代基增大可导致活性降低,但苯环被F原子取代或邻位被甲氧基取代的化合物其活性高于其他取代基的活性,如氟苯基或邻甲氧苯化合物的IC50与对照抗肿瘤药阿霉素相当,具有潜在的研究价值。初步药理筛选结果表明,氟喹诺酮C-3羧基并非是抗肿瘤活性所必要的药效团,用稠杂环不饱和酮替代有利于提高其抗肿瘤活性,为抗肿瘤氟喹诺化合物分子的构建提供新思路。
