腹腔镜下全面分期手术治疗早期卵巢癌疗效观察
2018-02-10仝玉珠
仝玉珠
(许昌市中医院妇产科,河南 许昌 461000)
卵巢癌是常见的女性生殖系统肿瘤,其发病率在女性生殖系统肿瘤中居第3位,但其病死率则位于第1位,对女性的生命造成严重威胁[1]。早期卵巢癌患者症状不明显,大部分患者在确诊时已处于晚期。临床研究表明,早期卵巢癌和晚期卵巢癌患者治疗后的5 a生存率差别较大[1-2]。因此,尽早诊断并治疗能够有效改善卵巢癌患者的生存率。目前,随着腹腔镜技术的广泛应用,国外有学者对早期卵巢癌患者采取腹腔镜下分期手术,具有一定的疗效[3]。但又有文献报道,腹腔镜下全面分期手术治疗早期卵巢癌并发症较多[4]。为进一步了解腹腔镜下手术治疗早期卵巢癌的可行性,本研究对比分析了腹腔镜下全面分期手术和开腹手术治疗早期卵巢癌的安全性及远期随访情况,现报道如下。
1 资料与方法
1.1一般资料选择2008年3月至2012年3月在许昌市中医院行全面分期手术治疗的86例早期卵巢癌患者为研究对象,患者均予以病理检查后确诊,并根据国际妇产科联盟分期标准(2013年)评估为Ⅰ~Ⅱ期患者[5]。全部患者按照手术方式分为开腹组和腹腔镜组。开腹组38例,年龄37~62岁(49.2±11.5)岁;体质量指数19.2~27.1(22.9±3.8)kg·m-2;肿瘤直径3.2~9.8 (7.8±3.9)cm;肿瘤分化程度:高分化10例,中分化9例,低分化19例;病理类型:子宫内膜样腺癌5例,黏液性癌3例,浆液性癌19例,透明细胞癌3例,低分化腺癌2例,混合型癌6例。腹腔镜组48例,年龄39~65(51.3±10.6)岁;体质量指数为19.8~27.6(23.1±3.5)kg·m-2;肿瘤直径2.5~9.7 (7.6±3.4)cm;肿瘤分化程度:高分化12例,中分化11例,低分化25例;病理类型:子宫内膜样腺癌6例,黏液性癌4例,浆液性癌26例,透明细胞癌4例,低分化腺癌3例,混合型癌5例。全部患者肿瘤病灶仅局限于卵巢,均无腹膜、大网膜及其他部位的肿瘤转移灶,无腹水症状。2组患者的年龄、体质量指数、肿瘤直径、肿瘤分化程度、病理类型比较差异无统计学意义(P>0.05),具有可比性。
1.2手术方法腹腔镜组患者采取腹腔镜下全面分期手术,患者全身麻醉,取膀胱截石位,经阴道放置举宫器。于患者脐下1 cm处取一切口,将气腹穿刺针置入,建立CO2气腹,气腹压力维持在1.8~1.9 kPa,置入直径为10 mm的套管针和腹腔镜光源镜,在患者右下腹麦氏点取一5 mm小切口用于助手操作,并分别在左下腹麦氏点和腹直肌外侧缘平脐位置取5 mm和10 mm切口,作为操作孔。术中首先探查腹腔,观察肿瘤的部位、质地及包膜情况,术中行快速冰冻病理检查,对于确诊且有生育需要者,予以切除患侧卵巢、大网膜、阑尾及盆腔淋巴结,并对另一侧的卵巢进行病理活检;无生育需要者,则予以切除子宫、双侧附件、大网膜、阑尾、盆腔及腹主动脉旁淋巴结。如患者在术中快速冰冻病理检查显示正常而术后病理检查确诊为卵巢癌,则采取再分期手术进行治疗。主要手术步骤如下:(1)将腹水或盆腔冲洗液进行细胞学检测,切除单、双侧附件行快速冰冻病理检查,或对卵巢动静脉进行高位结扎,切除病变一侧附件放入标本袋扎紧后放置在右侧髂窝位置;(2)将子宫切除并自阴道取出,同时将留置在右侧髂窝位置的附件标本、切除的盆腔淋巴结、腹主动脉旁淋巴结一并取出;(3)切除横结肠以下的大网膜及阑尾;(4)对结肠旁沟及盆侧壁腹膜进行多点活检;(5)对阴道残端进行关闭缝合;(6)对创面止血后进行冲洗,并置入引流管。开腹组患者全身麻醉下行开腹全面分期手术。在患者下腹部正中旁取一切口后进行手术,首先对腹腔情况进行探查,其余手术步骤及范围操作同腹腔镜组。2组患者术后均予以3~6个疗程的化学治疗。
1.3观察指标(1)2组患者的手术一般情况和住院时间。手术一般情况包括手术时间、术中出血量、腹主动脉旁淋巴结切除数、盆腔淋巴结切除数、子宫切除例数、肛门排气时间、术毕至下床时间、引流管留置时间、疼痛视觉模拟评分[6]。(2)2组患者术后并发症发生情况,包括术后发热、下肢浅静脉血栓、呕吐、尿潴留、感染等。(3)2组患者随访期间的复发率及5 a生存率。
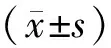
2 结果
2.12组患者手术一般情况及住院时间比较结果见表1。腹腔镜组患者均手术顺利,无中转开腹病例。2组患者手术时间、腹主动脉旁淋巴结切除数、子宫切除例数比较差异无统计学意义(P>0.05);腹腔镜组患者术中出血量低于开腹组,盆腔淋巴结切除数多于开腹组,差异均有统计学意义(P<0.05)。术后腹腔镜组患者肛门排气时间、术毕至下床时间、引流管留置时间及住院时间显著短于开腹组,疼痛视觉模拟评分低于开腹组,差异有统计学意义(P<0.05)。
2.22组患者术后并发症发生率比较开腹组患者术后发热2例,下肢浅静脉血栓2例,尿潴留1例,感染3例,术后并发症发生率为21.1%(8/38);腹腔镜组患者术后发热4例,下肢浅静脉血栓1例,呕吐1例,感染1例,术后并发症发生率为14.6%(7/48);2组患者术后并发症发生率比较差异无统计学意义(χ2=0.622,P>0.05)。
2.32组患者随访情况比较全部患者均获随访,随访时间6~86个月。随访期间,开腹组患者复发6例,复发率为15.8%;腹腔镜组患者复发8例,复发率为16.7%;2组患者的复发率比较差异无统计学意义(χ2=0.010,P>0.05)。开腹组和腹腔镜组患者5 a生存率分别为84.2%(32/38)和83.3%(40/48),2组患者5 a生存率比较差异无统计学意义(χ2=0.436,P>0.05)。
3 讨论
目前,腹腔镜手术在妇科手术领域中的应用已十分广泛,但将腹腔镜技术应用于卵巢癌的治疗目前仍然存在一定的分歧。有文献报道显示,腹腔镜手术治疗卵巢癌通常因治疗不彻底而导致临床疗效不佳,同时在治疗过程中,可造成肿瘤包膜破裂、CO2气腹扩散或切口种植而导致肿瘤转移风险增加[7]。本研究中腹腔镜组均手术顺利,无中转开腹病例,这可能与本研究选择的早期卵巢癌患者的肿瘤直径均在10 cm以下有关,肿瘤直径较小,从而降低了因肿瘤体积较大而在腹腔镜手术中发生肿瘤破裂的风险,减少了中转开腹的发生率。
本研究结果显示,2组患者的手术时间、腹主动脉旁淋巴结切除数、子宫切除例数比较差异无统计学意义,而腹腔镜组患者术中出血量显著低于开腹组,盆腔淋巴结切除数多于开腹组。有研究显示,腹腔镜手术时间较传统开腹手术明显延长或差异不明显,这主要与临床医生对手术的熟练度、手术配合效果及冰冻病理检查时间等因素有一定关系[3-4,8]。同时,在腹腔镜下,患者盆腔内组织显示较为清晰,从而能够对紧贴的邻近组织或器官的淋巴组织进行彻底清除。同时,本研究结果显示,腹腔镜组患者术后肛门排气时间、术毕至下床时间、腹腔引流管留置时间及住院时间显著短于开腹组,疼痛视觉模拟评分低于开腹组,且2组患者术后并发症发生率比较差异无统计学意义。由于腹腔镜手术属于微创,且在术中对胃肠道的影响较小有关,故患者恢复较快;而且腹腔镜下治疗早期卵巢癌患者的术后安全性与开腹手术较为一致,且本研究中未出现大血管损伤或邻近血管及组织损伤的情况。
NASU等[9]报道显示,早期卵巢癌分期手术中,患者的术后复发率约为6.2%,但本研究中开腹组和腹腔镜组患者的复发率分别为15.8%和16.7%,考虑这与本研究中肿瘤低分化患者较多有关。有研究显示,早期卵巢癌患者治疗后5 a生存率较高[10]。本研究结果显示,2组患者的5 a生存率均较高,且2组患者的5 a生存率比较差异无统计学意义。
综上所述,腹腔镜下全面分期手术治疗早期卵巢癌患者较开腹手术具有出血少、创伤小、术后恢复快等优点,且其术后并发症、复发率及5 a生存率与开腹手术比较差异不明显,可作为一种治疗早期卵巢癌的有效方法。但在早期卵巢癌的具体治疗过程中,需要严格按照手术适应证来选择治疗方式,对于肿瘤体积较大的患者仍需要采取开腹手术进行治疗。
