依托考昔引起皮肤不良反应的文献分析
2018-02-05许娟娟
唐 静,许娟娟
0 引言
皮肤的药物不良反应(Cutaneous adverse drug reactions,CADR)包括轻度斑丘疹的皮疹(Mild maculopapular exanthems,MPE),固定性药疹(Fixed drug eruption,FDE),史蒂文斯-约翰逊综合征(Stevens-Johnson Syndrome,SJS),中毒性表皮坏死松解症(Toxic epidermal necrolysis,TEN),药物反应与嗜酸性粒细胞、全身症状(Drug reaction with eosinophilia and systemic symptoms,DRESS)和急性全身发疹样脓疱症(Acute generalized exanthematous pustulosis,AGEP)等[1]。依托考昔(Etoricoxib)是一种高选择性环氧化酶-2(COX-2)抑制剂,COX-2主要参与前列腺素的产生,而前列腺素可引起疼痛、炎症和发热等,依托考昔因其良好的止痛疗效、高抗炎活性、较低的胃肠道刺激性,以及对COX-2/COX-1的高选择性,在临床应用日益广泛。笔者对依托考昔所致的皮肤不良反应文献进行分析,以期为临床用药提供参考。
1 资料与方法
以“依托考昔”、“不良反应”、“皮肤不良反应”、“药疹”为中文关键词,以“etoricoxib”、“drug adverse reaction”、“cutaneous adverse drug reactions(CADR)”、“drug eruption”为英文主题词,分别检索CNKI、万方数据库、PubMed、EMBase数据库,时间范围为从建库至2016年12月。利用Excel软件对入选的文献进行分析,包括性别、年龄、原患疾病、药物过敏史、给药剂量、临床表现、出现时间等方面。
2 结果
2.1 文献基本情况 通过检索共获得文献14篇,其中中文文献3篇,英文文献11篇,共得到有效病例15例。其中,男6例(40%),女9例(60%);平均年龄(52.8±11.74)岁,最小31岁,最大69岁,具体情况见表1。
2.2 CADR类型 依托考昔出现的CADR以FDE(7例)、TEN(3例)为主,还有AGEP(1例)、麻疹样药疹(2例)、全身严重脱屑性药疹(1例),有1例为TEN合并SJS,严重CADR比例较高。见表2。
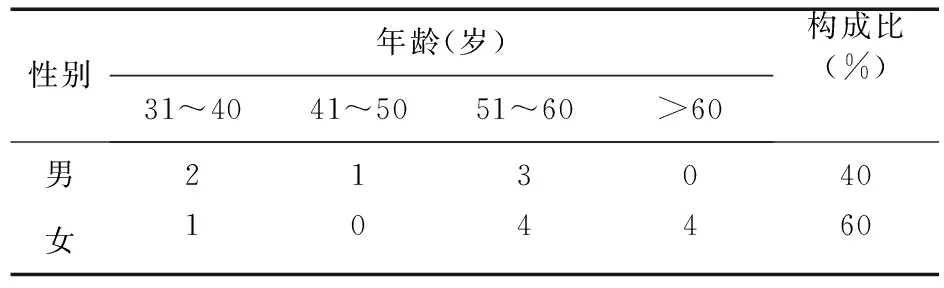
表1 依托考昔CADR患者的年龄和性别分布
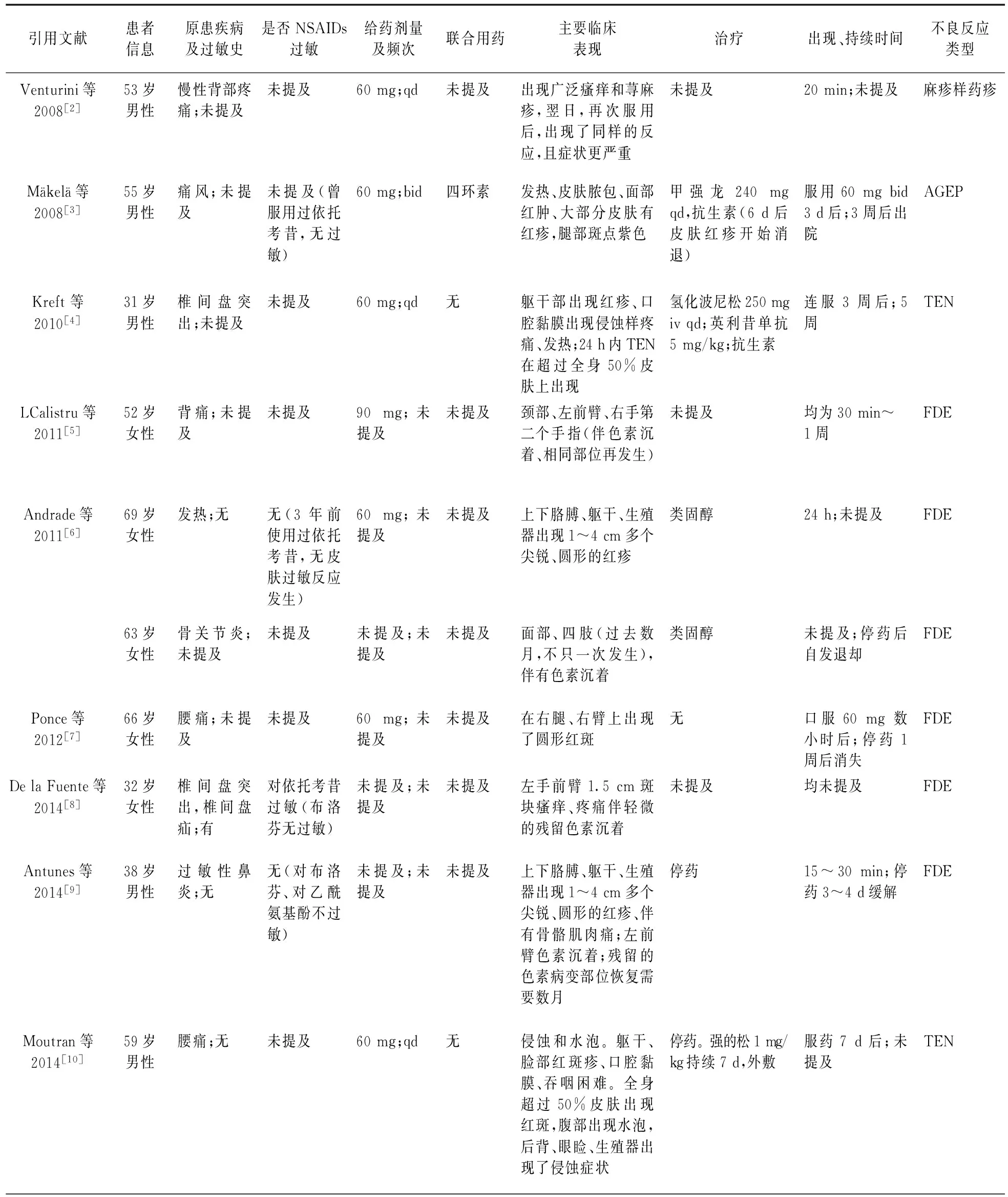
表2 依托考昔不良反应病例基本情况
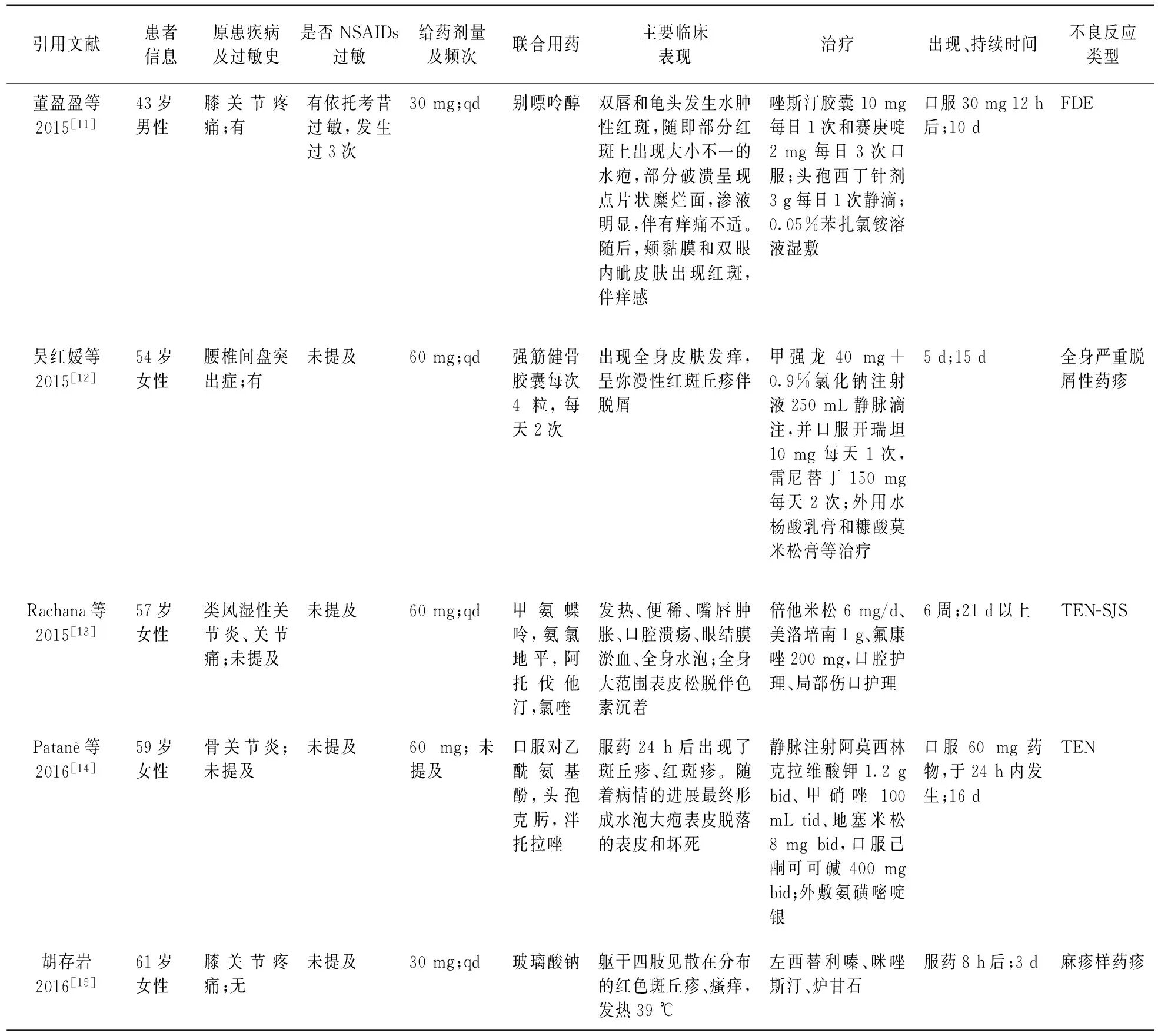
续表
2.3 CADR与原患疾病、药物过敏史 本研究的病例中,以痛风、骨关节病患者居多,均能遵照适应证用药。其中,有3例有药物过敏史,具体药物均未提及,有4例无药物过敏史,余下病例均未提到是否有药物过敏史。有2例对NSAIDs药物有过敏史,另有2例曾经使用过NSAIDs药物不过敏,使用依托考昔后过敏。从表2中可以看出,无药物过敏史的患者使用依托考昔后有一定几率发生CADR,而有使用NSAIDs过敏的患者,CADR发生率较高。Dona等[16]研究发现,对NSAIDs过敏的患者,有1/4的患者对COX-2抑制剂不耐受,易出现过敏现象。药师可以根据药物过敏史,对此类不良反应给予重视。
2.4 用药情况 依托考昔说明书关节炎、骨关节炎推荐剂量为30 mg每日1次,病情不能缓解可增加至60 mg每日1次;急性痛风性关节炎推荐剂量为120 mg每日1次,最长使用8 d。从给药剂量看,本研究中,除3例未注明使用剂量,余下12例每日使用剂量在30~90 mg之间;从给药频次看,7例未注明给药频次,1例给药剂量为60 mg每日2次,与说明书规定不符,余下均为每日给药1次;有6例在常规用法用量和规范用药的情况下出现了CADR不良反应。有6例患者有合并用药情况,均在发生CADR后给予了停药措施,合并用药是否会增加CADR的发生,有待进一步探讨。
2.5 CADR发生时间分布 依托考昔CADR最快发生时间在用药20 min后,最迟为连续服药6周后,CADR发生时间跨度较大,为临床的判断增加了难度,应引起临床医药人员的高度重视。
2.6 不良反应预后 依托考昔引起的不良反应以严重的居多,对原患疾病都造成一定影响,在不同程度上导致患者住院或增加了住院天数,且因CADR引起皮肤受累部位的色素沉着现象需要3个月甚至更长时间才能缓解。
3 讨论
药物引起的皮肤不良反应是药物不良反应的一种,此类CADR以抗癫痫药卡马西平、苯妥英钠,痛风药别嘌呤醇、NSAIDs、表皮生长因子受体抑制剂、抗生素类等药物的相关报道较多。
3.1 依托考昔导致CADR的临床特点和治疗 从笔者收集的关于依托考昔CADR的信息源看,我国报道的文献资料较少且以近2年报道为主,国外报道较多,这可能与其在2013年在我国获得批准文号,临床使用逐渐增多,CADR逐渐显现有关。
在依托考昔引发的CADR中,以50岁以上中老年居多,这可能与中老年患者关节炎、痛风发病率较高,依托考昔使用率增高,同时中老年人代谢水平降低,造成药物的蓄积作用有关;从性别分布上看,女性略多于男性,由于本研究纳入的病例数不多,性别对CADR的影响需进一步的观察。
本研究中,FDE的发病常以皮肤瘙痒、出现红斑起病较多,以四肢、生殖器部位出现频率较高,有2例再次服用后在相同部位再次发生类似症状。TEN疾病临床表现为表皮大片脱落,临床上常认为TEN和SJS是同一种疾病的不同表现形式,皮肤脱落大于体表面积30%为TEN,少于10%为SJS,介于10%~30%者为SJS与TEN共存[17],本研究中,除了皮肤变化,还常伴有发热、口腔黏膜侵蚀样疼痛等症状,且疾病进展较快。
本研究中依托考昔导致的FDE的治疗,以抗过敏药、类固醇药治疗为主,辅以外用制剂。TEN疾病的治疗较为复杂,以抗过敏、抗感染治疗、激素治疗为主,同时配合营养支持、皮肤护理等方法,其中激素冲击治疗尚存在争议,有研究发现,冲击治疗除非在大面积皮肤损害发生之前使用,否则可能增加脓毒血症并发症的风险[18]。
3.2 依托考昔引起CADR的发生机制 固定性药疹以每次发病常于相同部位出现皮损为特征,再次服用同类药物后于相同部位再发皮损,皮损逐渐增多,症状逐渐加重。Andrade等[19]研究发现,NSAIDs易引发固定性药疹,在依托考昔引起的大泡性FDE患者中,CD8+T细胞是主要的效应性T细胞[20],CD4+T细胞、B细胞浸润较少。TEN病原学尚不清楚,可能与药物诱导的免疫机制有关,CD8+T细胞、细胞凋亡因子FasL、颗粒溶素是影响TEN疾病的关键物质,有研究显示,在TEN的早期,药物活性代谢产物对角质形成细胞有直接细胞毒性作用,会导致T细胞内CD2+浓度升高,T细胞活化,细胞毒性T细胞使自身淋巴细胞或皮肤角质形成细胞发生死亡,进而损伤相应细胞的活性,但其具体的作用机制仍需进一步的研究[21]。
3.3 依托考昔CADR与基因多态性 近年的研究证实,一些过敏性疾病人群可能与FCER1A、FCER1B、FCER1G、HDC、DAO、HNMT等基因多态性存在联系,这些优势基因会对IgE受体和组胺代谢酶主导的信号通路造成影响[22],从而增加了部分人群对药物的敏感性。本文中依托考昔CADR与HLA基因、白三烯相关基因、嗜酸粒细胞相关基因以及与代谢相关酶的基因多态性有关,不同人群HLA等位基因的多态性及表型决定了不同药物所致的皮肤损伤,Yang等[1]研究发现,在中国汉族人群中,HLA-B*15∶02、HLA-B*58∶01、HLA-B*59∶01和HLA-B*13∶01与皮肤不良反应发生有关;而HLA、IKZF1基因多态性可能与TEN的发病有关[23]。
3.4 临床用药注意事项 英国药品和健康产品管理局(MHRA)在2016年10月发布药品安全提示信息称,依托考昔使用的风险包括:增加冠状动脉和血栓形成事件、心力衰竭、高血压以及水肿(与安慰剂和一些非甾体抗炎药相比),其他需要考虑的重要风险还包括对胃肠风险。
依托考昔属于上市不久的新药,在我国人群的应用中,可能存在未知的风险,需要对此给予重视。该药在使用过程中,要询问患者是否有药物过敏史,特别是对有NSAIDs类过敏史的患者,在用药过程中应特别注意是否存在发生过敏反应的风险。同时,临床药师应了解该药常见、罕见的不良反应,在使用过程中要注意观察、监测,尤其是对中老年患者。
4 小结
CADR临床表现类型及特点多、致病机制复杂,严重CADR发生比例较高,在用药前应注意询问患者家族史、药物过敏史,用药的过程中剂量、频次应合理,且用药期间应定期观察患者情况,加强对患者的用药教育。本文通过对依托考昔引起的CADR进行分析,旨在做好依托考昔ADR监测和防治工作,提高临床用药的安全性。
[1] Yang F,Yang Y,Zhu Q,et al.Research on susceptible genes and immunological pathogenesis of cutaneous adverse drug reactions in Chinese Hans[J].J Investig Dermatol Symp Proc,2015,17(1):29-31.
[2] Venturini DM,De la Parra S SJ,Segura AN.Selective immediate hypersensitivity to etoricoxib[J].J Investig Allergol Clin Immunol,2008,18(6):485-487.
[3] Mäkelä L,Lammintausta K.Etoricoxib-induced acute generalized exanthematous pustulosis[J].Acta Derm Venereol,2008,88(2):200-201.
[4] Kreft B,Wohlrab J,Bramsiepe I,et al.Etoricoxib-induced toxic epidermal necrolysis:successful treatment with infliximab[J].J Dermatol,2010,37(10):904-906.
[5] Calistru AM,Cunha AP,Nogueira A,et al.Etoricoxib-induced fixed drug eruption with positive lesional patch tests[J].Cutan Ocul Toxicol,2011,30(2):154-156.
[6] Andrade P,Gonçalo M.Fixed drug eruption caused by etoricoxib--2 cases confirmed by patch testing[J].Contact Dermatitis,2011,64(2):118-120.
[7] Ponce V,Muoz-Bellido F,Moreno E,et al.Fixed drug eruption caused by etoricoxib with tolerance to celecoxib and parecoxib[J].Contact Dermatitis,2012,66(2):107-108.
[8] De la Fuente EG,Pampín FA,Caro GD,et al.Fixed drug eruption due to etoricoxib in a patient with tolerance to celecoxib:the value of patch testing[J].Actas Dermosifiliogr,2014,105(3):314-315.
[9] Antunes J,Prates S,Leiria-Pinto P.Fixed drug eruption due to etoricoxib-a case report[J].Allergol Immunopathol (Madr),2014,42(6):623-624.
[10]Moutran R,Maatouk I,Hélou J.Etoricoxib-induced toxic epidermal necrolysis[J].Int J Dermatol,2014,53(4):e275-e277.
[11]董盈盈,陈岚,段铱,等.依托考昔致固定性药疹国内首报及文献复习[J].实用皮肤病学杂志,2015,8(6):419-421.
[12]吴红媛,宗黎琼.依托考昔片合用强筋健骨胶囊致1例全身严重脱屑性药疹[J].药学与临床研究,2015,(5):508.
[13]Rachana PR,Anuradha HV,Mounika R.Stevens Johnson syndrome-toxic epidermal necrolysis overlap secondary to interaction between methotrexate and etoricoxib:a case report[J].J Clin Diagn Res,2015,9(7):FD01-FD03.
[14]Patanè M,Isola S,Gangemi S,et al.Mucosal exfoliation as a selective reaction to etoricoxib[J].J Clin Pharm Ther,2016,41(6):722-724.
[15]胡存岩.依托考昔致麻疹样药疹1例[J].世界最新医学信息文摘,2016,16(96):225.
[16]Doa I,Blanca-López N,Jagemann LR,et al.Response to a selective COX-2 inhibitor in patients with urticaria/angioedema induced by nonsteroidal anti-inflammatory drugs[J].Allergy,2011,66(11):1428-1433.
[17]Poletti-Jabbour J,Wiegering-Rospigliosi A,Pereyra-Elías R,et al.Carbamazepine and oxcarbazepine:reflections after an oxcarbazepine-induced Stevens-Johnson syndrome/toxic epidermal necrolysis overlap[J].Eur J Clin Pharmacol,2016,72(8):1031-1032.
[18]陈晨,江祎,师少军,等.奥卡西平致Stevens-Johnson综合征和中毒性表皮坏死松解症的特点及基因相关性分析[J].中国药房,2017,28(5):620-625.
[19]Andrade P,Brinca A,Gonçalo M.Patch testing in fixed drug eruptions--a 20-year review[J].Contact Dermatitis,2011,65(4):195-201.
[20]Duarte AF,Correia O,Azevedo R,et al.Bullous fixed drug eruption to etoricoxib--further evidence of intraepidermal CD8+T cell involvement[J].Eur J Dermatol,2010,20(2):236-238.
[21]Gao TT,Long Q.Recent progress in research of pathogeneses of Stevens-Johnson syndrome and toxic epidermal necrolysis[J].Zhonghua Yan Ke Za Zhi,2016,52(9):708-713.
[22]Amo G,Cornejo-García JA,García-Menaya JM,et al.FCERI and histamine metabolism gene variability in selective responders to NSAIDS[J].Front Pharmacol,2016,7:353.
[23]Ueta M,Sawai H,Sotozono C,et al.IKZF1,a new susceptibility gene for cold medicine-related Stevens-Johnson syndrome/toxic epidermal necrolysis with severe mucosal involvement[J].J Allergy Clin Immunol,2015,135(6):1538-1545,e17.
