自由基引发剂对环糊精整体柱手性分离能力的影响研究
2018-01-30郭嘉亮汪锦才邓秋莹欧阳永中李艳萍黄文柱
郭嘉亮,汪锦才 ,邓秋莹 ,欧阳永中 ,严 文,李艳萍,黄文柱
(1.佛山科学技术学院医药工程学院,广东 佛山 528000; 2.广东药科大学,广东 广州 510006;3.广东省佛山市第五人民医院,广东 佛山 528000)
整体材料(monolith)由于具有通透性强、传质快、反压低、易于制备与修饰等优势,被广泛应用于多个分离科学领域[1],被誉为“第4代色谱分离介质”。随着固载方法的进步,将重要的手性拆分剂环糊精(β-cyclodextrin,β-CD)固定于石英毛细管整体柱上制备而成的“环糊精整体柱”,因可避免制塞的难题而得到快速发展,尤其在手性药物的分离分析领域有举足轻重的地位,并在富集、固相萃取等方面发挥着越来越重要的作用[2-4]。
近年来,β-环糊精整体柱的制备研究成了相关研究领域的重点与热点[5]。本课题组一直致力于环糊精有机聚合物整体柱的制备工艺研究[5-7],对包括交联剂、致孔剂、间隔臂、制备策略在内的多种因素对其手性分离能力的影响进行了一系列探讨。现有的环糊精有机聚合物整体柱,如丙烯酸酯类(acrylates)、丙烯酰胺类(acrylamides)和苯乙烯类(styrenes)等[2],一般通过“原位”(in situ)自由基聚合方式实现,故自由基引发剂(radical initiator)作为单体进行聚合反应的起源,对整体材料的聚合情况产生重要作用,对其色谱学性能也有不可忽视的影响。当前制备β-环糊精的甲基丙烯酸酯类整体柱采用的引发剂主要为偶氮类引发剂偶氮二异丁腈(azobisisobutyronitrile,AIBN)[6-8]。它有油溶性,其—N=N—双键易于分裂并生成高活化能的自由基;同时,反应稳定,属一级反应,只产生一种自由基,无其他副反应产生,因此易控制且基本不发生诱导分解。然而,由于水溶性不佳,AIBN在制备整体柱时,难以用于强溶剂极性的聚合体系。据了解,另一种水溶性的偶氮引发剂偶氮类引发剂2,2′-偶氮二异丁腈脒二盐酸盐[2,2′-Azobis(2-methylpropionamide)dihydrochloride,AIBA]可克服 AIBN水溶性差等缺点,但目前仍未见AIBA用于环糊精有机聚合物整体柱的制备研究。
因此,本研究中首次采用AIBN和AIBA 2种性质不同的自由基引发剂,以单-6-乙二胺基-β-环糊精(6-EDA-β-CD)为手性选择剂,分别制备获得了2款不同的 100 μm内径毛细管整体柱 poly(GMAEDA -β -CD -co-MBA)(Column A 和 Column B),并进行系统对比,以分析不同引发剂对环糊精整体柱各种性能(尤其是手性分离能力)的影响。
1 仪器与试药
1.1 仪器
Vario EL元素分析仪(德国Elementar公司);Merlin高分辨场发射扫描电子显微镜(德国Zeiss公司);DSC 214差示扫描量热仪(德国Netzsch公司);DiNa-S纳流泵(日本KYA公司);100 μm内径弹性熔融石英毛细管(河北锐沣色谱器件公司)。
1.2 主要试剂
N,N′-亚 甲 基 双 丙 烯 酰 胺 (N,N′-methylene bisacrylamide,MBA)、甲基丙烯酸缩水甘油酯(Glycidyl methacrylate,GMA)、AIBN、AIBA、4-氯-扁桃酸、2-溴-扁桃酸、2-(3-氯苯氧基)丙酸、2-苯氧基丙酸、布洛芬、舒洛芬均购自阿拉丁试剂(上海)有限公司;单-6-乙二胺基 -β-环糊精(6-EDA-β-CD)购自山东滨州智源生物科技有限公司。
2 方法和结果
2.1 毛细管整体柱的制备
毛细管预处理:参考文献[9],以1 mol/L的氢氧化钠、去离子水、甲醇(MeOH)、γ-甲基丙烯酸氧丙基三甲氧基硅烷(γ-MAPS)和MeOH的混合液先后冲洗石英毛细管,得预处理好的毛细管空管,氮气吹干,待用。
整体柱制备:参考文献[7,10]所报道的混合物配比,分别将适量的单体化合物 6-EDA-β-CD和GMA,助溶剂二甲基亚砜(DMSO),致孔剂MeOH混合,加热至60℃反应30 min;加入交联剂MBA和引发剂(AIBN或AIBA);灌入预处理好的毛细管空管中,封闭,继续加热进行自由基聚合反应;最后,用MeOH冲洗掉毛细管内部未反应物、残留溶剂、低聚杂质等,得到相关的整体柱 Column A(AIBN引发)与 Column B(AIBA引发)整体柱(制备过程见图1)。同时,考察各个节点的反应温度和时间变化的影响。
2.2 引发条件的优化
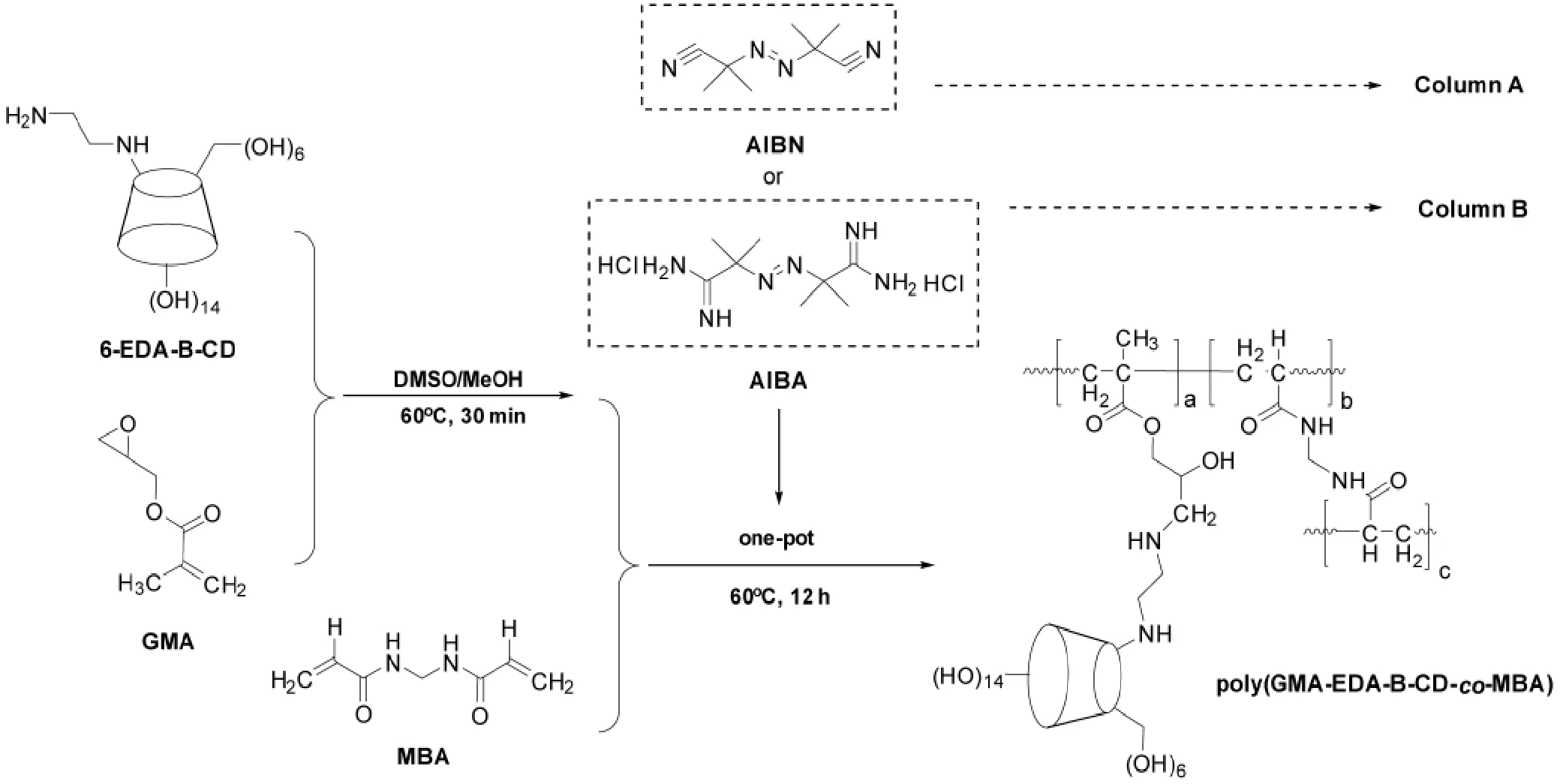
图1 Column A和Column B制备过程
环糊精整体柱的优化方法参考本课题组的前期工作[6-7]。对引发剂使用量的研究结果显示,引发剂用量增多,反应加快,即无论是AIBN还是AIBA,成核与核聚结速率均明显变快,且用量为单体质量的2%时效果最佳。此外,还重点考察了引发温度和引发时间的影响,优化方案见表1。AIBA所引发的原位聚合反应,温度和时间对引发效果的影响非常明显。如以温度为55℃为例,反应时间为6~24 h,整体柱聚合不佳,过于疏松(too slack),说明 55℃下 AIBA无法充分引发聚合反应;当温度升至60℃时,整体柱聚合情况大为改善;当反应时间为6 h时,内部聚合最均匀,通透性良好,内部孔道相互贯通,形成一个网状结构,但24 h后则变得太紧(too hard),结构过于严密,无法形成有效的传质;升温至65℃后,制备得到的整体柱聚合物均呈凝胶状态(gel),背压(backpressure)非常高。故选择反应温度为60℃,反应时间为6 h作为引发剂AIBA的引发条件,较之引发剂AIBN引发速率更快,聚合时间需要更短(Column B 为 6 h,而 Column A 为 12 h)。
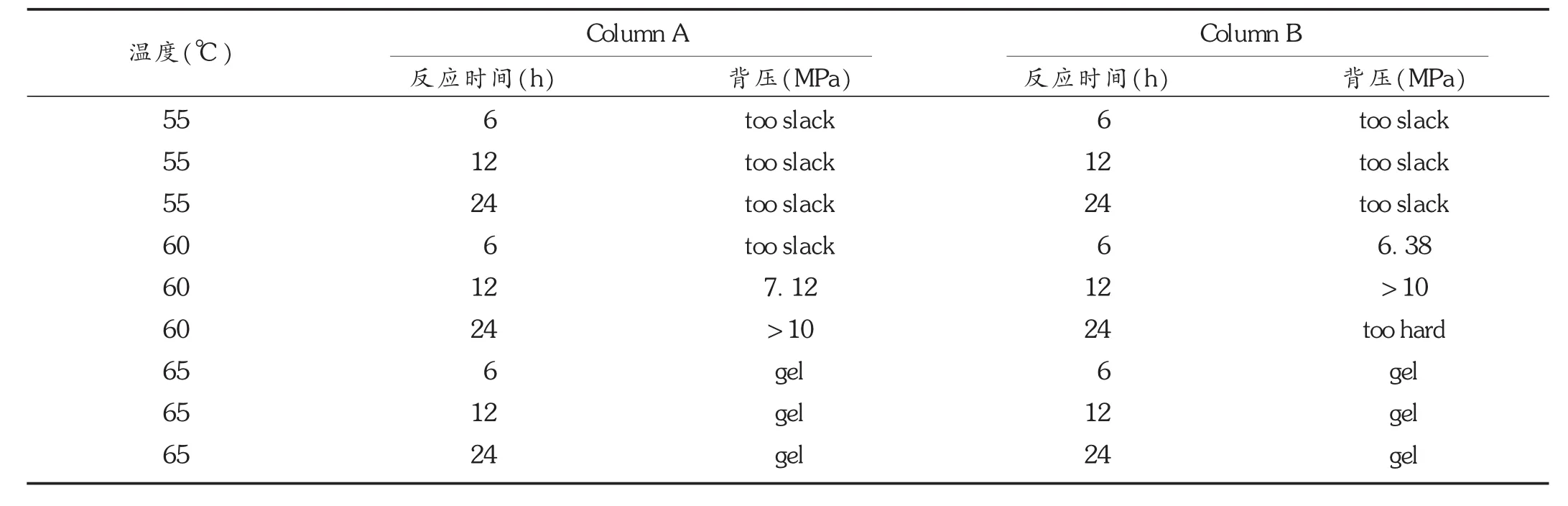
表1 Column A和Column B引发温度与时间优化表
2.3 整体柱的化学表征
2.3.1 差示扫描量热分析
[5]的具体操作,通过差示扫描量热(DSC)分析来测定整体柱聚合物材料的热稳定性,初步推断β-环糊精是否成功键合在整体柱骨架材料上。差示扫描量热分析结果显示,整体材料具有良好的热稳定性,310℃处有明显的吸热峰,分析为β-环糊精的热分解峰[5],可大致判断β-环糊精成功键合在交联聚合物上。
2.3.2 元素分析
通过元素分析的结果考察,采用不同引发剂制备得到的Column A与Column B整体柱的组成。结果见表2。可见,Column A与Column B中6-EDA-β-CD的含量基本一致,Column B中环糊精含量略高。
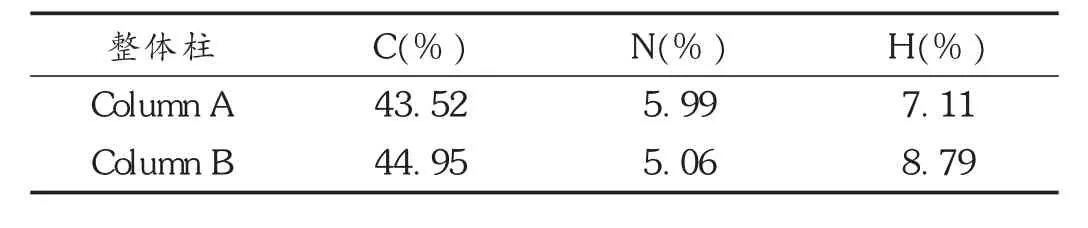
表2 Column A和Column B的元素分析测定结果
2.4 整体柱的物理表征[6-7]
2.4.1 通透性和重复性
整体柱的通透性数据是衡量其性能的重要依据之一。以不同流动相[乙腈、甲醇、乙腈-水(等体积)]作比对,并根据 Darcy方程公式计算而得[6]。以乙腈为例,Column A和 Column B的通透性分别为 6.70×10-14m2和 3.10×10-14m2;以甲醇为例,Column A 和 Column B的通透性分别为 6.40 ×10-14m2和 2.37 ×10-14m2;以乙腈-水为例,Column A和Column B的通透性分别为4.80 ×10-14m2和 1.96 ×10-14m2。上述结果表明,两者均具有较好的通透性(同一数量级),并未随流动相的改变而发生显著的形变或溶胀。这也从侧面反映了柱子具有稳定性良好的骨架结构。
此外,以乙腈 -水(50∶50,V∶V)为流动相,甲苯和硫脲作为测试化合物,测定Column A与Column B的范迪姆特方程曲线(图 2)。Column B在最佳线性流速(0.381 mm /s)下其理论板高为 26.03 μm,曲线斜率较大,呈“斜坡状”,说明其在高流速下理论板数较低;Column A在最佳线性流速(0.424 mm/s)下的理论高度为21.49 μm,曲线斜率较小,这说明其在较高的流速下仍能保持较理想的理论板数,更有利于快速分离。可见,Column A比Column B更适宜快速分离分析。此外,还对Column A和 Column B的重复性,包括 day-to-day(n=3)、 batch-to-batch(n=5)、 column-to-column(n=10)进行了考察。结果相对标准偏差(RSD值)均在5%以下,表明方法重复性良好,且尝试连续进针30 d以后,未出现较大误差。
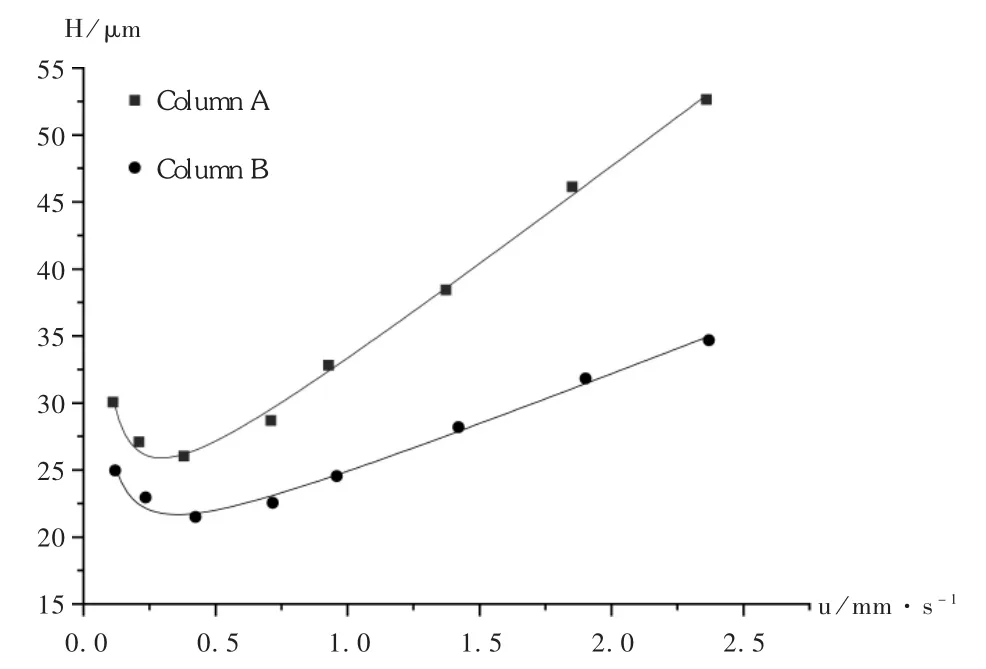
图2 Column A和Column B的范迪姆特方程曲线
2.4.2 扫描电镜分析
对比Column A和Column B毛细管横截面的扫描电镜情况,见图3。发现两者孔状分布较均匀,不同部位的基本型貌非常相似:不规则的球形结构堆积成其基本骨架,并形成典型的网状外观;同时与石英毛细管内壁结合紧密,整体聚合情况良好。但观察其微观形貌可发现聚合物形态仍有差异。Column A的聚合物在孔径和粒径分布上显然更均匀而明显;Column B的聚合物粒径内部结构相较Column A稍显疏松,聚合物颗粒黏连在一起,成核形态也不如Column A显著。结果表明,引发剂对整体柱的整体骨架无明显作用,但对其内部聚合情况有显著影响。骨架结构改变可减小传质阻力,降低整体柱背压,但具体形貌对高流速下的快速分析和分离效果更重要。

图3 Column A和Column B扫描电镜图
2.5 整体柱的色谱性能表征
2.5.1 保留机制研究
通过对比极性化合物保留机理的变化,有助于判断整体柱色谱性能。本研究中采用甲苯(非极性标志物)和硫脲(极性化合物)作为测试标准,乙腈和水为流动相,通过改变流动相中有机相与水相比例,考察Column A与Column B的极性保留因子(k)的变化。当乙腈含量从60%降低至30%时,甲苯的保留因子(k)显著增加,硫脲的保留因子基本不变;当乙腈含量从60%升高至90%时,甲苯的保留因子基本不变,硫脲的保留时间有所增长,可见,Column B与Column A整体柱的保留机理一致。研究结果证明,引发剂并未对整体柱骨架的极性及保留机理产生影响。
2.5.2 手性选择性评估
本研究中参考文献[7,10]的方法配制缓冲盐溶液,以4-氯-扁桃酸、2-溴-扁桃酸、2-(3-氯苯氧基)丙酸、2-苯氧基丙酸、布洛芬、舒洛芬6种手性药物及中间体作为评估对象,对Column A和Column B的手性拆分能力进行评估,考察引发剂对β-环糊精整体柱手性分离能力的影响。结果Column A和Column B对上述手性化合物基本实现基线分离,且分离时间较短(4~8 min),完全体现了整体柱在快速分离上的优势。Column A的手性分离效果明显优于Column B(表3)。以4-氯-扁桃酸为例,在分离条件一致的情况下,其在Column A和Column B整体柱上的分离度 Rs分别为5.03和 3.17,对应的分离因子 α分别为 1.90和 1.80。综合比较,Column A和Column B对几种酸性手性化合物的分离效果均较理想,但对碱性手性化合物却基本无法实现基线分离。
手性拆分能力为评价环糊精整体柱关键标准之一,Column A整体柱该能力优于Column B。可见,引发剂的性质同样能对整体柱的柱性能和手性分离能力造成影响,分解反应较平稳的脂溶性引发剂AIBN可能更适合β-环糊精有机聚合物整体柱的制备。分析其原因,应该是由于引发剂AIBN引发所形成的整体材料(ColumnA)虽然环糊精含量较低,但由于聚合反应的差异,材料表面上所暴露的有效环糊精却高于AIBA引发所形成的整体材料(Column B)。Column B尽管环糊精含量高,但可能由于包埋作用,实质上可用于手性分离的有效环糊精含量却不如Column A。
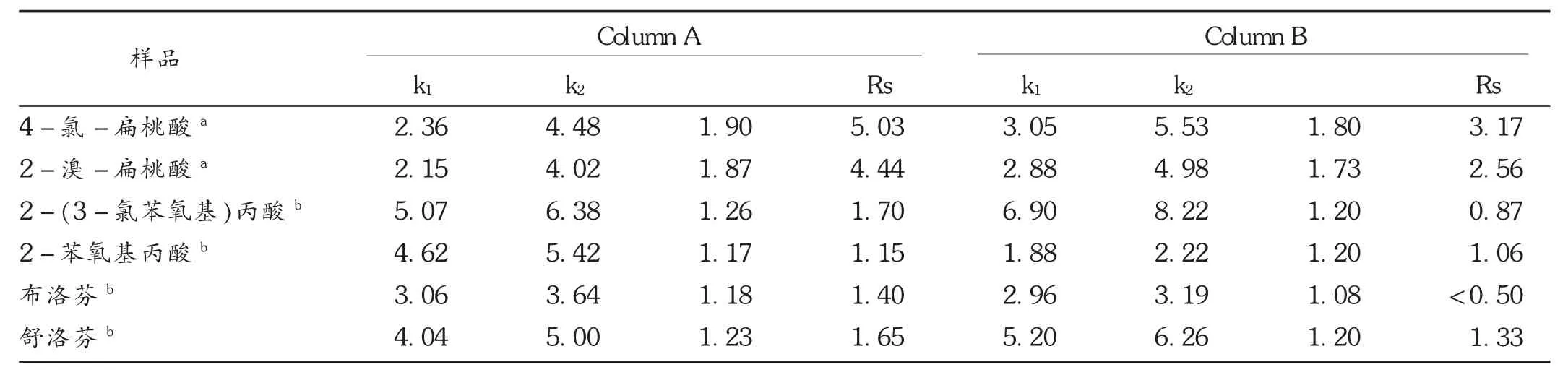
表3 6种手性化合物在Column A和Column B上的手性分离效果
3 讨论
近年来,引发剂对整体柱色谱性能的影响已有大量报道[11-13],并成为了有机整体柱研究领域的热点。然而,在手性整体柱研究领域,相关研究尚处于空白阶段。大分子手性配体如环糊精、奎尼丁、万古霉素等由于自身的理化性质,在整体材料固定化过程中,需考察大量制备因素,而自由基引发剂的选择将发挥重要作用。
本研究中创新性地取代常用的油溶性引发剂AIBN,以水溶性引发剂AIBA通过一锅法成功制备了整体柱Column B,并系统考察了引发剂用量、引发温度和引发时间等重要因素;通过表征整体柱的化学性质(差示扫描量热分析和元素分析)、物理性质(通透性、重复性和扫描电镜)以及色谱性能(保留机制和手性拆分评估),对Column A与Column B进行了全面对比。研究表明,2种引发剂的使用量为单体质量的2%时,效果最佳,且引发条件差异不大。Column B所需制备时间及键合环糊精的量也比较高;同时,其聚合物粒径内部结构较疏松,相对而言不如Column A理想。在关键的手性拆分效果上看,以AIBN为引发剂制备得到的Column A的实际分离效果明显优于以AIBA为引发剂制备得到的Column B。
综合两款整体柱的一系列对比结果进行判断,引发剂AIBA属水溶性偶氮类引发剂,在该致孔剂条件下,聚合速度快,反应条件更温和;但在水溶液聚合与乳液聚合过程中,对于有机聚合物的引发效果不佳,难以进行平和、稳定、可控制的分解反应,导致Column B整体柱内部的聚合物粒径较小,孔径分布不均匀。AIBN虽然水溶性较差,但在DMSO的助溶作用下,仍可达到相应的聚合效果。
本研究结果提示,引发剂对β-环糊精整体柱的手性分离能力有一定影响,选用水溶性引发剂虽可大幅缩短反应时间,但并不能改善β-环糊精整体柱的手性分离能力,脂溶性AIBN引发剂尽管反应时间稍长,但更适用于β-环糊精有机聚合物整体柱的制备。本研究为手性单体尤其是大极性手性单体的整体材料引发系统研究提供了科学的参考依据。后续研究将从具有相转移能力的引发剂着手,以期获得更加理想的引发系统。
参考文献:
[1]Svec F,Frechet JMJ.Continuous rods of macroporous polymer as high-performance liquid chromatography separation media[J].Anal Chem,1992,64(7):820 - 822.
[2]Zhang Z,Wu M,Wu R,et al.Preparation of perphenylcarbamoylated -cyclodextrin-silica hybrid monolithic column with″one - pot″approach for enantioseparation by capillary liquid chromatography[J].Anal Chem,2011,83(9):3616 - 3622.
[3]李英杰,张馨予,高立娣,等. -环糊精基氧化钨毛细管电色谱整体柱的制备及应用[J].化学试剂,2016,38(4):297 -300.
[4]李英杰,于春杰,高立娣,等.均苯四甲酸酐修饰 -环糊精微球电色谱柱的制备及应用[J].化学试剂,2015,37(6):552-554.
[5]Guo JL,Lin YJ,Xiao Y,et al.Recent developments in cyclodextrin functionalized monolithic columns for the enantioseparation of chiral drugs[J].J Pharmaceut Biomed,2016,130:110 - 125.
[6]Guo JL,Zhang QX,Peng YB,et al.A facile and efficient onestep strategy based on click chemistry for preparation of -cyclodextrin functionalized monoliths[J].J Sep Sci,2013,36(15):2441-2449.
[7]Guo JL,Xiao Y,Lin YJ,et al.Effect of the crosslinker type on the enantioseparation performance of -cyclodextrin functionalized monoliths prepared by the one-pot approach[J].J Chromatogr A,2016,1467:288 - 296.
[8]Zhang QX,Guo JL,Wang F,et al.Preparation of a - cyclodextrin functionalized monolith via a novel and simple one-pot approach and application to enantioseparations[J].J Chromatogr A,2014,1325(5):147 - 154.
[9]林苑靖,林 航,郭嘉亮.基于修饰环糊精的新型模拟酶反应器的制备[J].暨南大学学报(自然科学与医学版),2016,37 (6):454 - 459.
[10]Ghanem A,Ahmed M,Ishii H,etal.Immobilized - cyclodextrin -based silica vs polymer monoliths for chiral nano liquid chromatographic separation of racemates[J].Talanta, 2015, 132:301-314.
[11]Vlakh EG,Tennikova TB.Preparation of methacrylate monoliths[J].J Sep Sci,2007,30(17):2801 - 2813.
[12]Vaast A,Terryn H,Svec F,et al.Nanostructured porous polymer monolithic columns for capillary liquid chromatography of peptides[J].J Chromatogr A,2014,1374:171 - 179.
[13]Lubbad SH,Buchmeiser MR.Highly cross-linked polymeric capillary monoliths for the separation of low,medium,and high molecular weight analytes[J].J Sep Sci, 2009, 32(15 - 16):2521-2529.
