Chirp编码激励用于高频医学超声系统的实验及性能评价
2018-01-29张耀楠付强唐亮
张耀楠,付强,唐亮
1.西安思源学院 电子信息工程学院,陕西 西安 710038;2.东北大学 中荷生物医学与信息工程学院,辽宁 沈阳 110169
引言
当前市场主流的医学超声成像系统中,大多数均采用传统脉冲激励模式。脉冲激励模式下,因为发射时间极短,所以当发射的峰值声功率接近安全范围内最大值时,平均声功率仅为最大允许值的1%左右[1]。在这样的背景下,医学超声领域的研究者受雷达技术的启发,也采用了雷达技术中广泛应用的编码激励模式。该激励模式通过延长发射时间,在不增加发射能量峰值的前提下,增加了发射功率,改善了穿透深度等成像效果参数[2-11]。同时利用脉冲压缩技术,将回波信号进行解调,得到与传统脉冲激励信号持续时间相似,但是幅度远远增强的信号,进而改善了信噪比。
众所周知,分辨率和穿透深度一直是医学超声成像效果的重要评价参数,但医学超声成像设备一直面临着一个鱼和熊掌难以兼得的问题:较高的激励频率可以获得较好的分辨率,但是会牺牲一定的穿透深度;反之,较低的激励频率可以获得较深的穿透深度,但是分辨率会变差。造成以上现象的原因是根据超声波的衰减机制,频率越高,超声波的衰减越快,所以穿透深度越浅;反之,较低的成像频率会导致超声成像系统的分辨率变差。
针对以上情况,人们曾设想在满足医学要求的分辨率的情况下,通过增加换能器两端的电压来增加换能器输出的声波能量,进而达到增加穿透深度的目的。但FDA及各国的监管机构均对于超声成像系统的声波能量剂量有着更为严格的要求,在医用超声安全剂量的限制下,发射幅度不可以无限制增大,所以,为了传输更多能量,具有更长发射时间的超声编码成像逐渐走进了人们的视野[12-14]。
编码激励技术在高频超声成像系统中的应用前景广阔[15-16],但在Chirp编码激励模式的性能评价上尚未进行较深入研讨。针对此,本文设计了一个可以进行Chirp编码/脉冲激励的实验系统并基于其进行了一系列实验,解决其应用过程中可能遇到的软硬件方面实际问题。并对比在应用编码激励方式与传统脉冲激励方式下,高频超声成像系统的分辨率、探测深度、信噪比、帧速率等一系列重要参数。然后将高频超声编码成像系统进一步应用于线模、体模等仿体以及离体组织的成像,与传统激励模式相对比,进而获得在实际应用场景下,编码激励方式与传统激励方式优劣势的对比。
1 实验系统实现
本文实验系统由FPGA芯片XC7K325T、激励模块、AD7982、T/R开关、探头、二维控制平台、软件部分等组成,以东软医疗N7系统TR电路板为核心进行构建。该系统可以完成传统脉冲激励和编码激励的发射,并可以存储、处理回波RF信号。实验系统结构框图,见图1。
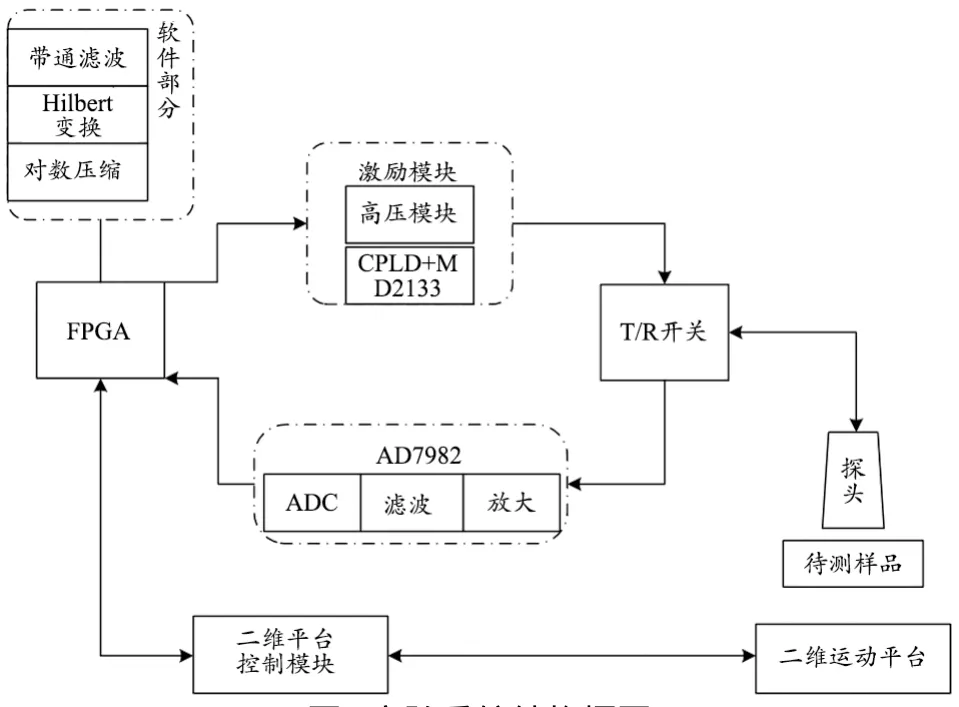
图1 实验系统结构框图
在系统运行时,由FPGA芯片XC7K325T控制激励模块(包含高压模块、编码激励模块)产生实验所需要的激励:脉冲激励采用高压模块、Chirp编码激励采用CPLD及MD2133。激励经过T/R开关,作用于单阵元探头上,然后T/R开关切换为接收模式,系统开始接收由探头回传的电压信号,这些电压信号经过T/R开关,进入AD7982芯片,在其中完成放大、滤波、模数转化等过程后进入FPGA,然后通过Chipscope软件将波形存储导出至Matlab中进行对数压缩、希尔伯特变换、带通滤波等操作,并最终形成用于分析的实验图像。除此之外,由FPGA控制二维平台带动样品运动,使探头可以完成整个样品的成像。
XC7K325T芯片主频200 MHz,负责控制激励模块产生激励、T/R开关进行收发转换,以及AD7982接收回波信号,二维平台运动等。实验系统中,图像帧频为2帧/s,每帧由1000条线构成,即FPGA控制激励模块每秒产生2 kHz的激励,二维平台每秒沿水平方向x轴运动2000步,步长0.5 mm,每次间隔500 μs。每帧图像由1000次激励-接收完成,每个激励-接收周期时间长度为500 μs,接收2048个点,理论探测深度7.68 mm。FPGA将AD7982处理后的数据通过Chipscope保存为prn格式,该格式文件可以由Matlab通过xlLoadChipScopeData()函数进行读取,读取后即可通过Matlab对其进行处理。FPGA芯片是整个系统的核心,负责整个系统各个部分的协同,因为其可编程性质,可以方便的为其加载新的程序进而调整整个系统的成像参数,例如帧频、线数、每条线采样点数等,可以较好的满足实验要求。
本文中所应用的MD2133是可以产生自定义波形的Chirp编码激励源,其设计目的为专门应用于医学超声系统和HIFU系统的激励,除此之外,该方案亦可应用于无损检测及其他超声相控聚焦方面的应用。 MD2133集成电路板由CMOS集成电路、8位高速实时孔径DAC构成。其支持PAM及PWM两种模式。其中PAM为高速脉冲电流幅度调制模式,PWM为采用脉冲发生器和内置cos/sin查表方式的模式。因为DAC的分辨率为8位,所以该电路板内置波形的角分辨率为1.4°,即一个周期由256个数据点存储组成。电路板中包括8个1 k位的波形存储空间用来存储4中预制波形及其相关参数:动态的波形数据的长度、起始地址、重复周期数、CW模式下的连续波形环、被预分频的传输速率、极性转置的快速启动、chirp_up/chirp_down调频和正向/反向传输时域对称波形保存数据点。电路板采用SSTL差分时钟,其控制及统一所有的波束写操作、读操作、传输延迟和波形的频率。MD2133的输出端采用一个双重耗尽型、高压的N-MOSFET( DN2625)作为驱动源。除此之外,MD2133还具有100 MHz的高速串行接口,使其可以在两次激励之间更新扫描所采用的幅度变迹模式。
在实验系统中,回波信号的放大、滤波、模数转化由AD7982芯片完成。AD7982是一款18位、逐次逼近型模数转换器(Analog-Digital Converter,ADC),采用单电源供电。它内置一个低功耗、高速18位采样ADC和一个多功能串行接口端口。在转换输入上升沿,AD7982对IN+与IN-引脚之间的电压差进行采样,这两个引脚上的电压摆幅通常在0 V至VREF之间、相位相反。基准电压(REF)由外部提供,并且可以独立于电源电压。其功耗和吞吐量呈线性变化关系。
因为本文实验中采取了两大类四小类(30 MHz Pulse,60 MHz Pulse,30 MHz Chirp,60 MHz Chirp)的激励模式,所以对于RF数据的处理方式也可以分为两大类四小类,与上面的激励方式一一对应。对于RF数据的处理,见图2。

图2 RF数据处理流程框图
根据图2可以看出,上位机中针对各种激励方式的处理都不相同。Chirp编码激励经过卷积解码后的回波会形成和Pulse激励模式相类似脉冲类回波,从此之后,4种激励模式的处理方式变得相同:首先利用希尔伯特变化求回波的包络信号,然后对包络信号根据动态范围进行对数压缩。下一步中,将压缩后的数据利用二维均值滤波器进行平滑,去除噪声,最终形成图像。
2 实验设计与实现
2.1 实验所用材料的制作
本实验中所采用的实验材料包括3类:分别是线模、体模、及离体组织,分别用于不同用途的测量。其中,线模采用4根直径20 μm的钨丝,以2.5 mm的间隔平行排列,用于测量高频编码激励血管内超声成像系统的各个深度的横向、轴向分辨率。体模采用8%的PVA粉末和1%的纤维素粉末经过加热、搅拌、去除气泡等系列工序制成,制成的仿体包含了3个大小不同用于评价超声系统信噪比、载波比的孔洞,其直径分别为0.9、1.4、3 mm。除此之外,体模的实验结果还被用来评价高频Chirp激励的穿透深度。离体组织采用新鲜的被屠宰的猪的血管组织,因为眼球、血管、肠等结构是高频Chirp激励潜在的应用场景。
2.2 线模的制作过程
取直径20 μm的钨丝一根,前段以较长头发牵引,依次“S型”穿过两块平行的特制PCB板上倾斜为30°的孔洞。穿过孔洞时,应多加小心以免钨丝断裂,完成穿线后,应缓慢逐渐加力,将两块PCB板之间的钨丝绷紧,并将多余钨丝剪短,并用胶带将钨丝两端与PCB板进行粘合固定。将钨丝绷紧的目的是为了保证钨丝与换能器扫描的横截面垂直,只有这样才能对线模清晰成像。
2.3 体模的制作过程
(1)制备材料:聚乙烯醇粉末、纤维素粉末、加热磁力搅拌器(带小磁体)、烧杯、电子秤、塑料血管模具、组织模具(需要2个可让血管穿过的直径略大的孔洞),去离子水。
(2)制备比例:8%聚乙烯醇+1%纤维素。
(3)制备步骤为:① 根据欲制作的仿体体积计算PVA、纤维素、去离子水的量,并使用烧杯称量;② 将PVA和去离子水加入烧杯,小磁体放在烧杯里,放在加热磁力搅拌器中,在30℃下,搅拌1~2 h,使PVA充分溶胀,以利于后续加热PVA的溶解;③ 加热温度调至95℃,在这一温度下加热搅拌1 h,无悬浮颗粒,均一透明即可,为防止水蒸发,用锡箔纸封盖住烧杯;④ 加入纤维素,继续加热搅拌15 min,使其均匀分布,呈乳白色,即可停止加热;⑤ 将烧杯放在超声清洗器中震荡15 min,以除去溶液内气泡;⑥ 静置冷却至30℃,将溶液缓慢倒入模具中,密封后,置于-20℃冷冻12 h,取出在20℃下解冻12 h。此为一个冷冻-解冻周期。不同周期可制作出不同硬度的仿体,制作过程中需注意平整表面。
3 各种模式的成像结果
根据以上描述的实验系统和上文实验方案分别获得了线模、体模、离体组织的图像,见图3。

图3 线模图像
各图右下角两条线对应的实际长度都是2 mm,图中横纵轴的显示比例是不一样。4个线模的深度分别为5.9、6.3、7.8、8.2 mm。该图可以用来评价4种不同的激励在不同深度上的横向和轴向分辨率。通过Matlab对于-6 dB分辨率的计算结果可以得到,系统的横向分辨力弱于纵向分辨力。随着深度的增加,系统的横向分辨率逐渐变差。
本次实验的体模图像,见图4。通过体模图像可以看出,较小的孔洞中信号载波比较差,较大的孔洞中信号载波比较好。
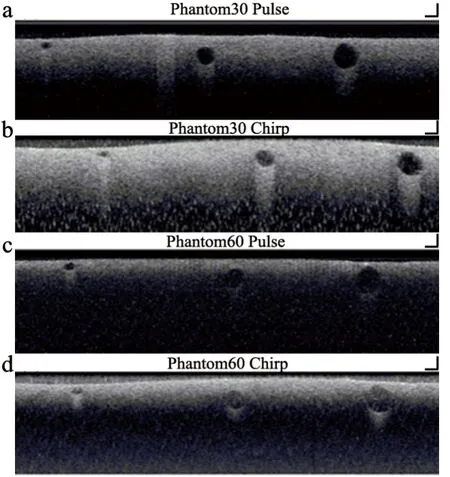
图4 仿体超声成像图
本次实验的离体组织图像,见图5。通过离体组织图像可以看出,高频激励的图像纹理要比低频图像更为细腻,但是穿透深度较浅,例如60 MHz的传统脉冲激励只能看到血管的内膜,而30 MHz的激励可以看到血管外膜的后壁,并可较清晰的看到血管内膜、血管外膜之间的分层。

图5 离体组织高频超声图像
4 各激励模式的性能分析
4.1 -6 d B分辨率结果分析
利用前文所述系统,对于线模实验结果进行分析,得到不同深度的线模的横向分辨率、轴向分辨率,见表1。
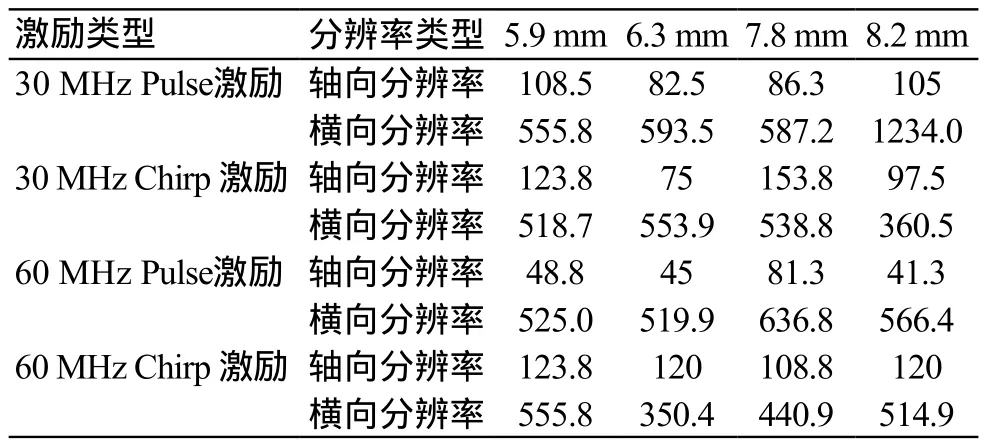
表1 -6 dB不同深度的线模分辨率(µm)
根据计算可以得到,30 MHz Pulse激励各个深度轴向分辨率的平均值为95.6 µm;30 MHz Chirp 激励的轴向分辨率的平均值为112.5 µm;60MHz Pulse激励轴向分辨率的平均值为54.1 µm;60 MHz Chirp激励轴向分辨率的平均值为118.2 µm。30 MHz Pulse激励横向分辨率的平均值为742.6 µm;30 MHz Chirp 激励横向分辨率的平均值为492.9 µm;60 MHz Pulse激励横向分辨率的平均值为562.0 µm;60 MHz Chirp激励横向分辨率的平均值为465.5 µm。通过观察,我们可以得到如下结论:
(1)与理论结果相同,频率越高,分辨率越好;频率越低,分辨率越差。60 MHz的激励,无论是Pulse激励还是Chirp激励,空间分辨率都比30 MHz的激励更佳。
(2)轴向分辨率普遍优于横向分辨率,与理论预期结果相同。
(3)无论是30 MHz还是60 MHz,Chirp激励的横向分辨率优于Pulse激励,但轴向分辨率弱于Pulse激励。
(4)对于比较关心的30 MHz Pulse激励和60 MHz Chirp激励,60 MHz Chirp激励虽然在轴向分辨率上略弱于30 MHz Pulse激励,但是横向分辨率上60 MHz具有较大的优势,这也说明,利用较高频Chirp激励替代传统较低频Pulse激励是具有较大意义的。
4.2 穿透深度
在本文实验中,对于穿透深度的计算是基于体模图像来完成的。首先,取未穿过孔洞的100条采样线。然后,将图像中对于水的回波区域标准化为0,取大于6 dB图像区域为有效区域。将100条采样线的数据平均,结果见图6~7,图中噪声是由电路产生的。
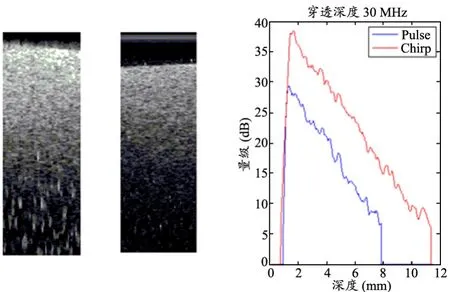
图6 30 MHz激励穿透深度对比图
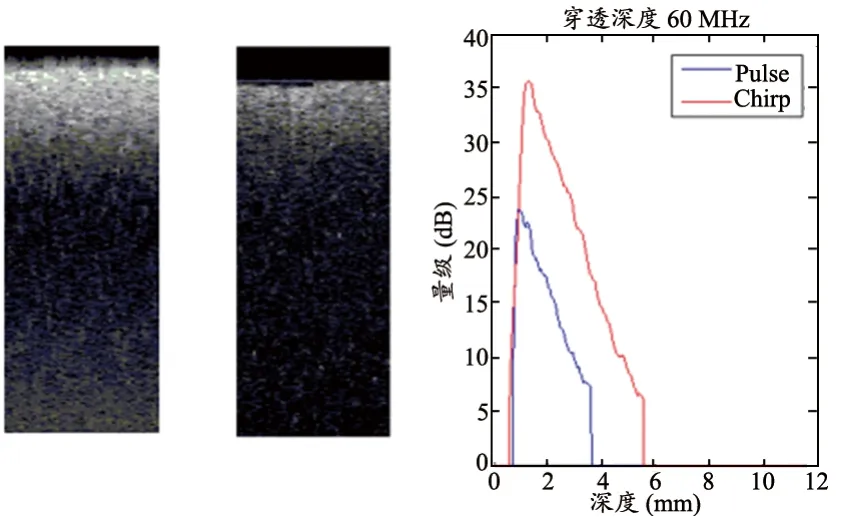
图7 60 MHz激励穿透深度对比图
根据计算得到,相同激励频率下,Chirp编码激励的穿透深度大于传统Pulse激励;相同激励模式下,低频的穿透深度大于高频。由此可见,Chirp激励模式对于高频超声系统穿透深度的提升是具有显著意义的。
4.3 CNR
CNR指的是对比噪声比,其被广泛的应用于评价超声成像系统组织图像区域与噪声的比值,其计算方法如下所示:
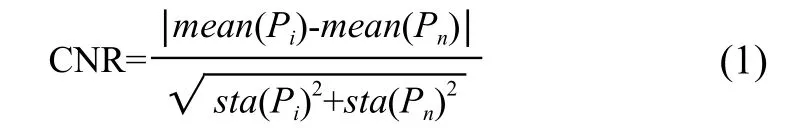
其中,Pi指的是组织区域内的取样像素;Pn指的是噪声区域内的取样像素;mean()为均值;sta()为标准差。CNR取样区域,见图8,图中红色区域为孔洞内的取样区域,蓝色区域为等深度的孔洞外的取样区域。以式(1)计算不同大小孔洞(0.9、1.4、3.0 mm)的CNR。

图8 CNR取样区域
经过计算可以得到,直径为0.9、1.4、3.0 mm的3个孔洞在Chirp激励模式下的CNR为2.7、5.1、5.2,而在Pulse激励模式下的CNR为3.6、3.9、4.3。Chirp激励的不同大小孔洞的平均CNR较比Pulse激励的CNR提升了0.4。
5 结果讨论
为了对比Chirp编码激励与传统Pulse激励的成像效果,我们完成了以FPGA芯片XC7K325T为核心,MD2133产生高频Chirp编码激励,AD7982进行回波电信号处理,Matlab进行RF信号成像及成像效果分析的实验系统。并利用该系统获得了4种激励模式(30 MHz Chirp、30 MHz Pulse、60 MHz Chirp、60 MHz Pulse)的线 模、仿体、离体组织超声图像,并基于这些超声图像计算了不同激励模式的分辨率、穿透深度、CNR等超声成像参数。
通过计算结果,可以看出:
(1)实验结果与理论结果相同,频率越高,分辨率越好;频率越低,分辨率越差。60 MHz的激励,无论是Pulse激励还是Chirp激励,空间分辨率都比30 MHz的激励更佳。
(2)通过线模实验,可以发现不同激励模式对超声成像横向和轴向分辨率的影响有一定的差异。因此,激励模式是影响探头横向、轴向分辨率的重要因素之一,而且在不同频率、不同深度上的影响不同,具体影响机制仍需要进一步探讨。通过体模实验实验可以看出,Chirp激励对于穿透深度具有约50%的提升能力,可以较为明显得增加图像的穿透深度。
(3)通过体模实验中对于不同孔洞的CNR计算结果可以得出,Chirp激励的平均CNR要优于Pulse激励,但是在较小孔洞中的CNR要弱于Pulse激励。
通过以上结果可以看出,Chirp激励模式的确可以对高频超声的穿透深度,横向分辨率、CNR等成像参数进行优化,但是会牺牲一定的轴向分辨率,这是由于其激励发射时间的增加而导致的。在固定频率下, Chirp激励的应用对于高频超声成像质量有着较为显著的提升,这对于进一步提升高频超声的分辨率有着极为重要的意义。
[1] 赵强,白宝平,陈晓冬,等.医学超声内镜中同步编码激励技术的设计与实现[J].纳米技术与精密工程,2014,(1):27-31.
[2] 齐敏超,高上凯.全数字超声多普勒血流测量系统研究[J].中国生物医学工程学报,2012,(3):349-353.
[3] 彭珏,覃正笛,刁现芬,等.医学超声关键技术研究和进展(一):超声换能器与超声编码技术[J].生物医学工程学进展,2013,(1):21-27.
[4] Smith PR,Cowell DMJ,Freear S.Width-modulated square-wave Pulses for ultrasound applications[J].IEEE Trans Ultrason Ferroelectr Freq Control,2013,60(11):2244-2256.
[5] Kamimura HAS,Wang S,Wu SY,et al.Chirp-and random-based coded ultrasonic excitation for localized blood-brain barrier opening[J].Phys Med Biol,2015,60(19):7695-7712.
[6] Novell A,Sennoga CA,Escoffre JM,et al.Evaluation of Chirp reversal power modulation sequence for contrast agent imaging[J].Phys Med Biol,2014,59(17):5101-5117.
[7] Ramalli A,Guidi F,Boni E,et al.A real-time Chirp-coded imaging system with tissue attenuation compensation[J].Ultrasonics,2015,60:65-75.
[8] Novell A,Legros M,Grégoire JM,et al.Evaluation of bias voltage modulation sequence for nonlinear contrast agent imaging using a capacitive micromachined ultrasonic transducer array[J].Phys Med Biol,2014,59(17):4879-4896.
[9] Satir S,Degertekin FL.Phase and amplitude modulation methods for nonlinear ultrasound imaging with CMUTs[J].IEEE Trans Ultrason Ferroelectr Freq Control,2016,63(8):1086-1092.
[10] Fouan D,Bouakaz A.Investigation of classical Pulse sequences for contrast-enhanced ultrasound imaging with a cMUT probe[J].IEEE Trans Ultrason Ferroelectr Freq Control,2016,63(10):1496-1504.
[11] Yu FT,Villanueva FS,Chen X.Radial modulation contrast imaging using a 20-MHz single-element intravascular ultrasound catheter[J].IEEE Trans Ultrason Ferroelectr Freq Control,2014,61(5):779-791.
[12] 周盛,王晓春,计建军,等.Barker编码激励在眼科高频超声成像中的应用研究[J].中国生物医学工程学报,2012,(5):671-678.
[13] 李明,陈晓冬,李妍,等.Chirp编码的鲁棒医学超声内窥合成孔径方法[J].声学学报,2012,(3):237-243.
[14] 李风从,赵宜楠,乔晓林.抑制特定区间距离旁瓣的恒模波形设计方法[J].电子与信息学报,2013,(3):532-536.
[15] 刘宝强,邱维宝,王祖麟,等.一种超高频血管内超声成像系统设计与实现[J].压电与声光,2015,(4):681-683.
[16] 益民,任晓萍,潘文倩,等.高频超声及钼靶X线检查在乳腺癌诊断中的应用价值[J].西安交通大学学报(医学版),2012,(5):572-575.
