毛细管电泳-间接化学发光法检测尿液与血液中吗啡含量
2018-01-25朱怀娇韩燕祯杜鹏男毕思远徐向东
朱怀娇,韩燕祯,杜鹏男,康 凯,毕思远,徐向东*
(1.河北医科大学 公共卫生学院,河北 石家庄 050017;2.深圳市易瑞生物技术有公司,广东 深圳 518101)
吗啡(Morphine,MOP)是由阿片提炼的一种阿片生物碱,为纯粹的阿片受体激动剂,具有显著的镇痛作用。作为麻醉性镇痛药,吗啡在使用初期有欣快感和梦幻现象,极易产生耐受性和成瘾,是阿片类毒品的重要组成之一,也是其它阿片类毒品如海洛因、可待因等在体内的最终代谢产物[1-2]。以海洛因为例,其进入人体后很快代谢为单乙酰吗啡,进而代谢为吗啡[3-4]。因此,尿液及血液中吗啡含量的测定,对法医鉴定、法医毒物分析以及毒品滥用证据的提供均具有重要意义。
由于时效性,法医鉴定所用的血液或尿液样品往往不易重复获得,样本量有限,因此与常规检测相比,对检测方法的灵敏度和样品消耗量有更高要求。目前,吗啡的测定方法主要有薄层色谱扫描法[5]、气相色谱法[6]、气相色谱-质谱联用法[7-8]、高效液相色谱法[9]、高效液相色谱-质谱联用法[10-11]、毛细管电泳法[12]、化学发光法[13]等。毛细管电泳分离技术具有分离效率高、分离速度快、样品消耗量小的特点,应用于毒品的分离分析有独特优势[14]。化学发光检测方法应用于毛细管电泳是一种非常理想的检测手段。相对于紫外可见分光光度法、荧光法等检测方法,化学发光无需激发光,避免了瑞利散射和拉曼散射等噪音,因而仪器简单,且提高了信噪比,具有灵敏度高的特点。与单纯使用化学发光检测技术相比,毛细管电泳-化学发光联用可实现高选择性与高灵敏度的结合。二者的联用技术已成为分析化学领域的研究热点之一[15],目前尚未见毛细管电泳-化学发光法用于吗啡检测的报道。
探索新的化学发光体系对于扩大化学发光检测技术的应用范围具有重要意义。Ag(Ⅲ)-鲁米诺化学发光体系具有反应速度快、氧化电位高、发光量子产率高等特点[16]。研究发现,吗啡在碱性条件下可抑制Ag(Ⅲ)-鲁米诺化学发光体系的发光强度,且在一定范围内,其抑制程度与吗啡含量呈现良好的线性关系。基于此,利用自制的毛细管电泳-化学发光检测仪,建立了毛细管电泳-间接化学发光检测体液中吗啡含量的方法。该方法应用于尿样与血样中吗啡含量的测定,结果满意。
1 实验部分
1.1 仪器与试剂
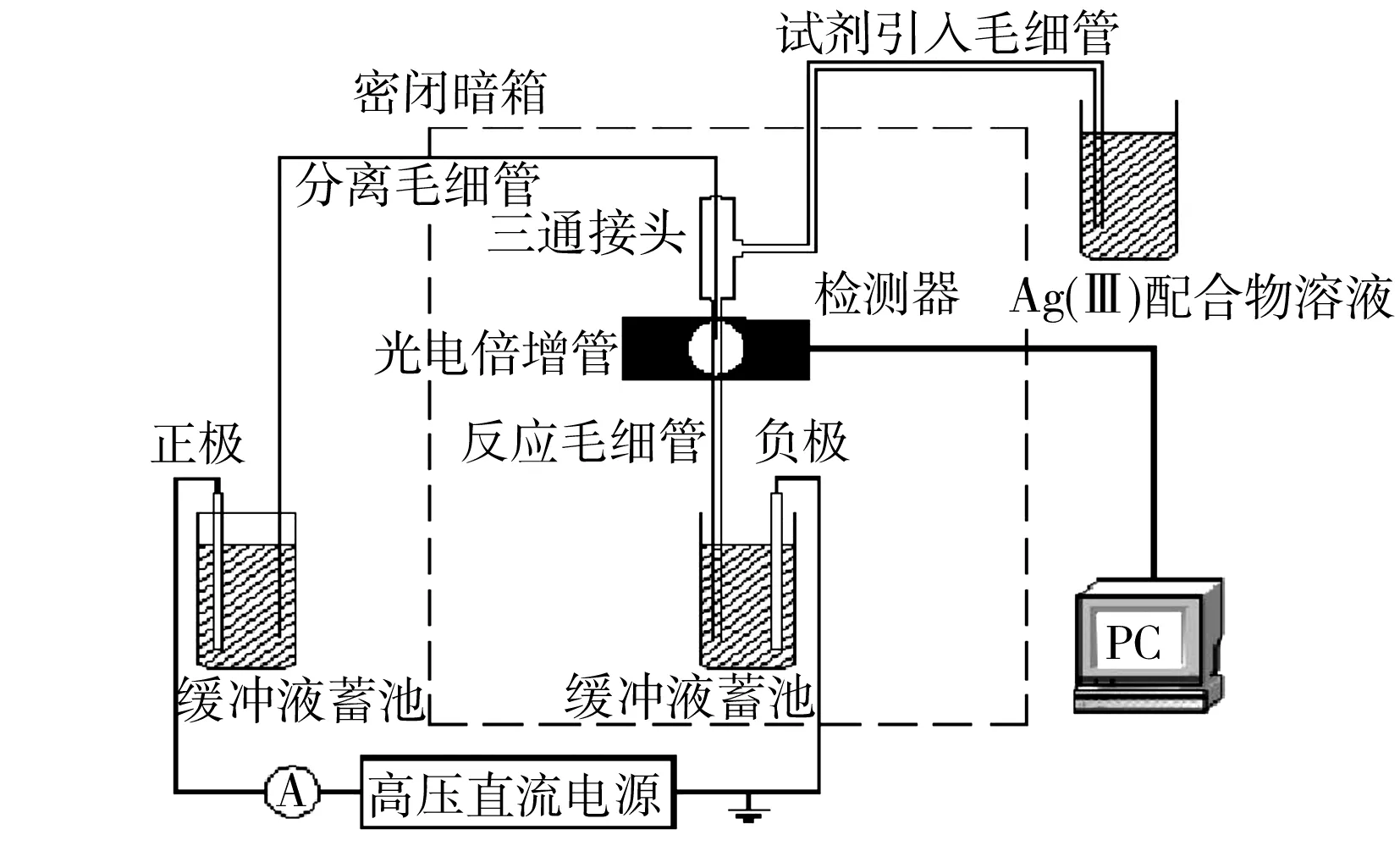
图1 毛细管电泳-化学发光检测仪装置示意图Fig.1 Schematic diagram of apparatus for the capillary electrophoresis-chemiluminescence detector
石英毛细管(河北永年县锐沣色谱器件有限公司);高压电源(北京安和光电仪器有限责任公司);光电倍增管(北京滨松光子技术有限公司);千谱色谱工作站(上海千谱软件有限公司);电子天平(丹佛仪器(北京)有限公司)。实验所用毛细管电泳-化学发光检测仪为自组装(图1),与文献[16]相同。将长度75 cm的电泳毛细管(内径50 μm)一端(长约8 cm)经氢氟酸刻蚀50 min后,将8 cm长的刻蚀段插入反应管(内径530 μm)中。将反应管中1 cm段烧去聚酰亚胺涂层作检测窗(电泳分离管的末端插入其中)。一根试剂引入管(内径200 μm)以重力方式引入氧化试剂,试剂池距缓冲液蓄池高20 cm。三根毛细管用三通接头固定。其中反应毛细管位置固定后,使检测窗正位于光电倍增管前。反应系统和光电倍增管置于密封的暗箱中。由光电倍增管收集化学发光信号,色谱工作站处理数据,以迁移时间定性,以峰高定量。
吗啡标准物质(中国食品药品检定研究院);鲁米诺(东京化成工业株式会社);氢氧化钠、四硼酸钠、磷酸二氢钠、AgNO3、KIO4、K2S2O8、KOH均为国产分析纯,实验用水为双蒸水。吗啡标准储备液(500 mg/L):准确称取吗啡标准品5.0 mg于容量瓶中,用50%甲醇定容至10 mL,避光于4 ℃冰箱保存;鲁米诺储备液(20 mmol/L):准确称取0.354 4 g鲁米诺,加入2.80 mL 1.0 mol/L NaOH,加水定容至100 mL,避光保存;硼砂储备液(50 mmol/L):准确称取4.767 3 g四硼酸钠溶于水,加热溶解后冷却,定容至250 mL。Ag(Ⅲ)配合物储备液:配制方法同文献[17]。
1.2 实验方法
1.2.1仪器条件新毛细管依次用1 mol/L NaOH冲洗20 min,0.1 mol/L HCl和双蒸水各冲洗10 min。每次实验前依次进行常规操作:分离管分别用0.1 mol/L NaOH与双蒸水各冲洗10 min,再用缓冲液平衡30 min后进样检测。
1.2.2样品处理方法尿样处理:取OASIS®HLB(6 mL/200 mg)固相萃取柱,依次用3 mL甲醇、3 mL水、3 mL磷酸盐缓冲溶液进行活化,加入2 mL尿样;用1 mL 0.1 mol/L HCl、1 mL H2O、1.5 mL 0.15 mol/L碳酸铵溶液依次淋洗柱子后,将柱子抽真空5 min除去残余水分;随后用3 mL 5%氨水/甲醇洗脱,收集洗脱液在60 ℃下氮气吹干,用1 mL水复溶待测。
血样处理:取1.5 mL血样以11 000 r/min离心15 min,取上清液加入等体积的0.2 mol/L pH 4.6磷酸盐缓冲溶液,混匀。取OASIS®HLB(6 mL/200 mg)固相萃取柱,依次用3 mL甲醇、3 mL水活化柱子,加入血样,用3 mL水淋洗柱子后将柱抽真空5 min除去残留水分,随后用3 mL甲醇洗脱,收集洗脱液经氮气吹干后,用1 mL水复溶待测。
2 结果与讨论
2.1 化学发光条件的选择
2.1.1Ag(Ⅲ)溶液碱度的选择pH值是影响化学发光的重要因素。为避免空气中二氧化碳对碱液的影响,实验采用NaOH-Na2CO3混合缓冲溶液调节Ag(Ⅲ)溶液的碱度。分别考察了NaOH浓度为0.01~0.05 mol/L和Na2CO3浓度为0.005~0.010 mol/L时对化学发光信号强度的影响。结果表明,NaOH为0.04 mol/L、Na2CO3为0.008 mol/L时,化学发光强度最大,且信号稳定。故将Ag(Ⅲ)溶液中NaOH浓度定为0.04 mol/L、Na2CO3浓度定为0.008 mol/L。
2.1.2Ag(Ⅲ)溶液浓度的选择实验考察了Ag(Ⅲ)溶液浓度为4.0×10-5~9.0×10-5mol/L时对发光体系的影响。结果表明,随着Ag(Ⅲ)溶液浓度的增大,发光强度随之增大。当Ag(Ⅲ)溶液浓度为7.0×10-5mol/L时,化学发光强度最大,且信号稳定。继续增大Ag(Ⅲ)溶液浓度时发光强度反而降低,这可能是由于高浓度溶液会部分吸收发光信号所致。故Ag(Ⅲ)溶液浓度定为7.0×10-5mol/L。
2.1.3鲁米诺浓度的选择实验考察了鲁米诺浓度在0.001~0.004 mol/L范围内对化学发光信号的影响。结果显示,当鲁米诺浓度为0.002 mol/L时,发光强度达到最大,继续增加鲁米诺浓度对提高化学发光强度并无显著效果。故鲁米诺溶液浓度定为0.002 mol/L。
2.2 电泳条件的选择
2.2.1硼砂缓冲溶液的选择实验在0.002~0.015 mol/L范围内对硼砂浓度进行优化。结果表明,硼砂浓度为0.005 mol/L时化学发光信号达到最大值,随后逐渐减小。故将硼砂浓度定为0.005 mol/L。
2.2.2分离电压的选择毛细管电泳分离电压不仅能影响迁移速度与分离效果,还会影响化学发光信号。电压过低,电泳速度较慢,峰形展宽。电压过高,电泳速度加快,但产生的焦耳热相应增加,易导致峰形展宽、分离效率下降[18]。实验考察了分离电压在5~18 kV范围内对化学发光信号和分离效果的影响。结果表明,分离电压为15 kV时,化学发光信号最大,分离效果较好,故将分离电压定为15 kV。
2.2.3进样时间的选择固定发光条件与其他电泳条件,采用重力进样方式,考察了进样时间在4~15 s范围内时对化学发光强度的影响。结果表明,进样时间为12 s时,化学发光强度达最大,且峰形尖锐,分离效果佳,故确定最佳进样时间为12 s。
综上,确定最佳检测条件为:Ag(Ⅲ)溶液浓度7.0×10-5mol/L,NaOH浓度0.04 mol/L、Na2CO3浓度0.008 mol/L、鲁米诺浓度0.002 mol/L、硼砂浓度0.005 mol/L、分离电压15 kV、进样时间12 s。
2.3 工作曲线、检出限与精密度
取吗啡标准储备液,用双蒸水稀释后得到一系列质量浓度分别为2.0、5.0、10.0、15.0、20.0、30.0 mg/L的标准工作溶液。在上述选定的最佳实验条件下,分别进样,得到不同质量浓度吗啡溶液的色谱图。以峰高值(Y)对吗啡质量浓度(X,mg/L)作图,得到线性回归方程为Y=3.826 5X+14.14(r=0.999 8)。结果表明,吗啡质量浓度在2.0~30.0 mg/L范围内线性良好,方法检出限(S/N=3)为0.75 mg/L。取20.0 mg/L吗啡进行7次平行实验,测得相对标准偏差(RSD)为2.0%。
2.4 样品回收率测定
取吗啡标准储备液加入2 mL空白尿样中,旋涡混匀2 min,冷藏40 min后以3 500 r/min离心5 min。取上清液1 mL,加入1 mL 0.2 mol/L pH 4.6磷酸盐缓冲溶液,混匀。制成3、8、20 mg/L 3个质量浓度的待测加标尿样。再取吗啡标准储备液加入到1.5 mL空白血样中,旋涡混匀3 min,冷藏40 min后于37 ℃ 11 000 r/min离心15 min。取上清液700 μL加入等体积的0.2 mol/L pH 4.6磷酸盐缓冲溶液,混匀,制备成3、8、20 mg/L 3个质量浓度的待测加标血样。
尿液与血液样品检测结果见图2。由图可见,吗啡在9 min内即可实现分离分析,尿液与血液中的其他物质对检测无干扰。利用相对峰高值定量,测得尿样与血样中吗啡的平均回收率分别为109.0%与101.3%(表1)。


SampleAdded(mg/L)Measured(mg/L)Recovery(%)Averagerecovery(%)Urine33.06102.0109.088.92111.52022.72113.6Blood32.5284.0101.388.58107.22022.52112.6
3 结 论
本研究基于一种新的化学发光体系(Ag(Ⅲ)配合物-鲁米诺化学发光体系),将毛细管电泳技术与之联用,建立了毛细管电泳-间接化学发光法用于尿样与血样中吗啡含量的检测。该方法结合固相萃取前处理技术,操作简便、灵敏度高、分辨率高、对环境友好且分析成本低,为生物样品中吗啡的含量测定提供了一种快速、有效的新方法。
[1] Shen M.AnalysisofAbuseDruginVivo.Beijing:Law Press China(沈敏.体内滥用药物分析.北京:法律出版社),2003:99.
[2] Huang G Z.ForensicToxicology.The 3rd Edition.Beijing:People’s Medical Publishing House(黄光照.法医毒理学,第3版.北京:人民卫生出版社),2004:86.
[3] Pei M Q,Cong P F,Di B.ForensicSci.Technol.(裴茂清,从培峰,狄碧.刑事技术),2004,(6):6-7.
[4] Lu H R.ForensicSci.Technol.(吕海茹.刑事技术),2008,(2):29-31.
[5] Xu P S,Ma H Y,Lei P,Ren W,Cai L Y.Chin.Pharma.J.(徐平声,马虹英,雷鹏,任维,蔡良音.中国药学杂志),2003,(8):59-60.
[6] He L.ChemicalReagents(贺岚.化学试剂),2015,(4):328-330.
[7] Dong L,Yu Z W,Yun K M,Wang Y J.Chin.J.HealthLab.Technol.(董镧,尉志文,贠克明,王玉瑾.中国卫生检验杂志),2010,(4):697-699.
[8] Wang Y Y,Meng P J,Li Y J,Wang Y J.Phys.Test.Chem.Anal.:Chem.Anal.(王燕燕,孟品佳,李燕京,王彦吉.理化检验:化学分册),2011,(4):442-444,448.
[9] Zhang X T,Sun L M,Liu J,Xu S Y.Chin.J.ForensicMed.(张小婷,孙立敏,刘娟,徐淑云.中国法医学杂志),2011,(1):16-18.
[10] Liang C,Ye H Y,Zhang Y R,Wang R,Chen Y S.J.Chin.MassSpectr.Soc.(梁晨,叶海英,张玉荣,汪蓉,陈永生.质谱学报),2011,(3):159-163.
[11] Wang Y,Liu Z Q,Wang J.Chin.J.ForensicMed.(王毅,刘子秋,王炯.中国法医学杂志),2014,(4):319-321,325.
[12] Huang X,Zhang C S,Ma G H,Bai Y P.Chin.J.Anal.Lab.(黄星,张春水,马果花,白燕平.分析试验室),2007,(S1):222-226.
[13] Li S J,Yang R,Qu L B,Li J J.Chin.J.Pharma.Anal.(李世君,杨冉,屈凌波,李建军.药物分析杂志),2011,31(7):1376-1378.
[14] Ban E,Song E J.J.Chromatogr.B,2013,929:180-186.
[15] Liu Y X,Huang X Y,Ren J C.Electrophoresis,2016,37(1):2-18.
[16] Xu X D,Li N,Li X,Shi H M,Ma C L,Kang W J,Cong B.Electrophoresis,2016,37(22):2992-3001.
[17] Balikungeri A,Pelletier M,Monnier D.InorganicaChimicaActa,1977,22:7-14.
[18] Ding X J,Guo L.CapillaryElectrophoresis:ExperimentalTechniques.Beijing:Science Press(丁晓静,郭磊.毛细管电泳实验技术.北京:科学出版社),2015:73.
