二氧化锰/石墨烯/N-取代羧基聚苯胺复合修饰电极对亚硝酸根的电化学催化研究
2018-01-25叶小爱章家立关婷婷史怡炜
叶小爱,章家立,关婷婷,史怡炜
(华东交通大学 材料科学与工程学院,江西 南昌 330013)
亚硝酸根作为氮的中间产物之一,在染料工业和食品工业中应用广泛,但人体中亚硝酸根含量过高时,会形成亚硝胺致癌物,对人体健康造成危害[1-2],因此对亚硝酸根的检测具有非常重要的实际意义。目前检测亚硝酸根的方法主要有分光光度法[3]、化学发光法[4]、色谱法[5]、电化学法[6]等,其中电化学方法因操作简单、无污染、快速等优点而备受关注[7]。但在电化学检测中,使用裸电极检测亚硝酸根所需电位高,且响应小[8-9],而修饰电极则克服了裸电极的缺陷,具有催化电位低、灵敏度高、响应大的优点,在电化学探测中具有广泛的应用。聚苯胺由于可以通过掺杂和去掺杂的方式来控制聚合物的导电率,被广泛用于电化学研究,但导电率低限制了其应用[10-11]。为改善这一缺点,研究者将具有比表面积大、导电率高的石墨烯添加到聚合物中以形成高导电的复合材料。石墨烯的加入改善了修饰电极的电化学行为,并且通过增加比表面积提高了修饰膜对化学物质的响应[12-14],但修饰电极缺乏对目标物质的专一选择性。而贵金属和过渡金属氧化物具有对特定物质的专一选择性,因此在修饰电极中加入这些物质可以达到高效、专一的电催化作用[15-18]。其中,二氧化锰因价格低、无毒和理论电容值较高在电催化中具有广泛的应用,但单独地修饰电极对亚硝酸根离子的催化灵敏度低、检测范围窄,而当MnO2与碳基材料复合时,对亚硝酸根离子的检测灵敏度则明显增高,检测范围也扩大[19-22]。
本文以N苯基甘氨酸为单体,利用循环伏安法制备N-取代羧酸聚苯胺(NPAN)膜,分别利用电沉积和滴涂法将氧化石墨烯和MnO2分散到聚合物膜上。氧化石墨烯在电沉积的过程中形成还原氧化石墨烯(rGO),然后利用电化学的方法来检测溶液中亚硝酸根离子的浓度。此方法制备的电化学传感器具有制备简单、成本低和灵敏度高等特点。
1 实验部分
1.1 试剂与仪器
N苯基甘氨酸(NAN,阿拉丁试剂有限公司);高氯酸(上海金鹿化工有限公司)、氯化钾和亚硝酸钠(天津市大茂化学试剂厂)、磷酸钾(国药集团化学试剂有限公司)、硫酸镁(上海实验试剂有限公司)均为分析纯;磷酸二氢钠、高锰酸钾、硝酸钾、无水乙醇、碳酸钾、十二水磷酸氢二钠(西陇化工股份有限公司)均为分析纯。
CHI430b石英晶体微天平(上海辰华仪器有限公司);扫描电子显微镜(SEM,日本JSM-6701F型);三电极体系(铂柱对电极,Ag/AgCl参比电极,3 mm直径玻碳电极为工作电极);CHI660c型电化学工作站(上海辰华仪器有限公司)。
1.2 修饰电极制备
rGO/NPAN/GCE:将GCE用0.05 μm的Al2O3粉抛光,再依次用无水乙醇和水超声洗涤干净后,在0.5 mol/L H2SO4溶液中于-0.3~1.5 V下扫描活化。将预处理后的GCE浸入含有0.5 mol/L N-苯基甘氨酸(NAN)的0.1 mol/L HClO4混合溶液中,于-0.3~1.1 V电位范围内以0.1 V/s的扫描速率循环伏安电化学聚合10圈,聚合完后用去离子水清洗电极以除去未聚合的NAN单体。取5 μL GO(1 mg/mL)分散液滴于聚合有NPAN的玻碳电极上,在氮气保护下晾干后形成GO/NPAN/GCE,再将电极插入0.1 mol/L磷酸盐缓冲溶液中,于-1.3 V电位下沉积200 s,电化学还原GO,得到rGO/NPAN/GCE,取出,用滤纸吸干表面的水,晾干待用。
二氧化锰的制备:将KMnO4和NaNO2(nKMnO4∶nNaNO2=2∶3)溶于一定量水中,在搅拌条件下缓慢加入一定量的硫酸,将溶液转移到反应釜中,置于烘箱中,170 ℃下反应12 h,取出,自然降温,离心,依次用乙醇、水洗涤,最后60 ℃干燥12 h。
MnO2/rGO/NPAN:将5 μL MnO2(1 mg/mL)水分散液滴涂到rGO/NPAN/GCE电极表面,自然晾干,用水洗去未吸附的MnO2,晾干待用。
1.3 电化学测试
所有的电化学测量均采用三电极体系,以铂丝电极为辅助电极,Ag/AgCl(饱和KCl)为参比电极,玻碳电极或修饰玻碳电极为工作电极。交流阻抗(EIS)谱图则在0.5 mol/L KCl+ 5.0 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1∶1)的溶液中测试。
2 结果与讨论
2.1 修饰电极的形貌表征
复合膜修饰电极的形貌表征结果见图1。图1A为电聚合形成的NPAN,呈现出一定的纤维状,长度达数百纳米,直径约60 nm。在电沉积的过程中,氧化石墨烯(GO)还原成的还原氧化石墨烯(rGO)负载到NPAN上的扫描电镜形貌见图1B,由图可见,覆盖在NPAN表面的片状rGO使得复合膜表面有许多褶皱形状,而rGO之间的π-π吸附作用使之分布较为均匀。图1C为rGO/NPAN复合膜负载MnO2的形貌图,MnO2颗粒均匀分散到复合膜上,其粒径大小约150 nm。同时表面还存在一些直径约为80 nm的MnO2纳米棒,其均匀分散可能是由于带正电荷的聚苯胺与带负电的纳米MnO2之间的静电吸引所致。
2.2 不同修饰电极的电化学表征
图2A为不同修饰电极在[Fe(CN)6]3-/4-溶液中的循环伏安曲线。裸电极在[Fe(CN)6]3-/4-中有1对对称的氧化还原峰,说明[Fe(CN)6]3-/4-在裸电极表面可以发生氧化还原反应,峰电流较大,而NPAN修饰的电极,氧化还原峰峰电流减小,而且峰电位增加,主要是因为NPAN弱的导电性以及对[Fe(CN)6]3-/4-的吸附所致。当在NPAN表面滴涂一层GO时,峰电流进一步下降,峰电位继续增大,这是由不导电的氧化石墨烯所致,但利用电沉积法将 GO沉积到NPAN膜上时,该修饰电极在[Fe(CN)6]3-/4-溶液中的循环响应电流明显增加,峰电流远大于裸电极,表明将氧化石墨烯电沉积到电极上时已有部分还原成石墨烯,提高了修饰膜的导电性能。若继续在电极上负载MnO2纳米颗粒,修饰电极的峰电流有所下降,但峰电位不变,这主要是由于添加了不导电的MnO2所致。图2B是5种修饰电极在[Fe(CN)6]3-/4-溶液中的交流阻抗图,裸电极的电阻为370 Ω,而用NPAN修饰的电极电阻则增至3 600 Ω(曲线b),这主要是由于NPAN膜的导电率低所致。

在NPAN表面覆盖一层氧化石墨烯(GO)后(曲线c),半圆直径进一步增大,这主要是因为增加了不导电的GO,所得修饰膜的电阻进一步加大。而如果采用电沉积的方法将GO沉积到NPAN修饰膜上,修饰膜的电阻降至120 Ω(曲线d),表明利用电沉积的方法将氧化石墨烯沉积到修饰膜表面,在增加电化学响应的同时,氧化石墨烯被还原成为石墨烯,提高了复合膜的导电能力。将MnO2纳米颗粒滴涂到上述复合膜上,阻抗电阻有所增加,但比裸电极小,这一结果与图2A一致,表明MnO2/rGO/NPAN修饰电极在电解质溶液中具有较好的电化学响应。
2.3 亚硝酸根在修饰电极上的电化学行为
不同修饰电极在含1 mmol/L亚硝酸根的缓冲溶液中的循环伏安曲线结果显示,MnO2/GCE修饰电极对亚硝酸根有较明显的电催化性能,其催化氧化电位为1.1 V,响应峰电流为37.27 μA。以rGO作为支撑材料时,rGO/MnO2/GCE修饰电极对亚硝酸根的催化行为明显增强,催化电位下降至0.9 V,响应峰电流却增加至57.35 μA,说明rGO作为二氧化锰的支撑材料可提高其电催化性能,这归因于rGO的高导电性及其大的比表面积。将MnO2负载在rGO/NPAN膜上形成复合修饰电极时,对亚硝酸根的催化电位减小至0.88 V,响应峰电流达75.16 μA,催化效果进一步增强,这主要是由NPAN独特的掺杂基质以及与高活性rGO之间复合产生的协同效应,加快了电极表面的电子转移速率所致。因此MnO2/rGO/NPAN修饰电极对亚硝酸根的催化效果最好。
2.4 MnO2/rGO/NPAN复合膜修饰电极条件优化
2.4.1聚合物NPAN电聚合圈数的影响图3A为NPAN不同电聚合圈数制备的MnO2/rGO/NPAN修饰电极催化亚硝酸根的循环伏安图,当聚合圈数从0圈增加到30圈时,响应峰电流先增加,在10圈时达到最大值,后逐步减小。其原因为:当NPAN电聚合圈数太少时,聚合物膜的电活性中心少,固定的rGO量相对减小;而电聚合圈数过多时,膜厚增加,NPAN的弱导电性又会阻碍电子在修饰电极上的传递,影响修饰电极的性能,因此本实验选择NPAN的电聚合圈数为10圈。
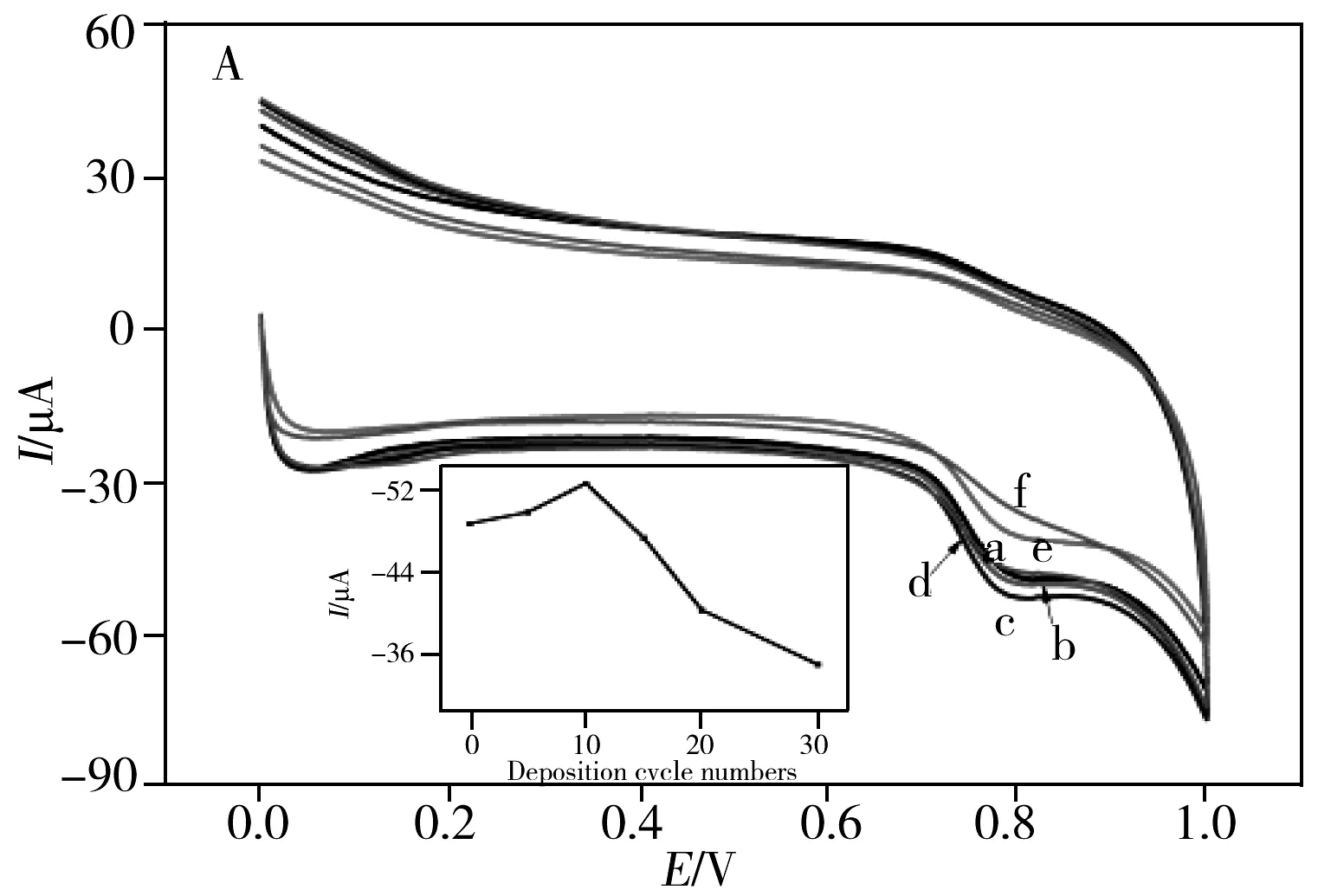
2.4.2GO浓度的影响当GO浓度较小时,随GO浓度的增加,沉积在修饰电极上的高活性rGO逐渐增加,使得修饰电极电活性增强,而当GO浓度进一步增大时,沉积在电极上的复合膜厚度增加,导致部分修饰物从电极表面脱落,阻碍电子在修饰电极上的传递,反而使修饰电极的电活性下降。当GO质量浓度从0.25 g/L增加到2 g/L,MnO2/rGO/NPAN修饰电极催化亚硝酸根的电活性先增强后减弱,当GO质量浓度达1.0 g/L时,响应峰电流最大(图3B),故选择GO的质量浓度为1.0 g/L。
2.4.3二氧化锰浓度的影响实验发现,随着亚硝酸根浓度的增加,峰电流逐步增加,二氧化锰质量浓度从0.02 g/L增加到0.25 g/L时,其催化响应电流逐渐增大,响应电流与亚硝酸根浓度之间线性关系的灵敏度也逐渐增大,当二氧化锰质量浓度为0.25 g/L时达到最大,而当二氧化锰质量浓度继续增大时,响应电流反而逐渐减小,对应的灵敏度也逐渐减小,因此最佳质量浓度为0.25 g/L。
2.4.4pH值的影响考察了MnO2/rGO/NPAN修饰电极在含亚硝酸根的不同pH值PBS溶液中的响应峰电流,随着pH值的增大,亚硝酸根的氧化峰电流增大,在pH 6.8时达到最大值(42.25 μA),当pH值大于6.8时,亚硝酸根的氧化峰电流随pH值的增大而降低,因此为保证修饰电极的催化活性,选择pH 6.8为溶液的最佳pH值。
2.5 MnO2/rGO/NPAN修饰电极电催化亚硝酸根离子的机理
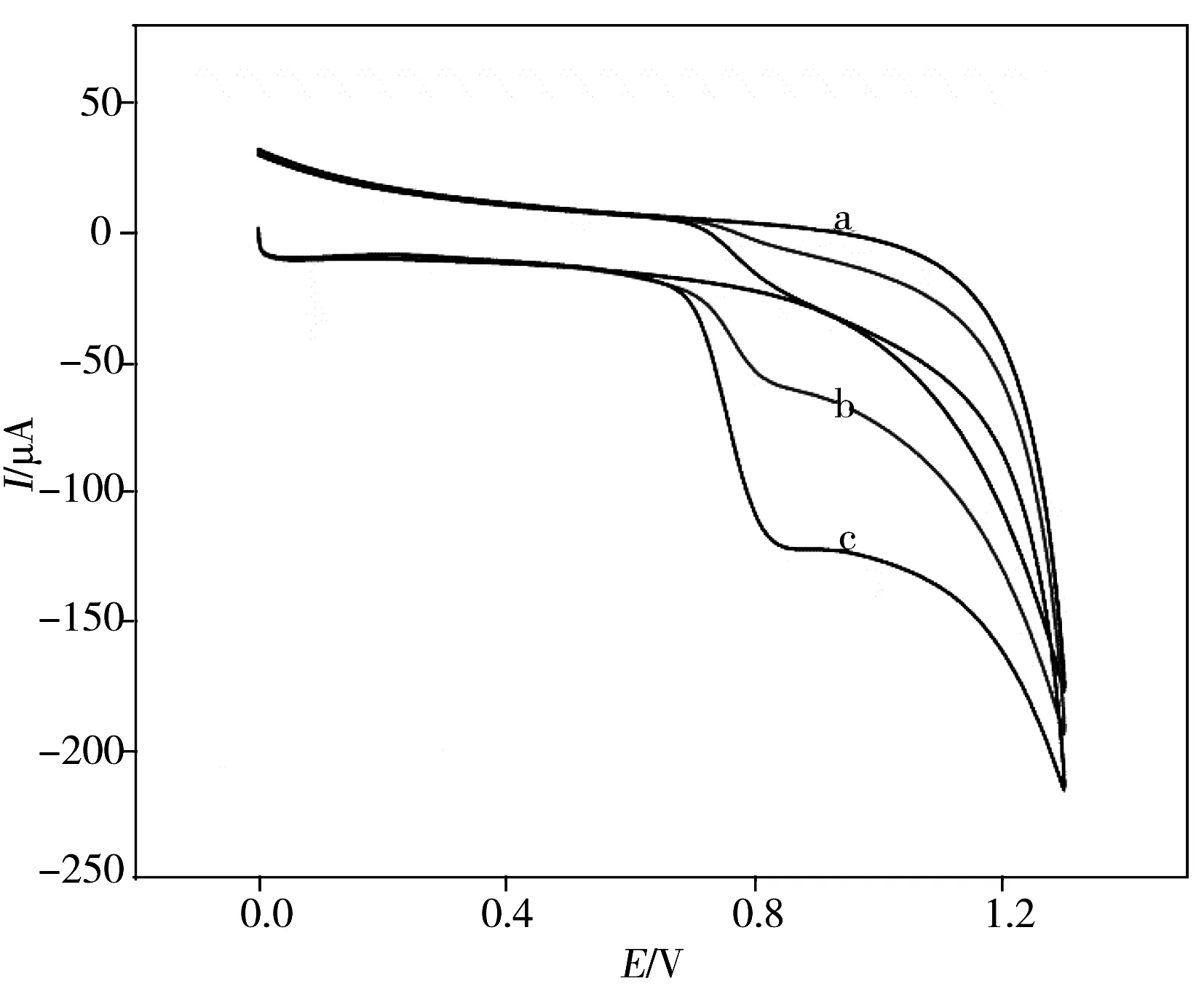
图4 MnO2/rGO/NPAN/GCE在含有不同浓度NaNO2的0.1 mol/L PBS(pH 6.8)中的循环伏安图Fig.4 Cyclic voltammetrys of MnO2/rGO/NPAN/GCE in 0.1 mol/L PBS(pH 6.8) containing different concentrations of NaNO2NaNO2 concentration(a-c):0 ,1.0 ,3.0 mmol/L ;scan rate:0.1 V·s-1
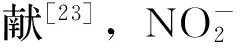
(1)

(2)
(3)
2.6 扫描速率对MnO2/rGO/NPAN修饰电极电催化活性的影响
在含亚硝酸根的 0.1 mol/L PBS(pH 6.8)溶液中,MnO2/rGO/NPAN修饰电极在10~1 000 mV/s扫速范围内的循环伏安曲线显示,随着扫速的增大,氧化峰响应电流也随之增大,亚硝酸根的氧化峰电流(I,μA)与扫速(v,mV/s)的平方根呈良好的线性关系,其线性方程为I= 0.790 51-5.079 38v1/2,相关系数为0.999,属于典型的扩散控制过程。
2.7 不同浓度亚硝酸根在MnO2/rGO/NPAN修饰电极上的电化学传感行为
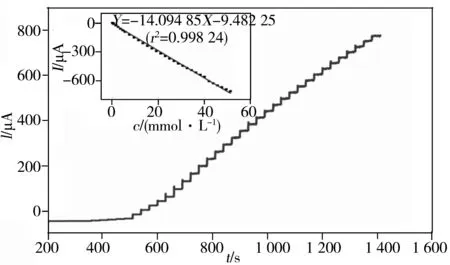
图5 MnO2/rGO/NPAN/GCE对NaNO2的计时电流响应曲线Fig.5 Chronoamperometric responses of MnO2/rGO/NPAN/GCE to NaNO2 applied potential:0.9 V;inset:linear calibration curve of chronoamp-erometric current of MnO2/rGO/NPAN/GCE vs.NaNO2 concentration
图5为MnO2/rGO/NPAN修饰电极对不同浓度亚硝酸根的动态安培曲线图。于10 mL 0.1 mol/L 的磷酸缓冲溶液中(pH 6.8)加入不同浓度亚硝酸根,在正向扫描过程中均出现亚硝酸根的特征电位和氧化峰电流,修饰电极的响应峰电流随亚硝酸根浓度的增加而增大,峰电位则逐步向正电位移动,可知MnO2/rGO/NPAN修饰电极对亚硝酸根的催化效果最好。将加入的NaNO2浓度与MnO2/rGO/NPAN修饰电极的响应峰电流值作校正曲线(内插图),峰电流与亚硝酸根浓度在0.5 μmol/L~51.3 mmol/L范围内呈良好的线性关系,相关系数达0.999,灵敏度为14.075 μA·(mmol/L)-1,检出限(S/N=3)为0.2 μmol/L。
2.8 干扰及实际样品测试
采用电流计法以修饰电极检测实验室配制的不同浓度亚硝酸根样品和河水样品中亚硝酸根离子的浓度。从表1可以看出,实际样品检测结果的相对标准偏差(RSD)为0.16%~2.7%,表明修饰电极具有优异的重现性。
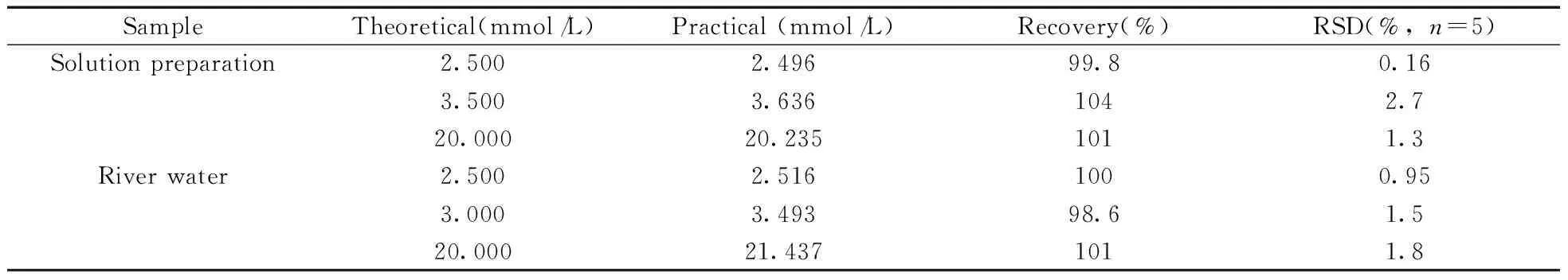
表1 修饰电极对实际样品溶液的检测Table 1 The determination of practical solution containing nitrite by modified electrodes
3 结 论
基于二氧化锰的独特性能,采用滴涂法将水热法制备的二氧化锰修饰于rGO/NPAN复合电极上,从而制备了MnO2/rGO/NPAN修饰电极并研究了该修饰电极的电化学行为。实验结果表明,MnO2/rGO/NPAN修饰电极对亚硝酸根有良好的电催化活性,且在二氧化锰质量浓度为0.25 g/L,支持电解质溶液的pH值为6.8时,催化效果最好。该修饰电极检测亚硝酸根的浓度范围为0.5×10-6~5.13×10-2mol/L,灵敏度为14.075 μA·(mmol/L)-1,响应时间短(小于4 s),检出限为0.2 μmol/L,相比于rGO/NPAN以及MnO2修饰电极,MnO2/rGO/NPAN修饰电极检测亚硝酸根有更宽的检测范围,更低的检出限以及更高的灵敏度。
[1] Han J T,Lu Y,Zhong X,Guo X H,Xu C X.Metall.Anal.(韩金土,芦洋,钟翔,郭晓海,许春萱.冶金分析),2015,35(2):12-17.
[2] Qin S J,Jin W Y ,Hai H.Mod.FoodSci.Technol.(覃世杰,金文英,海洪.现代食品科技),2013,(6):1400-1402.
[3] Rehman A U,Yaqoob M,Waseem A,Nabi A.Luminescence,2012,27(5):419-425.
[4] Wang N,Wang R Q,Zhu Y.J.Hazard.Mater.,2012,235/236(2):123-127.
[5] Peng G,Zhang M,Hou H,Xiao Q.Mater.Res.Bull.,2008,43(3):531-538.
[6] Lee J H,Hong H G.J.Appl.Electrochem.,2015,45(10):1153-1162.
[7] Kozub B R,Rees N V,Compton R G.Sens.ActuatorsB,2010,143(2):539-546.
[8] Zhang S L,Hang N T,Zhang Z J,Yue H Y,Yang W.Nanomaterials,2017,7(12):1-11.
[9] Khan U,Ryan K,Blau W J,Coleman J N.Compos.Sci.Technol.,2007,67(15/16):3158-3167.
[10] Zhang J L,Yang B,Guo Z R,Song Q,Ye X A,Zheng S.J.Electrochem.Soc.,2017,164(5):B3001-B3007.
[11] Nguyen K T,Li D H,Ma X,Liu Z N,Zhu L L,Gruner G,Qiong Q H,Zhao Y L.ACSAppl.Mater.Inter.,2013,5(16):8105-8110.
[12] Mani V,Periasamy A P,Chen S M.Electrochem.Commun.,2012,17(1):75-78.
[13] Sharma R K,Sahu V,Grover S,Goel S,Singh G.ACSSustain.Chem.Eng.,2015,3(7):1460-1469.
[14] Fan Y,Liu J H,Yang C P,Yu M,Liu P.Sens.ActuatorsB,2011,157(2):669-674.
[15] Lin K C,Chen Y H,Chen S M.Int.J.Electrochem.Sci.,2015,10(11):9205-9215.
[16] Huang Y,Cheng C M,Tian X Q,Zheng B Z,Li Y,Yuan H Y,Xiao D,Choi M.Electrochim.Acta,2013,89:832-839.
[17] Zhang J T,Zhao Z H,Xia Z H,Dai L M.Nat.Nanotechnol.,2015,10(5):444-452.
[18] Han G Q,Liu Y,Zhang L L,Kan E,Zhang S P,Tang J,Tang W H.Sci.Rep.,2014,4(4824):1-7.
[19] Yang S M,Zha W L,Sun Q,Li H,Li R Q,Shang P L.Chin.J.Appl.Chem.(杨绍明,查文玲,孙清,李红,李瑞琴,尚培玲.应用化学),2014,31(6):742-748.
[21] Feng J J,Zhang P P,Wang A J,Zhang Y,Dong W J,Chen J R.J.Colloid.Interf.Sci.,2011,359(1):1-8.
[22] Wei Z K,Hua X Z,Xiao K,Zhou X L,Ye Z G.J.Electrochem.(危震坤,华小珍,肖可,周贤良,叶志国.电化学),2015,21(4):393-398.
[23] Zhao K,Song H Y,Zhuang S Q,Dai L M,Hei P G,Fang Y Z.Electrochem.Commun.,2007,9(1):65-70.
