纳米金/石墨烯修饰电极测定食品中的诱惑红
2018-01-22,,
,,
(1.菏泽学院化学化工系,山东菏泽 274015; 2.山东省菏泽市疾病预防控制中心,山东菏泽 274000; 3.菏泽学院生命科学系,山东菏泽 274015)
食品色素广泛应用于食品行业,主要用于改善食品的外观以吸引消费者。与天然色素相比,合成色素因其稳定、颜色均匀、微生物污染程度低、生产成本低等优点得到了广泛应用[1]。然而,一些合成色素对人体是有害的,特别是用量过度时[2]。因此,许多食品色素用量的控制在食品工业中是相当重要的。
诱惑红(6-羟基-5-(2-甲氧基-4-磺酸-5-甲苯基)偶氮萘-2-磺酸二钠盐,AR)是一种食品色素,因其具有鲜艳的深红色,所以在食品工业中常添加于饮料和糖果中来改善它们的色泽。有文献报道,AR在大鼠中表现出毒性,并分解产生一些有毒的致突变和致癌的芳香胺类物质[3-4],可以诱导小鼠肠内DNA的损伤[5],在食品中过量使用会对人体造成许多危害。因此建立准确测定AR的方法是非常必要的。
目前,测定AR的方法主要有高效液相色谱法[6-9]、分光光度法[10]等,这些方法存在操作复杂、浪费大量有机溶剂、费时、成本高,而且灵敏度不高的缺点。而电化学方法成本较低,操作相对简单,检测速度相对快。例如有文献报道[11]用石墨烯和TiO2复合的修饰电极可以增大AR的氧化峰电流信号,建立了一种新的、灵敏的电化学检测AR的方法。氨基酸修饰电极也有良好的催化性能,利用甘氨酸[12]以及L-精氨酸与石墨烯修饰电极[13]也可以提高检测AR的灵敏性与选择性。
石墨烯具有独特的力学、热学、电学及光学等性能,已被广泛用于电极的制备[14-16]。金属纳米粒子(铂、金、银等)导电性好,电催化活性以及化学稳定性较好,也已广泛用作传感器的制备[17-19]。在各种金属纳米颗粒中,金纳米颗粒因为其独特的性能(良好生物相容性、导电性和有良好的协同作用)可以提高石墨烯修饰电极的灵敏度和稳定性。纳米金/石墨烯修饰电极已经用于检测对苯二酚和邻苯二酚,结果表明纳米金/石墨烯复合材料可作为一种高性能传感材料进行某些环境污染物的选择性检测[20]。此外,石墨烯作为生物传感器可以检测葡萄糖[21],表现出了非常高的灵敏性和非常好的选择性。
本研究利用纳米金和石墨烯这两种具有催化活性的物质制备修饰电极,讨论AR在纳米金/石墨烯修饰玻碳电极上的电化学行为,建立一种测定食品中诱惑红含量的新方法,具有良好的实际应用前景。
1 材料与方法
1.1 材料与仪器
诱惑红(AR) 纯度>99%,天津化学制剂研究所,配制8.00×10-4mol/L的标准溶液;石墨烯 自制;四氯金酸 分析纯,阿拉丁试剂有限公司,配成1.00×10-2mol/L溶液;金色的功能饮料和彩色硬质糖果 市售。
CHI660E型电化学分析系统 上海辰华公司;KQ-100型超声波清洗器 昆山市超声仪器有限公司;电化学工作用三电级系统:玻碳电极(工作电极)、铂丝电极(对电极)和Ag/Agcl电极(参比电极) 上海辰华仪器有限公司;85-1型恒温磁力搅拌器 中外合资深圳天南海北有限公司;SYZ-550型石英亚沸高纯水蒸馏器 江苏金坛仪器有限公司;GUOHUA800型低速电动离心机 中外合资深圳天南海北有限公司;红外灯(MT) 中山市古镇鑫煌灯饰电器厂。
1.2 实验方法
1.2.1 样品制备 饮料:取100 mL饮料放入烧杯,在电炉上加热浓缩至约40 mL以去除CO2的影响,冷却后蒸馏水定容至100 mL,备用。
硬质糖果:称取5.0 g糖果,用水溶解,蒸馏水定容至100 mL,备用。
1.2.2 修饰电极的制备
1.2.2.1 石墨烯修饰电极的制备 将玻碳电极(Φ=3.8 mm)在湿润的金相砂纸(粒度为2000)上磨光,然后用中性氧化铝(0.05 μm)悬乳液抛光成镜面,依次用硝酸(1∶1,v/v)、乙醇、亚沸蒸馏水超声清洗(1 min/次),然后用蒸馏水进行充分洗涤,用红外灯烘干水分。
在玻碳电极的表面滴加一定量的石墨烯悬浮液,在红外灯下烘干,制得了石墨烯修饰电极。石墨烯悬浮液用量对修饰电极的性能有一定的影响,固定石墨烯修饰液浓度为0.3 mg/mL,改变石墨烯修饰液的用量,每次制备的电极测定4.00×10-5mol/L的AR标准溶液,得到最佳的石墨烯用量。
1.2.2.2 纳米金/石墨烯修饰电极的制备 在5 mmol/L HAuCl4溶液中,以0.1 mol/L KNO3为支持电解质,以石墨烯修饰玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极为参比电极,在-0.2~1.0 V范围内采用循环伏安法制备纳米金/石墨烯修饰电极。扫描速度和扫描周数对修饰电极的性能也有一定的影响,采用固定HAuCl4浓度,改变扫描速度与扫描周数进行实验,找出最佳的扫描速率和周数。
1.2.3 底液pH的确定 底液的酸碱度对AR氧化还原峰有一定的影响。分别用pH2.2~8.0的缓冲溶液作为底液进行测定,得出最佳pH。
1.2.4 测试高低电位的确定 以纳米金/石墨烯修饰玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极作为参比电极。固定高电位为0.90 V,改变低电位测定4.00×10-5mol/L的AR标准溶液(pH=5.0),得到最佳低电位。用同样的方法改变高电位进行实验,确定最佳高电位。
1.2.5 搅拌时间的确定 以纳米金/石墨烯修饰玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极作为参比电极。在-0.8~0.8 V的电位范围内,扫描速率100 mV/s下扫描,测定4.00×10-5mol/L的AR标准溶液(pH=5.0),改变搅拌时间进行实验,根据所测AR氧化峰电流最大时确定搅拌时间。
1.2.6 扫描速率的确定 以纳米金/石墨烯修饰玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极作为参比电极。在-0.8~0.8 V的电位范围内,改变扫描速率测定4.00×10-5mol/L的AR标准溶液(pH=5.0),得出最佳扫描速率。
1.2.7 工作曲线、重现性、稳定性和干扰性实验 在最佳实验条件下,以纳米金/石墨烯修饰玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极作为参比电极浸入含有一定体积的AR标准溶液、10 mL PBS缓冲溶液和9 mL二次水的烧杯中。测定前搅拌40 s,在-0.8~0.8 V的电位范围内,扫描速率100 mV/s下扫描测定,记录相应循环伏安曲线。
1.2.8 回收率测定实验 在最佳实验条件下,以纳米金/石墨烯修饰玻碳电极为工作电极浸入10.00 mL的待测样品中,铂丝电极为对电极浸入一定量的标准液中,Ag/AgCl电极作为参比电极侵入10.00 mL pH=5.0 PBS磷酸盐缓冲溶液。测定前搅拌40 s,在-0.8~0.8 V的电位范围内,扫描速率100 mV/s下扫描测定,记录相应循环伏安曲线,分别对含有诱惑红的饮料和硬质糖果进行测定。
2 结果与讨论
2.1 石墨烯用量的选择
改变石墨烯滴涂体积进行实验。结果表明:当石墨烯用量为5 μL时,AR的氧化还原峰峰电流最大。而当石墨烯悬浮液体积大于5 μL时,AR在修饰电极上的的氧化还原峰峰电流随石墨烯滴涂体积的增大而逐渐降低。这可能是因为电极表面的修饰膜过厚,使得电极表面的电催化剂很难得到有效利用,阻碍催化底物扩散到电极的表面。因此,选择石墨烯用量为5 μL制备修饰电极。

图1 不同石墨烯体积对AR循环伏安曲线的影响Fig.1 Cyclic voltammograms of AR at different volume of grapheme on the gold nanoparticle/graphene modified electrode
2.2 纳米金修饰条件的选择与电极的表征
分别改变扫描速度和扫描周数制备纳米金/石墨烯电极,结果表明:扫描速度较低或扫描周数较多时,纳米金颗粒会发生聚集现象,颗粒较大,而且对AR的催化作用降低。当扫描速率为40 mV/s(图2a)、循环扫描3周(图2b)时,所制备的纳米金颗粒较为细小、均匀,而且对AR催化效果最好。因此选择扫描速率为60 mV/s、循环扫描3周制备修饰电极。对制备的石墨烯和纳米金/石墨烯电极用扫描电镜分别进行了表征,结果如图3所示。通过对比可以看出在石墨烯修饰电极表面生成了较为均匀的纳米金粒子。

图3 石墨烯修饰电极(A)、纳米金/石墨烯修饰电极(B)扫描电镜图Fig.3 SEM image of graphene modified electrode(A) and gold nanoparticle/graphene modified electrode(B)
2.3 AR在纳米金/石墨烯修饰电极上的电化学行为
图4为AR在四种电极上的循环伏安曲线,分别是:a裸电极、b纳米金修饰电极、c石墨烯修饰电极及和d纳米金/石墨烯修饰电极。可以看出,AR在裸电极上电流相应微弱,在纳米金修饰电极上氧化峰电流ipa=13.82 μA,还原峰电流ipc=18.93 μA;在石墨烯修饰电极上ipa=17.05 μA,ipc=19.33 μA;而在纳米金/石墨烯修饰电极ipa=38.31 μA,ipc=46.44 μA,即峰电流明显增大,大大提高了对AR的测定灵敏度,这可能是因为石墨烯的良好导电性和大量的活性官能团,使其具有良好的催化活性;而纳米金也具有良好的导电性能,二者的协同效应,使纳米金/石墨烯修饰电极对AR催化效果更佳明显,从而在此电极上峰电流值最大。AR在纳米金/石墨烯修饰电极上氧化还原峰电位分别为Epa=0.137 V,Epc=0.045 V,ipa/ipc=0.82<1,ΔE=Epa-Epc=0.09,因此AR在修饰电极上的电极反应为准可逆过程。
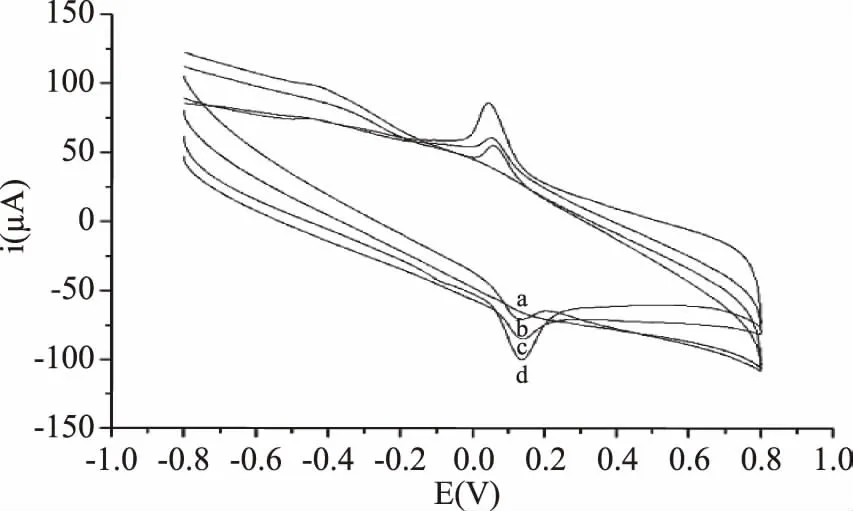
图4 4.00×10-5 mol/L AR在裸电极(a)、纳米金修饰电极(b)、石墨烯修饰电极(c)和纳米金/石墨烯修饰电极(d)上的循环伏安曲线Fig.4 Cyclic voltammograms of 4.00×10-5 mol/L AR at bare electrode(a),gold nanoparticle modified electrode(b),graphene electrode(c)and gold nanoparticle/graphene modified electrode(d)
2.4 测定AR的条件研究
2.4.1 测定底液的最佳pH 图5结果表明,在pH=2.2~5.0范围内随pH的增大AR氧化峰电流逐渐增大,pH5.0时峰电流值最大,pH>5.0时,峰电流值逐渐减小。因此测定底液的最佳pH为5.0。从图5还可看出,不同pH下测定的循环伏安曲线不同,随着pH增大,其氧化峰发生负移。当pH的范围在2.2~8.0之间时氧化峰电位与pH呈线性关系(图5内插图),回归方程为Epa(V)=-0.062pH+0.46,r=0.9935,其斜率0.062接近于能斯特理论电势值0.059,表明AR的氧化过程有质子参与,且质子转移数m等于电子转移数n。
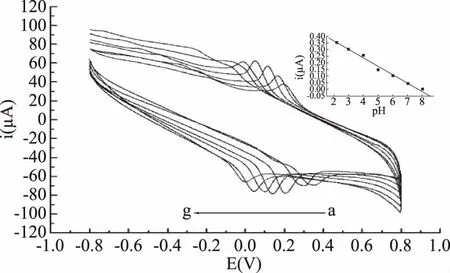
图5 不同pH对4.00×10-5 mol/L AR循环伏安曲线的影响Fig.5 Cyclic voltammograms of 4.00×10-5 mol/L AR at different pH on the gold nanoparticle/graphene modified electrode注:a~g分别对应pH为 2.2、3.0、4.0、5.0、6.0、7.0、8.0,υ=100 mV/s; 内插图为AR氧化峰电位与溶液pH关系曲线。
2.4.2 测试高低电位的选择 通过实验研究电位对峰电流的影响,结果表明,当低电位在-0.20~-0.80 V范围时,峰电流值逐渐增大,而在-0.80~-1.20 V范围内时,峰电流逐渐减小,即低电位为-0.80 V时,AR氧化峰电流值最大(图6)。
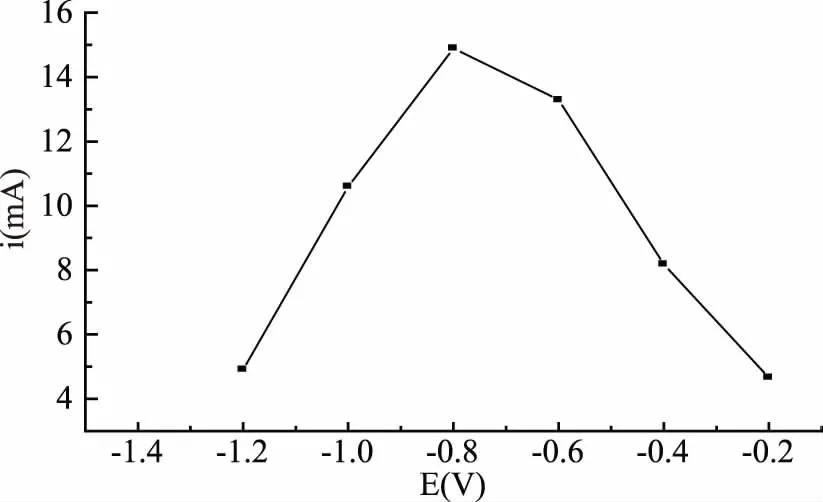
图6 不同低电位值对4.00×10-5 mol/LAR循环伏安曲线的影响Fig.6 Cyclic voltammograms of 4.00×10-5 mol/L AR at different low electric potential values on the gold nanoparticle/graphene modified electrode
固定低电位-0.80 V,改变高电位的值。实验结果表明:当高电位在0.40~0.80 V范围内时,峰电流值呈增大趋势,而在0.80~1.40 V范围内时,峰电流值呈减小趋势,因此选择测定的高电位为0.80 V(图7)。

图7 不同高电位值对4.00×10-5 mol/LAR循环伏安曲线的影响Fig.7 Cyclic voltammograms of 4.00×10-5 mol/L AR at different high electric potential values on the gold nanoparticle/graphene modified electrode
2.4.3 搅拌时间的选择 测定前对测定溶液进行搅拌(200 r/min),搅拌时间不同,AR在纳米金/石墨烯修饰电极表面上的吸附程度不同,影响实验测定结果。实验结果表明,测定的峰电流值随搅拌时间的增加而呈现先增加后减小的趋势,当搅拌时间为40 s时,峰电流值最大,因此测定AR溶液的最佳搅拌时间选定为40 s(图8)。
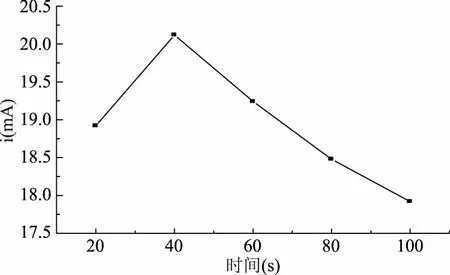
图8 不同搅拌时间对4.00×10-5 mol/LAR循环伏安曲线的影响Fig.8 Cyclic voltammograms of 4.00×10-5 mol/L AR at different stirring time on the gold nanoparticle/graphene modified electrode
2.4.4 扫描速率的影响 实验结果表明(图9)在20~300 mV/s的变化范围内,随扫描速率增大氧化峰电流也增大,并且氧化峰电流与扫描速率呈线性关系,即ipa(μA)=3.99+0.19 υ(mV/s),r=0.9977,说明AR在纳米金/石墨烯修饰电极上的氧化还原过程为吸附控制过程。但扫描速率过大导致灵敏度降低,因此选定100 mV/s为测定扫描速度。
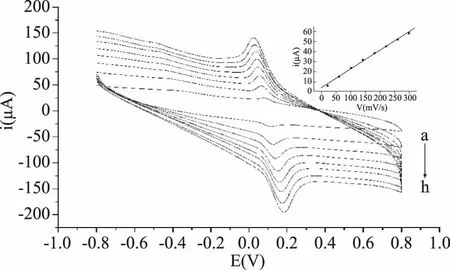
图9 不同扫描速率下的循环伏安曲线Fig.9 Cyclic voltammograms at different scan rate values注:a~h对应扫描速度分别为:20、60、100、140、180、220、260、300 mV/s;内插图为AR氧化峰电流与扫描速度关系曲线。
AR在纳米金/石墨烯修饰电极上的氧化峰与还原峰电位值随lg υ变化的关系曲线如图9所示,由描述准可逆薄层电化学的Laviron理论可知:
Epa=a+[2.303RT/(1-α)nαF]lgυ
式(1)
Epc=b-(2.303RT/αnαF)lgυ
式(2)
其中:α为电子传递系数,nα为电子转移数,a、b为常数。在最佳测试条件下,扫速在60~340 mV/s范围内,氧化峰与还原峰电位值随lgυ变化的关系可表示为Epa==-0.020+0.081lgυ,r=0.9973(图10a);Epc=0.170-0.059 lgυ,r=0.9961(图10b)。根据式(1)、(2)可求出电子转移数nα=0.54,电子传递系数α=0.58,接近于理论值0.5,符合准可逆过程的特征。
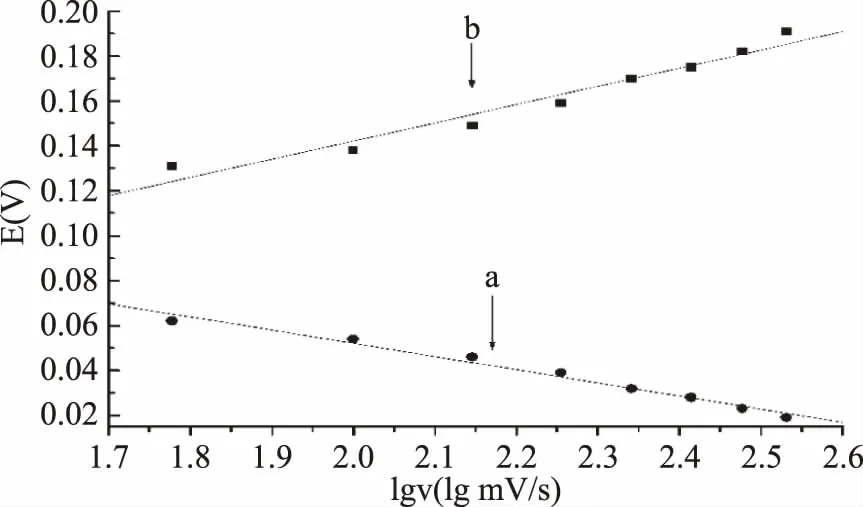
图10 4.00×10-5 mol/L AR氧化还原峰电位与扫描速度对数变化关系曲线Fig.10 Plots of the peak potentials of 4.00×10-5 mol/L AR versus the logarithms of the scan rates
2.5 AR测定的标准曲线、检出限和重现性
2.5.1 标准曲线和检出限 实验结果表明在8.00×10-8~1.00×10-5mol/L的范围内,AR的氧化峰电流值与AR溶液浓度呈良好的线性关系(图11),其线性方程为:ipa(μA)=1.87×10-6+1.02c,相关系数为r=0.9983,检出限为8.00×10-9mol/L。
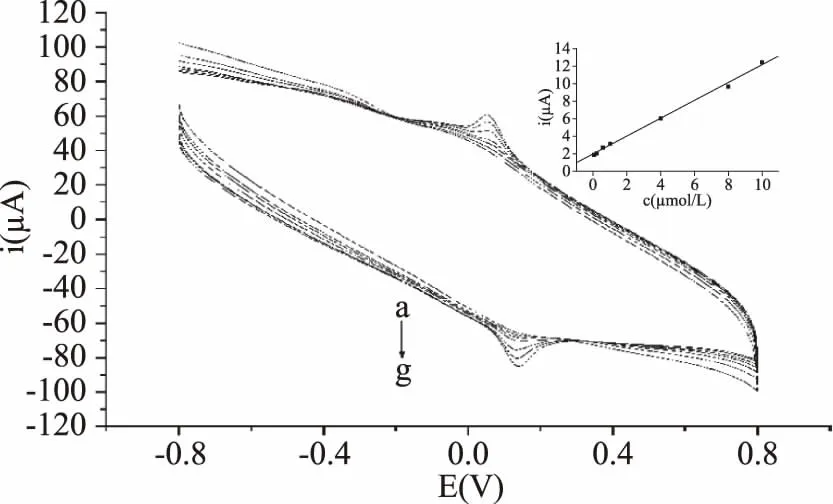
图11 不同浓度的AR在纳米金/石墨烯修饰电极上的循环伏安曲线Fig.11 Cyclic voltammograms of 4.00×10-5 mol/L AR at different consetrations on the gold nanoparticle/graphene modified electrode at different concentrations注:a~g对应AR溶液浓度分别为: 8.00×10-8、2.00×10-7、6.00×10-7、1.00×10-6、 4.00×10-6、8.00×10-6、1.00×10-5 mol/L; 内插图为AR氧化峰电流与浓度关系曲线。
2.5.2 重现性 对pH=5.0的4.00×10-5mol/L 的AR溶液平行测定6次,RSD=2.6%,可以看出电极具有良好的重现性。
2.6 干扰实验

2.7 回收率的测定
在最佳实验条件下,分别对含有AR的饮料和硬质糖果进行回收率实验,结果见表1,回收率为96.9%~101.6%。以上样品中诱惑红含量均符合国家标准。

表1 样品中AR回收率测定(n=6)Table 1 Recovery measurements of the AR in food samples(n=6)
3 结论
纳米金/石墨烯修饰电极对AR的电化学氧化具有良好的电催化作用,可明显增大其电流响应信号。利用纳米金/石墨烯修饰电极可以实现对食品中AR进行的检测,回收率在96.9%~101.6%之间。这种方法具有较高的灵敏度、重现性和稳定性,简单方便,建立了一种测定食品中诱惑红含量的新方法,具有良好的实际应用前景。
[1]Kashanian S,Zeidali S H,Omidfar K,et al. Multi-spectroscopic DNA interaction studies of sunset yellow food additive[J]. Molecular Biology Reports,2012,39(12):10045-10051.
[2]Pourreza N,Rastegarzadeh S,Larki A. Determination of allura red in food samples after cloud point extraction using mixed micelles[J]. Food Chemistry,2011,126(3):1465-1469.
[3]Tsuda S,Murakami M,Matsusaka N,et al. DNA damage induced by red food dyes orally administered to pregnant and male mice[J]. Toxicological Sciences,2001,61(1):92-99.
[4]Chung K T. Mutagenicity and carcinogenicity of aromatic amines metabolically produced from azo dyes[J]. Journal of Environmental Science & Health Part C,2000,18(1):51-74.
[5]Shimada C,Kano K,Sasaki Y F,et al. Differential colon DNA damage induced by azo food additives between rats and mice[J]. Journal of Toxicological Sciences,2010,35(4):547-554.
[6]沈坚,傅晓,潘旭,等.高效液相色谱法测定动物性食品中合成色素[J].理化检验-化学分册,2011,47(2):139-143.
[7]蒋晓彤,陈国松,姜玲玲,等.高效液相色谱法同时检测6种甜味剂[J].食品科学,2011,32(6):165-168.
[8]胡汉高,张红菱,李静娜,等. 二极管阵列高效液相色谱法测定果冻制品中诱惑红[J].武汉工业学院学报,2011,30(3):22-25.
[9]Yoshioka N,Ichihashi K. Determination of 40 synthetic food colors in drinks and candies by highperformance liquid chromatography using a short column with photodiode array detection[J].Talanta,2008,74(5):1408-1413.
[10]饶通德,陈书鸿,张六一,等.磁性分离富集-分光光度法测定食品中的诱惑红[J].光谱实验室,2012,29(4):2164-2168.
[11]Gan T,Sun J Y,Zhu H J,et al. Synthesis and characterization of graphene and ordered mesoporous TiO2as electrocatalyst for the determination of azo colorants[J]. Journal of Solid State Electrochemistry,2013,17(8):2193-2201.
[12]孙章华,陈美凤,尹明静,等.聚甘氨酸修饰电极测定食品中的诱惑红[J].食品与发酵工业,2014,40(12):185-189.
[13]胡晴晴,陶姣姣,刘旭,等.聚 L-精氨酸/石墨烯修饰电极测定诱惑红[J].化学传感器,2016,36(2):57-61.
[14]Pumera M. Graphene-based nanomaterials and their electrochemistry[J]. Chemical Society Reviews,2010,39(11):4146-4157.
[15]Zhu C Z,Yang G H,Li H,et al. Electrochemical sensors and biosensors based on nanomaterials and nanostructures[J]. Analytical Chemistry,2015,87(1):230-249.
[16]Zhang Y,Su M,Ge L,et al. Synthesis and characterization of graphene nanosheets attached to spiky MnO2nanospheres and its application in ultrasensitive immunoassay[J]. Carbon,2013,57(3):22-33.
[17]Zhang Y Y,Bai X Y,Wang X M,et al. Highly sensitive graphene-Pt nanocomposites amperometric biosensor and its application in living cell H2O2detection[J].Analytical Chemistry,2014,86(19):9459-9465.
[18]Zhang Y,Zeng G M,Tang L,et al. Electrochemical sensor based on electrodeposited graphene-Au modified electrode and nano-Au carrier amplified signal strategy for attomolar mercury detection[J]. Analytical Chemistry,2015,87(2):989-996.
[19]Aziz A,Lim H N,Girei S H,et al. Silver/graphene nanocomposite-modified optical fiber sensor platform for ethanol detection in water medium[J]. Sensors & Actuators B Chemical,2014,206:119-125.
[20]Ma X M,Liu Z N,Qiu C C,et al. Simultaneous determination of hydroquinone and catechol based on glassy carbon electrode modified with gold-graphene nanocomposite[J]. Microchimica Acta,2013,180:461-468.
[21]Hui J N,Cui J W,Liu L J,et al. An effective amperometric biosensor based on graphene modified gold nanowire arrays for glucose detection[J]. Chinese Science Bulletin,2014,59(17):2012-2016.
