外周血幼稚淋巴细胞、染色体、E2A/PBX1、TEL/AML1、MLL融合基因联合检测用于儿童淋巴细胞白血病的早期诊断
2018-01-20赵理平周传恩崔娓李科成苏文
赵理平,周传恩,崔娓,李科成,苏文
据报道,目前儿童急性淋巴细胞白血病(cALL)发病率有上升趋势,严重威胁儿童生命健康[1,2]。一直以来,实行骨髓穿刺术抽取骨髓,检查其细胞形态是白血病早期诊断的“金标准”,可这种取材方法创伤性大,对儿童尤其是低龄儿来说极其痛苦及不便。外周血细胞是由骨髓原始干细胞发育、分化而来,无论白血病的何种阶段,理论上外周血都有相应的改变。抽取外周血相比骨髓穿刺创伤性小,能很大程度减轻患儿痛苦。白血病作为一种造血细胞克隆性疾病,细胞遗传学改变在其发生、发展中起着重要作用[3],近年来,随着细胞遗传学和分子生物学技术的发展,染色体核型分析和融合基因检测在白血病的诊断中逐渐占据重要位置,其不仅从分子水平上进一步阐明白血病发病机制,还用于白血病的分子生物学分型,本文通过抽血这种无创式取材,联合检测外周血幼稚淋巴细胞、染色体、融合基因,以探讨其对儿童淋巴细胞白血病早期诊断或提示性诊断的临床意义。
1 资料与方法
1.1 研究对象 我院2012年8月至2017年6月门诊及住院儿童外周血涂片初查异常淋巴细胞的病例220例,年龄3月~12岁,其中男128例,女92 例,男:女=1.4:1。
1.2 试剂和仪器 外周血幼稚淋巴细胞形态学检查所用瑞氏染料及染色体制备所用吉姆萨染料由广州达晖生物技术有限公司提供;染色体培养基由广州白云山拜迪生物医药有限公司提供;Imager Z2型号蔡司全自动染色体核型分析仪扫片;Vysis探针试剂盒;荧光显微镜。
1.3 方法
1.3.1 外周血涂片 常规消毒行外周血采集后制成血涂片,干燥固定,瑞氏染色,OLYMPUSCH2显微镜油镜下观察异常淋巴细胞并进行分类计数。
1.3.2 染色体制备 对外周血细胞形态检查高度怀疑急性淋巴细胞白血病患者抽取静脉血进行染色体培养、制备、G显带,核型报告参照《人类细胞遗传学国际命名体制ISCN2013》进行描述。
1.3.3 融合基因检测 对外周血细胞形态检查高度怀疑急性淋巴细胞白血病患者抽取静脉血FISH技术检测融合基因。
2 结果
220例患者中,33例外周血异常淋巴细胞阴性,187例阳性,在阳性患者中有24例外周血涂片可观察到一种“特殊类型”的异常幼稚淋巴细胞,这种细胞异型性更明显,外形明显不规则,细胞核粗颗粒状,暂称为“白血病型”幼稚淋巴细胞(图1),在外周血细胞中占比范围在1%~38%,其中比例范围在1%~10%有3例,比例范围在11%~20%有11例,比例范围在21%~38%的有10例,这24例患者后经骨髓检查验证,除比例范围在1%~10%中的2例外,其余22例均诊断为急性淋巴细胞白血病。对比例在11%~20%的11例患者及比例在21%~38%的10例患者均抽取静脉血检查染色体、融合基因(因比例高易于染色体、融合基因阳性的检出),结果比例在11%~20%的11例患者染色体均未见异常,未检出融合基因9例,检出融合基因2 例,其中 1例 TEL/AML1 阳性(男性)(图 2),1 例E2A/PBX1(即 PBX1/TCF3)阳性(男性)(图 3)。 比例在21%~38%的10例患者中8例染色体未见异常,2例染色体异常(均为结构异常,男性),其中1例为 46,XY,t(1;19)(q23;p13)(图 4),1 例为 46,XY,t(4;11)(q21;q23)(图 5),未检出融合基因 4 例,检出融合基因6例,其中4例TEL/AML1阳性(男性2例, 女性2例),1例E2A/PBX1阳性 (男性),1例MLL阳性(男性)(图6),图中白色箭头所示为阳性信号。结果见表1。
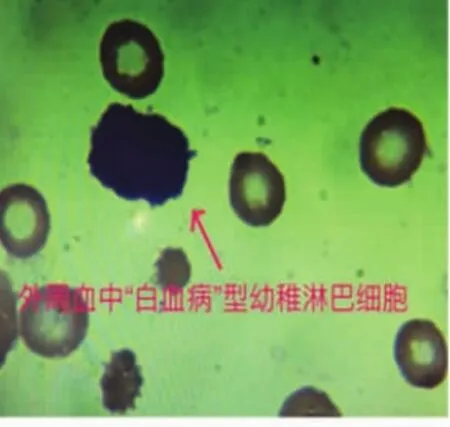
图1 “白血病型”幼稚淋巴细胞 (瑞氏染色,×1000)

图2 FISH检测TEL/AML1阳性

图3 FISH检测E2A/PBX1阳性
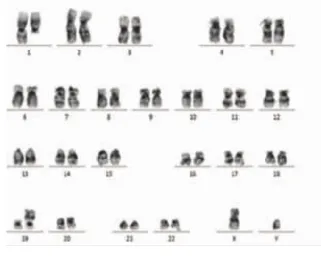
图4 G显带染色体核型 t(1;19)(q23;p13)

图5 G显带染色体核型 t(4;11)(q21;q23)

图6 FISH检测MLL阳性
3 讨论
外周血出现异常淋巴细胞增多一部分是由于病毒感染等因素刺激淋巴细胞增生亢进,使之发生不平衡而导致的一种机体反应,一部分却是恶性肿瘤细胞对骨髓及外周血的浸润,是恶性肿瘤的早期提示。本文24例患者外周血涂片观察到的“特殊类型”的异常幼稚淋巴细胞增多就是恶性肿瘤的早期提示,这种细胞(暂称为“白血病型”幼稚淋巴细胞)具有共同特点:异型性更明显,外形明显不规则,细胞核粗颗粒状,可见核沟等,本文研究中这种细胞在外周血细胞中占比范围在1%~38%。这24例患者后经骨髓检查验证有22例均确诊为急性淋巴细胞白血病,说明外周血幼稚淋巴细胞形态学检查对儿童淋巴细胞白血病具有一定的早期诊断及提示性诊断作用。
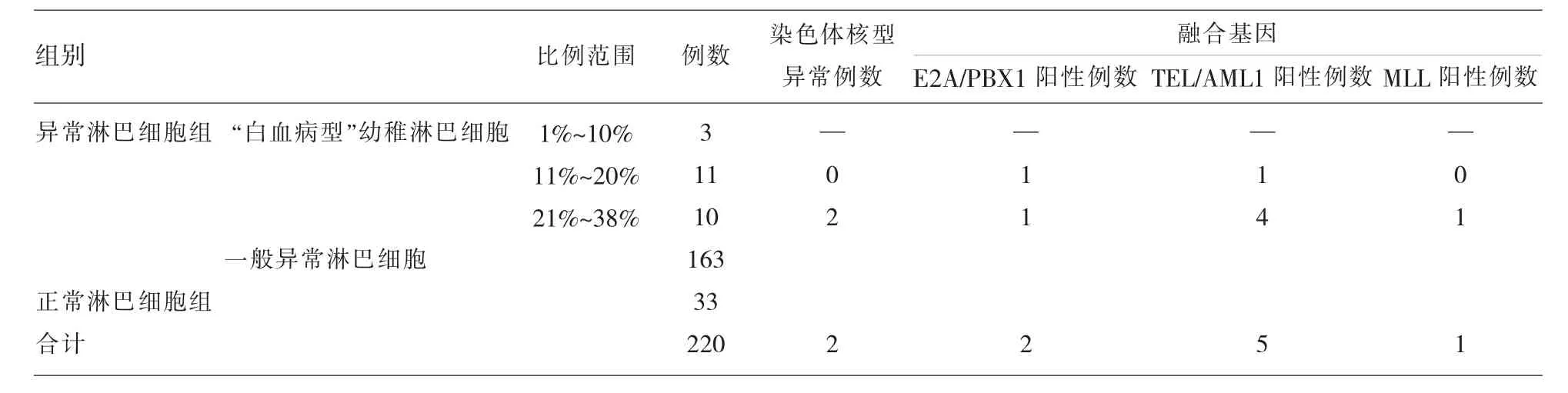
表1 220例患者外周血涂片结果及21例染色体、融合基因检查结果
染色体畸变与白血病发病密切相关[4]。染色体畸变导致原癌基因或抑癌基因结构变异,原癌基因激活或抑癌基因失活,产生新的融合基因,编码融合蛋白。迄今报道涉及50多种特异的染色体易位形成的融合基因[4]。儿童急性淋巴细胞白血病(cALL)中,染色体畸变检出率最高的核型是t(12;21)(p13;q22);t(1;19)(q23;p13);t(9;22)(q34;q11);t(4;11)(q21;q23)等。 文献[5-10]报道儿童 ALL 中最常见的融合基因包括t(12;21)易位形成的TEL/AML1融合基因,t(1;19)易位形成的E2A/PBX1融合基因,t(9;22)易位形成的BCR/ABL融合基因以及t(4;11)易位形成的AF4/MLL融合基因,而这4种融合基因中TEL/AML1是小儿ALL最常见的基因改变[11],本文21例检查融合基因E2A/PBX1、TEL/AML1、MLL,有 5例 TEL/AML1阳性,仅有 2例E2A/PBX1阳性,1例MLL阳性,说明TEL/AML1较其他融合基因常见,与之相符。TEL/AML1基因融合是由t(12;21)(p13;q22)易位使12号染色体上的TEL基因的螺旋2环2螺旋结构域融合到21号染色体上的AML1基因的DNA结合域和转录活化域而形成的,常伴有其他TEL基因的缺失[12]。二者融合之后,AML1由转录活化因子转变为抑制因子是白血病发病的分子基础。由于t(12;21)易位片段G显带十分相似,通常不引起染色体的形态改变,常规核型分析对其的检出率不足0.05%[13]。本文5例TEL/AML1阳性患者染色体核型未检出异常,检出率低,与报道相符。而FISH技术弥补了这一不足。染色体R显带与常规G显带相反,可使G显带不易检出的易位片段易于检出,建议染色体核型分析常规G显带的同时加做R显带可提高染色体畸变的检出率。
儿童ALL中有不足10%的患儿存在t(1;19)(q23;p13),该易位形成 E2A/PBX1 融合基因[14],PBX1蛋白参与细胞的分化调控,融合蛋白使正常PBX1蛋白失活,是导致ALL发病的主要因素[15]。本文21例患者中有1例染色体核型为46,XY,t(1;19)(q23;p13),占 4.8%,融合基因 E2A/PBX1 阳性2例,占9.5%,均不足10%,与报道相符。2例E2A/PBX1阳性患者中1例染色体核型为46,XY,t(1;19)(q23;p13),其外周血异常淋巴细胞比例在21%~38%,而另1例染色体核型正常,其外周血异常淋巴细胞比例在11%~20%,可见染色体核型阳性检出率可能与异常淋巴细胞比例有关。染色体核型分析技术有较多的影响因素,如培养成功率低、敏感性低等,FISH技术可直接检测间期细胞.不需要细胞培养,能分辨较小的染色体易位或缺失区域(相对分子质量50×103左右),因此可以弥补染色体核型分析的不足[16]。
MLL基因位于11q23,白血病时MLL基因会发生重排[17]。MLL基因重排包括缺失、重复、插入及易位。重排的MLL基因丢失了SET和PHD结构域而不能发挥其原有正常功能,即对造血祖细胞的细胞周期及分化的负调控作用,这是MLL基因重排导致白血病的发病机制之一。儿童急性白血病约有5%~10%可检测到MLL基因改变[4]。本文21例患者中有 1例染色体核型为 46,XY,t(4;11)(q21;q23),其融合基因 MLL 阳性,检出率 4.8%,与文献报道相近。此例患者染色体核型与融合基因检测结果相互验证及吻合,其外周血“白血病型”幼稚淋巴细胞比例在21%~38%,可见联合检测外周血幼稚淋巴细胞、染色体、融合基因,对儿童淋巴细胞白血病起到了早期诊断的作用。目前本文研究的例数有限,还有待后期进一步积累数据,加强研究。
综上所述,外周血幼稚淋巴细胞形态学检查对儿童淋巴细胞白血病具有一定的早期诊断及提示性诊断作用。而染色体核型分析与融合基因检测技术从分子水平上进一步阐明白血病发病机制,用于白血病的诊断分型,此两种技术之间又可相互验证及补充。联合检测外周血幼稚淋巴细胞、染色体、E2A/PBX1、TEL/AML1、MLL 融合基因可用于儿童淋巴细胞白血病的早期诊断及提示性诊断,与经典有创的骨髓检查相比,这种无创的检查模式值得临床推广借鉴。
