电喷雾萃取电离-四极杆飞行时间质谱快速分析一次性注射器中的挥发性有机物残留
2018-01-18周文钊黄超群沈成银储焰南
周文钊,陆 燕,夏 磊,黄超群,沈成银,储焰南
(1.中国科学院合肥物质科学研究院,医学物理与技术中心,医学物理与技术安徽省重点实验室,安徽 合肥 230031;2.中国科学技术大学,安徽 合肥 230026)
一次性注射器是一种使用极为广泛的医疗器械,在其生产制作过程中,会使用一些有机溶剂,如杀菌剂、粘合剂、以及橡胶活塞生产过程中添加的各种橡胶助剂等。这些残留在注射器内的有机物具有一定的毒性,进行静脉注射时,这些有机物残留会随着注射药物进入人体血液,从而危害人体健康。例如,用作粘合剂的环己酮进入人体会抑制中枢神经,并导致全身性血压、心率的降低[1]。
目前,检测一次性注射器等医疗器械中的挥发性有机物残留的方法有气相色谱法[2]、气相色谱-质谱法[3]、液相色谱法[4]等。但这些方法需要对样品进行预处理,过程耗时相对较长,无法实现快速检测分析。相比之下,在线质谱技术能够实现样品的快速检测,如质子转移反应质谱是一种快速在线分析技术,具有响应速度快、检测灵敏度高等特点,已成功用于快速检测分析一次性输液管中的环己酮[5]。电喷雾萃取电离质谱技术(EESI-MS)是最近发展起来的一种在线分析方法,该方法无需样品预处理,能够对气体样品进行快速分析[6-7]。本课题组采用电喷雾萃取电离-三重四极杆质谱法分析检测了一次性输液管中的环己酮[8]。
本工作拟在商用ESI离子源的基础上搭建一套EESI离子源,采用电喷雾萃取电离技术,并结合四极杆飞行时间质谱,对不同品牌、不同体积的一次性医用注射器进行快速质谱分析。利用飞行时间质谱的高分辨率,得到化合物的准确质荷比,结合串联质谱分析,实现待测物质的定性,希望为一次性注射器的质量控制提供技术参考。
1 实验部分
1.1 仪器装置与进样
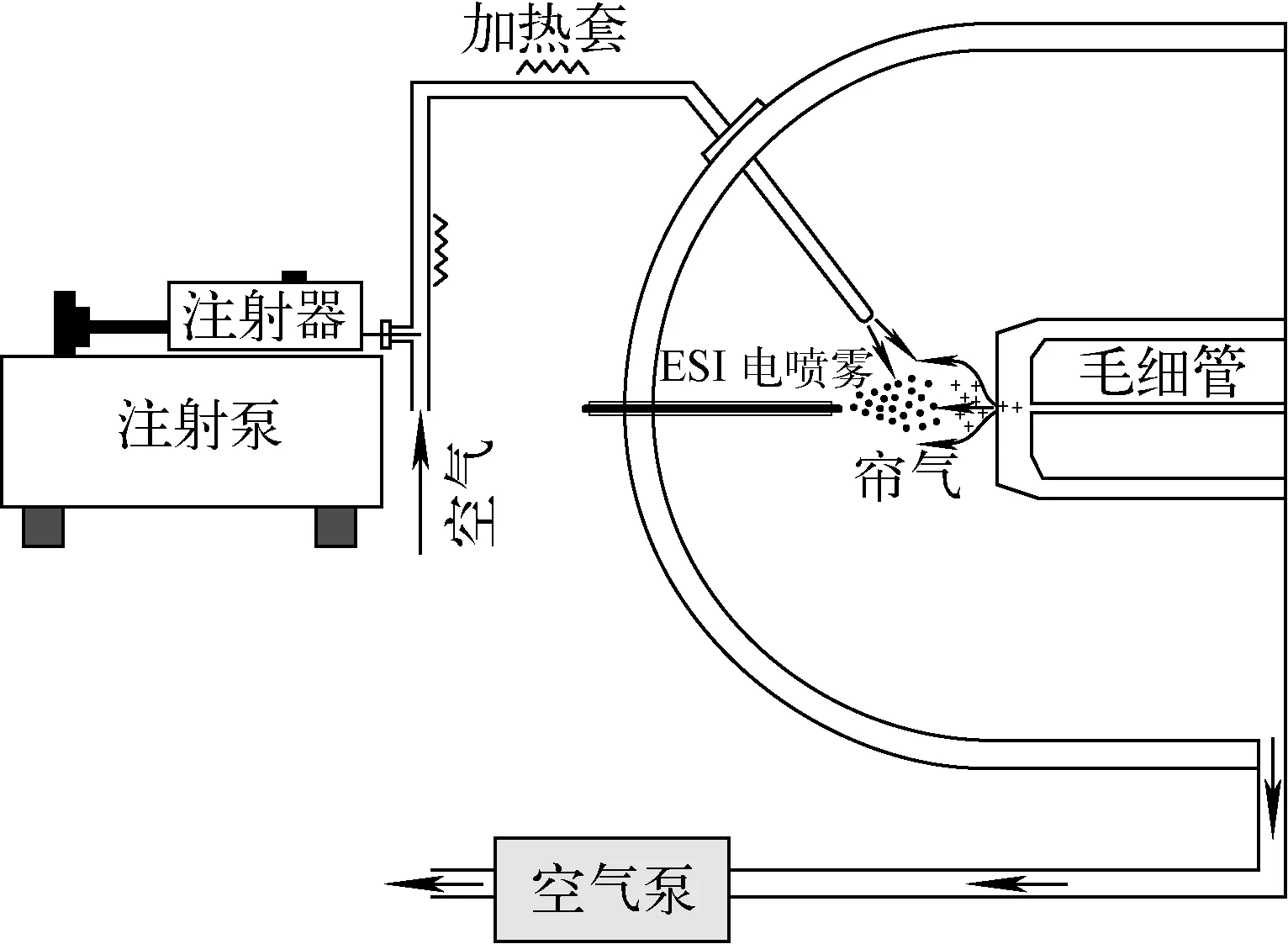
图1 电喷雾萃取离子源示意图Fig.1 Schematic diagram of EESI source
本实验所使用的EESI离子源是在商用ESI离子源基础上改造而成,其结构示于图1。实验中,首先使用一次性注射器抽入实验室空气,然后,利用注射泵把混合了挥发性有机物的空气作为样品气体直接推入三通管路中。样品气体经过长80 cm、内径1.5 mm的聚四氟乙烯管进入离子源内,被电喷雾萃取电离,产生的离子被引入质谱系统进行检测。电喷雾萃取电离所用电喷雾溶液的流量设置为5 μL/min,雾化气压力为60 Pa。为了减少质谱入口的污染,帘气流量和温度分别为4.0 L/min和200 ℃。整个进样管路和三通管都采用聚四氟乙烯材料,管路外包裹加热带,温度维持在100 ℃,以防止样品黏附在管路内壁。另外,由于一次性注射器通常在常温下使用,因此控制实验温度约25 ℃,以考察注射器中有机物的挥发情况。这与一次性注射器的实际使用环境基本相符,可以确保实验结果的可信度。
质谱仪为四极杆飞行时间质谱(Micro-TOF-QⅢ, Bruker Daltonics Inc., Fremont, CA, USA)。实验中,分别利用正、负离子两种检测模式对样品气体进行检测分析。结果表明:正离子模式下的离子种类和信号强度均优于负离子模式,因此后续实验选取正离子模式进行分析。质谱的扫描范围设置为m/z20~200,对化合物进行串联质谱分析时,碰撞诱导解离(CID)的碎裂能量设置为(20±10) eV。
1.2 样品与试剂
一次性注射器样品:医用级注射器,购自当地医院。离子源的电喷雾试剂:含0.1%甲酸的甲醇水溶液(1∶1,V/V);甲醇、甲酸:均为色谱级,德国Sigma公司产品;实验用水:由Thermo Barnstead Micro-Pure纯水系统制得。
1.3 数据处理
由于样品以空气作为载气,因此在数据处理过程中,需对采集到的原始谱扣除空气背景。质谱数据采用DataAnalysis 4.0软件进行处理。
2 结果与讨论
2.1 仪器参数的优化
2.1.1载气流量 环己酮是一次性医疗器械中常见的残留有机物,为了考察载气流量对离子强度的影响,选取环己酮作为检测对象,进行载气流量优化。首先,用500 μL玻璃注射器抽取环己酮标准样品顶空气体,通过注射泵以60 μL/min的速度推入三通管路中,保持其他参数不变,调节载气流量依次为2.0、2.5、3.0、3.5、4.0 L/min,监测环己酮离子(m/z99.080 2)强度的变化,检测结果示于图2a。可以看出,环己酮离子信号强度随载气流量增大而增大,但当载气流量大于3.5 L/min时,环己酮离子强度反而降低。因此,本实验选取的载气流量为3.5 L/min。
2.1.2毛细管电压 毛细管电压的大小会影响样品的电离效率,因此有必要对其进行优化。用500 μL的玻璃注射器抽取环己酮顶空气体,通过注射泵以60 μL/min的速度推入三通管路中,载气流量为3.5 L/min,毛细管电压依次设置为3 000、3 500、4 000、4 500、5 000 V,监测环己酮离子强度的变化,结果示于图2b。可见,环己酮离子的信号强度随毛细管电压增大而增大,但当毛细管电压大于4 000 V后,环己酮离子强度趋于稳定。因此,本实验设置毛细管电压为4 000 V。
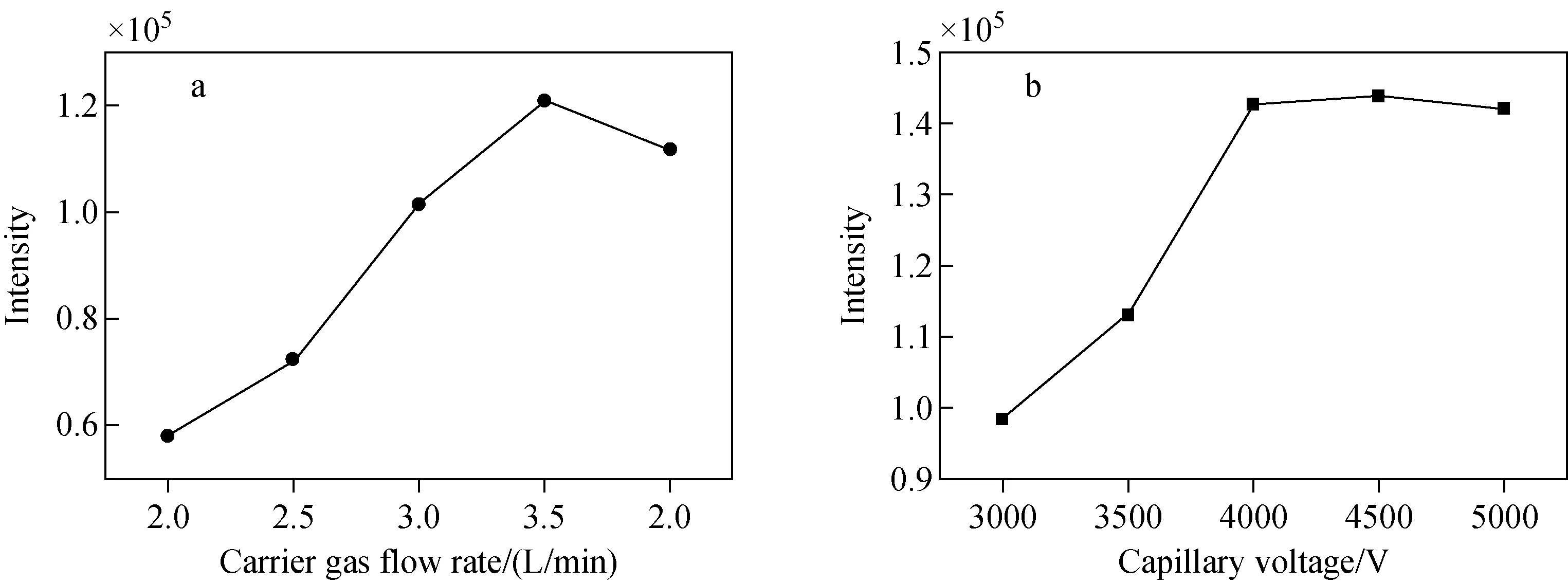
图2 不同的载气流量(a)和毛细管电压(b)下环己酮离子强度的变化趋势Fig.2 Dependence of ion intensity of cyclohexanone on sampling flow rate (a) and capillary voltage (b)
2.2 不同品牌注射器的快速质谱分析
首先选取3种不同品牌(分别标示为①,②,③)、体积均为10 mL的一次性注射器各3个,抽取10 mL实验室空气,再用注射泵以60 μL/min注入离子源,进行质谱检测分析。
扣除空气本底后,从品牌①的2支注射器中得到的质谱图示于图3。可以看出,m/z74.060 2、109.101 6、136.021 9离子的信号强度相对较高,除此之外,还检测到m/z79.021 1、88.076 5、99.080 2、107.085 9、127.075 6、158.154 5离子。结果表明,在这2支一次性注射器中检测到的离子种类及强度较为接近。
随后,对3种品牌注射器分别进行检测分析,各自的特征质谱图示于图4。可以看出,在不同品牌的一次性注射器中检测到的物质种类和强度差别较大。如前所述,品牌①注射器中,m/z74.060 2、109.101 6、136.021 9离子的信号强度相对较高;品牌②注射器的m/z74.060 2、88.076 5、136.021 9离子的相对强度较高;而在品牌③注射器中,m/z136.021 9离子的相对强度较高。可见,不同品牌注射器中检测到的离子种类及相对强度存在较大差异,这可能是由不同厂家的生产工艺不同、生产过程中添加的有机物种类不同导致的。
根据离子准确质荷比以及同位素丰度,利用串联质谱得到的CID碎片,并结合已有的文献研究结果,可实现检测物质的定性分析。如Chen等[9]利用EESI-Q TOF分析检测了人体皮肤等各种活体生物样品表面的化合物,并对其中的物质进行了定性分析。本研究在3个品牌的一次性注射器中检测到较多离子,选出信号强度大于5 000的10种离子,利用上述方法,并结合在线数据库(HMDB、Metlin、Massbank)做定性分析。以m/z136.021 9离子为例,根据同位素丰度和准确质荷比,可确定其为[C7H5NS+H]+离子,进一步对该离子做串联质谱分析,示于图5。可见,在20 eV碎裂能量下只得到1个碎片离子[C6H5S]+(m/z109.011 1),在30 eV碎裂能量下进一步得到碎片离子[C5H5]+(m/z65.039 1),由此认为该化合物是苯并噻唑。据报道,该物质可能来源于注射器橡胶活塞在生产过程中添加的硫化促进剂[10]。以同样的方法,对其他9种离子进行鉴别分析,对应的化合物信息列于表1。
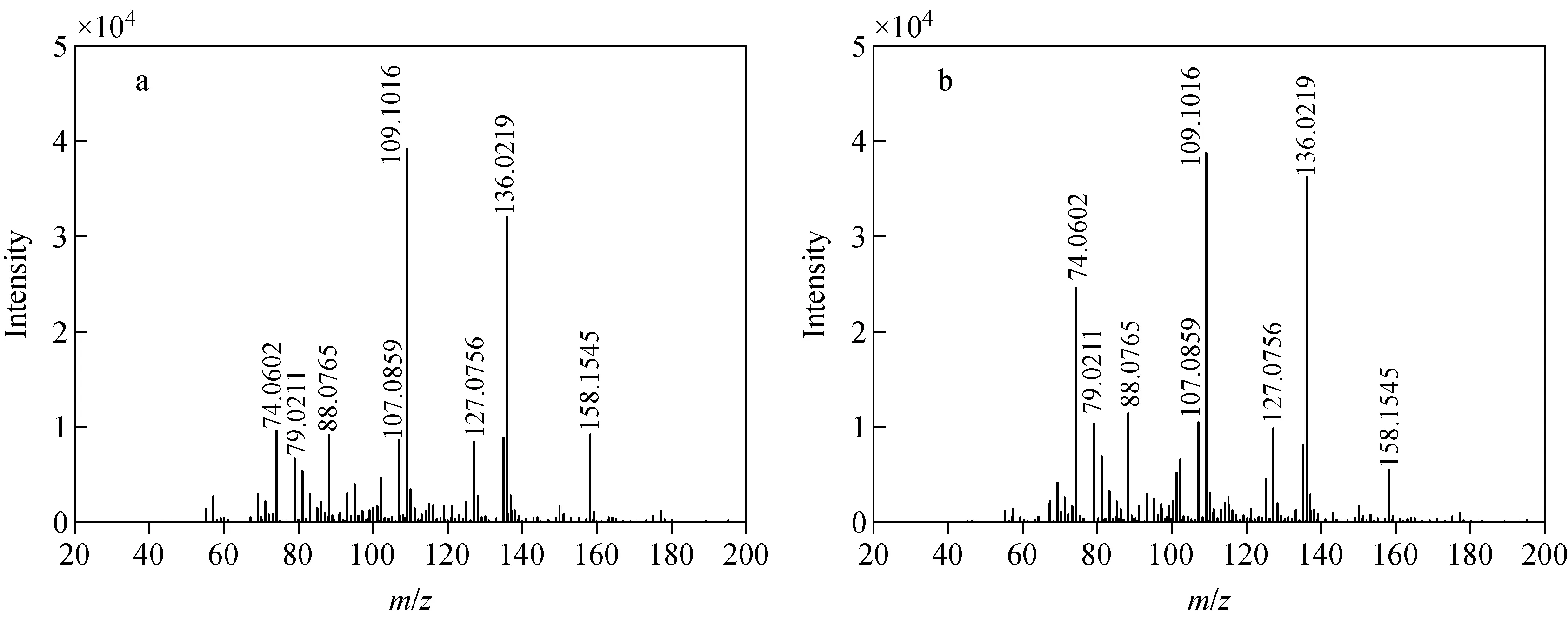
注:a.第1支注射器;b.第2支注射器图3 2支品牌①的10 mL注射器的质谱图Fig.3 Mass spectra of two 10 mL syringes with brand ①
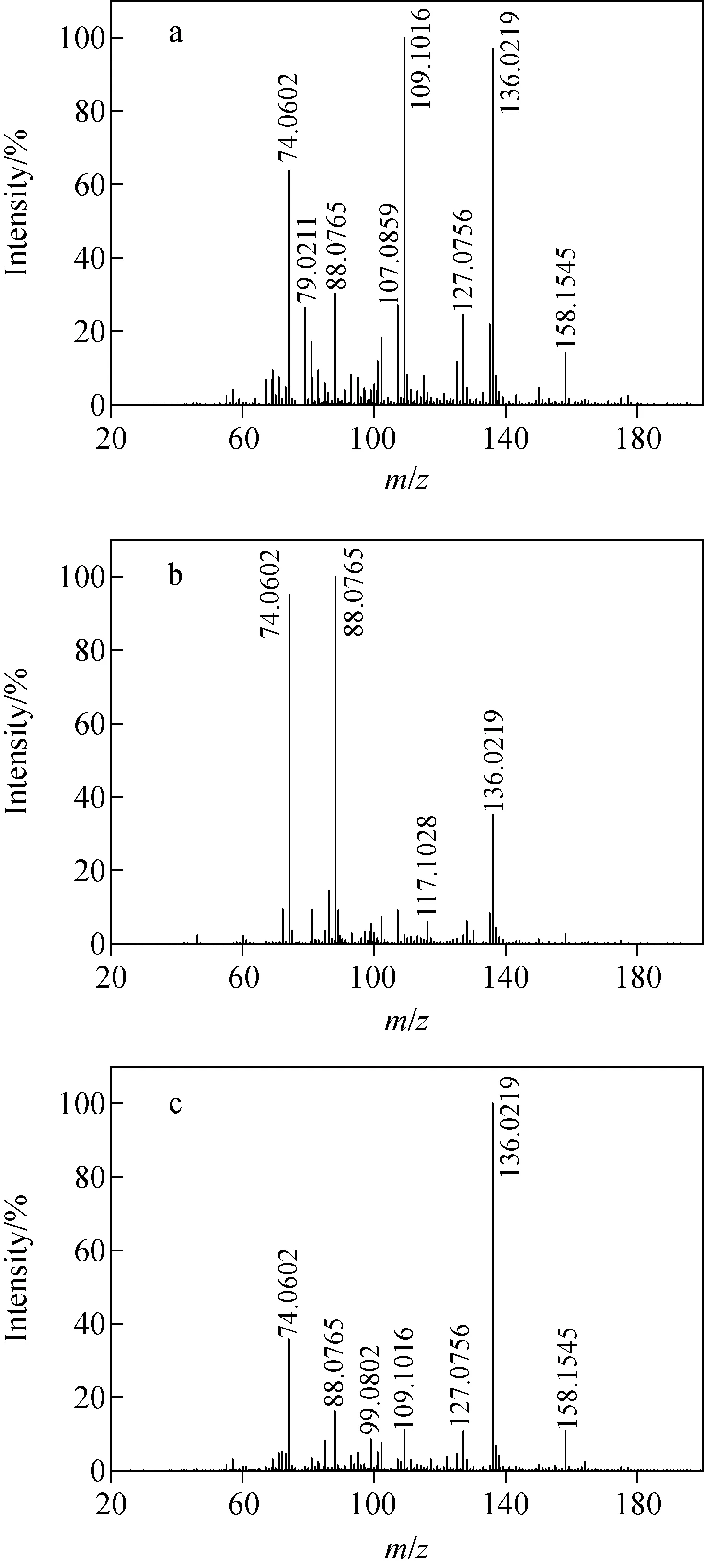
注:a.品牌①;b.品牌②;c.品牌③图4 3种不同品牌10 mL注射器的质谱图Fig.4 Mass spectra of 3 brands syringe with capacity of 10 mL
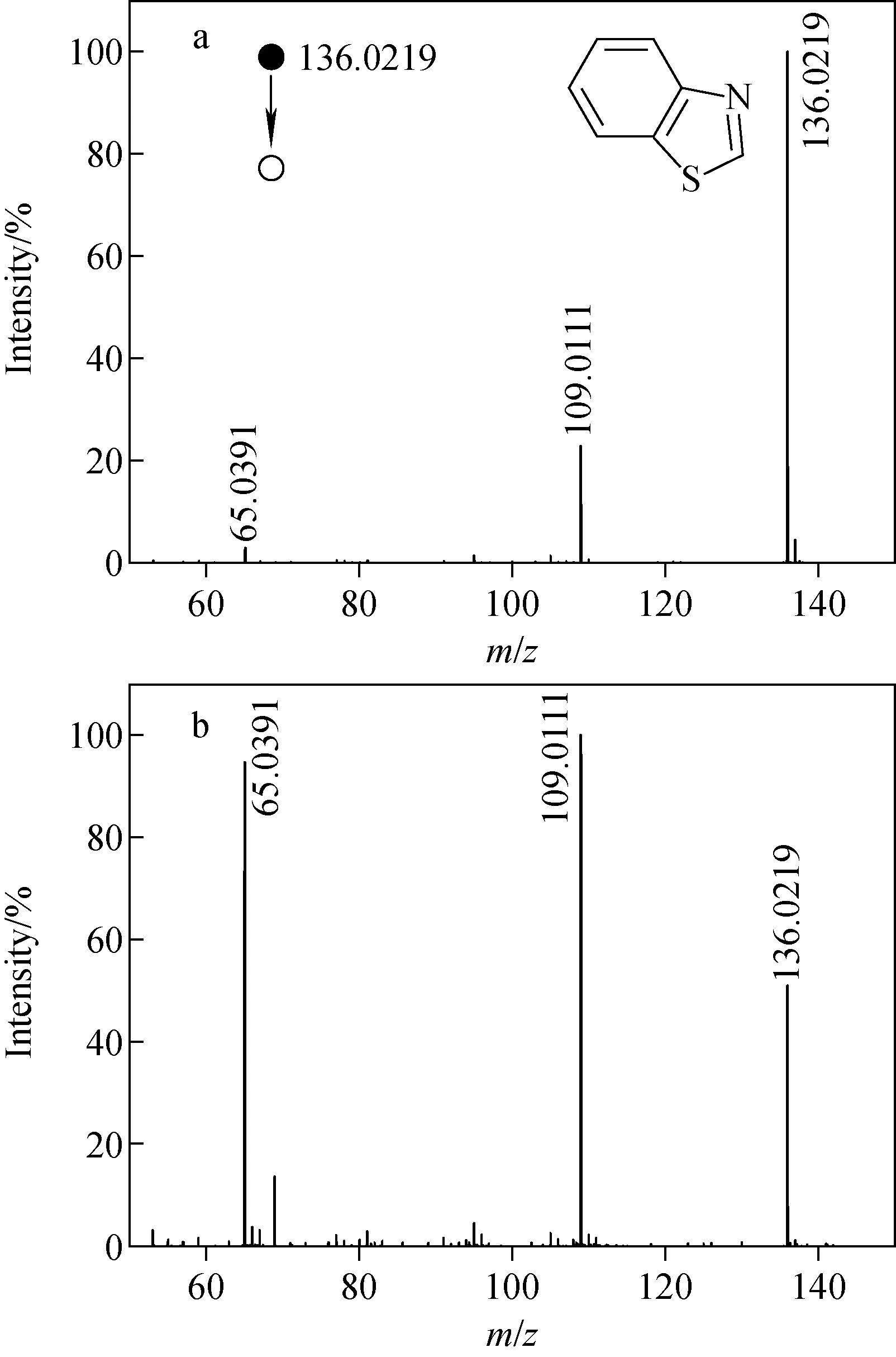
注:a.碎裂能量20 eV;b.碎裂能量30 eV图5 离子m/z 136.021 9的串联质谱图Fig.5 Tandem MS spectra of m/z 136.021 9
2.3 不同体积注射器的快速质谱分析
为了考察不同体积注射器的有机物残留情况,分别对品牌③的10、20、50 mL注射器进行快速检测,结果示于图6。随着注射器体积的增大,检测到的m/z136.021 9、99.080 2、88.076 5、74.060 2等主要离子的浓度均有所增高,这是由于一次性注射器体积越大,所用到的粘合剂以及活塞橡胶材料越多,释放出来的苯并噻唑、环己酮、吗啉等有机物残留越多。
2.4 环己酮半定量分析
为了考察注射器中有机物的残留量,以环己酮为例,配制了浓度分别为0.26、0.53、2.63、5.25 μg/L的环己酮标准样品气体,标准曲线示于图7。
离子强度和环己酮浓度的拟合方程为y=-3 124.52+30 598.51x,相关系数R2=0.993。根据文献[11],该方法的检出限LOD可由式(1)计算。

表1 一次性注射器中检测到的10种挥发性有机物Table 1 10 volatiles detected in disposable syringe

图6 4种碎片离子信号强度随注射器体积的变化Fig.6 Relationship of ion intensity with injector volume

图7 环己酮标准曲线Fig.7 Calibration curve of cyclohexanone
(1)
对浓度C为0.26 μg/L的环己酮样品气体进行检测,获得的平均离子强度S为5 455(n=10),标准偏差σ为890,由此计算得到的检出限约为0.13 μg/L。
不同品牌的10 mL注射器中环己酮离子强度范围在8 890~16 480,根据拟合方程,计算得到环己酮在10 mL注射器中的浓度范围为0.39~0.64 μg/L,在50 mL注射器中其残留量最高(对应离子强度为74 113),达到2.52 μg/L。尽管我国对一次性注射器中的环己酮残留限量并没有明确的标准,但研究表明,这些挥发性有机物对人体具有潜在的危害[12-19],因此对这类医疗器械中的有机物残留的监测应该引起足够的重视。
3 结论
本研究采用电喷雾萃取电离技术结合四极杆飞行时间质谱,对一次性医用注射器进行了快速检测分析。通过优化载气流量和毛细管电压等参数,获得最佳的实验条件。在对3个不同品牌的一次性医用注射器检测研究中发现:同一品牌注射器中残留的有机物种类及含量较为接近;而不同品牌注射器中残留的有机物种类及含量差异明显。选取信号强度大于5 000的10个离子,根据离子准确质荷比以及同位素丰度,利用串联质谱得到其CID碎片,结合在线数据库的CID碎裂谱和已有的文献报道,对这些物质进行了定性分析。最后,对注射器中的环己酮进行了半定量分析,得到该方法下环己酮的检出限约为0.13 μg/L,不同品牌的10 mL注射器中环己酮的含量为0.39~0.64 μg/L,50 mL注射器中环己酮的残留浓度约为2.52 μg/L。本研究可为一次性注射器中挥发性有机物残留的快速检测提供技术参考。
[1] CAITLIN S, THOMPSON-TORGERSON, HUN-TER C, et al. Cyclohexanone contamination from extracorporeal circuits impairs cardiovascular function[J]. Ajp Heart & Circulatory Physiology, 2009, 296(6): H1 926-H1 932.
[2] SNELL R P. Gas chromatographic determination of cyclohexanone leached from hemodialysis tubing[J]. Journal of Aoac International, 1993, 76(5): 1 127-1 132.
[3] COLARETA U U, PRAZAD P, PUPPALA B L, et al. Emission of volatile organic compounds from medical equipment inside neonatal incubators[J]. Journal of Perinatology Official Journal of the California Perinatal Association, 2014, 34(8): 624-628.
[4] GAIND V S, JEDRZEJCZAK K. HPLC determination of rubber septum contaminants in the iodinated intravenous contrast agent (sodium iothalamate)[J]. Journal of Analytical Toxicology, 1993, 17(1): 34-37.
[5] WANG Y, HAN H, SHEN C, et al. Control of solvent use in medical devices by proton transfer reaction mass spectrometry and ion molecule reaction mass spectrometry[J]. Journal of Pharmaceutical & Biomedical Analysis, 2009, 50(2): 252-256.
[6] CHEN H, WORTMANN A, ZHANG W, et al. Rapid in vivo fingerprinting of nonvolatile compounds in breath by extractive electrospray ionization quadrupole time-of-flight mass spectrometry[J]. Angewandte Chemie, 2007, 46(4): 580-583.
[7] LI X, HU B, DING J, et al. Rapid characterization of complex viscous samples at molecular levels by neutral desorption extractive electrospray ionization mass spectrometry[J]. Nature Protocols, 2011, 6(7): 1 010-1 025.
[8] ZOU X, WANG H, LU Y, et al. Rapid analysis of residual cyclohexanone in PVC infusion set by extractive electrospray ionization-mass spectrometer/mass spectrometer[J]. Acta Chimica Sinica, 2015, 73(8): 851-855.
[9] Dr H C, PROF S Y, Dr A W, et al. Neutral desorption sampling of living objects for rapid analysis by extractive electrospray ionization mass spectrometry[J]. Angewandte Chemie International Edition, 2007, 46(40): 7 591-7 594.
[10] GHOSH P, KATARE S, PATKAR P, et al. Sulfur vulcanization of natural rubber for benzothiazole accelerated formulations: from reaction mechanisms to a rational kinetic model[J]. Rubber Chemistry & Technology, 2003, 76(3): 411-412.
[11] DING J, GU H, YANG S, et al. Selective detection of diethylene glycol in toothpaste products using neutral desorption reactive extractive electrospray ionization tandem mass spectrometry[J]. Analytical Chemistry, 2009, 81(20): 8 632-8 638.
[12] GESCHER A. Metabolism ofN,N-dimethylformamide: Key to the understanding of its toxicity[J]. Chemical Research in Toxicology, 1993, 6(3): 245-251.
[13] RUBIN L F. Toxicity of dimethyl sulfoxide, alone and in combination[J]. Annals of the New York Academy of Sciences, 1975, 243(1): 98-103.
[14] LAM H F, VANSTEE E W. A re-evaluation of the toxicity of morpholine[J]. Federation Proceedings, 1978, 37(3): 679-679.
[15] LIJINSKY W, KOVATCH R M. Chronic toxicity study of cyclohexanone in rats and mice[J]. Journal of the National Cancer Institute, 1986, 77(4): 941-949.
[16] CRAGG S T, CLARKE E A, DALY I W, et al. Subchronic inhalation toxicity of ethylbenzene in mice, rats, and rabbits[J]. Fundamental & Applied Toxicology Official Journal of the Society of Toxicology, 1989, 13(3): 399-408.
[17] HOYER P B, DEVINE P J, HU X, et al. Ovarian toxicity of 4-vinylcyclohexene diepoxide: a mechanistic model[J]. Toxicologic Pathology, 2001, 29(1): 91-99.
[18] WEVER H D, VERACHTERT H. Biodegradation and toxicity of benzothiazoles[J]. Water Research, 1997, 31(11): 2 673-2 684.
[19] KHALFI F, DINE T, LUYCKX M, et al. Determination of cyclohexamone after derivatization with 2,4-dinitrophenyl hydrazine in intravenous solutions stored in PVC bags by high performance liquid chromatography[J]. Biomedical Chromatography Bmc, 1998, 12(2): 69.
