黄芪甲苷、人参皂苷Rg1对慢性萎缩性胃炎大鼠Hedgehog信号通路的调控影响
2018-01-12赵唯含史瑞杨美娟高康丽李宁飞李军祥
赵唯含 史瑞 杨美娟 高康丽 李宁飞 李军祥
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是临床常见的消化系统疾病,以胃黏膜上皮和腺体萎缩或伴有肠化生及不典型增生为特征表现[1]。现代医学对于本病的治疗主要是缓解症状,如应用促胃动力药、胃黏膜保护剂及抑酸剂等,而中医药凭借其优势在治疗CAG中扮演着重要角色[2]。黄芪和三七是健脾益气和活血化瘀药的代表,黄芪中的主要有效成分是黄芪甲苷,三七中的主要有效成分是人参皂苷Rg1。以往研究发现黄芪及三七可以通过激活Hedgehog信号通路关键因子改善萎缩性胃炎大鼠胃黏膜的萎缩状态。本次实验将进一步对黄芪和三七的有效成分黄芪甲苷及人参皂苷Rg1治疗CAG的作用机制进行探讨。
1 材料与方法
1.1 实验动物
健康雄性Wistar大鼠80只,体重(160±20) g,SPF级,由北京华阜康生物科技股份有限公司提供,动物许可证编号:SCXK(京)20090007,饲养于北京市中医研究所SPF级动物饲养间,12小时光照/黑夜循环,相对恒温(25℃),恒湿(75%)。
1.2 试剂与药物
黄芪甲苷(Astragaloside IV,AST)分子式:C41H68O14,分子量784,标准品,购自北京市药品检验所,编号:110781;人参皂苷Rg1(Ginsenoside Rg1,GSS):标准品,购自北京万诚科贸有限公司,纯度≥98%(HPLC); Purmorphamine购自上海浩然生物有限公司; 特异性抗体Shh购自美国CST公司,Gli-1、Ptch、SUFU、CyclinD1和β-actin购自美国abcam公司;辣根过氧化物酶(horse radish peroxidase,HRP)标记羊抗鼠或兔抗羊二抗购自北京中杉金桥生物技术有限公司;组织裂解液和BCA蛋白浓度测定试剂盒购自美国Promega公司;ReverTra Ace qPCR RT Kit和THUNDERBIRD SYBR qPCR Mix购自日本Toyobo公司;PV-9001、PV-9003免疫组化检测试剂购于北京中杉金桥生物技术有限公司。
1.3 实验动物分组及给药
采用幽门弹簧植入术配合高盐热淀粉糊灌胃法制备萎缩性胃炎大鼠模型[3]。造模结束后,运用随机数字表法将造模动物分为模型组、人参皂苷Rg1低剂量组、人参皂苷Rg1高剂量组、黄芪甲苷低剂量组、黄芪甲苷高剂量组、Purmorphamine组及叶酸组,每组10只,另设10只空白组。空白组和模型组予去离子水灌胃2 mL/天;黄芪甲苷低剂量予水溶液1.5 mg/(kg·d)灌胃;高剂量予3 mg/(kg·d),人参皂苷Rg1低剂量予0.5 mg/(kg·d)灌胃, 高剂量予1 mg/(kg·d);Purmorphamine组予Purmorphamine水溶液1.6 mg/(kg·d)灌胃,共治疗8周。
1.4 标本的采集
实验大鼠禁食水16小时,10%水合氯醛4 mL/100 g体重腹腔注射麻醉,腹主动脉取血后,沿胃大弯剪开,除去胃内容物,生理盐水冲洗干净,展开照相,大体观察;取幽门与前胃与腺胃交界线连线的2/5部分,放入冻存管内,液氮条件下保存,用于Western blot及PCR实验;胃窦部横向条状取材,用10%中性福尔马林液固定,石蜡包埋,切片用于HE染色及免疫荧光。
1.5 Western Blot检测胃组织Shh、Ptch、Gli-1的蛋白表达
组织块称重,加入液氮,研磨并粉碎组织,加细胞裂解液50 μL,在冰上进行匀浆离心处理,取蛋白上清液,测定总蛋白浓度。调整浓度以后进行电泳分离,把蛋白转至硝酸纤维素膜,用5%的脱脂牛奶封闭2小时。将封闭膜放入一抗中,4℃过夜,洗净未结合的一抗,然后放入二抗工作液中,室温孵育2小时。灰度值分析采用ImageJ软件。
1.6 RT-PCR检测胃组织Shh mRNA、Ptch mRNA、Gli-1 mRNA表达
把组织放入研钵中,研磨成粉末状,Trizol试剂法提取样本的总RNA,经ReverTra Ace qPCR RT Kit逆转录为cDNA。再将此设为模板,利用特异性引物合成PCR产物。大鼠的引物序列及产物大小见表1。以β-actin基因作为内参,将标本的待测指标和内参进行标准化,相对定量数据处理使用2-△△Ct法。

表1 引物序列及产物大小
1.7 量子点介导的免疫荧光法检测胃黏膜组织SUFU、CyclinD1蛋白的表达
石蜡切片脱蜡、水化、微波抗原修复、TBS洗涤,封闭缓冲液37℃湿盒孵育60分钟,分别滴加SUFU、CyclinD1抗体,37℃孵育2小时,TBS-T漂洗5 分钟/次×3次,封闭缓冲液37℃湿盒孵育20分钟,滴加QDs-SA标记的二抗,37℃湿盒孵育30分钟,TBS-T漂洗5分钟/次×3次,滴加缓冲甘油封片剂封片。荧光显微镜下观察,每个组织随机采集5张图片拍照。用image pro plus 6.0 软件分析图像。
1.8 统计学处理

2 结果
2.1 各组大鼠胃黏膜组织肉眼及病理观察
2.1.1 肉眼观察 空白组大鼠黏膜红润;模型组大鼠前胃无明显变化,腺胃黏膜表面黄染,暴露黏膜颜色发白。
2.1.2 病理学评价 空白组大鼠黏膜结构正常,腺体整齐紧密;模型组胃黏膜变薄,出现萎缩,固有层腺体减少,排列稀疏,有炎性细胞浸润,个别可见淋巴滤泡形成;各给药组较模型组比较黏膜萎缩情况有不同程度的改善,腺体排列较整齐,其中以黄芪甲苷高剂量组和人参皂苷Rg1高剂量组为最佳。见图1。
2.2 各组大鼠胃组织Shh、Ptch、Gli-1蛋白表达的比较
与空白组比较,模型组大鼠胃组织Shh、Ptch、Gli-1蛋白含量均显著降低(P<0.05);与模型组比较,人参皂苷Rg1低剂量组、人参皂苷Rg1高剂量组及叶酸组Shh蛋白表达明显升高(P<0.05),各给药组均能显著升高Ptch蛋白含量(P<0.05)。人参皂苷Rg1高剂量组、Purmorphamine组Gli-1蛋白表达明显升高(P<0.05),见表2、图2。

注:A:空白组;B:模型组;C:黄芪甲苷低剂量组;D:黄芪甲苷高剂量组;E:人参皂苷Rg1低剂量组;F:人参皂苷Rg1高剂量组;G:Purmorphamine组;H:叶酸组
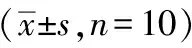
表2 各组大鼠胃组织Shh、Ptch、Gli-1蛋白表达
注: 与空白组比较,aP<0.05,bP<0.01;与模型组比较,cP<0.05,dP<0.01。

表3 各组大鼠胃组织Shh、Ptch、Gli-1 mRNA表达
注: 与空白组比较,aP<0.05,bP<0.01;与模型组比较,cP<0.05,dP<0.01。
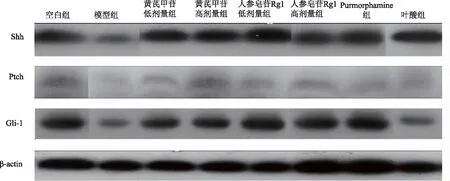
图2 胃组织Shh、Ptch及Gli-1的Western Blot表达
2.3 各组大鼠胃组织Shh、Ptch、Gli-1基因表达的比较
与前述Western Blot检测结果基本一致, 与空白组比较, 模型组大鼠胃组织Shh、 Ptch、 Gli-1的mRNA含量均显著降低(P<0.05); 与模型组比较, 人参皂苷Rg1高剂量组对Shh、 Ptch有改善作用(P<0.05), 黄芪甲苷低剂量和高剂量组均可显著改善Gli-1的基因表达(P<0.05), Purmorphamine组对于Shh、 Ptch、 Gli-1均疗效显著(P<0.05)。 见表3。
2.4 各组大鼠SUFU蛋白表达情况
与空白组相比较,模型组SUFU蛋白表达明显增强(P<0.01);与模型组比较,黄芪甲苷高剂量组、人参皂苷Rg1高剂量组和Purmorphamine组SUFU蛋白表达明显减弱(P<0.05)。见图3、表4。
2.5 各组大鼠CyclinD1蛋白表达情况
与空白组相比较,模型组CyclinD1蛋白表达明显减弱(P<0.01);与模型组比较,黄芪甲苷高剂量组和Purmorphamine组均表达增强(P<0.05)。见图4、表5。

注:A:空白组;B:模型组;C:黄芪甲苷低剂量组;D:黄芪甲苷高剂量组;E:人参皂苷Rg1低剂量组;F:人参皂苷Rg1高剂量组;G:Purmorphamine组;H:叶酸组
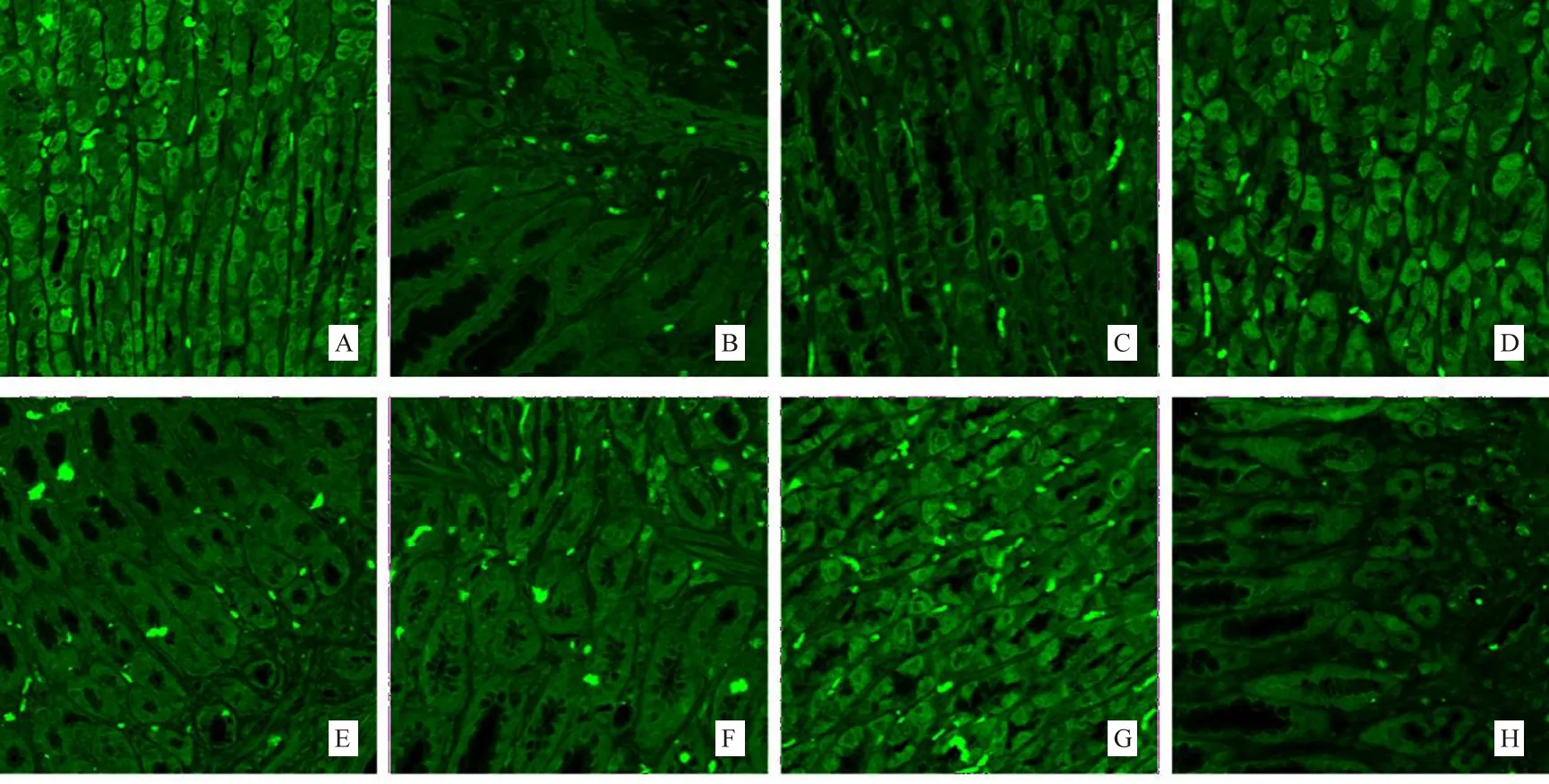
注:A:空白组;B:模型组;C:黄芪甲苷低剂量组;D:黄芪甲苷高剂量组;E:人参皂苷Rg1低剂量组;F:人参皂苷Rg1高剂量组;G:Purmorphamine组;H:叶酸组

表4 量子点标记各组大鼠SUFU的表达情况
注: 与空白组比较,aP<0.01;与模型组比较,bP<0.05,cP<0.01。

表5 量子点标记各组大鼠CyclinD1的表达情况
注:与空白组比较,aP<0.01;与模型组比较,bP<0.05,cP<0.01。
3 讨论
Hedgehog信号通路几乎涉及哺乳动物发育的所有过程,目前关于其与肿瘤的调控研究较为透彻[4]。Hedgehog信号通路主要由三部分组成:Hh信号肽(Shh、Ihh、Dhh)、跨膜受体(Ptch、Smo)和下游转录因子(Gli)。Shh参与多种诱导过程,在胚胎胚芽不对称性发育和中枢神经系统发育过程发挥成形素、分裂素以及分化因子等作用[5]。Shh蛋白释放后与Ptch结合,解除了Ptch对Smo的抑制作用,进而将信号向细胞质内传递,激活下游的Gli转录因子[6]。Gli-1是一种转录激活剂,Hh信号通路的激活可以上调Gli-1的表达,有研究发现,当Shh表达不足时,Gli-1也会降低,而Shh被激活时,Gli-1将会表达上调,因此Gli-1也常被作为检测Hedgehog信号通路是否激活的代表性分子[7]。Sufu是Hedgehog通路中处在Smo和Gli之间的Fused抑制物,Gli基因的活化需要Sufu处于抑制状态,而Smo的活化可以抑制Sufu的功能。CyclinD1是细胞周期的正调节因子,在G1期含量最高且活性最大,通路异常活化后可以上调CyclinD1蛋白表达[8]。Purmorphamine是一种小分子嘌呤衍生物,可以作为Hedgehog信号通路的特异性激活剂[9]。
黄芪甲苷(又称黄芪皂苷Ⅳ,Astragaloside Ⅳ)为中药黄芪主要有效成分之一,现代药理研究其有镇静、降压、消炎、影响蛋白合成、促进NK细胞活性等作用,是黄芪的重要生理活性成分[10]。三七中皂苷成分是三七的主要有效成分之一,目前已从三七的不同部位分离得到60余种单体皂苷成分,其中人参皂苷Rg1是三七总皂苷中最具代表性的特征化合物,现代药理学研究表明,人参皂苷Rg1在体内可被代谢为Rh1,起到促进免疫应答的作用,表现为一定的抗肿瘤活性[11]。
本实验采用幽门弹簧植入术配合高盐热淀粉糊灌胃法构建CAG大鼠模型,该模型以胃窦萎缩为主,炎症浸润明显,符合一般萎缩性胃炎特征。在前期实验中,黄芪、三七作为益气活血法的代表药物,可以显著升高Hedgehog信号通路中正反馈因子,降低负反馈因子表达,进一步维护细胞凋亡与增殖的动态平衡,保护胃黏膜[12]。黄芪甲苷是中药黄芪的主要单体成分,人参皂苷Rg1是中药三七的主要单体成分,且含量最高,因此本次实验选择了黄芪甲苷和人参皂苷Rg1探索中药黄芪、三七的有效成分对大鼠CAG的作用机制。由实验结果可知,黄芪甲苷和人参皂苷Rg1的高低剂量组对慢性萎缩性胃炎大鼠的病理情况均有不同程度的改善,抑制萎缩及炎症发生。对CAG大鼠Hedgehog通路相关因子进行检测,人参皂苷Rg1低剂量组和高剂量组可升高Shh、Ptch的表达,其中以高剂量组改变明显;黄芪甲苷高剂量组显著改善Gli-1的表达,及升高CyclinD1的蛋白表达。
综上,在慢性萎缩性胃炎发生发展过程中,中药黄芪及三七的主要单体成分黄芪甲苷、人参皂苷Rg1对Hedgehog信号通路关键因子均有一定的激活作用,由结果发现,人参皂苷Rg1主要作用于Hedgehog通路的上游因子,而黄芪甲苷主要作用的靶点因子处于Hedgehog通路的下游,其具体机制还有待进一步研究。
[1] 陈灏珠.实用内科学[M].北京:人民卫生出版社,2005:1880.
[2] 杨印智,王继栓,王晓琴,等. 慢性萎缩性胃炎的诊断与中医药治疗[J].现代中西医结合杂志,2014,23(24):2686-2687.
[3] 史瑞,李晓红,方蕾,等.弹簧幽门植入术结合高盐热淀粉糊灌胃诱导大鼠萎缩性胃炎模型的方法及评价[J].世界华人消化杂志,2011,19(10):1001-1008.
[4] Ingham PW,McMahon AP.Hedgehog signaling in animal development: paradigms and principles[J]. Genes Dev, 2001, 15(23): 3059-3087.
[5] Bijlsma MF, Spek CA, Zivkovic D, et al. Repression of smoothened by patched-dependent (pro-)vitamin D3 secretion[J]. PLoS Biol, 2006, 4(8): e232.
[6] Stamataki D, Ulloa F, Tsoni SV, et al. A gradient of Gli activity mediates graded Sonic Hedgehog signaling in the neuraltube[J]. Genes Dev 2005, 19(5): 626-641.
[7] Hui CC, Angers S. Gli proteins in development and disease[J]. Annu Rev Cell Dev Biol, 2011,27(1): 513-537.
[8] Yue S, Chen Y, Cheng SY. Hedgehog signaling promotes the degradation of tumor suppressor Sufu through the ubiquitin-proteasome pathway[J].Oncogene,2009,28(4): 492-499.
[9] Faghihi F, Baghaban E M, Nekookar A, et al. The effect of purmorphamine and sirolimus on osteogenic differentiation of human bone marrow-derived mesenchymal stem cells[J]. Biomed Pharmacother, 2013, 67(1):31-38.
[10] 段立军,孙博航. 黄芪甲苷的研究进展[J]. 沈阳药科大学学报,2011,28(5):410-416.
[11] 王莹,禇扬,李伟,等. 三七中皂苷成分及其药理作用的研究进展[J].中草药,2015,46(9):1381-1392.
[12] 赵唯含,高康丽,李宁飞,等. 黄芪、三七及其配伍对慢性萎缩性胃炎大鼠胃组织Hedgehog信号通路的调节作用[J].中华中医药杂志,2016,31(5):1951-1955.
