衍生化GC-MS法测定甲磺酸萘莫司他原料药中甲磺酸甲酯与甲磺酸乙酯
2018-01-12刘晓强
刘晓强,丁 建
(常州市食品药品监督检验中心,常州 213101)
甲磺酸萘莫司他(nafamostat mesilate)化学名为6-脒基-2-萘基-4-胍基苯甲酸酯二甲磺酸盐,是Japan Tobacco公司研发的非肽类蛋白酶抑制剂[1],首次上市是在1986年的日本,主治临床急性胰腺炎[2-3]。在甲磺酸萘莫司他的制备工艺中,由于所用原料、试剂等多种因素影响,在制得的甲磺酸萘莫司他原料药中可能会有甲磺酸甲酯(MMS)和甲磺酸乙酯(EMS)等杂质生成[4-5]。而甲磺酸甲酯、甲磺酸乙酯等甲磺酸酯类化合物均具有较强的潜在性遗传毒性杂质,严重威胁患者的健康,故需要对其含量进行控制[5]。
1 仪器与试药
1.1仪器 GCMS-QP-2010气相色谱-质谱联用仪(日本岛津公司);XS105DU电子天平(梅特勒-托利多仪器有限公司)。
1.2试药 甲磺酸萘莫司他(江苏杜瑞制药有限公司,批号840901);甲磺酸甲酯对照品(百灵威科技有限公司,批号LSB0N36,质量分数99%);甲磺酸乙酯对照品(阿法埃莎化学有限公司,批号10169291,质量分数99%);乙腈为色谱纯(德国默克公司);实验用水为纯净水;碘化钠和无水硫代硫酸钠均为分析纯。
2 方法与结果
2.1色谱条件 色谱柱:HP-INNOWAX(安捷伦科技有限公司,30 m×0.250 mm,0.50 μm);进样口温度:200 ℃;柱温:采用程序升温法,起始温度设为35 ℃,维持3 min,再以30 ℃·min-1的速率升温至180 ℃,维持2 min;载气类型:氦气;载气流速:恒压模式(100 kPa);进样量:1.0 mL;分流比:1∶12;平衡时间:30 min;进样方式:顶空进样;平衡温度:60 ℃。
质谱:离子源温度:250 ℃;接口温度:150 ℃;电离源:电子轰击离子化(EI);分析器:四级杆质量分析器;离子源温度:250 ℃。选择性离子模式(SIM)检测,碘代丁烷(BuI)定量离子m/z为184,碘代甲烷(MeI)为142,碘代乙烷(EtI)为156,BuI、MeI和EtI依次由甲磺酸丁酯(BMS)、甲磺酸甲酯(MMS)及甲磺酸乙酯(EMS)经衍生化反应形成。
2.2溶液的制备
2.2.1衍生化溶液 称取碘化钠60.0 g和无水硫代硫酸钠30 mg,置于同一50 mL量瓶中,加水溶解并稀释至刻度,摇匀,即得(避光保存)。
2.2.2内标溶液 精密量取甲磺酸丁酯50 μL,置于50 mL量瓶中,用乙腈-水(8∶2)稀释至刻度,摇匀;精密量取上述溶液500 μL,置于250 mL量瓶中,用乙腈-水(2∶8)稀释至刻度,摇匀;再精密量取上述溶液100 mL,置于1 000 mL量瓶中,同样用乙腈-水(2∶8)稀释至刻度,摇匀,即得。
2.2.3对照品储备液 精密称取甲磺酸甲酯及甲磺酸乙酯各25 mg,共同置于5 mL量瓶中,用甲苯溶解并稀释至刻度,摇匀;精密量取上述溶液50 μL,移至25 mL量瓶中,加乙腈2 mL,用内标溶液稀释至刻度,制成每1 mL中含甲磺酸甲酯和甲磺酸乙酯各10 μg 的溶液,即得。
2.2.4对照品溶液(1) 精密量取2.2.3项下制备的对照品储备液50 μL,置于50 mL量瓶中,用内标溶液稀释至刻度;依次精密量取2.2.1项下制备的衍生化溶液与上述溶液各0.5 mL,共同置于20 mL顶空瓶中,压盖密封,摇匀,即得。
2.2.5对照品溶液(2) 精密量取2.2.3项下制备的对照品储备液150 μL,置于20 mL量瓶中,用内标溶液稀释至刻度;依次精密量取2.2.1项下制备的衍生化溶液与上述溶液各0.5 mL,共同置于20 mL顶空瓶中,压盖密封,摇匀,即得。
2.2.6供试品溶液 精密称取本品25 mg,置于20 mL顶空瓶中,依次精密加入2.2.1项下制备的衍生化溶液与2.2.2项下制备的内标溶液各0.5 mL,压盖密封,摇匀,即得。
2.3方法学验证
2.3.1标准曲线 分别取2.2.3项下制备的对照品储备液30,50,50,150和1 000 μL,分别置于100,50,20,20和50 mL量瓶中,用内标溶液稀释至刻度,使其质量浓度分别为3,10,25,75 和200 ng·mL-1。再依次量取上述各溶液0.5 mL,与2.2.1项下制备的衍生化溶液0.5 mL,共同置于20 mL顶空瓶中,压盖密封。
结果表明,甲磺酸甲酯拟合曲线为y=0.015 5x+0.152 1,r=0.997 5;甲磺酸乙酯拟合曲线为y=0.016x+0.007 1,r=0.999 9。甲磺酸甲酯和甲磺酸乙酯质量浓度在3.0~200.0 ng·mL-1的范围内线性关系良好。
2.3.2检出限和定量限 甲磺酸甲酯的定量限为2.892 8 ng·mL-1,信噪比为19.5∶1,检测限为0.964 3 ng·mL-1,信噪比为16.5∶1;甲磺酸乙酯的定量限为3.022 3 ng·mL-1,信噪比为13.8∶1,检测限为1.007 8 ng·mL-1,信噪比为9.7∶1。
2.3.3精密度 取2.2.3项下制备的对照品储备液150 μL,置于20 mL量瓶中,用内标溶液稀释至刻度,摇匀;依次取上述溶液及2.2.1项下制备的衍生化溶液各0.5 mL,共同置于20 mL顶空瓶中,立即密封。
甲磺酸甲酯的峰面积之比的RSD值为0.9%,甲磺酸乙酯的峰面积之比的RSD值为1.3%。
2.3.4加样回收率 分别取2.2.3项下制备的对照品储备液120,150和180 μL,分别置于20,20和20 mL量瓶中,用内标溶液稀释至刻度,摇匀;依次取上述各溶液0.5 mL、2.2.1项下制备的衍生化溶液0.5 mL及样品25 mg,共同置于20 mL顶空瓶中,压盖密封,制成含甲磺酸甲酯和甲磺酸乙酯分别为低、中、高质量浓度的溶液各3份。
甲磺酸甲酯的平均回收率为102%,RSD值为2.9%;甲磺酸乙酯的平均回收率为106%,RSD值为1.2%,见表1~2。
表1甲磺酸甲酯加样回收率实验结果

Tab.1 The results of recovery tests of mthylmesylate (n=9)
表2甲磺酸乙酯加样回收率实验结果

Tab.2 The results of recovery tests of ethylmesylate (n=9)
2.4样品测定 样品中甲磺酸甲酯的含量为0.000 01%,甲磺酸乙酯的含量为0,甲磺酸酯的总含量为0.000 01%,见图1。结果表明,甲磺酸酯的总含量符合规定(标准规定:甲磺酸酯总含量不得超过0.000 5%)。
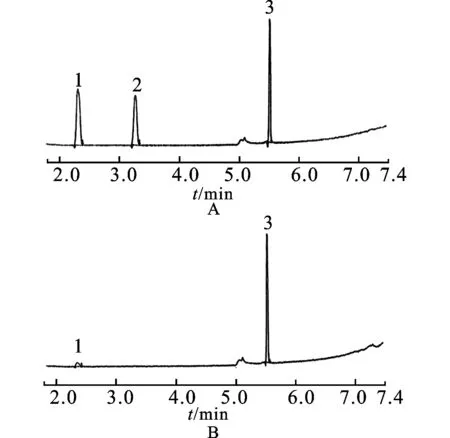
图1GC-MS图
A.对照品;B.样品;1.碘化甲烷;2.碘化乙烷3.碘化丁烷。
Fig.1 GC-MS chromatograms
A.reference substance;B.sample;1.methyl iodide;2.ethyl iodide;3.butane iodide.
3 小结
近年来,对各种原料药中甲磺酸酯类杂质检测研究的较多,常用的方法包括气相色谱法(GC-FID、GC-ECD)、气相色谱-质谱联用法(GC-MS)、液相色谱-串联质谱联用法(LC-MS/MS)以及离子色谱等[6-12],笔者参考《欧洲药典》(EP)8.0版附录提出使用衍生化顶空GC-MS法测定甲磺酸酯类杂质含量的方法,本实验采用衍生化顶空GC-MS法,同时为了减少进样误差等因素对检测结果的影响,采用内标法进行样品的测定,选择待测物同系物甲磺酸丁酯为内标。
甲磺酸甲酯、甲磺酸乙酯和甲磺酸丁酯沸点较高,均大于200 ℃[13],无法对其进行气化测定,因此实验采用柱前衍生化法,使甲磺酸甲酯、甲磺酸乙酯、甲磺酸丁酯与碘离子作用分别转化为碘代甲烷、碘代乙烷和碘代丁烷,沸点明显降低,适用于气相色谱法进行测定。同时,通过柱前衍生化法将原先的盐转化为中性物质,增强其在色谱柱上的保留行为,改善峰形,提高了柱效和检测灵敏度[14-17],有益于更好地控制甲磺酸萘莫司他中上述2种成分的含量。
直接进样法或顶空进样法均可测定甲磺酸酯类化合物的含量,但由于直接进样法操作简便,会将大量其余物质带入系统,增加系统污染风险,而顶空进样法可有效控制污染,通过柱前衍生化法,将待测物及内标物质转化为沸点降低的小分子物质,便于顶空进样的实施。
本次实验通过上述方法测定,得到甲磺酸甲酯和甲磺酸乙酯的线性范围分别为3.0~200.0(r=0.997 5)和3.0~200.0 ng·mL-1(r=0.999 9);检测限分别为0.964 3 和1.007 8 ng·mL-1;定量限分别为2.892 8和3.022 3 ng·mL-1;进样精密度的RSD值分别为0.9%和1.3%;平均加样回收率分别为102%(RSD=2.9%)和106%(RSD=1.2%)。
综上所述,本实验建立了柱前衍生化和GC-MS联用的方法测定甲磺酸萘莫司他中甲磺酸甲酯和甲磺酸乙酯的含量,该方法简单、灵敏度高、重复性好,可用于甲磺酸萘莫司他中甲磺酸酯类化合物的含量测定。
[1] 陆美贞.抗胰腺炎药甲磺酸萘莫司他[J].国外药学——合成药、生化药、制剂分册,1988,9(4):234-235
[2] 李博,步芬,徐光富.甲磺酸萘莫司他中有机溶剂残留的测定[J].中国医药科学,2011,1(23):41-42.
[3] 陈宝泉,赵煜松,欧阳杰,等.甲磺酸萘莫司他的合成[J].中国医药工业杂志,2007,38(8):545-546.
[4] Elder D P,Teasdale A,Lipczynski A M.Control and analysis of alkyl esters of alkyl and aryl sulfonic acids in novel active pharmaceutical ingredients (APIs).[J].J Pharm Biomed Anal,2008,(46):1-8.
[5] Bolt H M,Foth H,Hengstler J G,et al.Carcinogenicity categorization of chemicals-new aspects to be considered in a European perspective[J].Toxicol Lett,2004,(151):29-41.
[6] 毛颐晴,李纬,朱丽君,等.GC-MS法测定甲磺酸萘莫司他原料药中的遗传毒性杂质[J].中国药房,2016,27(18):2555-2557.
[7] 连小刚,李孝壁,程红艳.衍生气相色谱法测定甲磺酸伊马替尼中甲磺酸烷基酯类[J].中国医药科学,2013,3(17):128-130.
[8] 丁逸梅,吴娟,陆春晓,等.盐酸决奈达隆中甲磺酸甲酯和甲磺酸乙酯的GC-MS法测定[J].中国医药工业杂志,2014,45(11):1069-1071.
[9] 冯慧敏,杭太俊,高新桃,等.LC-MS法同时检测甲磺酸伊马替尼中3个磺酸酯基因毒杂质[J].药物分析杂志,2014,34(12):2202-2206.
[10]刘立云,张倩如,孙连福,等.GC-MS法同时测定盐酸决奈达隆中的3种甲磺酸酯[J].中国药师,2014,17(8):1274-1276.
[11]孙营营,阮佳威,胡方剑,等.离子色谱法测定齐多夫定中甲磺酸甲酯的质量浓度[J].浙江大学学报:理学版,2015,42(1):116-119.
[12]张萌萌,潘红娟,陈佳,等.盐酸达泊西汀中甲磺酸甲酯、甲磺酸乙酯及甲磺酸异丙酯的顶空毛细管GC-ECD法测定[J].中国医药工业杂志,2015,46(1):55-58.
[13]刘立云,张倩茹,孙连福,等.GC-MS法同时测定盐酸决奈达隆中的3种甲磺酸酯[J].中国药师,2014,17(8):1274-1276.
[14]黄丽丹,邢亚东,王玲玲,等.2,4-二硝基氟苯柱前衍生化HPLC法测定保健食品中牛磺酸含量[J].药物分析杂志,2016,36(1):171-175.
[15]冯欢,李新霞,冯崴,等.柱前衍生化HPLC法测定不同产地胡芦巴中4-羟基异亮氨酸的含量[J].西北药学杂志,2016,31(2):136-138.
[16]栾维励,朱乐亭,杨莉,等.柱前衍生化HPLC法测定人血浆丙戊酸浓度的研究进展[J].中国药房,2016,27(11):1577-1579.
[17]马经明,赵吉平.柱前衍生化HPLC法测定维U颠茄铝胶囊中维生素U的含量[J].药物分析杂志,2016,36(7):1293-1298.
