干血滤纸片类固醇激素质控品制备及评价
2018-01-03韩连书邱文娟顾学范
占 霞 韩连书 叶 军 邱文娟 顾学范
上海交通大学医学院附属新华医院 上海市儿科医学研究所小儿内分泌/遗传科(上海 200092)
干血滤纸片类固醇激素质控品制备及评价
占 霞 韩连书 叶 军 邱文娟 顾学范
上海交通大学医学院附属新华医院 上海市儿科医学研究所小儿内分泌/遗传科(上海 200092)
目的 探讨用于类固醇激素液相色谱-串联质谱(LC-MS/MS)检测,室内质控干血滤纸片(DBS)类固醇激素质控品的制备方法。方法 收集全血,分离血细胞和血浆,生理盐水洗涤血细胞,活性炭过夜吸附血浆,添加标准品,制成低、中、高三个浓度的DBS类固醇激素质控品,LC-MS/MS检测并分析其精确度、准确度、稳定性及不同血斑间的差异。结果 DBS类固醇激素质控品批内精确度和准确度分别为2.4%~7.0%,102.0%~111.0%;批间精确度和准确度分别为5.1%~9.8%,99.0%~114.8%;-20℃保存5个月,月间差异无统计学意义(P>0.05);不同血斑间变异系数为3.3%~8.2%,变异系数较小。结论 配制的DBS类固醇激素质控品具有良好的精确度、准确度及稳定性,血斑间差异小,符合室内质控品要求,可用于LC-MS/MS检测类固醇激素的室内质控。
干血滤纸片; 类固醇激素; 质控品; 串联质谱
类固醇激素的检测在临床疾病的诊断和治疗中具有重要的作用。目前多采用荧光免疫分析法试剂盒进行类固醇激素检测,但一次试验只能测定一种激素,且存在交叉反应和基质干扰[1,2]。国外部分实验室以液相色谱-串联质谱(liquid chromatographytandem mass spectrometry,LC-MS/MS)法测定血清及干血滤纸片(dried blood spots,DBS)中类固醇激素谱,用于先天性肾上腺皮质增生症(congenital adrenal hyperplasia,CAH)的诊断、治疗效果评价及二次筛查[3-6]。目前国内外主要采用荧光免疫分析法测定新生儿DBS样本17-羟孕酮(17-hydroxyprogesterone,17-OHP)水平作为新生儿CAH一级筛查方法,但存在较高的假阳性率,患儿的阳性预测值低[7]。采用LC-MS/MS法作为新生儿CAH二级筛查方法,测定DBS中类固醇激素谱,并考察酶反应的底物与产物比值,可有效降低筛查假阳性[5-7]。上海市儿科医学研究所已经建立了LC-MS/MS测定DBS中类固醇激素的方法。室内质量控制在临床检验中至关重要,而良好的质控品是室内质量控制的关键。然而目前国内尚无厂商可提供LCMS/MS测定DBS中类固醇激素的试剂盒或质控品,国外也无固定的供应商。本研究采用自制的DBS类固醇激素质控品,用于实验室的室内质控,并对其性能进行评价。
1 材料和方法
1.1 材料
1.1.1 DBS类固醇激素标准品制备 收集健康成人全血50 mL,1 500×g离心5 min,分离血细胞及血浆。血细胞用生理盐水洗涤3次,储存于4℃待用;血浆加入100 mg/mL活性炭,搅拌吸附过夜,60 000×g高速离心1 h去除活性炭,取上清液,重复一次。LC-MS/MS测定活性炭处理前、吸附一次后及吸附两次后血浆中的内源性类固醇激素含量。将血细胞及处理后的血浆按55∶45比例混合,以混合后的全血作为基质配制标准溶液,浓度分别为0.125、0.250、0.500、1.000、2.000、10.000、50.000、200.000 ng/mL,将含标准品的全血滴至滤纸片上,滤纸片型号为S&S 903#,Whatman公司,制成一系列DBS标准品,晾干,-20℃保存待用。
1.1.2 DBS类固醇激素质控品制备 以混合后的全血作为基质添加标准溶液,使其终浓度分别0.8、25.0、150.0 ng/mL,分别制成低、中、高3个浓度水平的质控品,晾干,-20℃保存待用。
1.2 方法
1.2.1 质控样品检测方法 ①质控样品处理。直径3.2 mm打孔器取样2个DBS血斑,置于96孔过滤筛板中(滤膜0.45 μm,美国Millipore公司),每孔加入100 μL含0.5 ng/mL类固醇激素内标的甲醇/乙腈(容积1∶1,美国Fisher Scientific公司,质谱级)萃取溶剂;37℃密封孵育震荡50 min,970×g离心2 min,将萃取液离心至尖底96孔聚丙烯板(德国Greiner公司)中;50℃加热氮气吹干,50%甲醇70 μL复溶,铝箔覆盖,超高效液相色谱仪-串联质谱系统(UPLC-Xevo-TQ-S,美国Waters公司)上样检测。②采用Waters ACQUITY UPLC HSS T3色谱柱(2.1 mm×50 mm, 1.8 μm),流动相A为H2O含2 mmol/L醋酸铵和0.1%甲酸(美国Sigma-Aldrich公司);流动相B为MeOH含2 mmol/L醋酸铵和0.1%甲酸;采用梯度洗脱:0~1 min,55%A;1~3.5 min,55%~35%A;3.51min2%A;5.0min,55%A;流速为0.45 mL/min。柱温为40℃,进样体积为5μL。③在电喷雾电离阳离子检测模式下,采用多反应监测的质谱模式采集数据,雾化温度450℃,离子源温度150℃。类固醇激素的定量离子对分别为,雄烯二酮287.3/97.03(美国剑桥化学公司)、睾酮289.2/97.03(美国剑桥化学公司)、17-OHP 331.3/97.03(挪威Chiron公司)、孕酮315.3/97.03(美国剑桥化学公司)、11-脱氧皮质醇347.30/109.07(挪威Chiron公司)、21-脱氧皮质醇347.30/109.07(加拿大TRC公司)、皮质醇363.3/121.1(美国剑桥化学公司)。7种类固醇激素定量检测采用相应的内标及标准曲线法,其中孕酮以D8-17-OHP(美国Cambridge Isotope Labs公司)为内标,21-脱氧皮质醇以11-脱氧皮质醇-D2(美国Cambridge Isotope Labs公司)为内标进行定量。
1.2.2 精确度测定 用变异系数(coefficient variation,CV)表示精确度,CV(%)=100×标准偏差/均值;采用低、中、高,3组干血滤纸片质控品,对质控品重复6次分析,计算6次的类固醇激素测定值的变异系数作为批内变异;连续6天测定质控品,计算6天的类固醇激素测定值作为批间变异。
1.2.3 准确度测定 采用低、中、高3组干血滤纸片质控品,对质控品重复6次分析计算批内准确度,连续6天测定质控品计算批间准确度;准确度的评价基于平均测定浓度与质控品添加浓度的百分比,即准确度(%)=100%实测值/参考值。
1.2.4 稳定性试验 质控样品储存于-20℃,每月检测低、中、高质控品,连续测定5个月,统计分析月间质控品检测值差异。
1.2.5 干血斑间变异系数分析 随机选取低、中、高浓度的质控品各10个不同的干血斑,每个血斑检测3次,计算均值,标准差和CV(%),CV(%)≤15%方能达到检测要求。
1.3 统计学分析
采用SPSS 18.0统计软件进行数据处理。符合正态分布的计量资料以均数±标准差表示,多组间比较采用单因素方差分析。计数资料以百分比表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 血浆内源性类固醇激素测定
LC-MS/MS测定活性炭处理前、吸附一次后及吸附两次后血浆中的内源性类固醇激素含量。见表1。
2.2 质控品DBS批内精确度和准确度测定
质控品DBS的批内精确度为2.4%~7.0%,批内准确度为102.0%~111.0%,见表2。
2.3 质控品DBS批间精确度和准确度测定
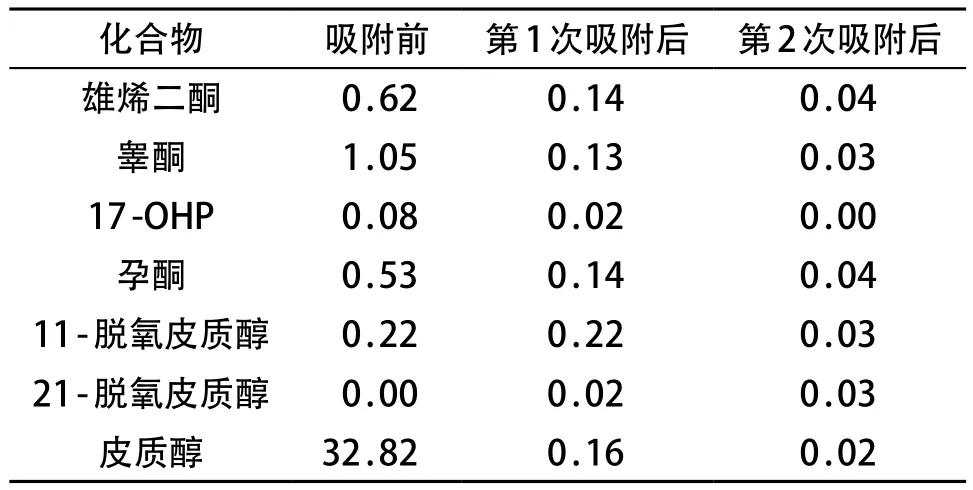
表1 LC-MS/MS测定活性炭吸附前后血浆中内源性类固醇激素含量 (ng·mL-1)
质控品DBS的批间精确度为5.1%~9.8%,批间准确度为99.0%~114.8%,见表3。
2.4 稳定性试验
将质控品DBS保存于-20℃,每月取出检测,检测5个月,月间比较差异无统计学意义(P>0.05),稳定性较好。见表4。
2.5 血斑间变异系数分析
质控品不同血斑间变异系数分析见表5,不同血斑间CV%为3.3%~8.2%,变异系数较小。
3 讨论
类固醇激素的测定在临床诊断中至关重要。目前多采用荧光免疫分析法试剂盒进行类固醇激素检测,一次试验只能测定一种激素,样本量需要较多,需采用不同的试剂盒来完成不同类固醇激素的检测,耗时长[1]。因血液中不同类固醇激素间结构相似存在交叉反应和基质干扰,荧光免疫分析法灵敏度和特异性相对不高,检测结果的假阳性率增加[2]。串联质谱法可检测多种物质,具有快速、特异度和灵敏度高等优点,国外一些实验室已将该技术应用于血清及DBS中类固醇激素谱的检测,可用于先天性肾上腺皮质增生症的筛查和诊断[8-10]。
荧光免疫分析法测定新生儿DBS样本中17-OHP水平是国内外普遍采用的新生儿CAH一级筛查方法,但其存在较高假阳性率[7]。国际上较为公认LC-MS/MS法作为新生儿CAH二级筛查方法,可测定DBS中类固醇激素谱,并考察酶反应的底物与产物比值,有效降低筛查假阳性[5,6,8]。本实验室已经建立了LCMS/MS测定DBS中类固醇激素方法。
室内质量控制是保证结果准确的重要手段,拥有良好的质控品是做好室内质量控制的关键。然而目前国内尚无LC-MS/MS测定DBS中类固醇激素试剂盒或质控品销售,而国外已建立此方法的实验室也未指出有可购买的试剂盒或者商业化的质控品。好的质控品应满足:①较低的基质效应;②至少有正常和异常两个浓度水平;③较小的质控样本间差异;④稳定期要较长;⑤无传染性。
本实验中收集全血后分离血细胞和血浆,血细胞利用生理盐水洗涤,血浆通过活性炭吸附去除内源性类固醇激素。处理后的血细胞及血浆按55∶45混合,添加不同浓度水平的标准品,将含类固醇激素的全血滴至干血滤纸片上,制成DBS类固醇激素质控品。本研究评价了低、中、高三个浓度水平自制DBS类固醇激素质控品的精确度、稳定性及血斑间差异。批内、批间精确度小于9.8%;质控品保存于-20℃,连续5个月取出测定,结果显示月间无显著性差异,稳定性较好;随机选取10个不同的大血斑取样检测,变异系数CV<8.2%,血斑间差异较小;本研究制备了低、中、高三个浓度水平的质控品,浓度分别为0.8、25.0、150.0 ng/mL,依据以往文献报道,包含了正常和异常浓度水平[3,11]。综上所述,自制的DBS类固醇激素质控品能满足上述要求。

表2 质控品DBS批内精确度和准确度 (%)
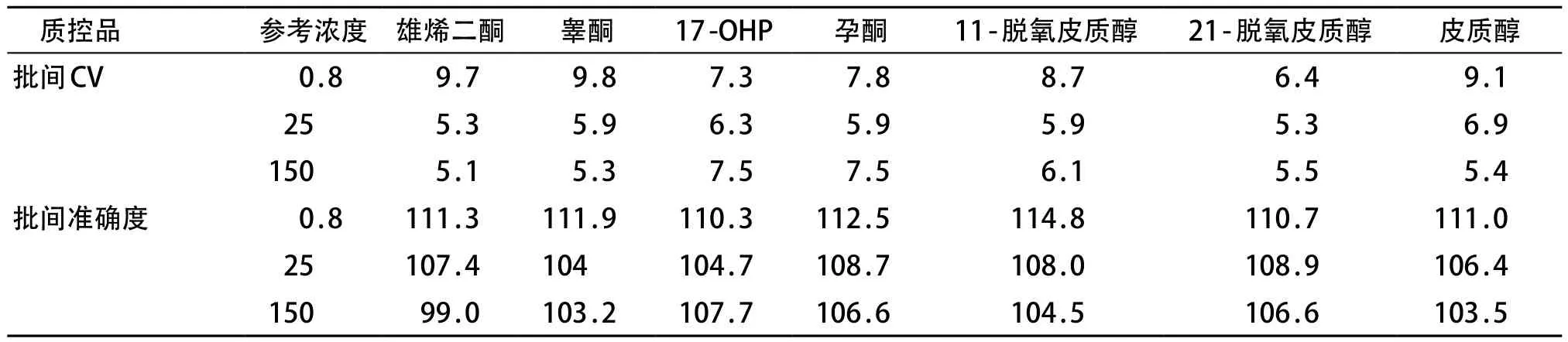
表3 质控品DBS批间精确度和准确度 (%)
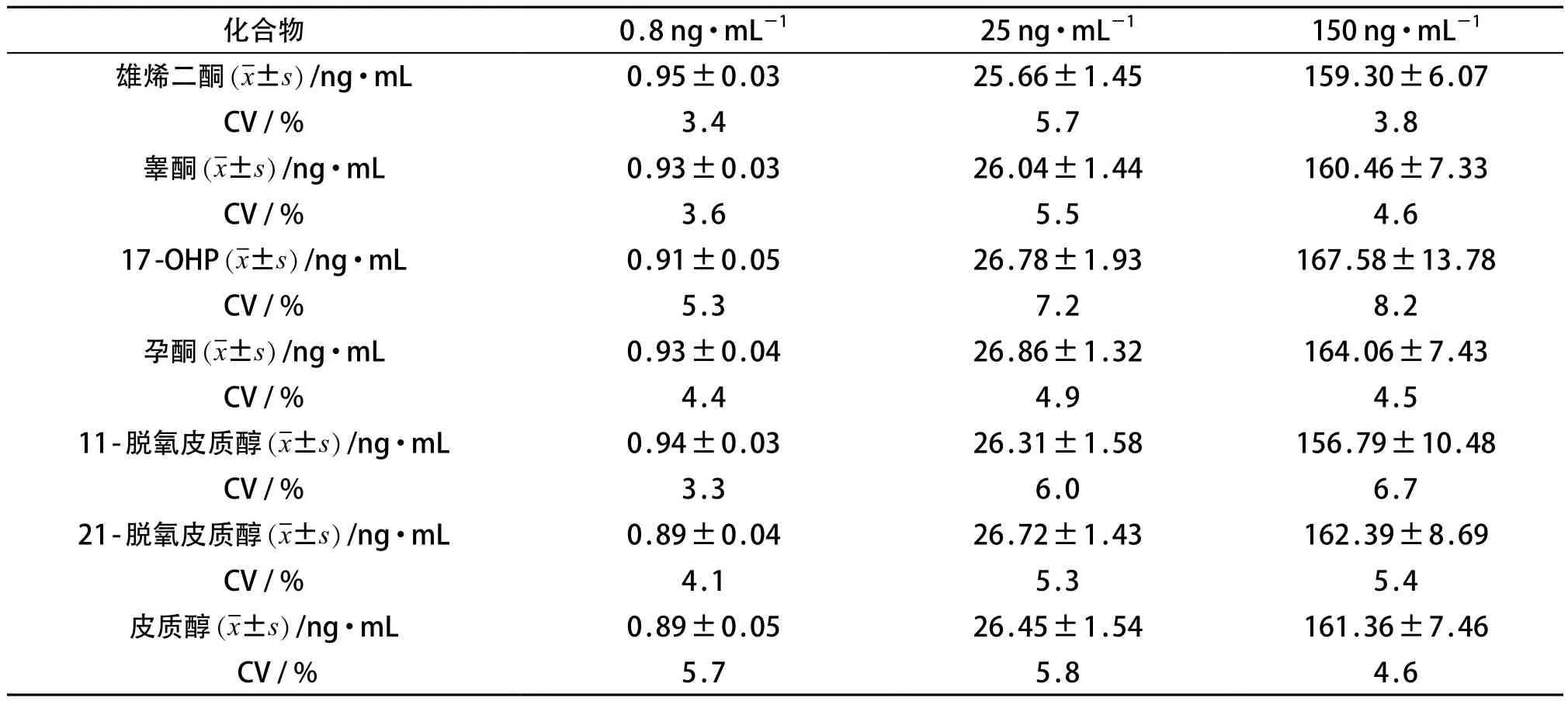
表5 质控品DBS不同血斑间变异系数分析
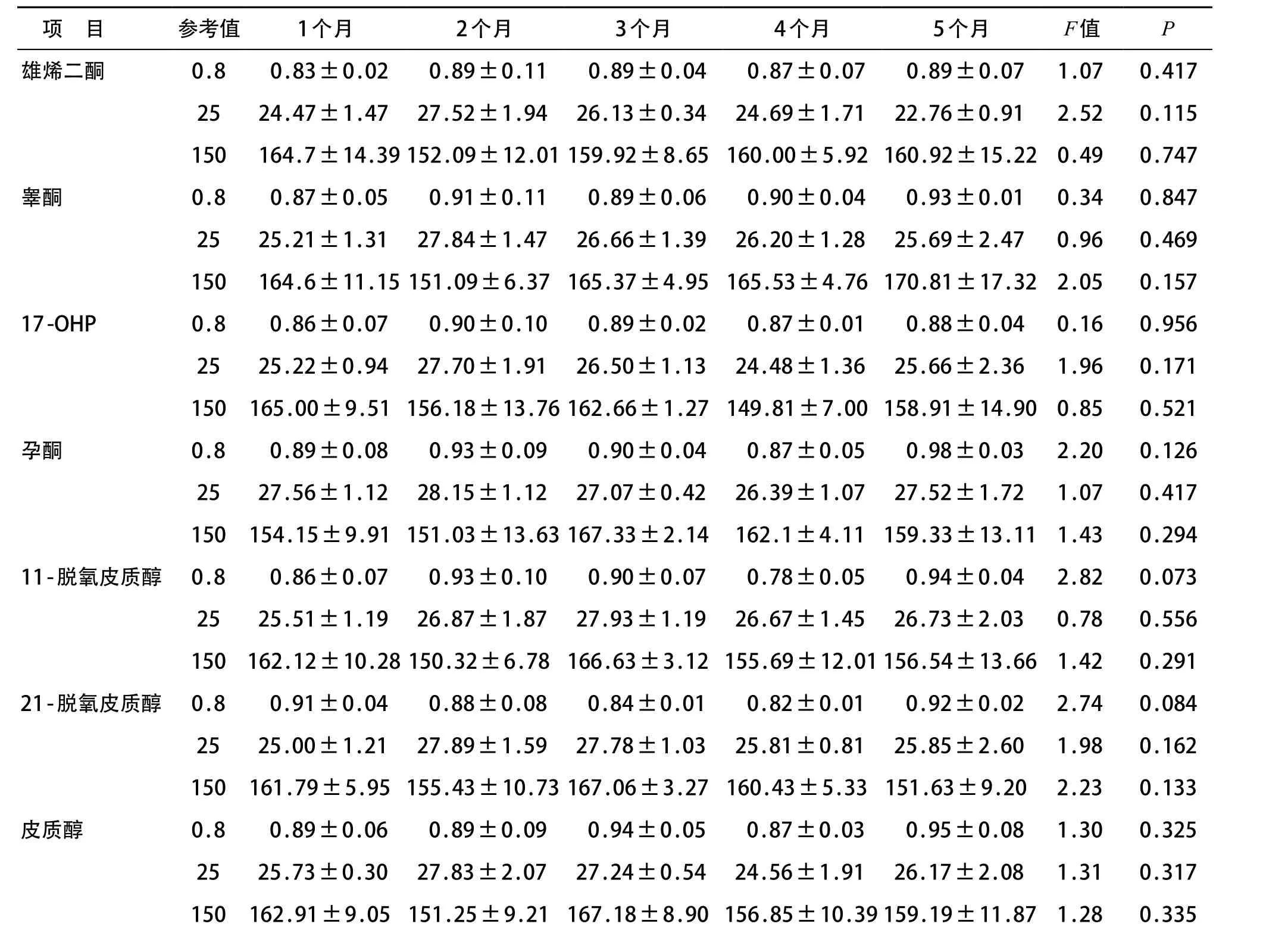
表4 质控品DBS稳定性分析 (x±s,ng·mL-1)
因全血中含有内源性类固醇激素,本实验中分离血细胞和血浆,血细胞利用生理盐水洗涤3次,血浆通过活性炭过夜吸附去除内源性类固醇激素[3,12]。本实验同时测定了活性炭处理前后血浆中内源性类固醇激素含量并比较,结果显示,经两次吸附后,血浆中内源性类固醇激素含量大大降低,小于0.04 ng/mL或者仪器未检出,表明使用活性炭吸附过夜能够去除血浆中大部分的内源性类固醇激素。目前国内极少的实验室建立了LC-MS/MS测定DBS中类固醇激素的方法,这可能与国内尚无厂商提供DBS类固醇激素试剂盒或质控品有关。
本研究自制的DBS类固醇激素质控品,符合室内质控品的要求。鉴于目前国内尚未有DBS类固醇激素质控品供应,本研究制备的DBS类固醇激素质控品可以提供给所需实验室作为内质控使用,有助于LCMS/MS测定干血滤纸片中类固醇激素方法的推广及应用。
[1] Stanczyk FZ, Clarke NJ. Advantages and challenges of mass spectrometry assays for steroid hormones [J]. J Steroid Biochem Mol Biol, 2010, 121(3-5)∶ 491-495.
[2] Taylor AE, Keevil B, Huhtaniemi IT. Mass spectrometry and immunoassay∶ how to measure steroid hormones today and tomorrow [J]. Eur J Endocrinol, 2015, 173(2)∶1-12.
[3] Boelen A, Ruiter AF, Claahsen-van der Grinten HL, et al.Determination of a steroid profile in heel prick blood using LC-MS/MS [J]. Bioanalysis, 2016, 8(5)∶ 375-384.
[4] White PC. Neonatal screening for congenital adrenal hyperplasia [J]. Nat Rev Endocrinol, 2009, 5(9)∶ 490-498.
[5] Choi JH, Kim GH, Yoo HW. Recent advances in biochemical and molecular analysis of congenital adrenal hyperplasia due to 21-hydroxylase deficiency [J]. Ann Pediatr Endocrinol Metab, 2016, 21(1)∶1-6.
[6] Sarafoglou K, Gaviglio A, Hietala A, et al. Comparison of newborn screening protocols for congenital adrenal hyperplasia in preterm infants [J]. J Pediatr, 2014, 164(5)∶1136-1140.
[7] White PC. Optimizing newborn screening for congenital adrenal hyperplasia [J]. J Pediatr, 2013, 163(1)∶ 10-12.
[8] Monostori P, Szabó P, Marginean O, et al. Concurrent confirmation and differential diagnosis of congenital adrenal hyperplasia from dried blood spots∶ application of a secondtier LC-MS/MS assay in a cross-border cooperation for newborn screening [J]. Horm Res Paediatr, 2015, 84(5)∶ 311-318.
[9] Rossi C, Calton L, Brown HA, et al. Confirmation of congenital adrenal hyperplasia by adrenal steroid profiling of filter paper dried blood samples using ultra-performance liquid chromatography-tandem mass spectrometry [J]. Clin Chem Lab Med, 2011, 49(4)∶ 677-684.
[10] Kulle AE, Riepe FG, Hedderich J, et al. LC-MS/MS based determination of basal- and ACTH-stimulated plasma concentrations of 11 steroid hormones∶ implications for detecting heterozygote CYP21A2 mutation carriers [J]. Eur J Endocrinol, 2015, 173(4)∶ 517-524.
[11] Kim B, Lee MN, Park HD, et al. Dried blood spot testing for seven steroids using liquid chromatography-tandem mass spectrometry with reference interval determination in the Korean population [J]. Ann Lab Med, 2015, 35(6)∶578-585.
[12] Lin N, Zhang H, Qiu W, et al. Determination of 7-ketocholesterol in plasma by LC-MS for rapid diagnosis of acid SMase-deficient Niemann-Pick disease [J]. J Lipid Res,2014, 55(2)∶ 338-343.
Preparation and evaluation of dried blood spots control materials for steroids
ZHAN Xia, HAN Lianshu, YE Jun, QIU Wenjuan, GU Xuefan (Department of Pediatric Endocrinology and Genetics, Shanghai Institute for Pediatric Research, Xinhua Hospital Aff i liated to Shanghai Jiaotong University School of Medicine, Shanghai 200092, China)
Objective To investigate the preparation method of dry blood spots (DBS) control materials for steroids used for internal quality control by liquid chromatography tandem mass spectrometry (LC-MS/MS). Methods Whole blood was collected and the blood cells and plasma were separated. The blood cells were washed by saline. The activated charcoal was added to the plasma. Standard substance was added to make different concentrations (low, medium, and high) of DBS control materials for steroids. The precision, accuracy, stability, and differences among different blood spots were detected and analyzed by LC-MS/MS. Results The inter-day precision and accuracy of DBS control materials for steroids were 2.4%-7.0% and 102.0%-111.0%, respectively, and the intra-day precision and accuracy were 5.1%-9.8% and 99.0%-114.8% respectively. The DBS control materials for steroids were stored for 5 months, and there was no difference among the different months (P>0.05).The coeff i cients of variation among different blood spots were small, 3.3%-8.2%. Conclusions The DBS control materials for steroids has good precision, accuracy and stability. The difference among different blood spots is small and meet the requirements of indoor quality control products. They can be used for the internal quality control in steroids detection by LC-MS/MS.
dried blood spots; steroid hormones; quality control products; tandem mass spectrometry
doi∶10.3969/j.issn.1000-3606.2017.12.016
上海市卫生局科研基金(No.2009210,20164Y0171);国家重点研发计划(No.2016YFC0901505,2016YFC0905100)
韩连书 电子信箱:hanlianshu@xinhuamed.com.cn
2017-07-12)
邹 强)
