一种新的基于微透析技术研究靶器官药代动力学方法
2017-12-27,,,,
, ,,,
(皖南医学院 药学院,安徽 芜湖 241002)
·基础医学·
一种新的基于微透析技术研究靶器官药代动力学方法
费佳丽,朱岳,马张庆,年四辉,洪宗元
(皖南医学院 药学院,安徽 芜湖 241002)
目的:采用微透析技术结合液相色谱-质谱联用法(LC-MS/MS)研究金刚烷胺在大鼠纹状体细胞外液中的药代动力学(药动学)过程,探讨靶器官药动学研究方法。方法SD大鼠(雄性,8~10周龄)行乌拉坦麻醉(1.0 g/kg)后,手术植入微透析探针于大鼠纹状体,以人工脑脊液恒速(2 μL/min)灌注探针。灌注1 h后,腹腔注射盐酸金刚烷胺(1.0 mg/kg),注射后立即收集透析液样本,样本收集间隔时间为12 min,连续 6 h。用LC-MS/MS法检测透析样本中金刚烷胺浓度,药物浓度-时间曲线及计算药动学参数用DAS软件拟合。结果金刚烷胺在大鼠纹状体细胞外液中浓度-时间变化呈一室开放模型,其主要药动学参数Tmax、Cmax、t1/2和 AUC0-∞为(1.78±0.59)h、(38.56±9.10)μg/L、(2.07±0.35)h和(591.84±278.39)μg/(L·h)。结论本实验建立了一种基于微透析采样结合LC-MS/MS法研究金刚烷胺在大鼠纹状体细胞外液中药代动力学过程的实验方法,该方法操作简单、灵敏度高,为研究药物在靶器官中的药动学过程提供了方法学基础。
金刚烷胺;微透析;靶器官;液相色谱-质谱联用;药代动力学
帕金森病[1](Parkinson′s disease,PD)是一种常见的中枢神经系统变性疾病,目前药物是主要的治疗手段[2],金刚烷胺是治疗PD的经典药物之一。据报道,金刚烷胺可促进脑内纹状体中多巴胺能神经元合成、释放和减少多巴胺重摄取,并加强中枢神经系统多巴胺与儿茶酚胺的作用而发挥抗PD作用[3]。与此同时,金刚烷胺可引起精神不安、失眠和运动失调等不良反应[4],这些不良反应的发生与其用量和(或)给药间隔时间不当相关联,其原因为目前临床制定给药方案的依据是金刚烷胺在血液中的药代动力动学参数。研究表明,合理的临床给药方案应以靶器官内药物浓度为基础,计算药动学参数,并制订给药方案。但是,由于方法学的限制,目前金刚烷胺在其靶器官纹状体内的药动学研究尚未见报道。
在体微透析(invivomicrodialysis,MD)是一种新型的生物采样技术,可对动物靶器官或靶组织进行在体采样,借助于现代高灵敏度的检测技术可检测样本中的药物浓度,研究药物在靶器官或靶组织中的药动学过程。由于微透析探针具有截留大分子的特点,所采集的透析液中只含有具有药理活性的游离药物(不包含蛋白结合药物),且所得样本干净,不需特殊处理即可直接进样分析等优点[5-6],故此目前该技术已被应用于药动学研究。
本实验将采用MD技术结合LC-MS/MS检测方法,研究金刚烷胺在大鼠纹状体中的药动学过程,计算药动学参数,并以此为基础制订合理的金刚烷胺临床给药方案。同时,也为研究药物在靶器官中的药动学过程提供新的实验方法学。
1 材料与方法

1.2 药品与试剂 盐酸金刚烷胺(含量为99%,批号:A1508047,上海阿拉丁生化科技股份有限公司),乌拉坦(上海化学试剂厂),甲醇、乙腈和甲酸(均为色谱纯,德国默克股份有限公司)。
1.3 主要仪器 色谱-质谱系统:Agilent 1260高效液相色谱仪,Agilent 6460三重四级杆串联质谱仪;色谱柱(ZORBAX SB-C18 2.1 mm×50 mm,Agilent),预柱(ZORBAX SB-C18 2.1 mm×50 mm,Agilent)。微透析系统:微透析探针(瑞典CMA12 Elite 14型长探针,半透膜长4 mm,日本),注射器(型号Hamilton,规格5.0 mL,美国),微量注射泵(型号RS232,KD Scientific,美国),微量样本自动收样器(型号 MAB85,瑞典)。脑立体定位仪(深圳市瑞沃德生命科技有限公司)。
1.4 色谱条件及质谱条件 色谱条件:流动相,乙腈∶0.05%甲酸=12∶88(v∶v);流速0.2 mL/min;柱温25℃;进样量17 μL。质谱条件:采用电喷雾离子源(ESI),在正离子模式下以多反应监测(MRM)的质谱扫描方式进行检测,金刚烷胺的选择监测离子反应为m/z152.1→m/z134.8和m/z152.1→m/z92.8。干燥气温度为325℃,干燥气流量为10 L/min,雾化气压力为20 psi,鞘气温度为400℃,鞘气流量为11 L/min,毛细管电压3500 V,喷嘴电压1000 V,碰撞电压18 eV。
1.5 标准曲线制备及线性范围 精密称取一定量的盐酸金刚烷胺,依次加入按1.6方法收集的空白透析液稀释成0.3125、0.625、1.25、2.5、5.0、10.0 ng/mL系列的标准溶液。取上述系列标准溶液17 μL,依次进样分析。以金刚烷胺浓度(x)对峰面积(y)进行回归计算,绘制标准曲线。
1.6 微透析采样与药物浓度测定 在麻醉状态下(乌拉坦,1.0 g/kg,腹腔注射),将大鼠头部固定于脑立体定位仪上,消毒、手术,植入微透析探针于大脑一侧纹状体,定位坐标[7]为前囟前1.7 mm,深度1.4 mm,旁开5.4 mm。以恒定速度2 μL/min向微透析探针灌流aCSF。1 h后,腹腔注射1.0 mg/kg盐酸金刚烷胺,连续收集透析样本6 h,样本收集间隔时间为12 min。透析液样本离心后进样测定金刚烷胺浓度。
1.7 微透析探针回收率测定 采用增量法[8]测定微透析探针的回收率。将探针分别浸入3种不同浓度(0.25、2.0、8.0 ng/mL)的盐酸金刚烷胺标准溶液中,用aCSF灌流微透析探针(灌流速度为2 μL/min),每种浓度下分别收集5个透析液样本,测定样本中金刚烷胺浓度(C测),计算探针回收率R=C测/C标,C标为标准品中金刚烷胺浓度。
1.8 细胞外液中药物实际浓度计算 纹状体细胞外液中金刚烷胺实际浓度C实际=C透析液/R,C透析液为透析液样本中检测浓度。
2 结果
2.1 色谱行为与回归方程 图1为按1.4方法测得的金刚烷胺标准品和脑纹状体透析液样本的LC-MS/MS色谱图。由图可见,基线噪音小,金刚烷胺分离完全,不受溶剂和透析液中杂质干扰,峰形良好,保留时间约为2.31 min。金刚烷胺在0.3125~10.0 ng/mL范围内线性关系良好,回归方程为y=45.439x+11.07(r2=0.9987,n=6),检测限为0.5 ng/mL(S/N=3)。
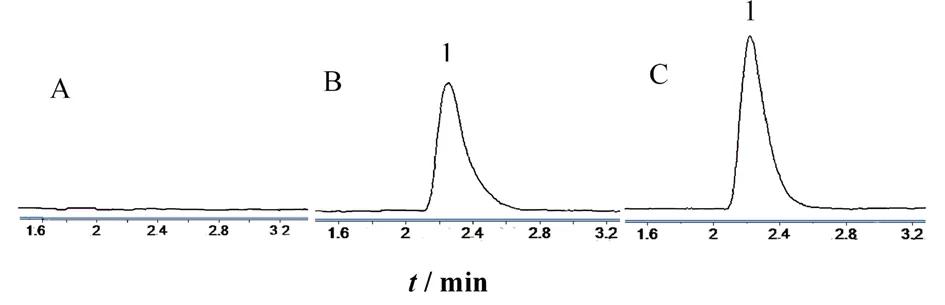
A:人工脑积液;B:空白微透析液 + 金刚烷胺标准品(1.25 ng/mL);C:纹状体透析液样本(注射金刚烷胺1.0 mg/kg后);1:金刚烷胺。
图1 金刚烷胺LC-MS/MS色谱图
2.2 精密度与回收率 用aCSF配制高、中、低(5.0、2.5、0.625 ng/mL)3种浓度的金刚烷胺标准溶液,取17 μL进样检测分析。于一天内平行进行5次测定计算日内精密度,连续5 d重复操作计算日间精密度(n=5)。结果见表1,金刚烷胺样品日内RSD和日间RSD分别为1.19%~7.83%和1.68%~8.28%,均<10%,相对回收率为96.83%~104.98%,均满足方法学验证要求。

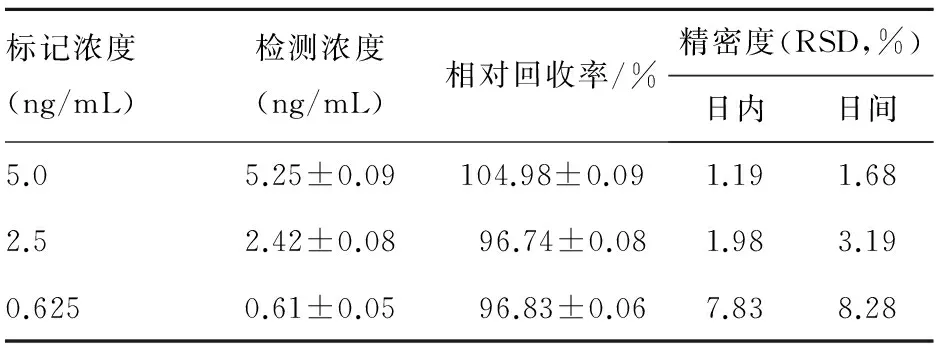
标记浓度(ng/mL)检测浓度(ng/mL)相对回收率/%精密度(RSD,%)日内日间5.05.25±0.09104.98±0.091.191.682.52.42±0.0896.74±0.081.983.190.6250.61±0.0596.83±0.067.838.28
2.3 探针回收率的计算 配制3种不同浓度的金刚烷胺标准溶液,按1.7方法测定微透析探针的回收率约为20.1%,见表2。

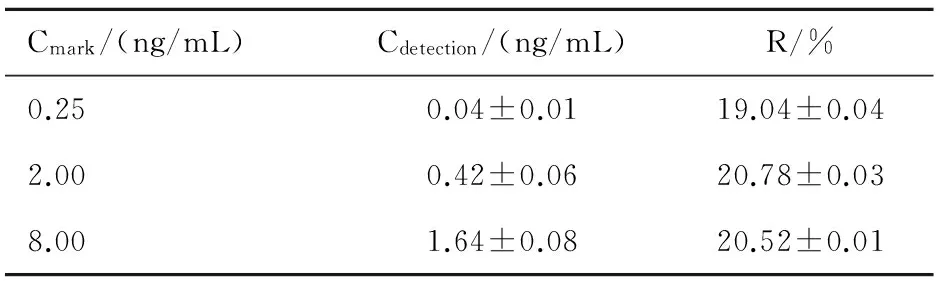
Cmark/(ng/mL)Cdetection/(ng/mL)R/%0.250.04±0.0119.04±0.042.000.42±0.0620.78±0.038.001.64±0.0820.52±0.01
2.4 金刚烷胺在大鼠纹状体细胞外液中的药动学
2.4.1 金刚烷胺浓度-时间曲线 大鼠腹腔注射1.0 mg/kg盐酸金刚烷胺后,纹状体中金刚烷胺算术浓度-时间曲线及对数浓度-时间曲线(C-T)分别见图2A和2B。DAS3.0软件计算结果显示,金刚烷胺在纹状体细胞外液中的浓度变化过程呈一室开放模型,达峰时间药为1.78 h。
2.4.2 药动学参数 用DAS3.0软件计算金刚烷胺在纹状体细胞外液中的药动学参数,结果见表3。
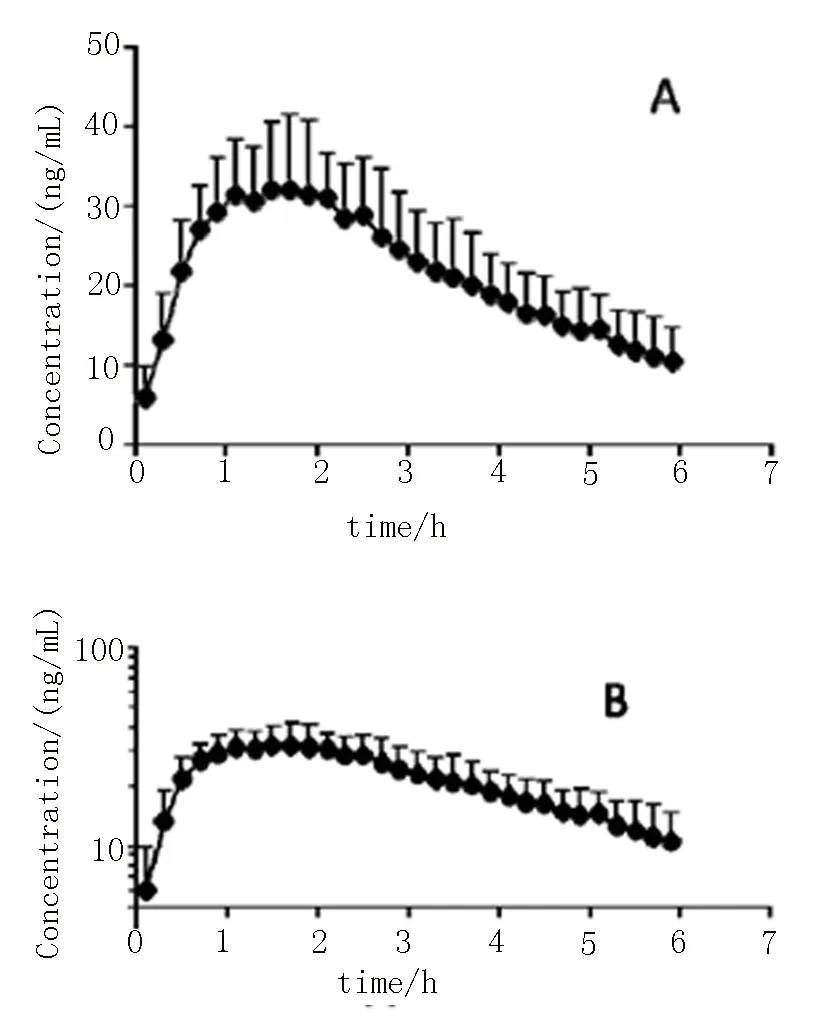
A.算术C-T曲线;B.对数C-T曲线。


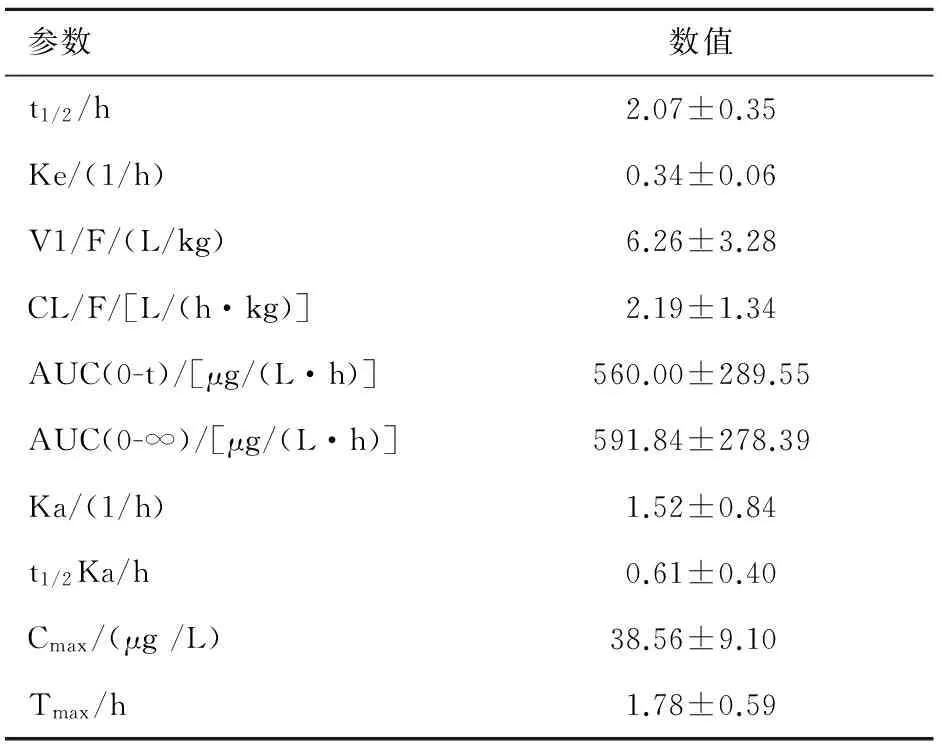
参数数值t1/2/h2.07±0.35Ke/(1/h)0.34±0.06V1/F/(L/kg)6.26±3.28CL/F/[L/(h·kg)]2.19±1.34AUC(0-t)/[μg/(L·h)]560.00±289.55AUC(0-∞)/[μg/(L·h)]591.84±278.39Ka/(1/h)1.52±0.84t1/2Ka/h0.61±0.40Cmax/(μg/L)38.56±9.10Tmax/h1.78±0.59
3 讨论
本文采用MD技术结合LC-MS/MS检测方法研究了金刚烷胺在大鼠纹状体中的药动学过程。结果显示金刚烷胺在大鼠纹状体中呈一室开放模型变化,Tmax、Cmax、t1/2等主要药动学参数分别为(1.78±0.59)h、(38.56±9.10)μ/L、(2.07±0.35)h。与以传统给药后采集血液,分离血浆并检测血浆中药物浓度计算的药动学参数(数据未列)比较,大鼠纹状体细胞外液中金刚烷胺t1/2长于血浆(血浆t1/2为1.77 h,P<0.05),表明金刚烷胺在脑纹状体内的消除速度比血浆慢;纹状体细胞外液中金刚烷胺的达峰时间Tmax也显著延长(血浆Tmax为0.5 h,P<0.01),导致这种差异的原因可能与血脑屏障有关;纹状体细胞外液中金刚烷胺的达峰浓度Cmax则显著降低(血浆Cmax为100.84 μg/L,P< 0.01),这是因为血浆中金刚烷胺浓度为混合浓度(即游离浓度和与血浆蛋白结果浓度之和),而用MD技术采样测得的仅为游离药物浓度所致。
以上数据间的差异表明,金刚烷胺在大鼠纹状体细胞外液中的药动学过程与其在血液中不同,因此以血浆药物浓度代替非靶器官内药物浓度进行药动学研究,结果不够准确,以该药动学参数制订的给药方案也不够合理。首先血浆中的药物浓度是一种混合浓度,既包括了发挥药效作用的游离型药物浓度,也包括了暂时不发挥药效的结合型药物浓度;其次对于靶器官为中枢神经系统的药物,也存在血脑屏障而对药物吸收入脑的影响[9-10]。临床资料显示,金刚烷胺在发挥抗PD作用时,会引起精神不安、失眠和运动失调等不良反应[4],并认为这些不良反应的发生为其用量过大致靶器官浓度过高所致。因此,最优的临床用药方案应该根据药物在其作用的靶器官中的药动学参数来制定。
应用MD采样技术研究药物药动学过程除了以上优点外,尚具有以下特点[11-13]:①取样量小,连续长时间取样不引起取样部位的容积变化,对生物体内的平衡干扰小,所得数据更加可靠;②样品纯净,不含大分子物质,不需进行样本处理而直接进样检测;③可与多种分析仪器如HPLC、LC-MS/MS等联用,实现连续在线检测;④可在动物清醒状态(生理状态)或麻醉状态下进行采样,达到研究药物在动物生理和病理状态下的药动学特征。
总之,本实验建立了一种基于在体MD采样技术,结合LC-MS/MS检测方法测定金刚烷胺在靶器官纹状体中药物浓度的方法。该方法操作简单,所测结果准确可靠,为临床合理应用金刚烷胺提供了药动学依据,同时也为研究药物在靶器官中的药动学过程提供了方法学基础。
[1] CAPRIOTTI T,TERZAKIS K. Parkinson Disease[J]. Home Healthc Now,2016,34(6):300-307.
[2] QUINN N. Drug Treatment Of Parkinson′s Disease[J]. BMJ,2015,310(6979):575.
[3] PAHWA R,TANNER CM,HAUSER RA,etal. Amantadine extended release for levodopa-induced dyskinesia in Parkinson′s disease (EASED Study)[J]. Movement Disorders Official Journal of the Movement Disorder Society,2015,30(6):788-795.
[4] 杨宝峰. 药理学[M].8版.北京:人民卫生出版社,2013:135.
[5] LINDQVIST A,JANSSON B,HAMMARLUND-UDENAES M. Quantitative analysis of the opioid peptide DAMGO in rat plasma and microdialysis samples using liquid chromatography-tandem mass spectrometry[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2012,900:11-17.
[6] BARKER SA,BORJIGIN J,LOMMICKA I,etal. LC/MS/MS analysis of the endogenous dimethyltryptamine hallucinogens,their precursors,and major metabolites in rat pineal gland microdialysate[J]. Biomed Chromatogr,2013,27(12):1690-700.
[7] YONG Z,YAN L,ZHOU P,etal. Effects of thienorphine on release of dopamine and noradrenalin:An in vivo microdialysis study in rats[J]. Neuroscience Letters,2012,513(2):132-136.
[8] 马博,孙桂波,李明,等. 钩藤碱微透析探针回收率测定及影响因素研究[J]. 中国新药杂志,2012,21(20):2371-2375.
[9] 马张庆,陶芳,方浩,等. 应用微透析技术研究盐酸曲马多在小鼠额叶皮质细胞外液中的药动学[J]. 药学学报,2013,48(3):406-410.
[10] 马爱梅,赵永波,陈英辉. 苯妥英钠在大鼠血液和脑细胞外液药动学研究[J]. 中国临床神经科学,2005,13(2):118-122.
[11] 李范珠,冯健. 脑微透析技术及其在脑内药动学中的应用[J]. 中国药学杂志,2006,41(6):405-407.
[12] 赵宁,程巧鸳,俞文英,等. 微透析技术在药动-药效学结合研究中的应用[J].国际药学研究杂志,2008,35(2):100-106.
[13] LIU X,VAN NATTA K,YEO H,etal. Unbound Drug Concentration in Brain Homogenate and Cerebral Spinal Fluid at Steady State as a Surrogate for Unbound Concentration in Brain Interstitial Fluid [J]. Drug Metabol Disp,2009,37(4):787-793.
Aninnovationexperimentalmethodforstudyingpharmacokineticsofdrugsintargetorgansusinginvivomicrodialysis
FEIJiali,ZHUYue,MAZhangqing,NianSihui,HONGZongyuan
School of Pharmacy,Wannan Medical College,Wuhu 241002,China
Objective: To explore the research method for pharmacokinetics of drugs in target organs via examining the pharmacokinetic process of amantadine in the extracellular fluid of striatum of rats usinginvivomicrodialysis and liquid chromatography tandem mass spectrometry (LC-MS/MS) technique.Methods:Male SD rats,aged 8-10 weeks were anaesthetized with urethane in dosage of 1.0 g/kg. A microdialysis probe was implanted into the striatum and artificial cerebrospinal fluid (aCSF) was injected at flow rate of 2 μL/min. After 1 h of aCSF perfusion,amantadine was intraperitoneally administered in dose of 1.0 mg/kg,and dialysate was instantly collected in 6 h by interval of 12 min. Amantadine concentration in the dialysate was measured using LC- MS/MS. The concentration-time profile and pharmacokinetic parameters of amantadine were calculated by DAS software.Results:The concentration-time profile of amantadine in the striatum of rats was fitted to one-compartment open model. The main pharmacokinetic parameters Tmax,Cmax,t1/2and AUC0-∞were (1.78±0.59)h,(38.56±9.10)μg/L,(2.07±0.35)h and (591.84±278.39)μg/(L·h) in the striatum extracellular fluid,respectively.Conclusion:We have successfully created the experimental method for studying pharmacokinetic process of amantadine in the striatum of rats usinginvivomicrodialysis with LC-MS/MS. This technique may provide methodology basis for research pharmacokinetics of drugs in target organs due to its simple performance and higher sensitivity.
amantadine;microdialysis;target organ;LC-MS/MS;pharmacokinetics
1002-0217(2017)05-0409-04
国家自然科学基金项目(81671318,81171255);安徽省科技攻关项目(1501041157)
2017-03-06
费佳丽(1990-),女,2014级硕士研究生,(电话)15156319032,(电子信箱)535865611@qq.com;洪宗元,男,教授,(电子信箱)zyhongwnmc@aliyun.com,通信作者。
R 96
A
10.3969/j.issn.1002-0217.2017.05.001
