锌镁铝层状双氢氧化物对煤自燃的阻化特性
2017-12-22张玉涛史学强李亚清李山山刘宇睿
张玉涛,史学强,李亚清,文 虎,黄 遥,李山山,刘宇睿
(西安科技大学 安全科学与工程学院,陕西 西安 710054)
锌镁铝层状双氢氧化物对煤自燃的阻化特性
张玉涛,史学强,李亚清,文 虎,黄 遥,李山山,刘宇睿
(西安科技大学 安全科学与工程学院,陕西 西安 710054)
煤炭自燃的发生严重影响着煤矿的安全生产,添加阻化剂是预防煤炭自燃的常用技术手段之一。采用热重/差热扫描-傅里叶红外光谱(TG/DSC-FTIR)联用技术研究了锌镁铝类水滑石(Zn1Mg2Al1-CO3-LDHs)对煤炭自燃的阻化特性和机理,测试了该阻化剂作用下,煤自燃过程中质量、特征温度、热效应和气体产生量等参数的变化规律。测试结果表明,吸热是Zn1Mg2Al1-CO3-LDHs抑制煤自燃的主要原理,煤样中阻化剂的添加能够提高煤的脱水脱附最大速率点、缓慢氧化温度和煤样的起始放热温度,而且可以降低煤样的最大释热功率,同时对煤样氧化过程中CO2的产生有轻微的促进作用,阻化率随添加量的增大呈线性增加,研究表明Zn1Mg2Al1-CO3-LDHs对煤自燃有良好的抑制作用。
煤自燃;阻化剂;Zn1Mg2Al1-CO3-LDHs;TG/DSC-FTIR联用;氧化过程
煤炭是我国的主要能源,但随着煤矿开采深度和强度的增大,煤的自然发火也越来越频繁,严重影响到煤矿的安全生产,威胁着国家的利益和人民的生命财产安全[1-2]。向煤体喷洒阻化剂是当前预防煤自燃的主要技术手段之一[3-4],常见的煤体阻化剂主要有MgCl2、CaCl2、水玻璃、NaCl、Ca(OH)2以及有机物质如甲基纤维素、聚氨树脂、离子型表面活性剂等[5-8],其主要作用是惰化煤体表面活性结构,阻止煤炭的氧化或者吸热降温,使煤体处于潮湿状态。但其大多不容易均匀分散在煤体上,且喷洒工艺较难实施,有些阻化剂(如含卤阻燃剂)还会腐蚀井下设备,影响井下工人的身体健康[9-10]。
近年来,随着金属离子层状双氢氧化物(通常也称为水滑石类化合物,缩写为LDHs)在聚合物阻燃领域的应用,其高效环保抑烟的阻燃性能,已经得到人们的广泛认可[11-13]。另外,LDHs阻燃剂不含卤素,其丰富的性能能够满足不同煤种的阻化需求,且具有物理和化学双重作用机理[14-15]。因锌镁铝类水滑石(Zn1Mg2Al1-CO3-LDHs)在阻燃领域应用较为广泛,且其中含有的金属Zn2+,Mg2+和Al3+离子兼具环保抑烟的特性[16-17],能够进一步加强水滑石的阻化效果。本文制备了阳离子比例为1∶2∶1的Zn1Mg2Al1-CO3-LDHs阻化剂,并将其与东川矿区烟煤进行混合,借助热重/差热扫描-傅里叶红外光谱(TG/DSC-FTIR)联用技术从煤自燃特征温度、煤的热效应和煤自燃产生的氧化气体等方面系统分析了Zn1Mg2Al1-CO3-LDHs对东川矿区烟煤的阻燃效果及阻化机理。该研究可为理解阻化剂的阻化机理和开发新型阻化剂提供借鉴。
1 实验方法及装置
1.1 Zn1Mg2Al1-CO3-LDHs的制备
Zn1Mg2Al1-CO3-LDHs阻化剂的制备方法为原位共沉淀法,所用到的主要原料有ZnCl2,MgCl2,AlCl3,Na2CO3和NaOH。制备时,首先分别在2 000 mL的容量瓶中配置ZnCl2,MgCl2,AlCl3各0.2 mL/L;然后按n(Zn2+)∶n(Mg2+)∶n(Al3+)=1∶2∶1的比例将3种配置好的盐溶液混合后加入到四口烧瓶中,得到2 000 mL 混合盐溶液A,并将其搅拌均匀。用Na2CO3和 NaOH配置 OH-浓度为0.75 mol/L的混合碱溶液B,借助恒压漏斗用配置好的混合碱溶液B逐滴滴定盐溶液A,滴定过程中不停地快速搅拌,控制滴定终点的pH值为10.0,滴定完成后继续剧烈搅拌1 h;最后将溶液置于 75℃水浴中晶化24 h,用去离子水离心洗涤直至无 Cl-且pH=7;75 ℃真空干燥 24 h,研磨成粉末即可得到阻化剂Zn1Mg2Al1-CO3-LDHs,其分子结构如图1所示。
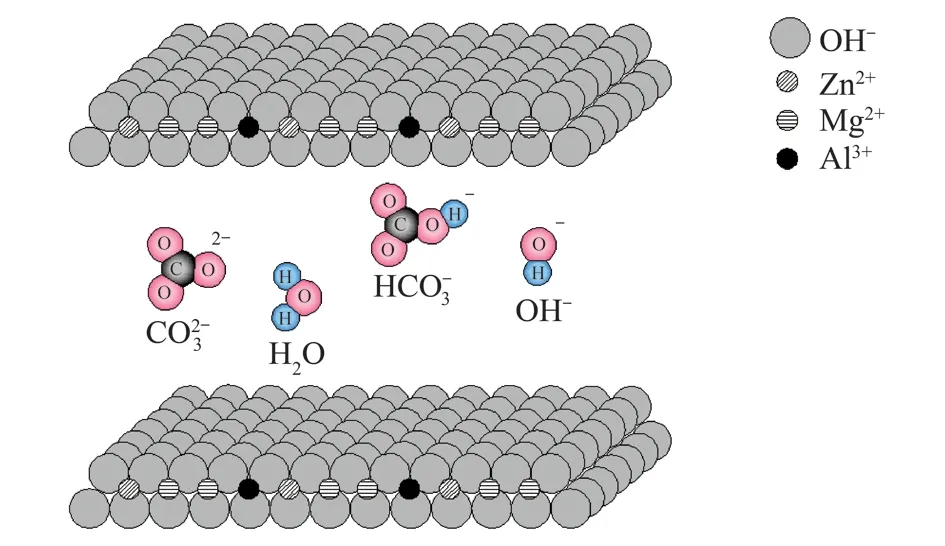
图1 Zn1Mg2Al1-CO3-LDHs分子结构Fig.1 Molecular Structure of Zn1Mg2Al1-CO3-LDHs
Zn1Mg2Al1-CO3-LDHs比表面积较大,且具有层状结构,层间距为0.7~0.8 nm。层内原子以共价键连接,并具有可交换的 CO2-3等阴离子,在某些溶液中可稳定存在,整体具有良好的热稳定性,而且在一定情况下,所含的OH-可以参与化学反应,吸收热量,因而在理论上应具有一定的阻化效果。
1.2 测试煤样制备
实验选取陕北东川矿区烟煤作为实验煤样,实验煤样的工业分析结果见表1。将原煤块剥去表皮部分(3 cm左右),在空气中破碎至粒径小于0.098 mm。将破碎好的煤样装入密封塑料袋抽真空放置阴凉处储存备用。实验前24 h将破碎好的煤样分别与Zn1Mg2Al1-CO3-LDHs以不同比例进行混合,制得Zn1Mg2Al1-CO3-LDHs添加量分别为0(即原煤样),5%,10%,15%,20%和25%的混合实验煤样。
表1东川矿区煤样工业分析结果
Table1ProximateanalysisofDongchuancoalsample%

水分灰分挥发分固定碳9.023.5230.4157.05
1.3 实验装置及过程
实验所采用的装置是TG/DSC-FTIR联用系统,该系统由德国耐驰(NETZSCH)公司的STA449F3型同步热分析仪和德国布鲁克(BRUKER)公司的VERTEX70v型傅里叶红外光谱仪两部分组成。红外光谱仪与同步热分析仪通过专用接口连接,热重分析过程中,煤样氧化所释放出来的气体被同步输送至红外光谱仪进行官能团的特性分析,实验过程中该仪器可以辅助绘制三维坐标图谱,同时显示叠加的红外曲线随波数以及时间或温度的关系。
实验时每次称取10 mg准备好的煤样放入样品室内进行测试,设定实验起始温度为30 ℃,终止温度为800 ℃,在升温速度为10 ℃/min,供氧浓度为21%的条件下对煤样进行测试分析。为了保证热解逸出气体不发生冷凝和结构变化。实验中各个仪器的接口和气体传输线的温度均设定为200 ℃。实验保护气为高纯氮气,考虑逸出气体的返混和红外检测灵敏度问题,选择载气总流量为60 mL/min。
2 结果与讨论
2.1 Zn1Mg2Al1-CO3-LDHs热解特性分析
实验过程中Zn1Mg2Al1-CO3-LDHs阻化剂的TG-DTG变化趋势如图2所示。因Zn1Mg2Al1-CO3-LDHs在受热分解过程中主要释放出的气体是H2O和CO2,为了很好地对比Zn1Mg2Al1-CO3-LDHs分解过程中各个阶段的特性,从红外光谱图中将H2O(对应波数3 735 cm-1)和CO2(对应波数2 357 cm-1)的轨迹图解出来,如图3所示。
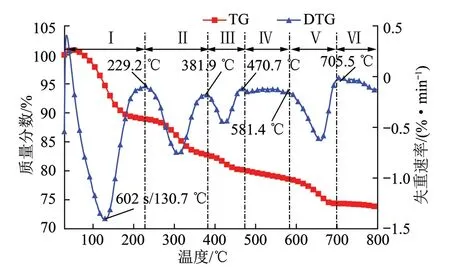
图2 Zn1Mg2Al1-CO3-LDHs的热重曲线Fig.2 TG-DTG graphs of Zn1Mg2Al1-CO3-LDHs
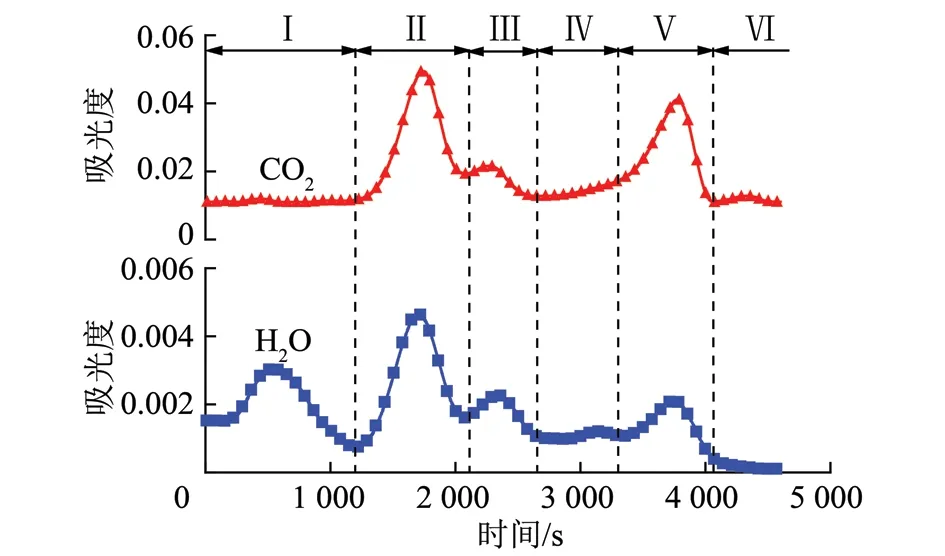
图3 Zn1Mg2Al1-CO3-LDHs受热分解产生的H2O和CO2的轨迹Fig.3 Evolution of H2O and CO2 during pyrolysis process of Zn1Mg2Al1-CO3-LDHs
结合图2和3可以看出,Zn1Mg2Al1-CO3-LDHs受热分解的全过程可以分成6个阶段,其各个阶段的主要特征如下:
(1)第I阶段(30~230 ℃或0~1 200 s):在该阶段有大量的水分产生,而CO2产量几乎没有任何变化,图2失重速率(DTG)的曲线与图3中对应阶段水分的蒸发量相吻合,随着水分蒸发强度逐渐增大到最大值,Zn1Mg2Al1-CO3-LDHs失重速率也几乎在同一点(约130 ℃或600 s)达到最大值。因此,可以判断该阶段的失重主要来自于Zn1Mg2Al1-CO3-LDHs吸附的水分和层间水分的蒸发,但其自身的结构几乎没有变化。
(2)第Ⅱ阶段(230~380 ℃或1 200~2 110 s):在这一阶段,Zn1Mg2Al1-CO3-LDHs进一步失去结晶水,同时产生CO2,并吸收大量的热。
(3)第III阶段(380~470 ℃或2 110~2 650 s):Zn1Mg2Al1-CO3-LDHs中的阴离子 CO32-在这一阶段受热转变生成CO2,同时生成双金属复合氧化物,Zn1Mg2Al1-CO3-LDHs有序的层状结构被破坏,表面积增加,孔隙容积增大。
(4)第IV阶段(470~580 ℃或2 650~3 300 s):该阶段Zn1Mg2Al1-CO3-LDHs的失重速率几乎保持不变,有少量的H2O和CO2生成。
(5)第V阶段(580~700 ℃或3 300~4 060 s):在该阶段Zn1Mg2Al1-CO3-LDHs分解产生的金属氧化物开始烧结,Zn1Mg2Al1-CO3-LDHs进一步热解生成H2O和CO2,致使表面积降低,孔隙容积减小。
(6)第VI阶段(>700 ℃或>4 060 s):Zn1Mg2Al1-CO3-LDHs基本热解完毕,质量不再发生变化。
2.2 Zn1Mg2Al1-CO3-LDHs对煤自燃阻化特性分析
2.2.1Zn1Mg2Al1-CO3-LDHs对煤自燃特征温度的影响
结合煤自燃过程的TG,DTG和DSC曲线,煤自燃的全过程有6个特征温度点,分别为:① 脱水脱附最大速率点(Trl):该点为DTG曲线上第1个极大值,即脱水脱附阶段煤样的最大失重速率点。在该点处,煤体的“脱水速率+脱附速率-吸氧速率”的代数和达到最大值,因为该温度时吸氧强度较小,吸氧速率较低,所以,可以认为该温度处脱水脱附速率达到最大;② 缓慢氧化温度(Tml):该点表观上为缓慢氧化阶段的起始点,实际上为吸氧增重速率超过煤样中气体产生速率的起始点,故该点为TG曲线上的第1个质量极小值点;③ 热解温度(Tmh):从该点开始,因温度升高,煤样开始热解,产生的CO,CH4等可燃挥发分逐渐增大,这些可燃组分释放出来以后与氧气进行反应,产生大量水蒸气和CO2。因此,气体产生量急剧增大,超过了煤样吸氧的增重量,煤样的总重量开始降低,所以该点为TG曲线上的质量极大值点。④ 燃点(Tig):我国国家标准《煤的着火温度测定方法》(GBT 18511—2001)将煤的着火温度定义为煤释放出足够的挥发分与周围大气形成可燃混合物的最低燃烧温度。当前在确定煤燃点的方法上,国内外学者的意见并不统一。本文基于国标对于燃点的定义,提出以DSC曲线的放热速率急剧增大点即DSC曲线在氧化阶段的最大极值点作为煤的燃点;⑤ 最大失重速率温度(Trm):为DTG曲线的最小极值点,在该点处,煤的燃烧强度达到最大,煤自燃的指标气体释放速率也达到最大值。最大失重速率温度值越小,表明煤氧化反应的速度越快;⑥ 燃尽温度(Tme):燃尽温度是评价煤燃烧性能的重要指标,同等质量下,燃尽温度越低,说明燃烧速度越快。本文采用TG-DTG相结合的方法确定燃尽温度,过最大失重速率温度做垂线交TG曲线于一点,过该点做TG曲线的切线与煤燃烧终止(重量不再变化)水平线的交点所对应的温度。表2汇总了东川烟煤在不同Zn1Mg2Al1-CO3-LDHs阻化剂添加量下的特征温度。
不同Zn1Mg2Al1-CO3-LDHs添加量下,煤样脱水脱附最大速率点和缓慢氧化温度的变化曲线如图4所示。从图中可以看出,随着Zn1Mg2Al1-CO3-LDHs添加量的增加,煤样脱水脱附最大速率点和缓慢氧化温度存在“滞后效应”,即向高温区偏移,且随着Zn1Mg2Al1-CO3-LDHs添加量的增大均近似呈线性增加。这是因为缓慢氧化温度以前属于脱水脱附阶段,由表2可见缓慢氧化温度处于130~160℃,而根据Zn1Mg2Al1-CO3-LDHs热解特性可知当温度低于230 ℃时,Zn1Mg2Al1-CO3-LDHs会随着温度的升高逐渐失去层间水分,从而导致煤样脱水脱附最大速率点和缓慢氧化温度均向高温区延迟。从图4还可以看出,两条直线近似平行,该现象表明脱水脱附最大速率点和缓慢氧化温度随Zn1Mg2Al1-CO3-LDHs阻化剂添加量的变化规律一致,但同等条件下缓慢氧化温度比脱水脱附最大速率点高约55~70 ℃(平均64 ℃)。

图4 不同Zn1Mg2Al1-CO3-LDHs添加量下的煤自燃的脱水脱附最大速率点和缓慢氧化温度曲线Fig.4 Maximum rate of dehydration and desorption and the slow oxidation temperature of coal spontaneous combustion as a function of the additive amount of Zn1Mg2Al1-CO3-LDHs
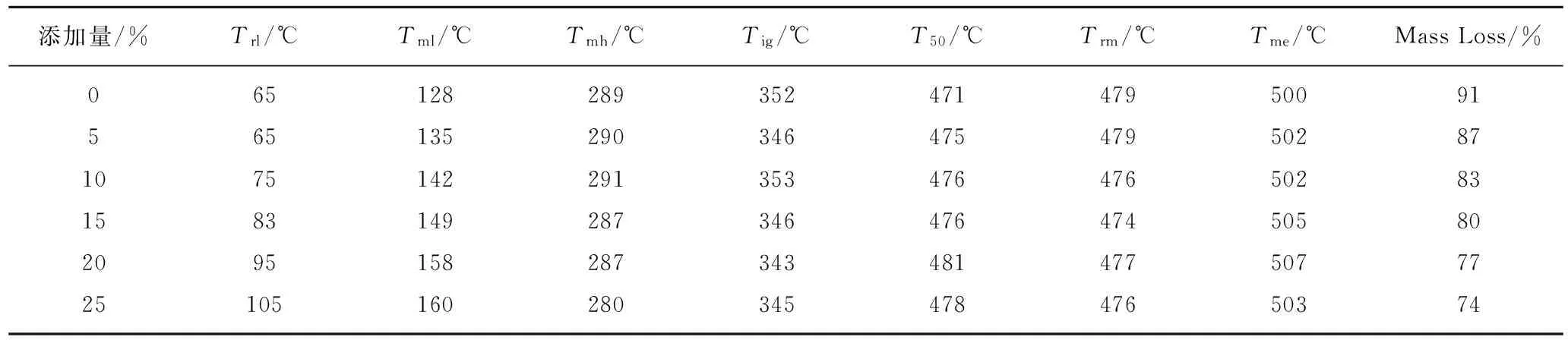
添加量/%Trl/℃Tml/℃Tmh/℃Tig/℃T50/℃Trm/℃Tme/℃MassLoss/%06512828935247147950091565135290346475479502871075142291353476476502831583149287346476474505802095158287343481477507772510516028034547847650374
从表2可以看出,Zn1Mg2Al1-CO3-LDHs阻化剂添加量对热解温度的影响很小,这主要是因为煤热解反应的发生主要取决于反应的活化能,其大小主要受煤自身的特性影响,Zn1Mg2Al1-CO3-LDHs的添加虽然能吸收煤自燃过程中产生的部分热量,导致煤体升温减缓,能够从时间上延迟煤体热解的发生,但对煤体的热解温度基本上不产生任何影响。此外,从表2可见,对于不同的Zn1Mg2Al1-CO3-LDHs添加量,该煤样的燃点大约位于340~350 ℃,总体来说Zn1Mg2Al1-CO3-LDHs的添加对煤的燃点影响较小。而比较发现,对于不同的Zn1Mg2Al1-CO3-LDHs添加量,煤的燃点比热解温度高56~64 ℃。
另外,表2中的数据显示Zn1Mg2Al1-CO3-LDHs添加量对最大失重速率温度影响也比较小,在不同的Zn1Mg2Al1-CO3-LDHs添加量下,煤样的最大失重速率温度均位于474~479 ℃之间。而燃尽温度随着Zn1Mg2Al1-CO3-LDHs添加量的增加有略微增大的趋势,但增加趋势并不明显,燃尽温度在实验范围的Zn1Mg2Al1-CO3-LDHs添加量下位于500~507 ℃。这两个温度均位于Zn1Mg2Al1-CO3-LDHs热解的第IV阶段,该阶段Zn1Mg2Al1-CO3-LDHs的失重速率几乎保持不变,生成的H2O和CO2也较少,因此对最大失重速率温度和燃尽温度影响都较小。由此可见,Zn1Mg2Al1-CO3-LDHs对煤自燃低温区(即煤氧化达到燃点之前)的影响较为显著,因此对煤自燃的发生能够起到非常重要的抑制作用。
2.2.2Zn1Mg2Al1-CO3-LDHs对煤自燃热效应的影响
不同Zn1Mg2Al1-CO3-LDHs添加量下,东川矿区烟煤的DSC曲线如图5所示。根据图5得到不同Zn1Mg2Al1-CO3-LDHs含量下的煤自燃热量参数(表3)。

图5 不同Zn1Mg2Al1-CO3-LDHs添加量下煤样的DSC曲线Fig.5 DSC curves of coal samples with different additive amounts of Zn1Mg2Al1-CO3-LDHs as a function of the temperature

添加量/%起始放热温度/℃最大释热功率对应温度/℃最大释热功率/(mW·mg-1)脱水脱附吸热量/(J·g-1)全过程放热量/(J·g-1)净放热量/(J·g-1)080.77480.632.963618111180755121.70482.132.1139165861654710113.10479.231.7067164121634515113.30477.928.97141162991615820137.90480.224.69151141631401225143.20477.823.501811260112420
由表3可见,Zn1Mg2Al1-CO3-LDHs的添加大大提高了煤样的起始放热温度,将该温度提高了大约30~60 ℃,Zn1Mg2Al1-CO3-LDHs添加量越大,起始放热温度越高,当添加量达到25%时,煤样的起始放热温度由80.77 ℃提高到了143.2 ℃。这主要是因为Zn1Mg2Al1-CO3-LDHs中含有层间水,随着煤温的升高层间水逐渐蒸发,从而吸收了部分煤氧复合产生的热量,造成起始放热温度的延迟。Zn1Mg2Al1-CO3-LDHs对最大释热功率对应温度的影响较小,因为该阶段Zn1Mg2Al1-CO3-LDHs的失重速率几乎保持不变,生成的H2O和CO2也较少。从最大释热功率来看,Zn1Mg2Al1-CO3-LDHs对煤自燃的影响较为明显,随着Zn1Mg2Al1-CO3-LDHs添加量的增大,最大释热功率也相应减小,当添加量增加到25%时,最大释热功率从32.96降低到23.5 mW/mg。
另外,从表3还可以明显看出,Zn1Mg2Al1-CO3-LDHs对煤自燃脱水脱附吸热量的影响较为显著,随着Zn1Mg2Al1-CO3-LDHs添加量的增加,脱水脱附吸热量逐渐增大,当添加量从0增加到25%时,煤样脱水脱附吸收的热量近似增大为原煤样的3倍,这主要是因为Zn1Mg2Al1-CO3-LDHs在温度低于200 ℃时,能够大量地释放出层间水分,从而吸收大量的热。也正是因为这种吸热效应,单位质量煤样在氧化和燃烧过程中的放热量也随着Zn1Mg2Al1-CO3-LDHs添加量的增大而减小,实验测定结果显示25%添加量的煤样比无添加的原煤样,每克煤少放出5 510 J的热量。
2.2.3Zn1Mg2Al1-CO3-LDHs对煤氧化气体产物的影响
根据实时采集的3D红外光谱图,将Zn1Mg2Al1-CO3-LDHs、原煤样和不同Zn1Mg2Al1-CO3-LDHs添加量下煤样产生的CO2轨迹图解出并绘制于图6中。从图中可以看出,Zn1Mg2Al1-CO3-LDHs的添加并不改变煤样氧化的规律性。CO2均是从1 200 s时开始大量产生,在2 700~2 800 s时产生量达到最大值,而且随着Zn1Mg2Al1-CO3-LDHs添加量的增加,CO2的最大瞬时产生量呈逐渐减小的趋势。煤样在3 200 s时基本上已经燃烧完毕,后面的CO2主要是Zn1Mg2Al1-CO3-LDHs热解产生。

图6 不同Zn1Mg2Al1-CO3-LDHs添加量下煤样产生的CO2轨迹Fig.6 Evolution of CO2 obtained at different additive amounts of Zn1Mg2Al1-CO3-LDHs
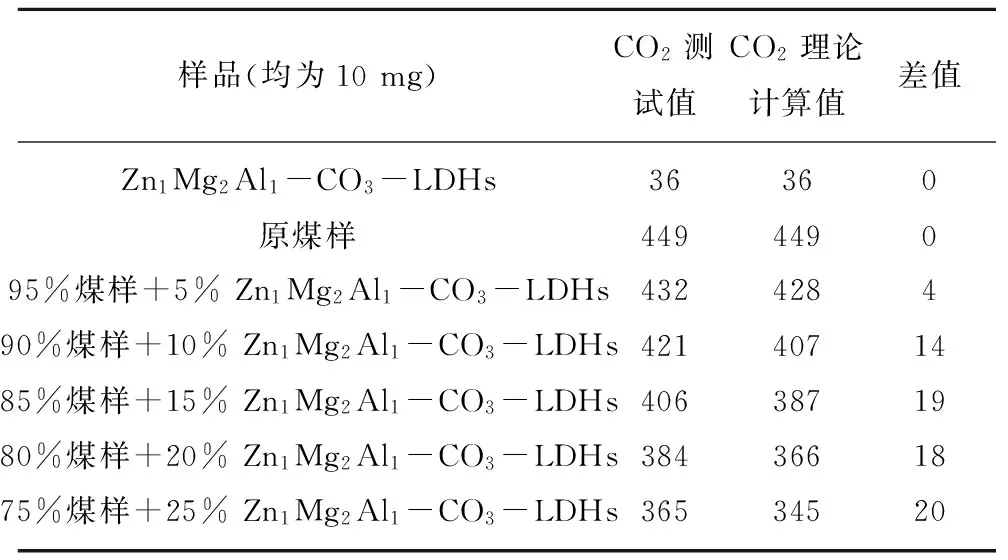
为抵消实验中因添加不同质量的Zn1Mg2Al1-CO3-LDHs而导致的煤样质量差异所带来的影响,采用式(1)对煤样和Zn1Mg2Al1-CO3-LDHs组成的混合样品产生的CO2量进行理论计算,并将理论计算值与直接对图6积分所得到的测试值进行对比分析。其结果见表4(注:表4的数字并不直接代表CO2的产生量,但却能代表真实CO2产生量的相对大小)。
式中,V为混合样品产生的某种气体的理论计算值;M为混合样品总质量;φ1和φ2分别为煤样和Zn1Mg2Al1-CO3-LDHs在混合样品中所占的质量比;N1和N2分别为单位质量煤样和单位质量Zn1Mg2Al1-CO3-LDHs所产生的气体含量值。
表4Zn1Mg2Al1-CO3-LDHs和不同Zn1Mg2Al1-CO3-LDHs添加比例下煤样产生CO2特性
Table4CO2characteristicsofZn1Mg2Al1-CO3-LDHsandcoalsampleswithdifferentadditiveamountsofZn1Mg2Al1-CO3-LDHs
样品(均为10mg)CO2测试值CO2理论计算值差值Zn1Mg2Al1-CO3-LDHs36360原煤样449449095%煤样+5%Zn1Mg2Al1-CO3-LDHs432428490%煤样+10%Zn1Mg2Al1-CO3-LDHs4214071485%煤样+15%Zn1Mg2Al1-CO3-LDHs4063871980%煤样+20%Zn1Mg2Al1-CO3-LDHs3843661875%煤样+25%Zn1Mg2Al1-CO3-LDHs36534520
由表4中CO2测试值可以看出,煤样热解产生的CO2是同样质量Zn1Mg2Al1-CO3-LDHs的12.5倍。从表面上看,随着Zn1Mg2Al1-CO3-LDHs添加比例的增大,煤样总体产生的CO2量逐渐减小。但考虑到含Zn1Mg2Al1-CO3-LDHs比例越多的煤样,其混合实验样品中煤样的含量也相对较少,直接比较CO2产生量并不科学。因此,本文以Zn1Mg2Al1-CO3-LDHs和原煤样为基准,采用线性比例叠加的方式对CO2产生量进行理论计算,再与实验测得的CO2产生量进行比较,如果二者接近,就说明Zn1Mg2Al1-CO3-LDHs的添加对CO2产生量基本上无影响。由表4可以看出理论计算的CO2值要略小于实验测得的CO2值,并且随着Zn1Mg2Al1-CO3-LDHs添加量的增大,二者的差值也变大,但当添加量达到15%时,差值基本上保持不变。这说明,Zn1Mg2Al1-CO3-LDHs的添加对煤样产生CO2有略微的促进作用。
图7为不同Zn1Mg2Al1-CO3-LDHs添加量下煤样产生的CO轨迹(波数2 175 cm-1)。图中曲线进一步证明Zn1Mg2Al1-CO3-LDHs的添加并不改变煤样氧化的规律性。CO几乎都是从1 200 s时开始大量产生,在2 700~2 800 s时产生量达到最大值,基本上在3 200 s时燃烧完毕。但是,随着Zn1Mg2Al1-CO3-LDHs添加量的增加,CO的最大瞬时产生量呈逐渐减小的趋势。

图7 不同Zn1Mg2Al1-CO3-LDHs添加量下煤样产生的CO轨迹Fig.7 Evolution of CO obtained at different additive amounts of Zn1Mg2Al1-CO3-LDHs
采用式(1)并结合图7,对不同Zn1Mg2Al1-CO3-LDHs含量下混合样品的CO理论值和测试值进行计算,结果见表5。表5表明,理论计算的CO值要略大于实验测得的CO值,并且大体上随着Zn1Mg2Al1-CO3-LDHs添加量的增大,二者的差值也变大。这表明,Zn1Mg2Al1-CO3-LDHs的添加对煤样产生CO有略微的抑制作用,可能有助于将部分CO转换成CO2,这也可能是CO2产生量随着Zn1Mg2Al1-CO3-LDHs添加比例的增加而增加的原因之一。
2.3 Zn1Mg2Al1-CO3-LDHs阻化率分析
阻化率是检验阻化剂阻化效果的常用方法之一,对煤体的阻化效果检验常采用CO指标气体法,其计算公式如下:
表5Zn1Mg2Al1-CO3-LDHs和不同Zn1Mg2Al1-CO3-LDHs添加比例下煤样产生CO特性
Table5COcharacteristicsofZn1Mg2Al1-CO3-LDHsandcoalsampleswithdifferentadditiveamountsofZn1Mg2Al1-CO3-LDHs

样品(均为10mg)CO测试值CO理论计算值差值Zn1Mg2Al1-CO3-LDHs000原煤样26.126.1095%煤样+5%Zn1Mg2Al1-CO3-LDHs24.524.8-0.390%煤样+10%Zn1Mg2Al1-CO3-LDHs23.323.5-0.285%煤样+15%Zn1Mg2Al1-CO3-LDHs20.622.2-1.680%煤样+20%Zn1Mg2Al1-CO3-LDHs17.920.9-3.075%煤样+25%Zn1Mg2Al1-CO3-LDHs15.919.6-3.7
式中,ρ表示阻化剂对煤样的阻化率;C是未添加阻化剂的原始煤样CO产生量;C′是添加阻化剂后煤样的CO产生量。
根据式(2),结合不同Zn1Mg2Al1-CO3-LDHs添加量下煤样放出的CO测试值,可得出阻化率随Zn1Mg2Al1-CO3-LDHs添加量的变化曲线,如图8所示,随着Zn1Mg2Al1-CO3-LDHs添加量的增大,其阻化效果越来越好,阻化率近似呈线性增长,拟合曲线表明,每添加1%的Zn1Mg2Al1-CO3-LDHs,阻化率可以提高1.6%,当添加量为25%时,阻化率已经达到近40%。表明,该阻化剂在煤自燃过程中,除了具有较大的热惯性,能够吸收热量外,还具有一定的阻化效果。
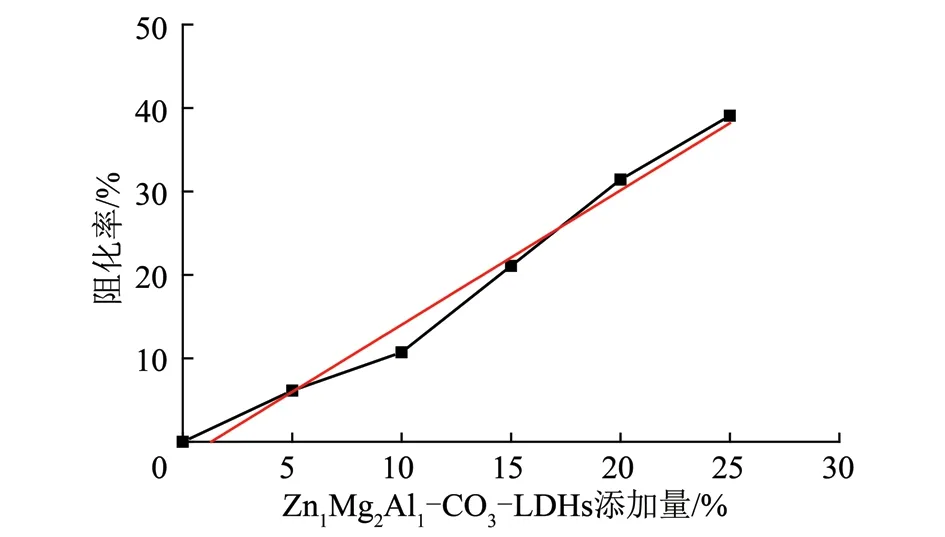
图8 阻化率随Zn1Mg2Al1-CO3-LDHs添加量的变化曲线Fig.8 Inhibition rate as a function of the additive amount of Zn1Mg2Al1-CO3-LDHs
3 结 论
(1)随着Zn1Mg2Al1-CO3-LDHs添加量的增加,煤样脱水脱附最大速率点和缓慢氧化温度均向高温区偏移,数值呈线性增加,但对热解温度、燃点、最大失重速率温度和燃尽温度等的影响不大。
(2)Zn1Mg2Al1-CO3-LDHs能够有效吸收煤自燃放出的热量,从而推迟煤自燃的发生。Zn1Mg2Al1-CO3-LDHs能够将煤样的起始放热温度推迟30~60 ℃,当添加量达到25%时,煤自燃脱水脱附阶段所吸收的热量是原煤样的3倍,每克煤样在氧化燃烧过程中的放热量减少5 510 J,最大释热功率也由无添加时的32.96降低到23.5 mW/mg。
(3)除了热效应,Zn1Mg2Al1-CO3-LDHs能够在一定程度上抑制煤自燃过程中CO的产生,其对煤自燃阻化率随添加量的增大呈线性增加,每添加1%的Zn1Mg2Al1-CO3-LDHs,阻化率提高1.6%。
[1] 曾凡桂,谢克昌.煤结构化学的理论体系与方法论[J].煤炭学报,2004,29(4):443-447.
ZENG Fangui,XIE Kechang.Theoretical system and methodology of coal structural chemistry[J].Journal of China Coal Society,2004,29(4):443-447.
[2] 许满贵,徐精彩,文虎,等.煤矿内因火灾防治技术研究现状[J].西安科技学院学报,2001,21(1):4-7.
XU Mangui,XU Jingcai,WEN Hu,et al.Current research status of mechanism and extinguishing methods of spontaneous combustion of coal mine[J].Journal of Xi’an University of Science & Technology,2001,21(1):4-7.
[3] 秦波涛,王德明,陈建华,等.高性能防灭火三相泡沫的实验研究[J].中国矿业大学学报,2005,34(1):11-15.
QIN Botao,WANG Deming,CHEN Jianhua,et al.Experimental investigation of high-performance three-phase foam for mine fire control[J].Journal of China University of Mining & Technology,2005,34(1):11-15.
[4] 彭本信.应用热分析技术研究煤的氧化自燃过程[J].煤炭工程师,1992,(2):1-10.
PENG Benxin.Application of thermal analysis technology to study process of coal spontaneous combustion[J].Coal Engineer,1992,(2):1-10.
[5] 郑兰芳.抑制煤氧化自燃的盐类阻化剂性能分析[J].煤炭科学技术,2010,38(5):70-73.
ZHENG Lanfang.Test and analysis on salty retardants performance to restrain coal oxidized spontaneous combustion[J].Coal Science and Technology,2010,38(5):70-73.
[6] 马砺,任立峰,艾绍武,等.氯盐阻化剂对煤自燃极限参数影响的实验研究[J].安全与环境学报,2015,15(4):83-85.
MA Li,REN Lifeng,AI Shaowu,et al.Experimental study on the impact of the chloride inhibitor upon the limited parameters of the coal spontaneous combustion[J].Journal of Safety and Environment,2015,15(4):83-85.
[7] 吴兵,娄鹏,王超,等.阻化剂防治煤自燃效果分析[J].煤矿安全,2014,40(6):117-118.
WU Bing,LOU Peng,WANG Chao,et al.Analysis of coal spontaneous combustion control by inhibitor[J].Safety in Coal Mines,2014,40(6):117-118.
[8] 周西华,李诚玉,李昂,等.以着火活化能变化为指标的优选煤自燃阻化剂研究[J].中国安全科学学报,2014,24(6):20-25.
ZHOU Xihua,LI Chengyu,LI Ang,et al.Study on inhibitors of coal spontaneous combustion based on activation energy of ignition[J].China Safety Science Journal,2014,24(6):20-25.
[9] 霍中刚,高玉峰,刘继文.凝胶-汽雾阻化防火技术在易燃分层复采工作面的应用[J].煤矿安全,2000,31(7):17-19.
HUO Zhonggang,GAO Yufeng,LIU Jiwen.Application of gel-aerial fog technology to prevent fire in the flammable and hierarchical mining working face[J].Safety in Coal Mines,2000,31(7):17-19.
[10] 李金亮,陆伟,徐俊.化学阻化剂防治煤自燃及其阻化机理分析[J].煤炭科学技术,2012,40(1):50-53.
LI Jinliang,LU Wei,XU Jun.Coal spontaneous combustion prevention and cure with chemical retarder as well as analysis on retarding mechanism[J].Coal Science and Technology,2012,40(1):50-53.
[11] 孙金陆,甄卫军,李进.LDHs材料的结构、性质及其应用研究进展[J].化工进展,2013,32(3):610-615.
SUN Jinlu,ZHEN Weijun,LI Jin.Structure,properties and applications of LDHs[J].Chemical Industry and Engineering Progress,2013,32(3):610-615.
[12] 刘博,贾雪梅,周安宁,等.锌镁铝类水滑石/煤复合材料协同阻燃乙烯-醋酸乙烯酯共聚物[J].高分子材料科学与工程,2014,30(11):145-150.
LIU Bo,JIA Xuemei,ZHOU Anning,et al.ZnMgAl hydrotalcite/coal composites synergistically flame-retardanted ethylene vinyl acetate[J].Polymer Materials Science and Engineering,2014,30(11):145-150.
[13] 覃耀慰,冷明哲,张良基,等.类水滑石基催化材料的研究进展[J].材料导报,2013,27(21):44-48.
QIN Yaowei,LENG Mingzhe,ZHANG Liangji,et al.Research progress of the catalytic materials based on hydrotalcite-like compounds[J].Materials Review,2013,27(21):44-48.
[14] 杨志斌,马莹,戴新,等.基于热重分析法的烟煤掺烧褐煤特性燃烧[J].电力科学与工程,2015,31(3):1-5.
YANG Zhibin,MA Ying,DAI Xin,et al.Combustion characteristics of bituminous coal blended with lignite using thermo-gravimetric method[J].Electric Power Science and Engineering,2015,31(3):1-5.
[15] 陈玲红,陈祥,吴建,等.基于热重-红外-质谱联用技术定量分析燃煤气体产物[J].浙江大学学报(工学版),2016,50(5):961-969.
CHEN Linghong,CHEN Xiang,WU Jian,et al.Quantitative analysis of gaseous products evolved by coal combustion using TG-FTIR-MS technique[J].Journal of Zhejiang University:Engineering Science,2016,50(5):961-969.
[16] 姜鹏,侯万国,韩书华,等.Zn-Mg-Al 型类水滑石纳米颗粒制备及晶体结构[J].高等学校化学学报,2002,23(1):78-82.
JIANG Peng,HOU Wanguo,HAN Shuhua,et al.Studies on preparation and crystal structure of ultrafine particles Zn-Mg-Al-Hydrotalcite like compound[J].Chemical Journal of Chinese Universities,2002,23(1):78-82.
[17] 张辛亥,丁峰,张玉涛,等.LDHs 复合阻化剂对煤阻化性能的试验研究[J].煤炭科学技术,2017,45(1):84-88.
ZHANG Xinhai,DING Feng,ZHANG Yutao,et al.Experimental study on LDHs composite inhibitor to coal resistance property[J].Coal Science and Technology,2017,45(1):84-88.
InhibitingeffectsofZn/Mg/Allayerdoublehydroxideoncoalspontaneouscombustion
ZHANG Yutao,SHI Xueqiang,LI Yaqing,WEN Hu,HUANG Yao,LI Shanshan,LIU Yurui
(CollegeofSafetyScienceandEngineering,Xi’anUniversityofScienceandTechnology,Xi’an710054,China)
Coal spontaneous combustion is a serious threat for the production of coal mines.Application of inhibitors is one of widely used method to prevent coal spontaneous combustion.TG/DSC synchronous analyzer coupling with Fourier infrared spectrometer (FTIR) was employed to investigate the inhibiting effects of Zn1Mg2Al1-CO3-LDHs on coal spontaneous combustion.Inhibiting effects were evaluated from standpoints of quality,characteristics temperatures,thermal characteristics,and gases products during the process of coal spon-taneous combustion.Experimental results show that the endothermic effect resulted from pyrogenic decomposition of Zn1Mg2Al1-CO3-LDHs was the main reason that Zn1Mg2Al1-CO3-LDHs inhibited coal spontaneous combustion.The temperature corresponding to the maximum rate of dehydration and desorption,slow oxidation temperature,and temperature started to release heat could be increased by Zn1Mg2Al1-CO3-LDHs.Nevertheless,Zn1Mg2Al1-CO3-LDHs can reduce the maximum heat release power of coal samples.Meanwhile,it can slightly promote the production of CO2during the oxidation process.All of these results indicate that Zn1Mg2Al1-CO3-LDHs exhibited great inhibiting effects on coal spontaneous combustion.
coal spontaneous combustion;inhibitor;Zn/Mg/Al layer double hydroxide;TG-DSC-FTIR coupling technology;oxidation process
张玉涛,史学强,李亚清,等.锌镁铝层状双氢氧化物对煤自燃的阻化特性[J].煤炭学报,2017,42(11):2892-2899.
10.13225/j.cnki.jccs.2017.0855
ZHANG Yutao,SHI Xueqiang,LI Yaqing,et al.Inhibiting effects of Zn/Mg/Al layer double hydroxide on coal spontaneous combustion[J].Journal of China Coal Society,2017,42(11):2892-2899.doi:10.13225/j.cnki.jccs.2017.0855
TD753
A
0253-9993(2017)11-2892-08
2017-06-22
2017-09-15责任编辑常明然
国家自然科学基金资助项目(51404192,51604218,51774233)
张玉涛(1982—),男,山东烟台人,副教授,硕士生导师,博士。Tel:029-85587436,E-mail:ytzhang@xust.edu.cn。
李亚清(1983—),女,陕西咸阳人,讲师。Tel:029-85583789,E-mail:lyqcumt@126.com
