喹喏酮类化合物的结构修饰及其抑菌活性研究
2017-12-19蔡东霖王宇光
李 钦,蔡东霖,赵 萃,王宇光
(浙江工业大学生物工程学院,浙江 杭州 310014)
喹喏酮类化合物的结构修饰及其抑菌活性研究
李 钦,蔡东霖,赵 萃,王宇光
(浙江工业大学生物工程学院,浙江 杭州 310014)
论文以2,3,4,5-四氟苯甲酰氯为原料,在三乙胺的催化下与N,N-二甲氨基丙烯酸乙酯缩合,再分别与苄胺、苯胺、对氯苯胺、异丙胺置换、环合,构建了喹诺酮类化合物骨架,并对这一骨架进行了结构修饰,得到了一系列喹诺酮类衍生物。对这些化合物进行了抑菌活性的研究,结果表明,化合物3~8都有较好的抑菌活性,其中,化合物6 a、6 b、6 d、7、8有较强的抑菌活性。
喹诺酮类化合物;合成;衍生化;抑菌圈;生物活性
喹诺酮类化合物具有非常广泛的生物活性,是一种潜在的生物活性结构。众所周知,喹诺酮类药物是20世纪70年代崛起的新药,这类药物有优异的抗感染作用,杀菌谱较广,毒副作用较小,能明显降低危重感染病死率,已成为近10年来发展最为迅速的一类化学合成抗菌药[1-3]。此外,有些喹诺酮类化合物还是良好的抗脑缺血剂[4]。但是随着它们的广泛应用甚至滥用,使其耐药菌迅速增加,迫切需要寻找到抗菌活性更强,尤其对各种耐药菌活性更强的新喹诺酮类抗菌药。所以对喹诺酮类化合物进行进一步的结构修饰,以便获得活性更强,活性谱更广的新喹诺酮类抗菌药,仍是抗感染化疗领域近几年的热点领域之一。作为一类全合成药物,喹诺酮类结构中可供修饰的位点较多,其化学性质稳定,易于合成。结构修饰不仅是寻找抗菌活性更强的新喹诺酮的重要途径,也成为拓展其生物活性的有效手段之一。
1 喹诺酮类化合物的合成
1.1 原料3的制备
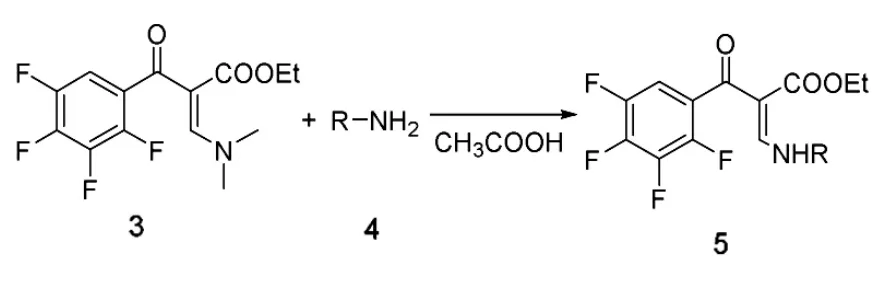
将N,N-二甲氨基丙烯酸乙酯2、三乙胺加入反应瓶中,溶剂为甲苯,50℃加热反应,缓慢滴加2,3,4,5-四氟苯甲酰氯 1 的甲苯溶液,1 h 滴毕,升温至110℃,保温搅拌反应2 h后,冷却至室温后得化合物3。投料比2,3,4,5-四氟苯甲酰氯:N,N-二甲氨基丙烯酸乙酯∶三乙胺=1∶1∶1.2。 反应3 h,反应过程中用TLC(薄层色谱)监测反应进程。
1.2 胺取代
用乙酸溶解化合物3,滴加胺4,室温搅拌反应 0.5 h,投料比化合物 3∶胺∶乙酸=1∶1∶1.1。反应过程中用TLC(薄层色谱)监测反应进程,反应完全后,加入蒸馏水,转移至分液漏斗,分去水层后,再用蒸馏水洗涤1次,水层用甲苯萃取,合并有机层,用旋转蒸发仪蒸发除去甲苯,抽滤出固体,干燥得黄色固体5,计算收率。
1.3 环合

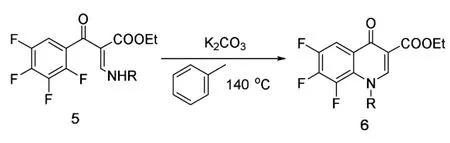
化合物5的甲苯溶液,加入碳酸钾,在反应瓶中于140℃下共沸除水(用分水器)投料比为化合物 5∶碳酸钾=1∶0.6,反应过程中用 TLC(薄层色谱)监测反应进程,7 h反应完毕,冷却,减压蒸除甲苯,有黄色固体析出,抽滤,用水洗涤3次,石油醚洗涤3次,干燥,得浅黄色固体6,计算收率。
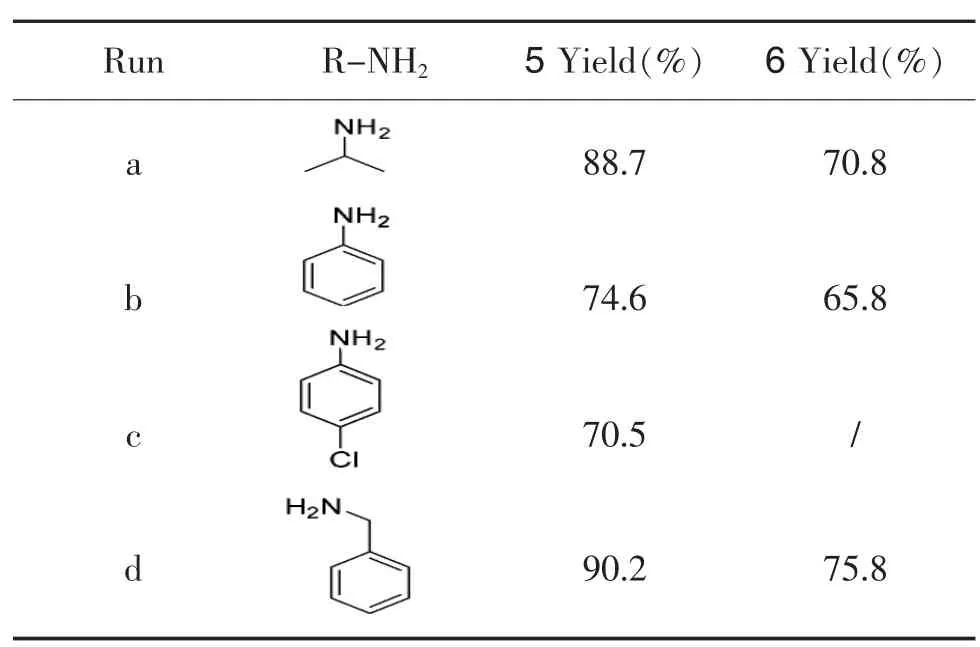
Run R-NH2 5 Yield(%) 6 Yield(%)a 88.7 70.8 b 74.6 65.8 c 70.5 /d90.2 75.8
1.4 衍生化

1.4.1 化合物6d水解
化合物6d在6 mol/L的HCl水溶液中加热回流反应,以TLC跟踪,2 h反应完毕。冷却至室温,用20%氢氧化钠调至中性,冷却过滤,滤饼用水洗,干燥后得白色固体7,产率71.4%。
1.4.2 制备化合物8
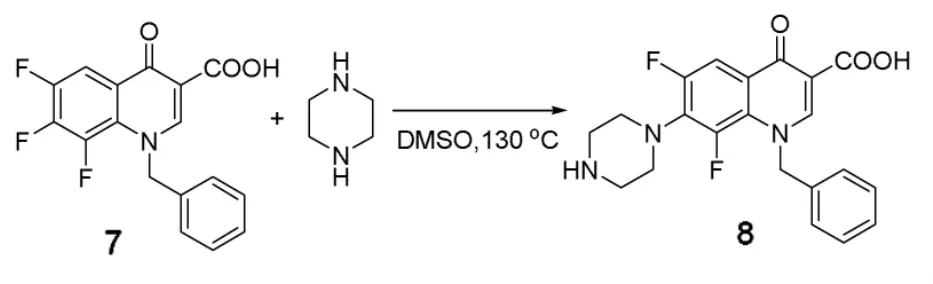
将DMSO(作为溶剂)、化合物7、哌嗪依次加入反应瓶中,130℃加热反应6 h,投料比为化合物7∶哌嗪=1∶3,减压蒸馏回收DMSO和过量的哌嗪,粗产品用95%乙醇重结晶,得到棕色固体8。
2 喹诺酮类抗菌活性研究
2.1 试剂与仪器
材料:(1)培养基:牛肉膏蛋白胨培养基,半固体牛肉膏蛋白胨培养基。(2)菌种:大肠杆菌。(3)样品药敏纸片:样品药物纸片(用滤纸自制直径1 cm),DMSO溶液对照纸片(用滤纸自制直径1 cm)。
仪器:(1)高压灭菌锅 MLS-3020;(2)隔水式电热培养箱 GNP-9270;(3)电子天平 FA1104。
2.2 实验方法(纸片法)
(1)取大肠杆菌于牛肉膏蛋白胨培养基中培养24 h后,将菌液分别均匀涂布于琼脂平皿上。(2)用无菌镊子分别取含有样品纸片,均匀放置在上述琼脂平板中央,使其密切接触。(3)用无菌镊子取含有DMSO溶液样品纸片,均匀放置在上述琼脂平板上,使其密切接触,作为对照。(4)置37℃培养24 h,观察纸片周围抑菌圈,测量抑菌圈直径并记录。
2.3 结果与讨论
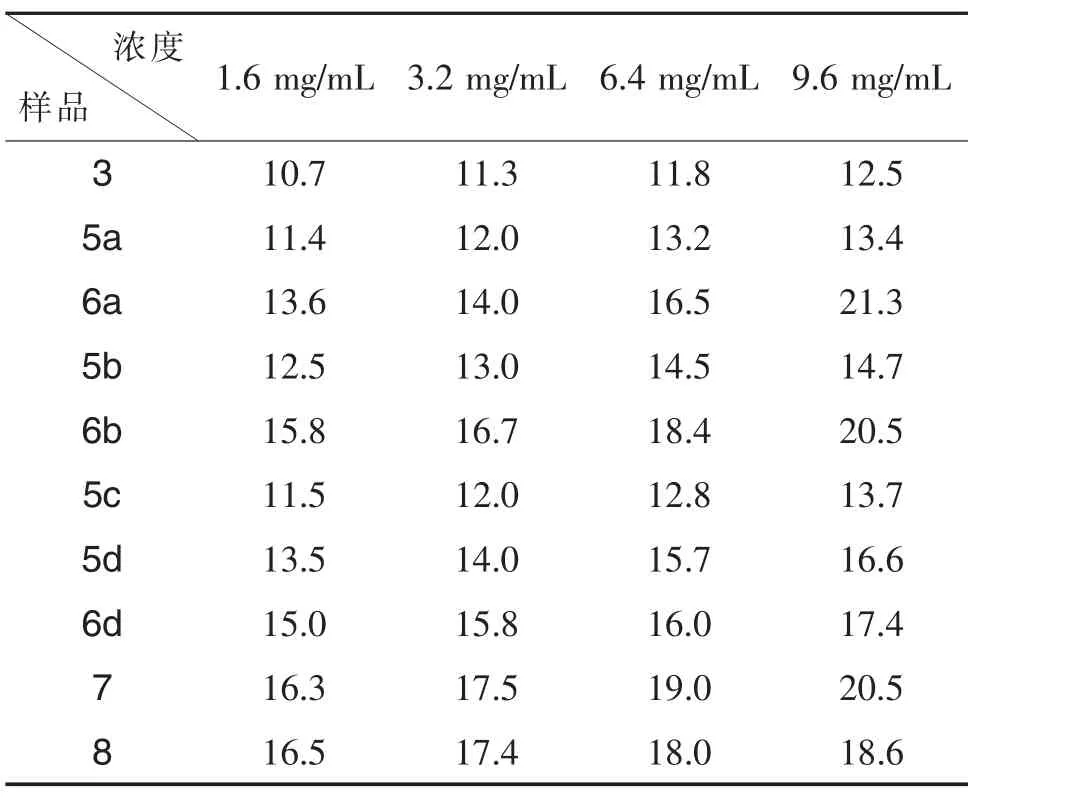
化合物3~8对大肠杆菌抑菌圈的测定
根据大肠杆菌对化合物敏感度测定(抑菌圈的测定),除原料3对大肠杆菌抑制效果稍低外,其余化合物均对大肠杆菌有一定的抑制效果,其中,化合物 6a、6b、6d、7、8 有较强的抑菌活性,且浓度越大抗菌活性越强。
[1] Mphahlele M J.Synthesis of 2-arylquinolin-4 (1h)-ones and their transformation to N-alkylated and O-alkylated derivatives[J].J.Heter.Chem., 2010,47: 1-14.
[2] Skyrianou K C, Perdih F, Turel I, et.al.Nickelquinolones interaction.Part 2-Interaction of nickel (II)with the antibacterial drug oxolinic acid[J].J.Inorg.Biochem., 2010, 104:161-170.
[3]Miyauchi R,Kawakami K,Ito M,et al.Design,synthesis and biological evaluations of novel 7-[3-(1-aminocycloalkyl) pyrrolidin-1-yl]-6-desfluoro-8-methoxyquinolones with potent antibacterial activity against multi-drug resistant Gram-positive bacteria[J].Bioorg.Med.Chem., 2009, 17(19):6879-6889.
[4] Park C H, Lee J,Jung H Y,et al.Identification, biological activity,and mechanism of the anti-ischemic quinolone analog[J].Bioorg.Med.Chem., 2007, 15:6517-6526.
[5] 沃尔夫森,胡珀.最新广谱喹诺酮类抗微生物药[M].姜素椿,宋克主译.北京:人民军医出版社,1991.
[6] Schellhorn C.Classification of quinoloncs by V Andriole[J].Infection,1998, 26(1):64.
[7] Aktas Z, Gönüllü N, Salcioglu M, et al.Moxifloxacin activity against clinical isolates compared with the activity of ciprofloxacin[J].International Journal of Antimicrobial A-gents, 2002, 20(3):196-200.
[8] Rolston K V,Frisbee-Hume S,Leblanc B,et al.In vitro antimicrobial activity of moxifloxacin compared to other quinolones against recent clinical bacterial isolates from hospitalized and community-based cancer patients[J].Diagn Microbiol Infect Dis, 2003, 47(2):441-449.
[9] 冯连顺,刘明亮.喹诺酮类药物的结构修饰及“非经典”生物活性研究进展[J].国际药学研究杂志,2010,37(2):139-143.
[10]Ping W,Laura E,Lawrence K L,et a1.Mechanism of action of the Des-F(6) quinolone BMS-284756 measured by supercoiling inhibition and cleavable complex assays[J].Antim.A.Chem., 2001, 45(14):3660.
[11]王文颖.氧氟沙星治疗泌尿系统感染的临床观察[J].首都医药, 2002, 9(9):64.
Study on the Structure Modification and Antibacterial Activity of Quinolone Compounds
LI Qin, CAI Dong-lin, ZHAO Cui, WANG Yu-guang
(College of Biotechology and Bioengineering ,Zhejiang University of Technology, Hangzhou,Zhejiang 310014,China)
In this paper, 2,3,4,5-Tetrafluorobenzoyl chloride was used as raw material, condensation with ethyl N,N-dimethylaminoacrylateunder the catalysis of triethylamine, then with benzylamine, aniline p-chloroaniline and isopropylaminereplacement,cyclization,the skeleton of quinolones was constructed, and the skeleton structure was modified,a series of quinolones derivatives were obtained.The antibacterial activity of these compounds was studied, The results showthat, compound 3~8 has good antibacterial activity, among them,compounds 6a,6b,6d,7 and 8 have strong antibacterial activity.
quinolones;synthesis;derivatization;bacteriostatic circle;biological activity
1006-4184(2017)11-0012-03
2017-04-11
李钦(1991-),男,江苏盐城人,硕士研究生在读,主要从事有机合成。E-mail:1049661006@qq.com。
