基于氨基作氢迁移桥梁天门冬酰胺的旋光异构机理及水的作用
2017-12-14崔凤午王佐成喻小继闫红彦
崔凤午,王佐成,喻小继,高 峰,闫红彦,佟 华
(1. 白城师范学院 数学学院,白城 137000;2. 白城师范学院 物理学院,白城 137000;3. 长春师范大学 外语学院,长春 131000;4. 白城师范学院 计算机科学学院,白城 137000)
基于氨基作氢迁移桥梁天门冬酰胺的旋光异构机理及水的作用
崔凤午1,王佐成2,喻小继3,高 峰2,闫红彦4,佟 华2
(1. 白城师范学院 数学学院,白城 137000;2. 白城师范学院 物理学院,白城 137000;3. 长春师范大学 外语学院,长春 131000;4. 白城师范学院 计算机科学学院,白城 137000)
采用密度泛函理论的B3LYP方法、微扰论的MP2方法和自洽反应场(SCRF)理论的smd模型方法,研究了天门冬酰胺分子2个稳定构型的旋光异构裸反应机理、水分子的催化作用及水溶剂化效应.反应通道研究发现: 构型1有2条通道a和b,a通道的第一基元反应质子迁移与羧基异构同时进行,是协同机理;b通道羧基先异构而后质子迁移,是分步机理.构型2有1条通道,是质子先以氨基氮为桥从手性碳的一侧迁移到另一侧,然后羧基和氨基再异构.势能面计算表明: 构型1的主反应通道是b,决速步自由能垒为252.7kJ·mol-1;构型2的决速步自由能垒为254.0kJ·mol-1,均来自于质子从手性碳向氨基氮迁移的过渡态.2个水分子作质子迁移媒介时,构型1主反应通道b的决速步能垒降到124.1kJ·mol-1,再考虑到水溶剂化效应时,决速步能垒降到104.0kJ·mol-1.结果表明: 水分子的催化和水溶剂助催化的共同作用,使质子迁移反应能垒大幅度降低.
旋光异构; 天门冬酰胺; 密度泛函理论; 过渡态; 微扰论; 自洽反应场
天门冬酰胺(Asparagine,简称为Asn),根据其构象和旋光性的不同分为左旋体(S-Asn)和右旋体(R-Asn).它虽然是非必需氨基酸,但却有着及其重要的作用.S-Asn可用于饮料的添加剂,其有助于大脑的发育,能解除高谷氨酰胺抑制引发的细胞凋亡,从而实现对肿瘤的治疗[1-2].S-Asn对蛋白质的结构与功能至关重要[3-4],也是动物细胞和微生物培养的添加剂[5].R-Asn主要用于药理研究和药物合成,还可用于治疗支气管炎,用于制备催产素[6].
由于Asn具有重要作用,人们对它进行了广泛的研究.马江权等人[7]通过马来酸酐氨解反应合成了外消旋Asn,并得到了最佳原料配比、反应温度、反应时间和催化剂用量.杨静琦等人[8]对S-Asn及其一水合物的太赫兹光谱进行了研究,研究表明,它及其一水合物的太赫兹光谱特征存在显著的差异.张璆[9]研究了高温和水热等不同因素对丙烯酰胺和类黑精生成量的影响,结果表明,高温短时间热处理利于丙烯酰胺的生成,长时间高温热处理利于类黑精的形成.王辉宪等人[10]研究了天门冬酰胺和天冬氨酸的热解机理,结果表明,Asn先失去一个NH3分子,后者先失去一个CO2分子.马士华等人[11]用太赫兹时域光谱技术研究了室温条件下多晶Asn样品的光谱,研究表明,Asn在实验测量有效光谱范围(0.5~2.4THz)内有两个吸收峰.
S-Asn和R-Asn具有不同的作用,S-Asn可以直接从其含量高的天然材料中分离,目前利用不对称合成法获得R-Asn成本很高,因此利用S-Asn旋光异构获得R-Asn变得十分重要,但目前关于Asn旋光异构具有重要意义的研究却鲜见报道.
已有研究[12-15]表明,手性C上的质子以氨基N为桥梁迁移,是赖氨酸、丙氨酸、半胱氨酸和缬氨酸等手性氨基酸分子实现旋光异构的主反应通道,水分子对其H迁移反应具有较好的催化作用.基于此,并考虑到大气环境含有大量的水分子以及生命体是富水环境,本工作系统地研究了2个最稳定构象的S-Asn分子基于为氨基N质子迁移桥梁,Asn分子旋光异构的裸反应机理和水分子的催化作用,考虑到S-Asn在生命体内是处在富水环境下,又考察了质子迁移过程的水溶剂效应.
1 研究与计算方法
采用密度泛函理论的B3LYP[16-17]方法,为较好地处理分子内氢键的作用,结合6-311++G(d, p)基组,优化S型Asn旋光异构过程中的各个驻点,计算吉布斯自由能热校正.通过对过渡态[18-19]虚频振动模式的分析和内禀反应坐标(IRC)[20-21]计算,确认过渡态.为获得高水平的势能面,采用微扰理论的MP2方法[22-23],选用6-311++G(3df, 2pd)基组,计算体系的单点能,利用Gtotal=ESP+Gtc(Gtotal为总自由能,ESP单点能,Gtc为吉布斯自由能热校正)计算总自由能.水溶剂效应采用自洽反应场(SCRF)理论的smd模型方法[24]计算.b通道的第一个S型中间体INT1与1个水分子的氢键络合物b_S-INT1·2H2O在水溶剂环境下记作b_S-INT1·2H2O@water,水环境下其他分子的表示法相似.文中计算均由Gaussian09[25]程序包完成.
2 结果与讨论
2.1 S-Asn向R-Asn旋光异构的裸反应机理
优化的S-Asn_1、S-Asn_2和它们的手性对映体结构如图1.结构分析表明: S-Asn_1具有氨基和羧基之间的分子内较强的单氢键,S-Asn_2具有氨基和羧基之间的分子内双氢键,它们十分稳定.高水平的计算表明,S-Asn_1比S-Asn_2略稳定些.

图1 天门冬酰胺分子的两对稳定的旋光异构对映体Fig.1 Two stable optical isomerism enantiomers of Asparagine molecules
对图1研究发现,质子以氨基N为桥迁移时,S-Asn_1的旋光异构反应可能存在2条通道a和b,分别是质子先迁移和羧基异构而后再质子迁移.构型2有1条通道,是质子以氨基氮为桥从手性碳的一侧迁移到另一侧.下面分别进行讨论.
S-Asn_1在a通道的旋光异构反应历程是协同机理,见图2(a),反应势能面见图3(见第512页).
首先,S-Asn_1经手性碳2C上的8H向氨基氮13N迁移同时羧基的7H绕1C-5O键轴旋转的协同过渡态a_TS1_1,异构成中间体a_INT1_1,同时实现了氨基质子化和羧基从反式平面结构向顺式平面结构的异构.在S-Asn_1到a_TS1_1过程中,2C-8H键长从0.10972nm增加到0.13890nm,键断裂;2C-13N键长从0.14695nm增加到0.15645nm,键断裂;7H绕1C-5O旋转,二面角7H-5O-1C-6O从177.90°变为-163.23°.两个化学键断裂与羟基旋转的协同过程需要较高的能量,a_TS1_1产生的能垒为300.8kJ·mol-1.接着,中间体a_INT1_1做为反应物,经过渡态a_TS2_1,实现12H在纸面里从氨基氮13N向手性碳2C的迁移,异构成中间体a_R-INT2_1,实现旋光异构.从a_INT1_1到a_TS2_1过程,13N-12H从键长从0.10254nm增加到0.11865nm,键断裂;13N-2C从键长从0.14884nm增加到0.15756nm,键断裂.a_TS2_1只是质子迁移,所以其能量是255.7kJ·mol-1;此过程键的拉伸幅度小于第一基元反应,没有键的旋转,同时中间体反应物a_INT1_1不稳定,具有较高的能量.因此,此基元反应能垒低于第一基元反应很多,只有121.4kJ·mol-1.然后,a_R-INT2_1经过11H和8H在纸面里外翻转的过渡态a_R-TS3_1进入纸面里,异构成中间体产物a_R-INT3_1.此过程二面角8H-13N-2C-11H从118.46°变为-123.43°,无断键,所以a_R-TS3_1产生的能垒较低,只有19.9kJ·mol-1.
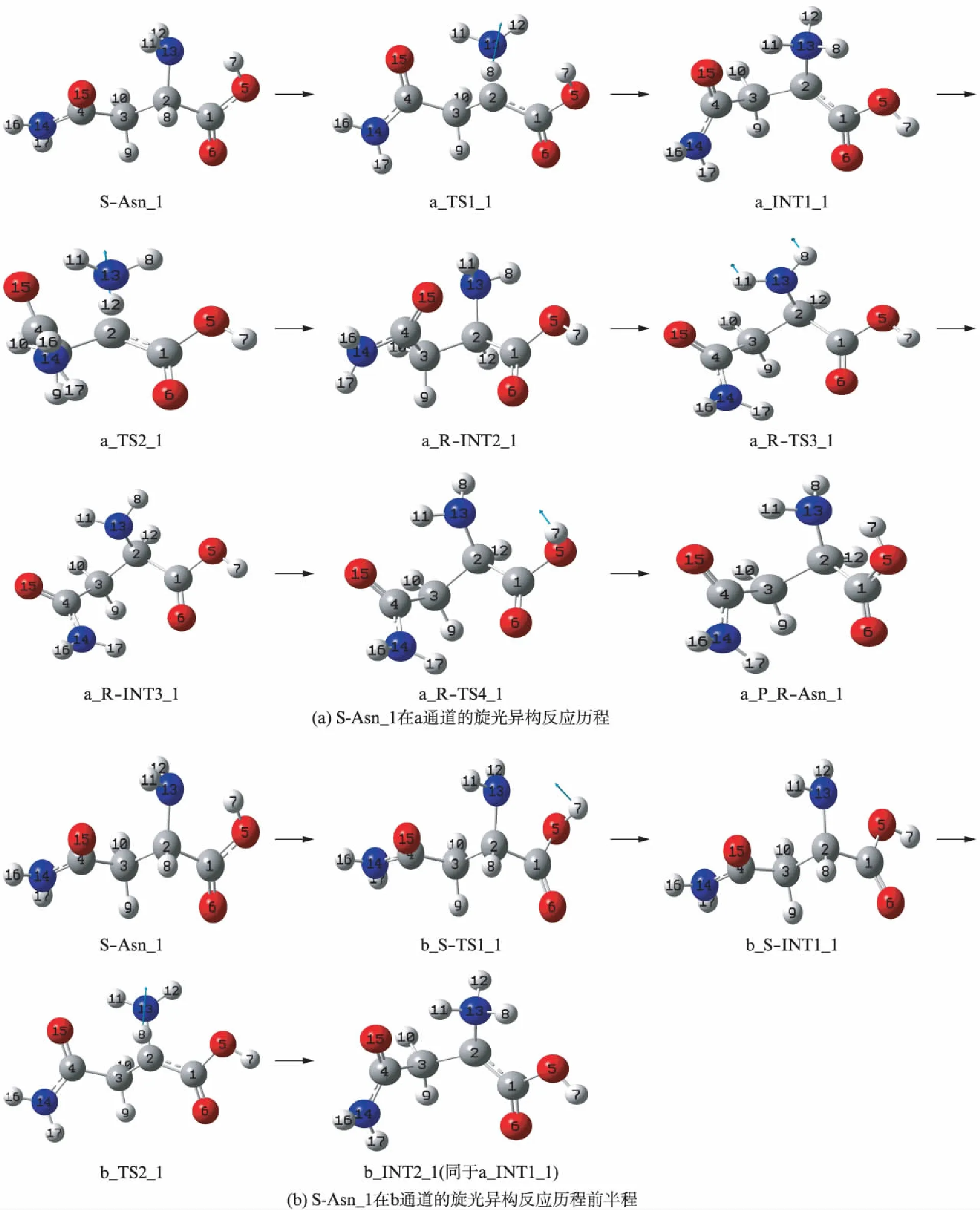
图2 S-Asn_1的旋光异构反应历程及驻点结构Fig.2 The reaction process of optical isomerism and the structure of stationary points of S-Asn_1
最后,a_R-INT3_1经过羧基异构的过渡态a_R-TS4_1,实现了羧基从顺式平面结构向反式平面结构的异构.异构成具有氨基和羧基之间的分子内较强的单氢键以及氨基和羰基氧15O之间的分子内单氢键作用的稳定产物a_P_R-Asn_1.从a_R-INT3_1到a_R-TS4_1,二面角7H-5O-1C-6O从-2.81°变为-85.88°,只是键旋转,无断键,产生的能垒较低,只有39.7kJ·mol-1.从图3可知,第3和4基元逆反应的势垒分别为9.3kJ·mol-1和57.6kJ·mol-1,常温下可以越过.因此,S-Asn_1在a通道旋光异构的产物是a_P_R-Asn_1,a_R-INT3_1以及a_R-INT2_1共存,只是a_P_R-Asn_1含量远高于后两个产物.
S-Asn_1在b通道的旋光异构反应历程是分步机理,见图2(b),反应势能面亦见图3.
首先S-Asn_1经过羧基上的7H绕1C-5O键轴旋转的过渡态b_S-TS1_1,异构成第一中间体b_S-INT1_1.二面角7H-5O-1C-6O从177.95°变为-2.20°,实现了羧基从反式平面结构向顺式平面结构的异构.此过程是羟基旋转无断键,活化能垒只有51.9kJ·mol-1.然后,b_S-INT1_1经过渡态b_TS2_1,实现8H从手性碳2C向氨基氮13N的迁移,异构成第二中间体b_INT2_1.b_S-INT1_1到b_TS2_1过程中,2C-8H键长从0.10926nm增加到0.13415nm,键断裂;2C-13N键长从0.14563nm增加到0.15576nm,键断裂.b_TS2_1两个化学键断裂,能量较高,是261.4kJ·mol-1,并产生了252.7kJ·mol-1高度的能垒.结构分析表明,b_INT2_1同于a_INT1_1,其以后的反应历程同于a_INT1_1后面的反应历程,不再赘述.

图3 S-Asn_1和S-Asn_2旋光异构反应的吉布斯自由能势能面Fig.3 Gibbs free potential energy surfaces diagram of the optical isomerism reaction of S-Asn_1 to S-Asn_2
反应势能面见图3,S-Asn_2的旋光异构反应历程见图4.首先,S-Asn_2经8H从手性碳2C向氨基氮13N迁移的过渡态TS1_2,异构成中间体INT1_2.在S-Asn_2到TS1_2过程中,2C-8H键长从0.10957nm增加到0.13286nm,键断裂;2C-13N键长从0.14635nm增加到0.15553nm,键断裂.两个化学键断裂导致TS1_2产生了258.8kJ·mol-1高度的能垒.然后,INT1_2的质子化氨基上在纸面里的11H经过渡态TS2_2在纸面里从13N迁移到2C,异构成中间体R-INT2_2,实现了旋光异构.此基元反应过程相似与第一基元反应,也是有2个键断再成键,过渡态TS2_2的能量较高,是251.8kJ·mol-1.但由于INT1_2在133.2kJ·mol-1的势垒上,导致此基元反应的能垒并不十分高,只有118.6kJ·mol-1.接着,R-INT2_2经质子7H在羧基内迁移的过渡态R-TS3_2,从羧基的6O迁移到5O,异构成中间体R-INT3_2.由于R-INT2_2到R-TS3_2过程,6O-7H键长从0.09736nm增加到0.13110nm,键长增幅不大;二面角7H-6O-1C-5O是0.30°,4元环过渡态R-TS3_2基本共面,较稳定.因此,R-TS3_2产生的能垒不是很高,只有128.4kJ·mol-1.最后,R-INT3_2经过和a_R-TS3_1相似的过渡态R-TS4_2异构成R-INT4_2,R-INT4_2 再经过和a_R-TS4_1相似的过渡态R-TS5_2,异构成具有氨基和羧基之间的分子内较强的单氢键以及氨基和羰基氧15O之间分子内单氢键作用的稳定产物a_P_R-Asn_2.从图3可知,第4和5基元逆反应的势垒分别为12.5kJ·mol-1和71.0kJ·mol-1,常温下可以越过.因此,S-Asn_2旋光异构的产物是R-INT3_2,R-INT4_2以及P_R-Asn_2共存,只是P_R-Asn_2含量远远高于前两个产物.
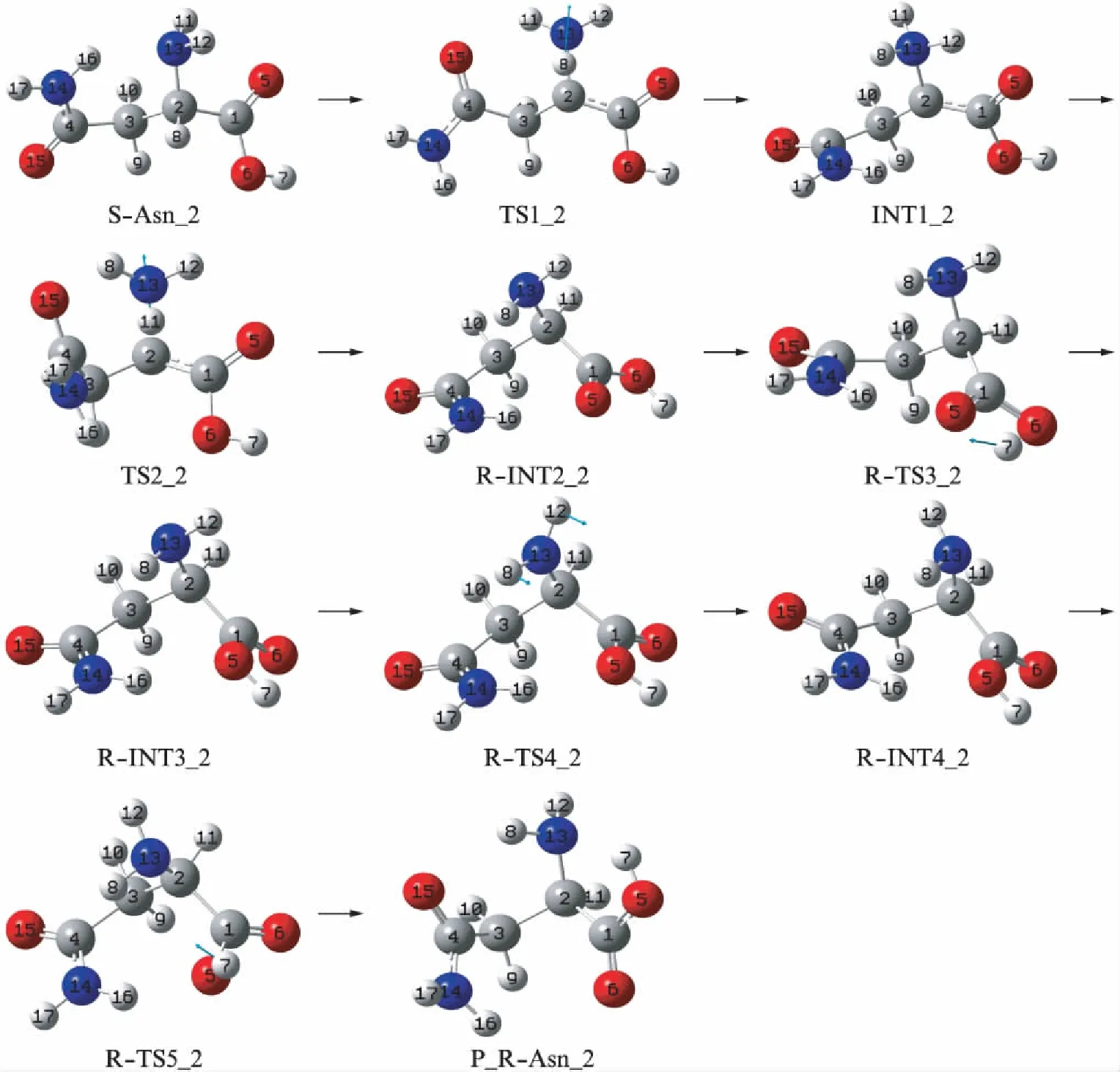
图4 S-Asn_2的旋光异构反应历程及驻点结构Fig.4 The reaction process of optical isomerism and the structure of stationary points of S-Asn_2
2.2 S-Asn旋光异构过程中水的作用
S-Asn旋光异构过程中水的作用,可分为两种情况.一是气相环境只考虑水分子的作用;二是液相环境,考虑水分子作用的同时,还要考虑水的溶剂效应.下面分别讨论:
对于气相环境下水分子的作用,篇幅所限,只讨论水分子对S-Asn_1旋光异构优势通道决速步b_S-INT1_1→b_TS2_1→b_INT2_1过程的催化作用,以获得水分子作用下S-Asn分子旋光异构的最低活化能垒.以往的研究[13-15,27]表明,3个水分子簇做H迁移桥梁,与2个水分子簇的催化作用相差不大;1个水分子做H迁移桥梁,与2个水分子簇的催化作用相比小很多,这里只讨论2个水分子簇的催化作用.
2个H2O分子催化b_S-INT1_1→b_TS2_1→b_INT2_1反应的驻点结构,见图5,势能面见图6(见第514页).
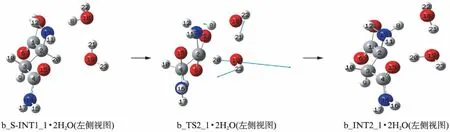
图5 2个H2O分子催化b_S-INT1_1→b_TS2_1→b_INT2_1反应过程的驻点结构Fig.5 The structure of stationary points of catalytic reaction of b_S-INT1_1→b_TS2_1→b_INT2_1 with two water molecules
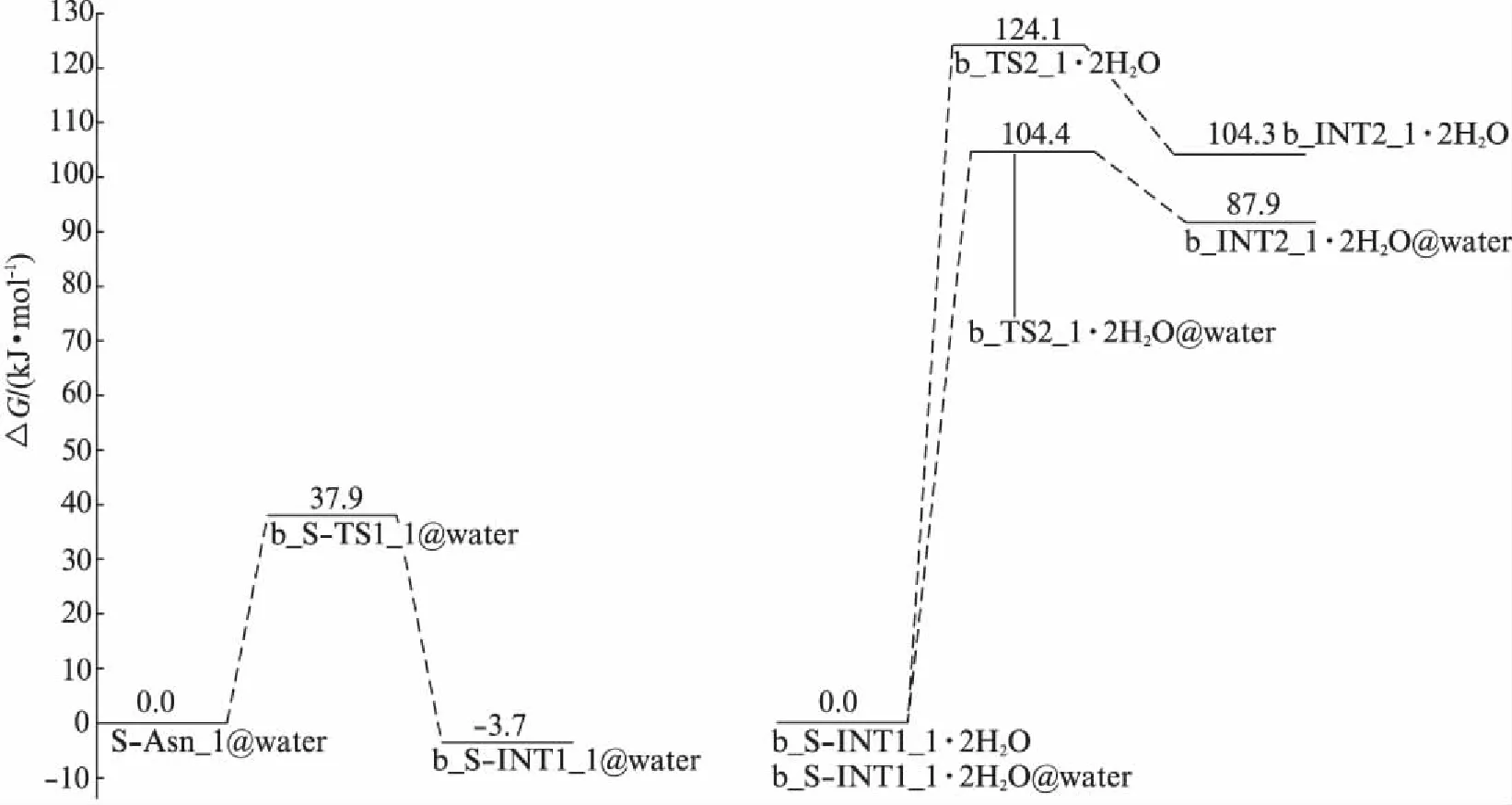
图6 水作用下S-Asn_1旋光异构优势反应通道b的主要反应过程的吉布斯自由能势能面Fig.6 Gibbs free potential energy surfaces diagram of the main reaction processes of the optical isomerism of S-Asn_1 in the dominant reaction path b with water addition
b_S-INT1_1与其20H和13N右侧的2个H2O分子通过氢键作用,形成络合分子,记作b_S-INT1_1·2H2O.经过渡态b_TS2_1·2H2O,实现了以2个H2O分子为媒介,质子从手性碳2C向氨基氮13N的转移,异构成中间体络合物b_INT2_1·2H2O.7元环过渡态b_TS2_1·2H2O的氢键角2C-20H-19O,19O-21H-18O和18O-8H-13N分别是165.54°,161.50°和162.47°,均接近180°,这些氢键较强;二面角2C-20H-19O-21H,19O-21H-18O-8H和18O-8H-13N-2C分别是7.04°,8.89°和5.40°,过渡态b_TS2_1·2H2O的7元环结构基本共面,因此,7元环过渡态较稳定.另一方面,b_S-INT1_1·2H2O与b_S-INT1_1相比较,手性碳与其上面的质子的距离从0.10926nm增加到0.11014nm,即b_S-INT1_1·2H2O的水分子把2C-20H键有效地活化.综合这两个原因,2个H2O分子的作用下,b_S-INT1_1→b_TS2_1→b_INT2_1过程的活化能不会太高,从图5可知,此基元反应的活化能是124.1kJ·mol-1.
比较图6和图3可知,2个H2O分子的作用,使b_S-INT1_1→b_TS2_1→b_INT2_1过程的活化能从裸反应的252.7kJ·mol-1降低到124.1kJ·mol-1,说明2个水分子簇对此质子迁移过程有较好的催化作用.此能垒低于常温298.15K质子迁移的“极限能垒”167.0kJ·mol-1[26],说明气相环境下的Asn分子在水蒸气存在时可以极其缓慢地实现旋光异构.
对于液相环境下水的作用,篇幅所限,只讨论水对S-Asn_1旋光异构优势通道b的主要过程(第1和2基元反应),对于第2基元反应,考虑2个H2O分子催化b_S-INT1_1→b_TS2_1→b_INT2_1反应的同时,再考虑水溶剂效应,以获得水分子的催化与水溶剂效应的共同作用对质子迁移过程的影响.富水环境下第一基元反应历程及驻点结构基本同于裸反应,参见图2(B),第二基元反应历程及驻点结构基本同于2个H2O分子催化的过程,参见图5,势能面见图6.
从图6可以看出: 2个水分子簇的催化与水溶剂化效应的共同作用与只是2个水分子簇催化时的能垒相比较,使能垒124.1kJ·mol-1降低到104.4kJ·mol-1.说明水溶剂对水分子催化的H迁移反应具有较好的助催化效应.比较图6和图3可以看出: 对于无键断异构的第1基元反应,水溶剂化效应使能垒从51.9kJ·mol-1降到37.9kJ·mol-1,说明水溶剂对羟基旋转异构反应也具有助催化作用.104.4kJ·mol-1远低于常温度下质子迁移的“极限能垒”167.0kJ·mol-1[26],人体正常温度约为310.00K,高于常温298.15K,再考虑到体内分子间碰撞、温度涨落等因素,此能垒在生命体内可以越过.这说明Asn分子在生命体内可以缓慢地实现旋光异构.
对2个稳定构型的S-Asn分子旋光异构裸反应、水分子的催化作用及水溶剂化效应的研究表明: 构型1有2条通道a和b,先进行的质子迁移过程分别是协同机理和分步机理,分步机理具有优势.构型2有1条通道,是质子先以氨基氮为桥从手性碳的一侧迁移到另一侧.裸反应时,构型1主反应通道的决速步吉布斯自由能垒为252.7kJ·mol-1,构型2的决速步吉布斯自由能垒为254.0kJ·mol-1,均来自于质子从手性碳向氨基氮迁移的过渡态.2个水分子作质子迁移媒介时,构型1主反应通道b的决速步吉布斯自由能垒降到124.1kJ·mol-1,水溶剂化效应使该能垒进一步降到104.0kJ·mol-1.结果表明: 孤立环境下的Asn分子具有稳定性;水蒸气环境下的Asn分子可以缓慢地实现旋光异构;Asn分子在生命体内富水环境下可以实现旋光异构.
[1] ZHANG J, FAN J, VENNETI S,etal. Asparagine plays a critical rolein regulating cellular adaptation to glutamine depletion [J].MolCell, 2014,56(2): 205-218.
[2] 张奇,张露,徐友强,等.生物转化法制备L-天冬酰胺 [J].中国生物工程杂志,2016,36(1): 63-67.
[3] BURDA P, AEBI M. The dolichol pathway of N-linked glycosylation [J].BiochimBiophysActa, 1999,1426(2): 239-257.
[4] PATTERSON M C. Metabolic mimics: the disorders of N-linked glycosylation [J].SeminPediatrNeurol,2005,12(3): 144-151.
[5] 张维燕,刘亚亚,刘旭平,等.谷氨酰胺和天冬酰胺对CHO细胞生长、代谢及抗体表达的影响 [J].中国生物工程杂志,2014,34(4): 9-15.
[6] 李琼瑶,蒋立建,韩冲,等.D-天冬酰胺和D-高丝氨酸的制备研究 [J].氨基酸和生物资源,2009,31(2): 43-45.
[7] 马江权,冷一欣,杨利民.DL-天冬酰胺合成工艺研究 [J].精细化工,2000,17(2): 112-114.
[8] 杨静琦,李绍限,赵红卫,等.L-天冬酰胺及其一水合物的太赫兹光谱研究 [J].物理学报,2014,63(13): 133203(1-7).
[9] 张璆.高温水热条件下天冬酰胺和葡萄糖的反应产物研究[D].南昌: 南昌大学,2014.
[10] 王辉宪,颜肖慈,罗明道,等.天冬酰胺热解机理的研究 [J].湖南大学学报(自然科学版),2000,27(6): 32-37.
[11] 马士华,施宇蕾,徐新龙,等.用太赫兹时域光谱技术探测天冬酰胺的低频集体吸收频谱 [J].物理学报,2006,55(8): 4091-4095.
[12] 李忠,佟华,王佐成,等.基于氨基作H转移桥梁单体α-Ala的手性转变机理 [J].复旦学报(自然科学版),2015,54(5): 102-108.
[13] 王佐成,范志琳,梅泽民,等.半胱氨酸分子手性转变及水分子的催化机理 [J].武汉大学学报: 理学版,2016,62(4): 368-374.
[14] 闫红彦,王佐成,邹晶,等.缬氨酸分子的手性转变及水分子的催化机理 [J].中山大学学报(自然科学版),2016,55(2): 68-75.
[15] 王晓玲,高峰,佟华,等.赖氨酸分子手性转变机制及水分子和羟自由基的催化作用 [J].吉林大学学报(理学版),2016,54(5): 1161-1167.
[16] BECKE A D. Density-functional thermochemistry. III. The role of exact exchange [J].ChemPhys, 1993,98(7): 5648-5652.
[17] PARR R G, YANG W. Density-functional theory of atoms and molecules [M]. New York, Oxford: Oxford University Press, 1994.
[18] GARRETT B C, TRUHLAR D G. Generalized transition state theory. Classical mechanical theory and applications to collinear reactions of hydrogen molecules [J].JournalofPhysicalChemistry, 1979,83(8): 1052-1079.
[19] GARRETT B C, TRUHLAR D G. Criterion of minimum state density in the transition state theory of bimolecular reactions [J].TheJournalofChemicalPhysics, 1979,70(4): 1593-1598.
[20] GONZALEZ C, SCHLEGEL H. Reaction path following in mass-weighted internal coordinates [J].JournalofPhysicalChemistry, 1990,94(14): 5523-5527.
[21] ISHIDA K, MOROKUMA K, KOMORNICKI A. The intrinsic reaction coordinate. An ab initio calculation for HNC→HCN and H-+ CH4→CH4+H-*[J].TheJournalofChemicalPhysics, 1977,66(5): 2153-2156.
[22] 徐光宪,黎乐民,王德民. 量子化学(中册) [M]. 北京: 科学技术出版社,1985: 962-986.
[23] BINKLEY J S, POPLE J A. Moeller-Plesset theory for atomic ground state energies [J].IntJQuantumChem, 1975,9(2): 229-236.
[24] MARENICH A V, CRAMER C J, TRUHLAR D G. Universal slovation model based on solute electron density and on a continuum model of the solvent defined by the bulk dielectric constant and atomic surface tensions [J].JPhyChemB, 2009,113(18): 6378-6396.
[25] FRISCH M J, TRUCKS G W, SCHLEGEL H B,etal. Gaussian 09. Revision E.01[CP]. Pittsburgh USA: Gaussian, Inc., Wallingford CT, 2013.
[26] GORB L, LESZCZYNSKI, J. Intramolecular asnton transfer in mono- and dihydrated tautomers of guanine: An ab initio post Hartree-Fock study [J].AmChemSoc, 1998,120: 5024-5032.
[27] 高峰,王佐成,闫红彦,等.布洛芬分子手性转变裸反应机理及水分子的催化作用—基于羰基和苯环作H迁移桥梁 [J].中山大学学报(自然科学版),2016,55(6): 115-124.
OpticalIsomerismMechanismofAsparaginesandtheRoleofWaterBasedonAminoGroupasProtonTransferBridge
CUIFengwu1,WANGZuocheng2,YUXiaoji3,GAOFeng2,YANHongyan4,TONGHua2
(1.CollegeofMathematics,BaichengNormalUniversity,Baicheng137000,China;2.CollegeofPhysics,BaichengNormalUniversity,Baicheng137000,China;3.ForeignLanguagesSchool,ChangchunNormalUniversity,Changchun131000,China;4.ComputerScienceCollege,BaichengNormalUniversity,Baicheng137000,China)
The bare optical isomerism reaction mechanism of two stable configurations of asparagine molecules, catalytic action of water molecules and water solvation effect were researched by using the B3LYP method of density functional theory, the MP2 method of perturbation theory and the SMD model method based on self consistent reaction field(SCRF) theory. The study of reaction channels showed that there were two channels a, b in the configuration one. In the channel a, the proton transfer of the first elementary reaction is in parallel with isomerism of the carboxyl group, that was the concerted mechanism. In b, it was the stepwise mechanism carboxyl first isomerism and then proton transfer. There was one channel in the configuration two where the proton was first transferred to the other side of the chiral carbon and then isomerism of the carboxyl and amino group. Calculations of potential energy surface showed that channel a was the dominant reaction path and the free energy barrier of the rate-determining step was 252.7 kJ·mol-1in the configuration one, and that was 254.0kJ·mol-1in the configuration two, which were both generated by the transition state of proton transfer from the chiral carbon to the amino N. When two water molecules were used as proton transfer carrier, the free energy barrier of the rate-determining step was reduced to 124.1kJ·mol-1in the dominant reaction path b of the configuration one, and that can be reduced to 104.0 kJ·mol-1considering the water solvation effect. The research results showed the catalytic action of water molecules and the co-catalysis of water solvent can greatly reduce the energy barrier of proton transfer reaction.
optical isomerism; asparagines; density functional theory; transition state; perturbation theory; self consistent reaction field
0427-7104(2017)04-0509-08
2017-01-05
吉林省科技发展计划资助项目(20160101308JC)
崔凤午(1962—),男,教授,E-mail: cuifengwu219@163.com;王佐成(1963—),男,副教授,硕士,通信联系人,E-mail: wangzc188@163.com;佟华(1970—),女,教授,通信联系人,E-mail: 164912372@qq.com.
O641.12
A
