慈姑多糖部位颗粒剂制备工艺研究△
2017-12-11王秀丽王晶王春国王欣怡柯秀慧李冰廖艳
王秀丽,王晶,王春国,王欣怡,柯秀慧,李冰,廖艳*
(1.北京中医药大学 中药学院,北京 100102;2.北京中医药大学 基础医学院,北京 100029;3.北京中医药大学 科研实验中心,北京 100029)
·中药工业·
慈姑多糖部位颗粒剂制备工艺研究△
王秀丽1,王晶2,王春国3,王欣怡1,柯秀慧2,李冰2,廖艳2*
(1.北京中医药大学 中药学院,北京 100102;2.北京中医药大学 基础医学院,北京 100029;3.北京中医药大学 科研实验中心,北京 100029)
目的优选慈姑多糖部位的提取方法及其颗粒剂的制备工艺,为慈姑多糖部位的开发利用提供实验依据。方法首先采用正交设计L4(23),以浸膏得率为指标,对影响慈姑提取工艺的因素进行考察并制备慈姑多糖部位;利用苯酚-硫酸法对慈姑多糖部位中的慈姑多糖含量进行测定;再以颗粒的吸湿性、成型性、溶化性、休止角及制粒的难易程度为评价指标,采用L9(33)正交试验设计对慈姑多糖部位颗粒剂的工艺条件进行优选;并采用固定漏斗法测定休止角,考察所添加辅料种类、慈姑多糖部位与辅料比例、乙醇浓度对慈姑多糖部位颗粒剂成型工艺的影响,借以优选成型工艺。结果慈姑的最佳提取工艺为6倍量70%乙醇,冷浸提取48 h;慈姑多糖部位中慈姑多糖的含量为20.22%;优选的慈姑多糖部位颗粒剂成型工艺的条件为以乳糖作为辅料,慈姑多糖部位与辅料比例为1∶2,并使用80%乙醇作为润湿剂;在优选的条件下,颗粒的成型性好、流动性好且不易粘连,溶化速度快且静置后无沉淀。结论优选的慈姑多糖部位的提取方法及其颗粒剂的制备工艺合理且简单可行,为慈姑多糖部位的开发利用提供了实验依据。
慈姑多糖部位;颗粒剂;制备工艺;休止角
慈姑为泽泻科植物慈姑SagittariasagittifoliaLinn.的干燥块根。本品性味苦甘,微寒,无毒[1],具有行血通淋、润肺止咳的功能[2]。慈姑可作药食两用,价格低廉,来源广泛,近年来日益受到学术界的重视。现代研究表明,慈姑中主要含有生物碱类、酚类等成分[2],还含有多种抗氧化营养物质[3]。现代药理研究表明,慈姑具有抑制蛋白酶作用[4],还对化学物质CCL4及镉所致肝损伤具有保护作用[5-7]。本课题组前期研究发现,慈姑提取部位对异烟肼和利福平合用所致肝损伤具有保护作用[8-9]。目前,有关慈姑深加工的产品报道较少,本实验采用正交试验对慈姑多糖部位颗粒剂的提取工艺和制备工艺进行优选,旨在为慈姑多糖部位的开发利用提供参考。
1 材料与仪器
1.1 材料
新鲜慈姑原产自云南,北京新发地批发市场购买,经北京中医药大学药学院王晶娟副教授鉴定为泽泻科慈姑属慈姑SagittariaSagittifoliaL.的球茎;乙醇、石油醚、乙酸乙酯、正丁醇等试剂均为分析纯;乳糖、蔗糖、糊精均为药用规格。
1.2 仪器
HENC手持式匀浆机(上海恒川机械设备有限公司);DY89-Ⅱ电动匀浆仪(浙江宁波新芝生物科技有限公司);KQ-500DE型数控超声波清洗器(上海楚定分析仪器有限公司);BSA2245型电子天平(德国赛多利斯公司);玻璃漏斗、坐标纸、铁架台、及休止角测定仪(自备)。
2 方法与结果
2.1 慈姑多糖部位制备
2.1.1 正交试验优选浸提工艺 取新鲜慈姑,去皮切片,烤箱55 ℃烘干,粉碎机打碎得慈姑粉。在浸提过程中主要影响因素有乙醇浓度、溶剂用量和浸提时间等。经查阅文献资料并考虑生产的可行性,本实验以慈姑浸膏得率为考察指标,根据单因素试验结果以乙醇浓度、溶剂用量、浸提时间3因素做正交试验。优选慈姑最佳提取工艺。实验因素水平见表1,结果见表2。
2.1.2 慈姑多糖部位制备 由正交试验结果可得,慈姑最佳提取工艺为A2B2C2,即6倍量70%乙醇,提取48 h。

表1 试验因素水平

表2 正交试验L4(23)结果分析
利用植化萃取分离方法对慈姑的不同极性段进行系统萃取。取慈姑原药1份,加乙醇6倍量,冷浸48 h,并时时振摇,溶液进行布氏抽滤及高速离心处理,取上清液进行减压旋蒸,回收乙醇,浓缩至原液体积的1/6。浓缩液置于分液漏斗中,分别依次加入3倍量的石油醚、乙酸乙酯和正丁醇逐次萃取,获得慈姑不同极性部位,共5部位,分别为总提取物(浓缩液部位)、正丁醇部位、乙酸乙酯部位、石油醚部位和剩余水部位(多糖部位),减压浓缩,真空干燥后石油醚部位得率约为0.32%、乙酸乙酯部位得率为0.76%、正丁醇部位得率为3.94%、多糖部位得率为3.28%。多糖部位干粉作为本实验原料,其他部位干燥物作为另项实验原料。
2.1.3 慈姑多糖部位中慈姑多糖含量的测定 利用苯酚-硫酸法对慈姑多糖部位中的慈姑多糖含量进行测定。测定波长490 nm,多糖换算因子f=1.82;在20 ~100 μg呈良好线性关系,r=0.992 8。结果表明,供试溶液在2 h内显色稳定,重现性好,测得多糖含量为20.22%。
2.2 慈姑多糖部位颗粒剂的制备
2.2.1 正交试验设计方法 配方颗粒在前期预实验的基础上,明确了影响最终流动性的因素主要有辅料种类(A)、提取物与辅料比例(B)、乙醇浓度(C),为进一步优选慈姑多糖部位颗粒剂的最佳制备工艺水平设计正交试验,以休止角作为其流动性的评价指标进行实验,采用L9(33)正交表优选慈姑多糖部位颗粒剂的最佳制备工艺条件,其因素水平表见表3。

表3 正交试验因素水平表
2.2.2 试验结果及分析 用SPSS2.0统计软件对所得正交试验结果进行方差分析,见表5。结果表明,各因素水平之间F值无明显差异,极差分析表明,A1>A3>A2,B2>B1>B3,C2>C3>C1,因此慈姑多糖部位颗粒剂的制作最佳条件为A1B2C2(即辅料用乳糖、慈姑多糖部位与辅料比例为1∶2、乙醇浓度为80%)。

表4 慈姑多糖部位颗粒剂制作正交试验设计及结果

表5 方差分析
2.2.3 颗粒剂指标及其测定方法 以制成颗粒的吸湿率、成型率、溶解率及休止角来评价所制颗粒的吸湿性、成型性、溶解性及流动性。
2.2.3.1 吸湿率的测定 将过饱和氯化钠溶液置于玻璃干燥器底部,在室温下放置48 h,使其达到平衡,此时干燥器内的相对湿度为75%。在已干燥恒重的5 mL扁称量瓶底部放入约1 g的样品(即正交试验所制得的颗粒样品),轻摇使其分布均匀,精确称量后,置于盛有氯化钠过饱和溶液的干燥器内(称量瓶盖揭开),48 h后称量,计算吸湿百分率[10],结果见表4中吸湿率一栏。
(1)
2.2.3.2 成型率的测定 取正交试验中每一批次样品颗粒20 g,依次通过1号筛与5号筛,以合格颗粒重(合格颗粒为能通过1号筛但不能通过5号筛的颗粒)除以样品重为成型率[11]。其成型率结果见表4中成型率一栏。
2.2.3.3 颗粒流动性的考察 本实验中颗粒流动性的考察主要通过测量休止角的大小,休止角的测量主要采用固定漏斗法。将3只漏斗串联并固定于铁架台上,最低的漏斗口下缘与坐标纸的高度为3 cm,小心地将颗粒沿漏斗壁倒入最上面的漏斗中,直到坐标纸上形成的颗粒圆锥体尖端接触到漏斗口为止,由坐标纸测出圆锥底部的直径(2R),计算出休止角α,tgα=H(高度)/R(半径)[12]。休止角(α)越小,说明摩擦力越小,流动性越好。一般认为α≤30°时流动性好,α≤40°时可满足生产过程中流动性的需求[13]。表4中正交试验结果表明,所优选的制粒工艺测得的休止角均小于40°,表明优选的工艺所制颗粒流动性可满足生产需求。
2.2.4 颗粒剂制备工艺的优选
2.2.4.1 辅料(稀释剂)种类选择 颗粒剂常用辅料有乳糖、糊精、蔗糖。且制粒时常用14目筛湿法对其成型性进行评价,2010年版《中华人民共和国药典》规定的粒度在1~5号筛之间[14],并且颗粒收率≥90%者为成型性好,收率70%~90%者为成型性一般,收率≤70%者为成型性差。以1∶2的比例称取慈姑多糖部位与辅料,分别混匀,制粒,以吸湿率、成型性、休止角及制粒情况为考察指标,确定辅料种类。结果见表6。根据结果可见,乳糖和蔗糖效果均可,但乳糖易溶于水,性质稳定,无吸湿性,与大多数药物不起化学反应,对主药含量测定的影响较小[15],同时考虑到此颗粒剂适用人群中有可能同时患有糖尿病,从低糖、降低对糖尿病患者的副作用角度考虑,可扩大其适用范围,故应选用乳糖作为辅料。
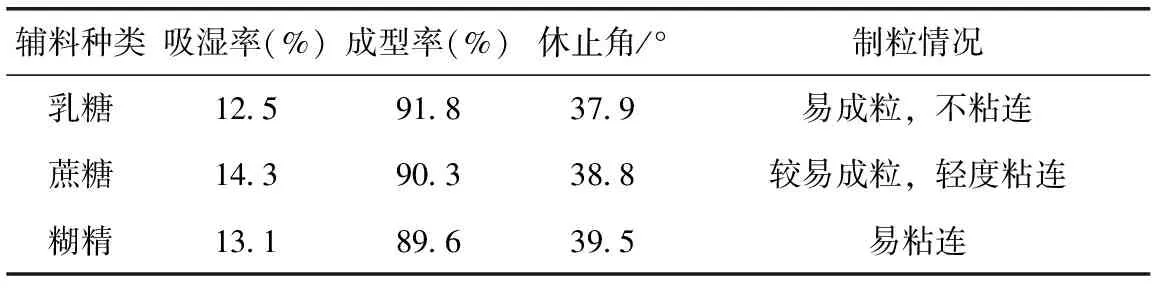
表6 慈姑多糖部位颗粒剂辅料种类优选
2.2.4.2 慈姑多糖部位与辅料比例的优选 在优选辅料种类的同时,记录慈姑多糖部位与不同比例的辅料制剂的情况,根据表7可知,辅料用量2倍或3倍均可,考虑辅料应以最小用量和无不良影响为原则,并考虑生产成本,在充分满足制剂工艺要求、保证产品质量的前提下,使辅料的用量减到最少[16],同时在辅料选择使用时应注意保证颗粒剂的成型性并降低颗粒剂的吸湿性[17],由实验所测得数据可得,2倍用量时制粒情况较好,成型率较高且吸湿率较低,故本实验选2倍用量(即1∶2)。
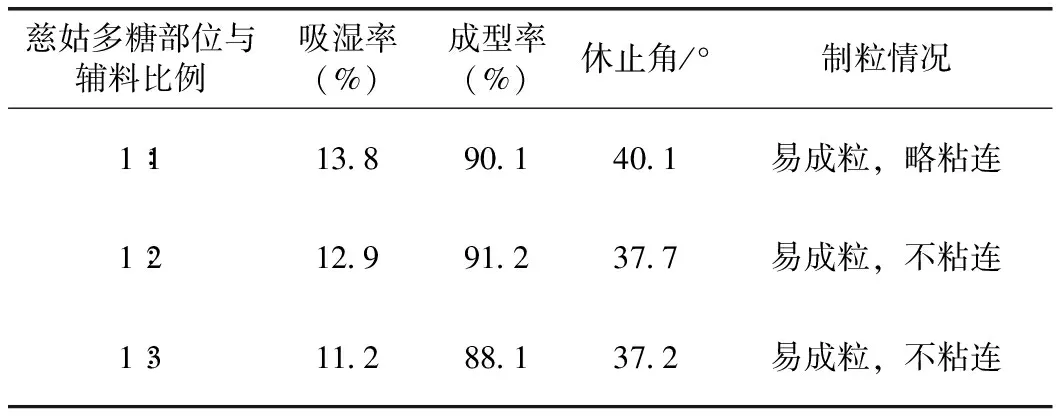
表7 慈姑多糖部位辅料乳糖用量优选
润湿剂能使药物细粉湿润、粘合,以便制成合格的颗粒[18]。常用的润湿剂有水和乙醇,但用水润湿易结块,且粘性大,难于过筛,而乙醇做为半极性润湿剂,可减少其结块,故常用不同浓度的乙醇作润湿剂[15]。本实验取慈姑多糖部位与辅料适量,用不同体积分数乙醇制粒,观察软材性状、过筛难易、颗粒性状等制粒情况,并以此为指标考察不同体积分数润湿剂的颗粒制备情况[19],同时注意用乙醇作润湿剂时要控制好其浓度及用量,并迅速搅拌,立即制粒,减少挥发[17]。结果表明,以70%乙醇为润湿剂时,所制软材较湿黏,过筛亦较困难,所制颗粒易黏结成团。以80%乙醇为润湿剂时,所制软材不湿黏,过筛较易,所制颗粒为松散小颗粒。以90%乙醇为润湿剂时,所制软材较干散,过筛容易,所制颗粒松散,但干粉较多。故根据以上结果并联合所测休止角大小可知,80%的乙醇做为润湿剂制粒效果最佳。
2.2.5 验证试验 根据筛选得到的最佳成型工艺参数进行3批次验证[20-21],其吸湿率、成型率、休止角和口感见下表8,根据表中数据可见,平均吸湿率为13.3%(RSD=3.45%),平均成型率为91.6%(RSD=2.79%),平均休止角为37.9°(RSD=3.18%),并且其口感较好,甜度适中,根据结果可知该工艺可靠、稳定、重复性好,表明该成型工艺试验得到的工艺条件切实可行。

表8 成型工艺验证结果
3 讨论
3.1 溶化性的测定
根据《中华人民共和国药典》2010年版一部1.2版附录部分颗粒剂溶化性测定要求及文献[22-23]的查阅,对于本实验中颗粒的溶化性测定:取所制颗粒样品10 g,加热水200 mL,搅拌5 min,立即观察。结果显示,所制颗粒全部溶化或呈混悬状,部分有轻微浑浊。而通过正交试验优选出的方案所制的颗粒溶化性好,符合《中华人民共和国药典》中颗粒剂溶化性的检查标准。
3.2 颗粒剂制粒情况的评价
由于中药提取物的粘性一般都较大,在制粒时难于成型,不易制成颗粒[24]。另外本实验的主要原料为慈姑多糖部位,所制备的颗粒剂中含有大量的多糖成分,因此制粒时粘性会较高[25],并且久放易吸潮吸湿[26],因此辅料及润湿剂的选择,包括其用量及比例关系至关重要,在保证其不粘连、易成粒的前提上,同时要以低吸湿率和高成型率作为考察指标,全方位综合考虑其制粒情况。
3.3 关于流动性的考察
休止角测量法为评价颗粒流动性的常用且简便的方法,但用此法虽简单但精确度不高,在测量锥高和底径及计算过程中很容易形成误差[27],因此要做平行试验3次,且在注入物料时也要特别注意尽量使其与标准圆锥形状接近,以减少实验的误差。本实验中通过正交试验的优化,对优化的工艺条件所制颗粒的休止角测量进行3次平行试验,取其平均值为39°(<40°),其流动性符合颗粒剂的生产需求。
4 结论
本文以慈姑多糖部位干粉为原料,采用乳糖作为辅料,慈姑多糖部位与辅料比例为1∶2,并使用80%乙醇作为润湿剂进行颗粒剂的制备,所得颗粒剂成型性好、流动性好且不易粘连,溶化速度快且静置后无沉淀,为其后期的研发奠定了基础。
[1] 中国科学院中国植物志编辑委员会.中国植物志:第8卷[M].北京:科学出版社,2004.
[2] 谭志静.HPLC法测定慈姑中几种分类组分和绿原酸[J].化学工程版社,2007,21(6):20-21.
[3] 陆祖福,吴小南,汪家梨,等.慈菇营养素成分分析与抗氧化作用机理探讨[J].海峡预防医学杂志2002,8(1):50-51.
[4] 杨慧玲,王丽秀.慈菇蛋白酶抑制剂的抑制特性及其活性中心的探讨[J].中国科学(B辑),1990,20(6):1271-1276.
[5] 吴小南,盛键,汪家梨,等.慈姑对CCL4致大鼠肝纤维化NO及TNF-α影响的观察[J].中国公共卫生,1999,15(1):16-18.
[6] 吴小南,汪家梨,盛键,等.慈姑对CCL4致大鼠肝纤维化血清cyfra21-1和CEA影响的探讨[J].中国公共卫生,2001,17(1):19-22.
[7] 陆祖福,黄芳,汪家梨,等.慈菇对镉致小鼠急性肝损伤的保护作用[J].福建医科大学学报,2001,35(2):116-118.
[8] 李冰,林殷,王春国,等.慈姑活性成分对体外肝细胞损伤的保护作用[J].环球中医药,2016:9(8):905-908.
[9] 李冰,王春国,王晶,等.慈姑水提部位对异烟肼和利福平合用致小鼠肝损伤的影响[J].吉林中医药,2016:36(8):818-821.
[10] 刘金城,杭清,楼云雁,等.复方茵柏颗粒剂成型工艺的研究[J].中华中医药学刊,2010,28(3):646-648.
[11] 陈梓贤,李建利,罗悦,等.痛风颗粒剂的成型工艺优选[J].中药与临床,2014,5(6):24-26.
[12] 李茜,蒋宇宁,张刚,等.太芪培元颗粒的成型工艺优选[J].中国实验方剂学杂志,2012,18(16)34-36.
[13] 江森,何燕,李冬利,等.簕菜胶囊的成型工艺考察[J].中国实验方剂学杂志,2014,20(13):12-15.
[14] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010.
[15] 罗友华,黄亦琦,杨辉,等.中药颗粒剂辅料的研究进展[J].海峡药学,2002,14(1):1-3.
[16] 尹华,张春霞,王知青,等.芪参健骨颗粒的制剂工艺研究[J].中华中医药学刊,2011,29(3):465-468.
[17] 庞丽.中药颗粒剂的研究进展[J].山东医学高等专科学校学报,2012,34(6):469-471.
[18] 张毓,钟晓明.中药颗粒剂成型工艺的研究进展[J].海峡药学,2010,22(1):27-28.
[19] 郭志烨,杨明,韩丽,等.乌芍止痒颗粒成型工艺[J].中成药,2015,37(9):1942-1946.
[20] 付美丽,严铭铭,邵帅,等.新扶正除疫颗粒剂的成型性工艺[J].中成药.2016,38(3):692-694.
[21] 王丽,高家荣,韩燕全,等.养肝益水颗粒成型工艺[J].中国实验方剂学杂志.2012,18(1):32-35.
[22] 苏春梅,杨红,姚金凤.益母草颗粒剂制备工艺研究[J].西部中医药,2015,28(2):27-29.
[23] 谢岱,易艳东,马威.归芪补肾颗粒成型工艺及其质量控制[J].中国医院药学杂志,2015,35(21):1928-1934.
[24] 李小强,潘小燕.复方芪丹颗粒成型工艺研究[J].新疆中医药,2012,30(4):68-70.
[25] 封宣伊,姜宇,左亚杰.一贯煎颗粒成型工艺的研究[J].中医药导报,2013,19(1):87-89.
[26] 涂星,周昌园,文德鉴,等.六味参花颗粒剂的制备及质量标准研究[J].湖北民族学院学报医学版,2016,33(1):56-59.
[27] 郭品,刘家成,王文婷,等.六味地黄颗粒流动性的测定及评价[J].大理学院学报,2008,17(2):87-92.
StudyonPreparationTechnologyofGranulesContainingPolysaccharidePartsofSagittariasagittifolia
WANGXiuli1,WANGJing2,WANGChunguo3,WANGXinyi1,KEXiuhui2,LIBing2,LIAOYan2*
(1.SchoolofChineseMateriaMedica,BeijingUniversityofChineseMedicine,Beijing100102,China;2.SchoolofPreclinicalMedicine,BeijingUniversityofChineseMedicine,Beijing100029,China;3.ScientificResearchandTestCenter,BeijingUniversityofChineseMedicine,Beijing100029,China)
Objective:To optimize the extracting process of polysaccharide parts inSagittariasagittifoliaand the preparing process of granules with such parts,in order to provide the experimental basis for the development and utilization of such parts.MethodsTaking extract yield as the evaluation index,the L4(23)table of orthogonal design was applied to optimize the extracting process of polysaccharide parts inS.sagittifoliaand such parts were prepared.The content of polysaccharide in the extraction was determined by phenol-sulfuric acid method.Then,taking moisture absorbability,formability,solubility,angle of repose and difficulty degree of granulation of the prepared granules as evaluation indices,the L9(33)table of orthogonal design was used to optimize the preparing conditions of granules with the extraction prepared above.Angle of repose,determined by the fixed funnel method,was applied to select the optimized forming process of the granules considering the impact of addition of auxiliary materials,the proportion of polysaccharide parts with auxiliary materials and the concentration of ethanol.ResultsExtractingS.sagittifoliafor 48 hours by cold leaching 6 times the amount of 70% ethanol was the optimized extracting process.The content of polysaccharide in such extraction was 20.22%.The optimized forming process of the granules was using lactose as the auxiliary material,which was mixed with the extraction in a ratio of 2∶1,and using 80% ethanol as wetting agent.These prepared granules had good particle formability,fluidity,anti-adhesion and dissolvability,whose solution was without precipitation after still standing.ConclusionThe optimized extracting process of polysaccharide parts inS.sagittifoliaand the preparing process of granules with such parts are reasonable,simple and feasible,which provide the experimental basis for the development and utilization of such parts.
polysaccharide parts in Sagittaria sagittifolia;granules;preparing process;angle of repose
国家自然科学基金项目(8150151383);北京中医药新奥奖励基金(1000062720044/004)
*
廖艳,副教授,研究方向:药理毒理;Tel:(010)64286859,Email:liaoyanaa@sohu.com
10.13313/j.issn.1673-4890.2017.11.024
2017-02-15)
