多指标优选金麻杏止咳片提取工艺
2017-12-09申玉龙安丽娜王立伟宋长国金艳敏
申玉龙,安丽娜,张 鹏,王立伟,徐 达,宋长国,金艳敏
(承德燕峰药业有限责任公司,河北 承德 067600)
研究
多指标优选金麻杏止咳片提取工艺
申玉龙,安丽娜,张 鹏,王立伟,徐 达,宋长国,金艳敏
(承德燕峰药业有限责任公司,河北 承德 067600)
目的 优选金麻杏止咳片最佳提取工艺。方法 采用正交试验,以麻黄碱、苦杏仁苷、黄芩苷、绿原酸为指标,分别对醇提和水提工艺进行优选,对水提工艺进行醇沉浓度考察。结果 醇提工艺优选为10倍量60%乙醇,提取2次,每次2 h;水提工艺优选为10倍量水,提取2次,每次2 h;水提工艺的醇沉浓度为70%。结论 优选的金麻杏止咳片提取工艺,麻黄碱等4种成分的提取率均超过70%。
金麻杏止咳片;提取工艺;麻黄碱;苦杏仁苷;黄芩苷:绿原酸;正交试验
目前,中医院遵循的中药提取工艺是传统的水煎煮[1],煎煮液直接服用。在制药工业中,根据中药所含的有效成分,提取工艺分为挥发油提取[2]、乙醇提取[3-5]、水提取[6-7]和水提醇沉[8],将中药制作成片剂、胶囊剂、滴丸[9]等不同剂型服用,服用剂量大幅减少,而功效成分游离、富集,利于释放、吸收[10]。在进行工艺研究时,多选用一种提取工艺,设定一个考察指标[11-14],难以综合作出工艺合理性评价。金麻杏止咳片由黄芩、蜜炙枇杷叶、蜜炙麻黄、苦杏仁、前胡、金银花等10味中药组方,本研究中对工艺进行了优选研究,根据其功能主治与有效成分性质,优选为醇提和水提两部分,使麻黄碱、苦杏仁苷、黄芩苷、绿原酸4个成分的提取率均在70%以上。现报道如下。
1 仪器与试药
1.1 仪器
LC-20AT型泵,SPD-M20A型二极管阵列检测器,LC-solution型色谱工作站,SIL-20A型自动进样器(日本岛津公司)。色谱柱为岛津-VP-ODS柱(150 mm × 4.6 mm,5 μm)。
1.2 试药
金麻杏止咳片处方中10味药材由承德燕峰药业股份有限公司提供;定量对照品为盐酸麻黄碱(批号为0714-9903)、苦杏仁苷(批号为 110820-200403)、黄芩苷(批号为0715-200212)、绿原酸(批号为110753-200413),均购自中国食品药品检定研究院。流动相所用的甲醇(批号为111228)、乙醇(批号为121112)为色谱纯,均购自天津市科密欧化学试剂有限公司;乙醇(批号为100511,天津市百世化工有限公司)和磷酸(批号为090903,天津市红岩化学试剂厂)均为分析纯。
2 方法与结果
2.1 醇提工艺研究
2.1.1 因素水平设定
根据本制剂的功能主治与处方中各药材的性味、归经及有效成分的性质,拟将蜜炙枇杷叶、蜜炙麻黄、苦杏仁、前胡用乙醇提取,以麻黄中的麻黄碱和苦杏仁中的苦杏仁苷为评价指标,以乙醇浓度(因素A)、醇倍数(因素 B)、提取时间(因素 C)、提取次数(因素 D)为因素,采用 L9(34)正交设计,因素水平表见表1。

表1 醇提工艺正交试验因素水平表
2.1.2 试验方法与结果
取枇杷叶(蜜炙)14.9 g、麻黄(蜜炙)8.94 g、苦杏仁 8.94 g、前胡 14.9 g,共 9 份,按表 1 各因素水平,采用 L9(34)正交试验,进行乙醇回流提取,滤过,滤液回收乙醇,并浓缩至约80 mL,定量转移至100 mL容量瓶中,加乙醇至刻度,摇匀,精密吸取2 mL,置25 mL容量瓶中,用70%甲醇稀释至刻度,摇匀,滤过,精密量取续滤液2 mL置中性氧化铝柱(φ1 cm,100~120目中性氧化铝1.1 g)上,用70%甲醇洗脱至10 mL容量瓶中至约9 mL,加1滴磷酸,用70%甲醇稀释至刻度,摇匀,微孔滤膜(0.45 μm)滤过,取续滤液作为供试品溶液。以盐酸麻黄碱(12 μg /mL)和苦杏仁苷(35 μg /mL)为指标[15],测定提取液中麻黄碱和苦杏仁苷的含量。其色谱图谱见图1,结果见表2和表3。可见,最佳醇提工艺为A2B3C1D3,但综合考虑工艺成本、时间、提取率等多因素,优选工艺为A2B2C2D2。
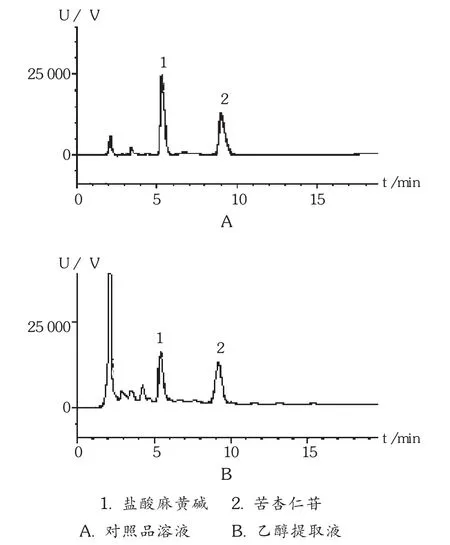
图1 醇提液高效液相色谱图
2.1.3 验证试验
以处方量的1/10,分别取4味药材,混合均匀。按正交试验结果的最佳提取工艺A2B3C1D3和优选工艺A2B2C2D2进行验证试验,结果见表4。可见,以盐酸麻黄碱与苦杏仁苷含量为指标,醇提最佳工艺与优选工艺差异不大,但优选工艺费时短,降低提取成本,故采用优选工艺进行提取,即加10倍量60%乙醇,提取2次,每次 2 h。

表2 醇提工艺 L9(34)正交试验结果
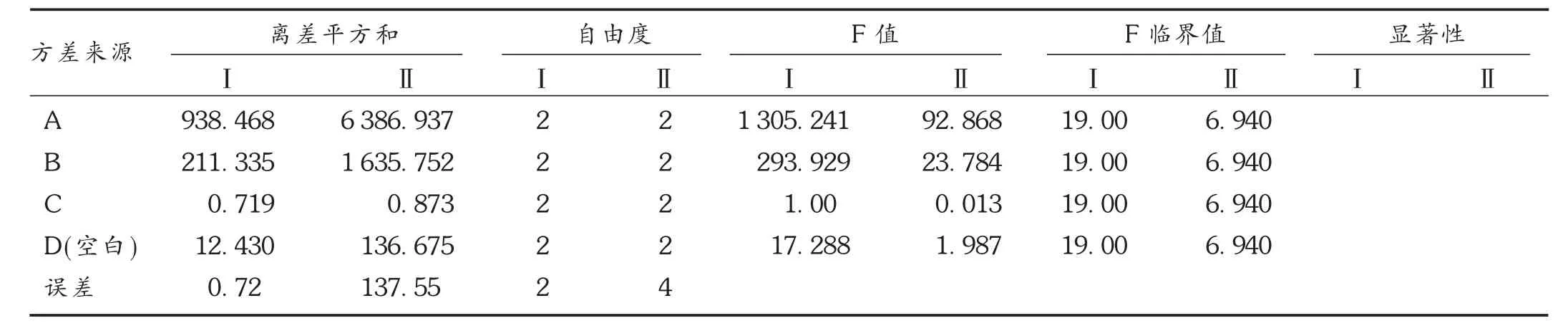
表3 醇提工艺方差分析
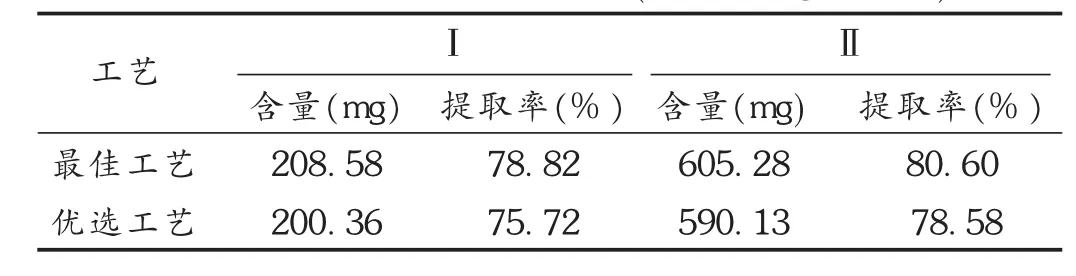
表4 醇提工艺验证试验结果(每17.88 g的含量)
2.2 水提工艺研究
2.2.1 因素水平设定
将黄芩、金银花、桔梗、桑白皮、瓜蒌、竹茹6味药材拟用水提取,但为防止黄芩苷酶解,黄芩要沸水投料。以黄芩中的黄芩苷和金银花中的绿原酸为指标,以提取次数(因素 A)、提取时间(因素 B)、加水倍数(因素 C)为因素,采用 L9(34)正交设计,因素水平见表5。

表5 水提工艺正交设计因素水平表
2.2.2 黄芩苷含量测定
1)色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;流动相为甲醇 - 水 - 磷酸(47 ∶53 ∶0.1);检测波长为 280 nm;进样量为理论板数按黄芩苷峰计算不低于2 500。在此条件下,色谱图见图2。
2)溶液制备
取黄芩苷对照品适量,精密称定,以70%甲醇制成每1 mL含25 μg的溶液,摇匀,即得对照品溶液。取定容于250 mL容量瓶的1~9号样品提取液混合均匀,取2 mL置25 mL容量瓶中,加70%甲醇稀释至刻度,摇匀,滤过,取续滤液1 mL置10 mL容量瓶中,加70%甲醇稀释至刻度,摇匀,滤过,即得供试品溶液。
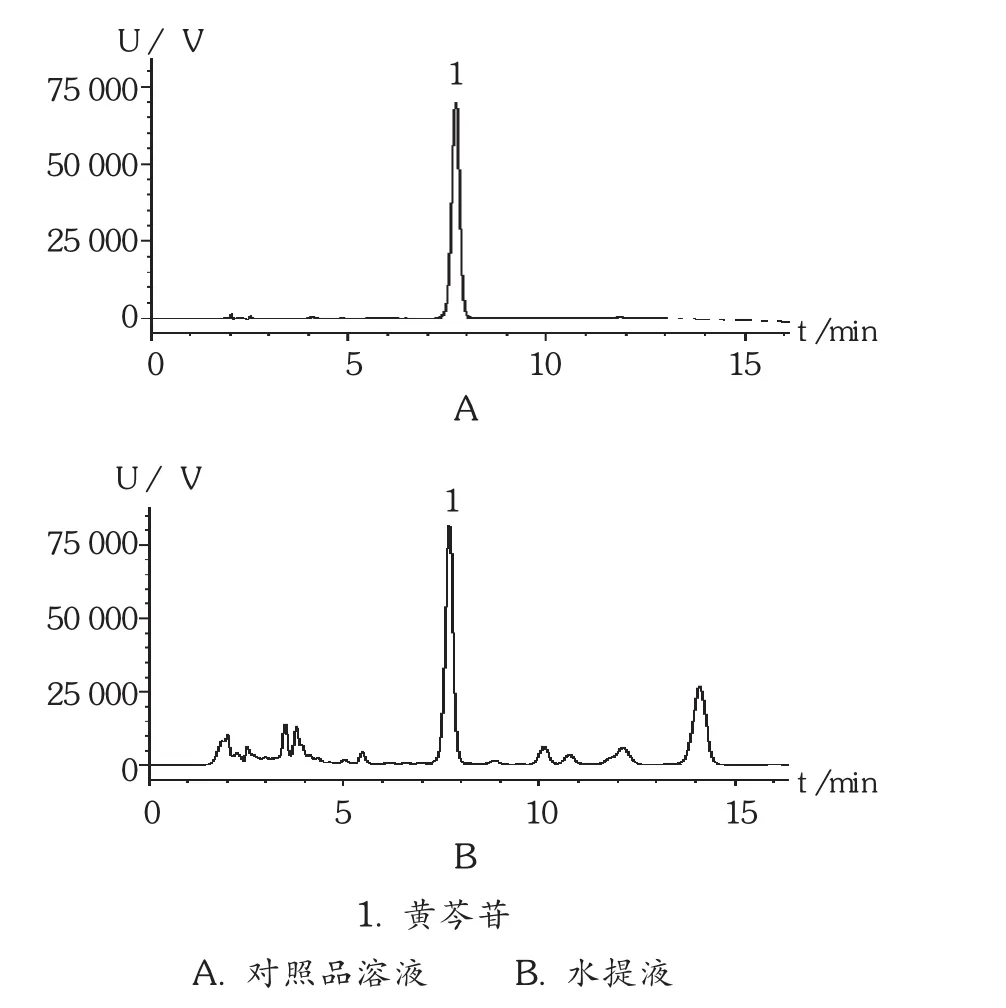
图2 水提液中黄芩苷高效液相色谱图
3)方法学考察
线性关系考察:精密吸取黄芩苷对照品溶液(146.5 μg /mL) 0.5,1.0,2.0, 3.0, 4.0, 5.0,10.0,20.0 μL,分别注入液相色谱仪,测定峰面积,以峰面积积分值(Y)为纵坐标、进样量(X)为横坐标绘制标准曲线,得回归方程 Y=2.318 700X+5.851 63,r=0.999 97,结果表明,黄芩苷进样量在73.25~2 930.00 ng范围内与峰面积线性关系良好。
精密度试验:吸取黄芩苷对照品溶液,注入液相色谱仪,进样5次,测定峰面积。结果的 RSD为 0.72%(n=5),表明仪器精密度良好。
稳定性试验:取精密度项下供试品溶液,每隔2,4,8,12,24 h,进样测定峰面积,测定 24 h内稳定性,结果的 RSD为1.44%,表明供试品溶液在24 h内稳定性良好。
重复性试验:取同一批样品,分别按高、中、低3个剂量量取,每个剂量平行3份,依法制备供试品溶液,分别进行提取,制备,测定。结果黄芩苷平均含量为20.824 mg/g, RSD 为 1.21%(n =9),表明方法重复性良好。
加样回收试验:取同一批样品9份,按高、中、低剂量加入相应量的对照品,依法制备供试品溶液,进行提取,制备,测定,计算回收率。结果黄芩苷的平均回收率为 96.96%,RSD 为 2.12%(n=9)。
2.2.3 绿原酸含量测定
1)色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;流动相为甲醇 - 乙腈 -0.1% 磷酸(4.5 ∶9 ∶86.5);检测波长为326 nm。理论板数按绿原酸峰计算不低于3 000。在此条件下,色谱图见图3。
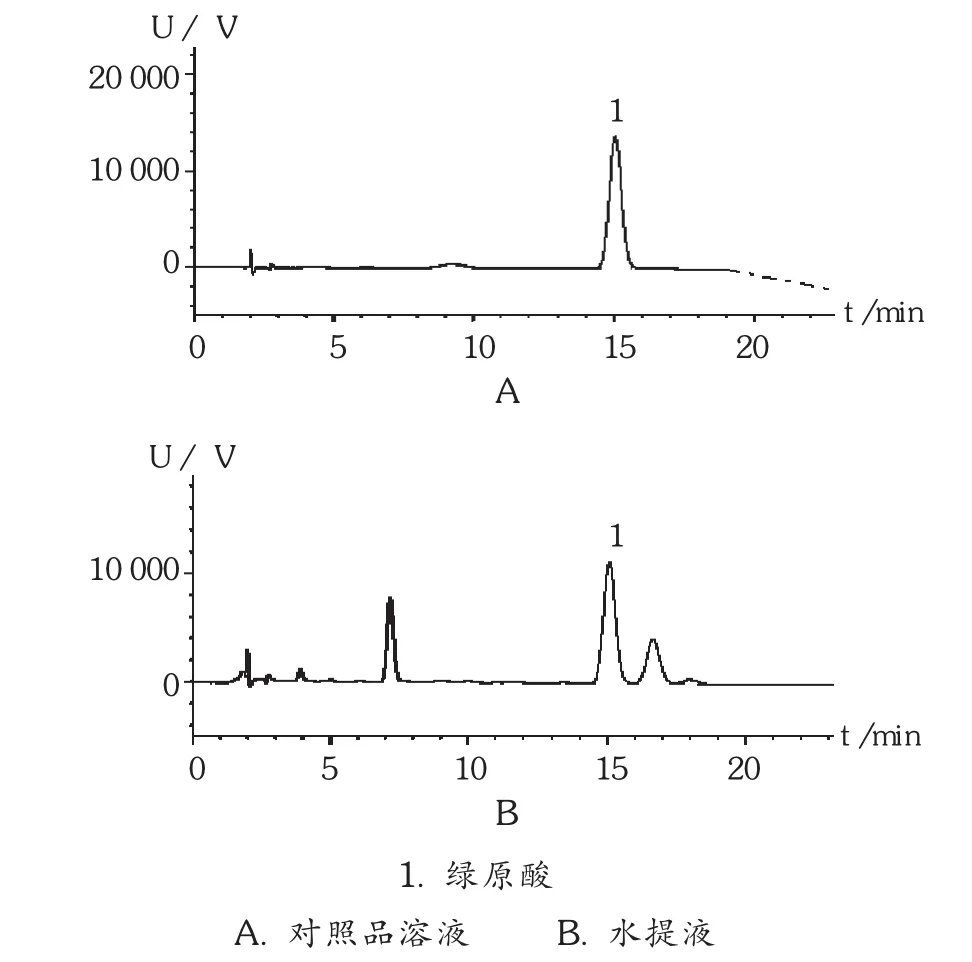
图3 水提液中绿原酸高效液相色谱图
2)溶液制备
称取绿原酸对照品适量,精密称定,加70%甲醇制成每1 mL含25 μg溶液,摇匀,即得对照品溶液。取定容于250 mL容量瓶的1~9号样品提取液混合均匀,各精密量取1 mL置25 mL容量瓶中,加70%甲醇稀释至刻度,摇匀,滤过,取续滤液5 mL,置10 mL容量瓶中,加70%甲醇稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。
3)方法学考察
线性关系考察:取绿原酸对照品溶液(0.046mg/mL),分别进样 2,5,10,15,20 μL,以峰面积(Y)为纵坐标、进样量(X)为横坐标绘制标准曲线,得回归方程 Y=2 931 322.4 X - 5 113(r= 0.999 9)。结果表明,绿原酸进样量在 0.092~0.92 μg范围内与峰面积线性关系良好。
精密度试验:精密吸取绿原酸对照品溶液,注入液相色谱仪,进样5次,测定其峰面积。结果的 RSD为0.86%(n=5),表明仪器精密度良好。
稳定性试验:取同一供试品溶液,每隔 2,4,8,12,24 h,进样测定峰面积,测定24 h内的稳定性。结果的RSD为1.42%(n=5),表明绿原酸供试品溶液在24 h内稳定。
重复性试验:取同一批样品,平行取6份,依法制备供试品溶液并测定。结果绿原酸的平均含量为8 g/L,RSD为1.21%(n=6),表明方法重复性良好。
加样回收试验:取同一批样品6份,按样品含量,加入等剂量的对照品,制备供试品溶液,依法进行提取,制备,测定,计算回收率。结果绿原酸的平均回收率为98.96%,RSD 为 2.02%(n=6)。
2.2.4 试验方法与结果
取黄芩 8.94 g,桑白皮 14.9 g,瓜蒌 14.9 g,桔梗8.94 g,金银花 14.9 g,竹茹 14.9 g,共 9 份,按正交试验因素水平表中的各因素水平,采用 L9(34)正交试验,其中黄芩是水沸后加入,进行水提取,滤过,滤液浓缩至约200 mL,定量转移至250 mL容量瓶中,加乙醇至刻度,摇匀,按 2.2.2 项下和 2.2.3 项下含量测定方法测定含量。结果见图2,正交试验结果见表6,方差分析结果见表7。可见,正交试验优选的最佳提取工艺的条件为A2B2C2,直接作为优选工艺,即以处方量的1/20,取6味药材,各2份,进行重复性试验,结果黄芩苷含量为933.99 mg/8.94 g, 提取率为 81.62% ,绿原酸含量为301.28 mg /14.9 g,提取率为 80.88% 。结果显示,以黄芩苷与绿原酸含量为指标,水提最佳工艺重复性良好,黄芩苷和绿原酸的提取率都比较高。
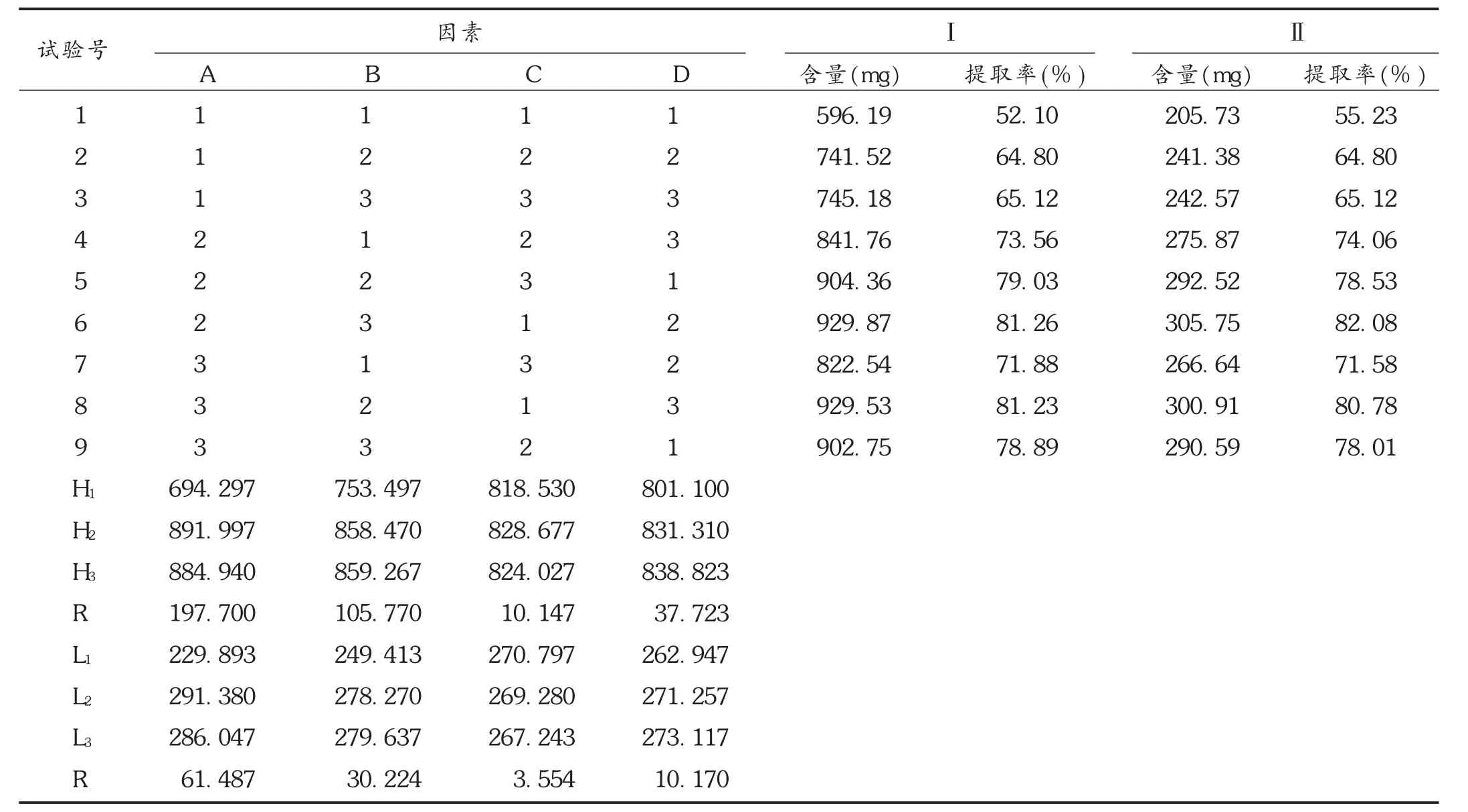
表6 水提工艺 L9(34)正交试验结果(以黄芩苷和绿原酸为指标)
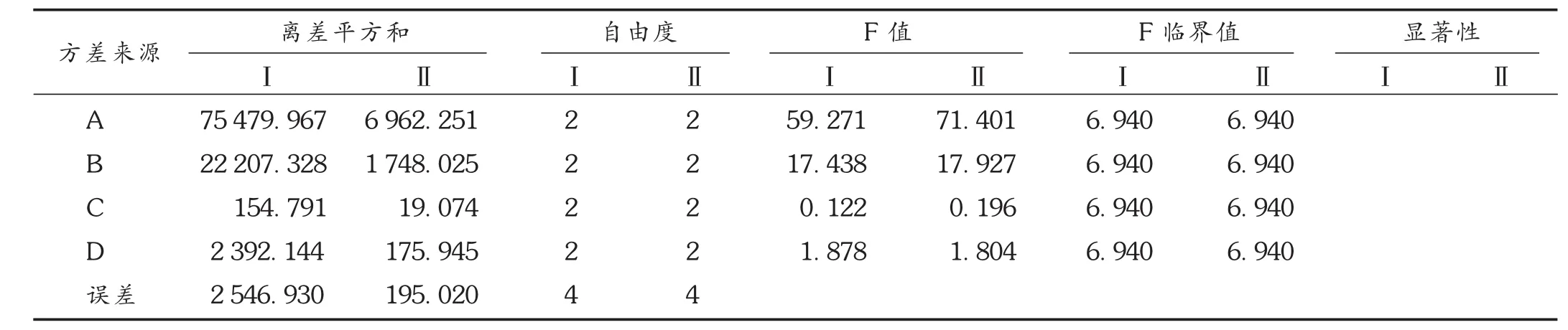
表7 水提取工艺方差分析(以黄芩苷为指标)
2.3 水提部分的醇沉研究
因本处方较大,且全浸膏粉容易吸潮,不易制粒,必须加辅料以降低黏性和吸湿性,导致服用剂量较多,故对水提液进行了醇沉研究。
称取选净的黄芩48 g,桑白皮80 g,瓜蒌80 g,桔梗48 g,金银花80 g,竹茹80 g,加10倍量水,回流提取2次,每次2 h,其中黄芩为沸水投料。提取液浓缩至相对密度1.05(60℃),分为4等份,其中3份分别加乙醇使含醇量达60%,70%,80%,充分搅拌,冷藏放置24 h,滤过,回收乙醇,转移至250 mL容量瓶中,未醇沉样品,直接转移至250 mL容量瓶中,均用水稀释至刻度,摇匀。按正交试验项下方法测定黄芩苷与绿原酸的含量,结果见表8。可见,醇沉对黄芩苷的含量影响不大,3个醇沉浓度之间黄芩苷含量亦差异不大,但70%含醇量的沉淀充分,容易过滤,节约能源,故选用醇沉浓度为70%乙醇。
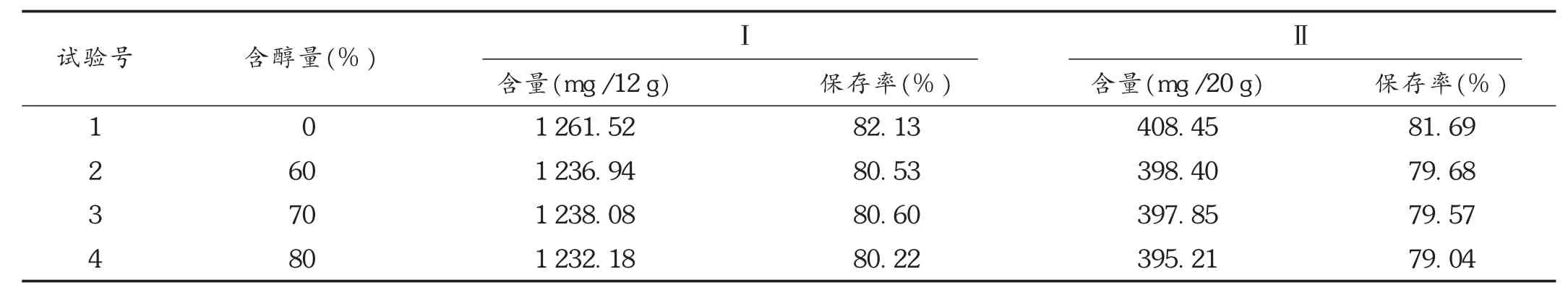
表8 醇沉浓度试验结果
2.4 优选的提取工艺
通过优选,确认的金麻杏止咳片提取工艺为:取处方中10味药材,枇把叶(蜜炙)、麻黄(蜜炙)、苦杏仁、前胡用10倍量60%乙醇提取2次,每次2 h,合并提取液,滤过,滤液回收乙醇至无醇味,备用;桑白皮、竹茹、瓜蒌、桔梗、金银花,加10倍量水煎煮至沸,加入黄芩,煎煮2次,每次2 h,合并提取液,滤过,滤液浓缩成相对密度为 1.05 ~1.10(60 ℃ 热测)的清膏,加 95% 乙醇,边加边搅拌,至醇浓度70%,冷藏放置24 h,滤过,滤液回收乙醇,与醇提液合并,浓缩至相对密度为1.1~1.15(60℃热测)的清膏,喷雾干燥。
3 讨论
提取工艺是决定药品质量的关键,在设计探讨的过程中,尽可能进行多因素多指标考察,保证多种有效成分都提取到位,确保工艺的整体水平,发挥药尽其效的最大功效,以获得良好的临床疗效。
本研究中根据制剂的功能主治与有效成分性质,分为醇提和水提部分,并以4种有效成分为指标,进行优选,使4种成分的提取效率均达到70%以上,有效保证了金麻杏止咳片的整体质量,获得了Ⅱ期与Ⅲ期临床止咳平喘的良好治疗效果。建议在今后复方制剂提取工艺优选中,有定量测定指标的药材,尽量进行多因素多指标优选,以整体提高制剂质量。
[1]谭毓秀.中药煎煮机制备汤剂的体会[J].现代中西医结合杂志,2001,10(23):2271.
[2]温 悦 .挥发油提取方法研究概况[J].中国药业,2010,19(12):84.
[3]魏金婷,叶 舟.枇杷仁中苦杏仁苷乙醇提取工艺研究[J].莆田学院学报,2007,14(5):38 - 40.
[4]杨 明,陶 蕾,王 文,等.黄芩中黄芩苷的正交提取工艺及体外抑菌活性研究[J].中兽医医药杂志,2011,30(3):43-45.
[5]乌 兰,张泽生.金银花中绿原酸的提取及检测[J].食品科学,2005,26(6):130 - 134.
[6]雷泞菲,彭书明,周嘉峪,等.黄芩中黄芩苷提取工艺研究[J].时珍国医国药,2007,18(11):2664 - 2666.
[7]翟 莲,宋凯凯,刘瑞锦.中药水提液纯化研究进展[J].齐鲁药事,2011,30(5):296 - 297.
[8]郑喜群,蒋继丰,刘晓兰,等.水提醇提法从葵花籽中提取绿原酸[J].食品科学,2006,27(1):159 - 161.
[9]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:制剂通则第3页,制剂通则第6页,制剂通则第11页.
[10]李雪静,范成龙,宋洪涛.谱效结合在中药提取纯化工艺研究中应用[J].药学实践杂志,2012,30(5):340 -343.
[11]刘克海,吴纯洁,刘彦君.正交设计优选复方感冒灵胶囊提取工艺[J].中国中医药信息杂志,2008,15(增刊):46 - 47.
[12]罗 燕,尹蓉莉,崔 妮,等.越鞠丸复方制剂提取工艺研究[J].中成药,2009,31(7):1124 - 1126.
[13]王 帆,挂双英,王举涛.正交试验法优选复方白芍颗粒提取工艺[J].安徽中医学院学报,2012,31(6):71 -73.
[14]谢宗明,彭素梅.复方金银花颗粒制剂工艺研究[J].中国现代药物应用,2010,4(14):124 -125.
[15]韩桂茹,张文臣,安丽娜,等.金麻杏止咳片快速TLC与三成分同时定量测定研究[J].中国药业,2012,21(14):41 -43.
Optimization of Extraction Process of Jinmaxing Zhike Tablets by Multi-Index
Shen Yulong,An Lina,Zhang Peng,Wang Liwei,Xu Da,Song Changguo,Jin Yanmin
(Chengde Yanfeng Pharmaceutical Group Co.,Ltd.,Chengde,Hebei,China 067600)
Objective To establish the optimum extraction process of Jinmaxing Zhike Tablets.Methods The orthogonal test was adopted with ephedrine,amygdalin,baicalin and chlorogenic acid as indexes,the alcohol extraction process and water extraction process were optimized,and the alcohol precipitation concentration of water extraction process was investigated.Results The optimum condition of alcohol extraction process was as follows:10 times of 60% ethanol,extraction 2 times,2 h each time.The optimum condition of water extraction process was as follows:10 times of water,extracting 2 times,2 h each time.The alcohol precipitation concentration of water extraction process was 70%.Conclusion Through the optimized extraction process of Jinmaxing Zhike Tablets,the extraction rates of ephedrine and other components are more than 70%.
Jinmaxing Zhike Tablets;extraction process;ephedrine;amygdalin;baicalin;chlorogenic acid;orthogonal test
TQ460.6;R284.2
A
1006-4931(2017)23-0004-06
10.3969 /j.issn.1006 - 4931.2017.23.002
申玉龙(1979-),男,大学本科,工程师,主要从事中药检验及质量标准研究工作,(电话)0311-83862259(电子信箱)277653233@ qq.com。
2017-06-06;
2017-08-15)
