健那绿B褪色光度法测定啤酒酵母中铬含量
2017-12-02李人宇黄金状李咏梅周家宏
李人宇,黄金状,李咏梅,周家宏
(1.连云港师范高等专科学校,江苏连云港222006;2.淮海工学院化学工程学院,江苏连云港222005;3.南京师范大学生命科学学院,江苏南京210023)
健那绿B褪色光度法测定啤酒酵母中铬含量
李人宇1,黄金状1,李咏梅2,周家宏3
(1.连云港师范高等专科学校,江苏连云港222006;2.淮海工学院化学工程学院,江苏连云港222005;3.南京师范大学生命科学学院,江苏南京210023)
采用微波消解样品,碱性条件下用高锰酸钾氧化铬(Ⅲ)为铬(VI),铬(VI)在磷酸介质中与碘化钾和健那绿B反应,使健那绿B褪色,据此建立褪色光度法测定铬含量的新方法。结果表明:最大褪色波长为618 nm,吸光度减小值与铬(VI)质量浓度在0~0.24 μg/mL范围内呈线性关系,检出限为2.95 μg/L。新建方法用于测定啤酒酵母中铬含量,结果与原子吸收光谱法一致,相对标准偏差为0.86%~1.29%(n=5),样品加标回收率为98.7%~101.0%。
褪色光度法;铬;健那绿B;啤酒酵母
铬(Ⅲ)是人体必需微量元素之一,参与糖、脂类和蛋白质的代谢,具有维持耐糖量于正常水平、促进生长发育的功能。人体内缺铬(Ⅲ)会引发糖尿病、冠心病、儿童发育不良等疾病;但铬(Ⅲ)过量则会危害人体健康[1-3]。啤酒酵母富含三价有机铬,人体吸收利用率高,是天然铬(Ⅲ)的良好来源[4],因品质优、产量大、经济环保等优势应用于食品工业中[5-6]。故准确测定啤酒酵母中铬含量具有重要意义。
据国内外文献报道,目前铬的测定方法主要有原子吸收光谱法[7-9]、分光光度法[10-13]、化学发光法[14-15]、电化学法[16-17]、色谱法[18-19]、质谱法[20-22]等。原子吸收光谱法、化学发光法和电化学法操作相对复杂,有的还存在较多干扰。色谱法和质谱法灵敏、准确、干扰少,但仪器昂贵,运行成本较高,需技术人员熟练操作,难以推广应用。分光光度法仪器廉价,操作简便,灵敏度较高,准确可靠,易于推广普及。试验发现,铬(VI)能氧化碘化钾生成I3-,I3-与健那绿B反应形成稳定的离子缔合物,使健那绿B褪色,本文详细研究了铬(VI)-碘化钾-健那绿B反应条件,采用微波消解样品,碱性条件下用高锰酸钾氧化铬(Ⅲ)为铬(VI),建立了褪色光度法测定啤酒酵母中铬的新方法。
1 材料与方法
1.1 仪器与试剂
UV-2550紫外-可见分光光度计:日本岛津公司;SYC-15C超级恒温水浴:南京桑力电子设备厂;pHS-3C型酸度计:上海精密科学仪器有限公司;ETHOS E微波消解仪:意大利Milestone公司;SYZ-B石英亚沸高纯水蒸馏器:宜兴新建石英玻璃器厂。
所用试剂重铬酸钾、磷酸、碘化钾和那绿B(分析纯):国药集团化学试剂有限公司生产;试验用水为二次蒸馏水。
铬(VI)标准储备溶液:100 μg/mL,称取 0.283 0 g经105℃烘至恒重的重铬酸钾,用水溶解,移入1 000 mL容量瓶中,稀释至刻度,冰箱中4℃保存。使用时稀释成2 μg/mL标准溶液;磷酸溶液:5 mol/L;碘化钾溶液:0.1 mol/L,用前新配;健那绿 B 溶液:5×10-4mol/L。
1.2 方法
取2支25 mL具塞比色管,其中一支依次加入3.0 mL 5 mol/L磷酸溶液,一定量铬(VI)标准溶液或待测试液,3.0 mL 0.1 mol/L碘化钾溶液和3.0 mL 5×10-4mol/L健那绿B溶液,用水定容至25 mL,摇匀;另一支不含铬(VI)为试剂空白。避光反应10min。用1 cm比色皿,以水作参比,在分光光度计上618 nm处测量离子缔合物体系的吸光度A和试剂空白的吸光度A0,计算△A=A0-A。
2 结果与讨论
2.1 吸收光谱
按1.2方法,以水为参比,分别扫描试剂空白、离子缔合物溶液,吸收光谱见图1。

图1 吸收光谱Fig.1 Absorption spectra
试剂空白的最大吸收峰位于618 nm,较大吸收峰位于406 nm(曲线1);铬(VI)在磷酸介质中与碘化钾和健那绿B反应形成稳定的离子缔合物,健那绿B褪色,618 nm处吸光度显著减小(曲线2)。试验选择测定波长为618 nm。
2.2 试验条件的选择
2.2.1 反应介质
分别试验了盐酸、硫酸和磷酸介质对反应的影响。结果表明,磷酸介质的灵敏度最高。但若磷酸浓度过大,体系不稳定;若磷酸浓度过小,△A值较小。选用5 mol/L磷酸溶液,用量为3.0 mL时(见图2),△A值最大。试验选用3.0 mL 5 mol/L磷酸溶液。

图2 磷酸用量的影响Fig.2 Effect of phosphoric acid amount
2.2.2 碘化钾用量
在离子缔合反应过程中,部分碘化钾未参加反应就已被空气氧化。为了保证铬(VI)反应完全,碘化钾的加入量应远大于理论量。结果表明:选用0.1 mol/L碘化钾溶液,用量为3.0 mL时,即可保证铬(VI)完全反应,△A值最大(见图3)。试验选用3.0 mL 0.1 mol/L碘化钾溶液。
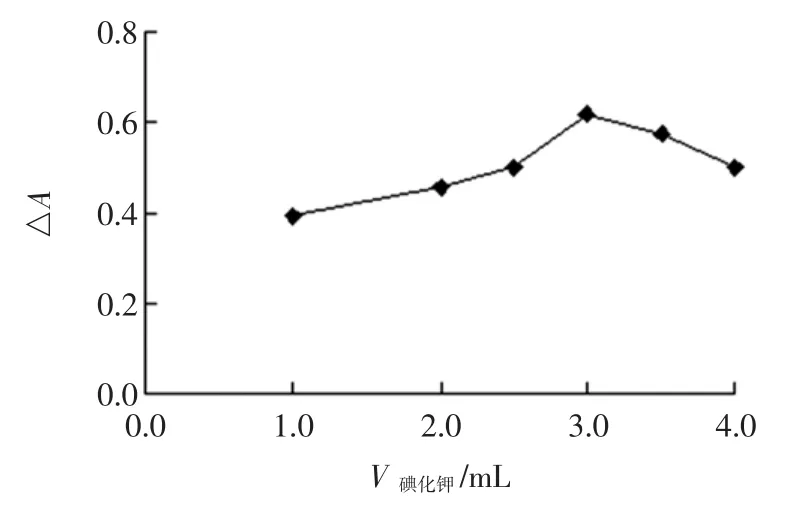
图3 碘化钾用量的影响Fig.3 Effect of potassium iodide amount
2.2.3 健那绿B用量
当5×10-4mol/L健那绿B溶液用量为3.0 mL时,△A值最大(见图4)。试验选用3.0 mL 5×10-4mol/L健那绿B溶液。
2.2.4 表面活性剂
试验考察了常见表面活性剂对反应的影响,结果见表1。

图4 健那绿B用量的影响Fig.4 Effect of janus green B amount

表1 表面活性剂的影响Table 1 Effect of surfactants
由表1可知,不加表面活性剂ΔA值更大,反应效果更好,故试验无需加表面活性剂。
2.2.5 反应温度
当温度在0~90℃范围内,温度对离子缔合反应影响不大,△A值变化幅度较小;最佳反应温度为15℃~30℃(见图5)。试验选择在室温条件下反应。
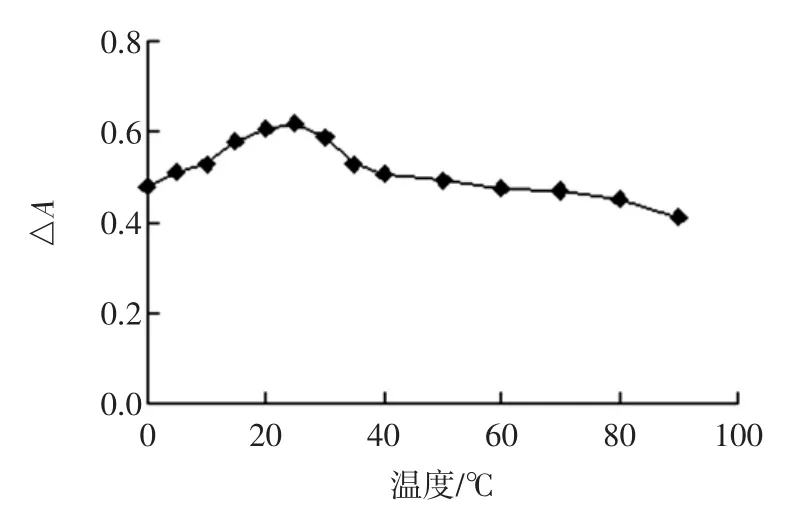
图5 反应温度的影响Fig.5 Effect of reaction temperature
2.2.6 反应时间
室温避光反应10min时,△A值达到最大(见图6)。试验选择避光条件下反应10 min。

图6 反应时间的影响Fig.6 Effect of reaction time
2.3 标准曲线
分别准确移取 0.5、1.0、1.5、2.0、2.5、3.0 mL 铬(VI)标准溶液,各置25 mL比色管中,按1.2方法操作并测量吸光度减小值△A,以△A为纵坐标,铬(Ⅵ)标准溶液质量浓度ρ为横坐标,绘制标准曲线(见图7)。

图7 标准曲线Fig.7 Standard curve
结果表明:△A与铬(VI)质量浓度在 0~0.24 μg/mL范围内呈线性关系,线性回归方程为ΔA=2.630 4ρ(μg/mL)+0.009 9,r=0.999 6,表观摩尔吸光系数 ε=1.37×105L/(mol·cm)。平行测定11次试剂空白,得A0的标准偏差为2.59×10-3,计算方法的检出限(3s/k)为2.95 μg/L。
2.4 共存离子的影响
在优化的反应条件下,考察了常见离子对0.24μg/mL铬(VI)标准溶液测定的影响,在相对误差±5%以内,共存离子的允许量(以 μg计)如下:Na+、K+、Zn2+、Co2+、Cl-、Br-、OH-(1000),Mg2+、Ca2+、Ba2+、Fe3+、Cu2+、Mn2+、NO3-、CO32-、Ac-、F-、PO43-、SiO32-(500),NH4+、Al3+、SO32-(100),Cr3+、Pb2+、Se(IV)(50)。结果表明:选择性良好,常见金属离子有较高允许量,一般样品可直接测定。
3 样品分析
将啤酒酵母样品粉碎,过60目筛,充分混匀。称取0.2 g(精确到0.000 1 g)酵母样品于微波消解罐中,加入6 mL硝酸和2 mL双氧水,置于微波消解仪中按设置程序消解。在5 min内由室温升至120℃并恒温5 min,再在5 min内升温至160℃并恒温10 min,然后在5 min内升温至180℃并恒温10 min,消解完毕得透明溶液。冷却后取出消解罐,在电热板上于140℃~160℃赶酸至剩余0.5 mL~1.0 mL。消解罐放冷后,将消化液转移至三角瓶中,用热水洗涤坩锅3次,洗涤液并入三角瓶中,加入40 mL水,加入2 mol/L氢氧化钠调节pH12,滴加2%高锰酸钾溶液,摇匀,溶液呈紫红色,在电炉上加热煮沸20 min,煮沸过程中溶液应保持紫红色。若紫红色褪去,需及时滴加高锰酸钾溶液。加热完毕取下后立即滴加95%乙醇使紫红色褪去,摇匀,用1 mol/L硝酸溶液调节pH近中性,趁热过滤,滤液置于50 mL容量瓶中,并用少量热水洗涤3次,洗涤液并入容量瓶中,定容至刻度,待测。取2.0 mL试样溶液按1.2试验方法测定,并与原子吸收光谱法[10]对照,结果见表2。同时做加标回收试验,结果见表3。

表2 样品中铬含量测定结果(n=5)Table 2 Results for the determination of chromium in samples(n=5)

表3 加标回收试验结果(n=5)Table 3 Results of spiked recovery test(n=5)
4 结论
本文采用微波消解样品,碱性条件下用高锰酸钾氧化铬(Ⅲ)为铬(VI),优化铬(VI)-碘化钾-健那绿 B体系反应条件,建立了健那绿B褪色光度法测定啤酒酵母中铬含量,在室温下反应,测定速度快,仪器操作简便,方法准确、灵敏、重现性好,所建新方法可用于啤酒酵母中铬含量的测定。
[1]杨克敌,张天宝,王爱国,等.微量元素与健康[M].北京:科学出版社,2003:139-148
[2]王永芳.铬与健康研究进展[J].中国食品卫生杂志,2001,13(1):45
[3]吴茂江.铬与人体健康[J].微量元素与健康研究,2014,31(4):72-73
[4]傅永怀.微量元素与临床[M].北京:中国医药科技出版社,1997:64-67
[5]吴振,江建梅,舒媛.啤酒酵母及其衍生品的应用研究进展[J].中国酿造,2014,33(10):10-13
[6]袁仲,杨继远.啤酒酵母抽提物的制备及其在食品工业中的应用[J].中国酿造,2008(10):67-69
[7]国家卫生和计划生育委员会.GB 5009.123-2014食品安全国家标准食品中铬的测定[S].北京:中国标准出版社,2015
[8]Liang Pei,Shi Taqing,Lu Hanbing,et al.Speciation of Cr(Ⅲ)and Cr(Ⅵ)by nanometer titanium dioxidemicro-column and inductively coupledplasmaatomicemission spectrometry[J].SpectrochimicaActa Part B,2003,58(9):1709-1714
[9]Monasterio R P,Lascalea G E,Martínez L D,et al.Determination of Cr(Ⅵ)and Cr(Ⅲ)species in parenteral solutions using a nanostructured material packed-microcolumn and electrothermal atomic absorption spectrometry[J].Journal of Trace Elements in Medi-cine and Biology,2009,23(3):157-166
[10]杨慧,刘俊华,丁良,等.催化动力学分光光度法测定粉丝中的微量铬[J].食品研究与开发,2014,35(6):75-78
[11]杨少江.罗丹明B双峰双波长分光光度法测定铬(VI)[J].广东化工,2016,43(23):110-112,105
[12]郭金全.5-溴-PADAP分光光度法测定水质中的铬(Ⅵ)含量[J].食品研究与开发,2008,29(10):102-104
[13]Thorburn D,Dangolle C D F.Spectrophotometric determination of chromium(Ⅵ)by extraction of the dichromate anion into propylene carbonate[J].Analytica Chimica Acta,1997,356(2-3):145-148
[14]高向阳,高遒竹,张小燕,等.微波消解-流动注射化学发光法快速测定调味品中的微量铬[J].中国调味品,2016,41(10):101-104,108
[15]高向阳,高遒竹,朱盈蕊,等.微波消解—流动注射化学发光法测定小麦中铬及其生物吸收比[J].粮油食品科技,2015,23(3):62-65
[16]王征帆.库仑分析法测定富铬酵母中铬含量研究[J].中国调味品,2013,38(8):102-103,120
[17]刘成伦,王晶.电化学方法在无机铬形态分析中的应用进展[J].冶金分析,2009,29(8):40-46
[18]周桂友,侯艳芳,封琳,等.反相高效液相色谱法测定陶瓷饰品中六价铬的溶出量[J].理化检验-化学分册,2015,51(1):86-90
[19]任华莉,李琪琳,曾文法.离子色谱法测定六价铬的研究进展[J].广东化工,2016,43(9):239-240
[20]杨瑞春,张伟,袁鹏等.电感耦合等离子体-质谱法测定食品中的总铬[J].光谱实验室,2013,30(4):1853-1855
[21]杨晓颖,丁春光,闫慧芳.电感耦合等离子体-质谱法检测全血中铬[J].中国职业医学,2014,41(2):208-210
[22]Krushevska A,Waheed S,Nóbrega J,et al.Interferences in the ICPMS determination of chromium and vanadium in biofluids and tissues[J].Applied Spectroscopy,1998,52(2):205-211
Fading Spectrophotometric Determination of Chromium Content in Beer Yeast with Janus Green B
LI Ren-yu1,HUANG Jin-zhuang1,LI Yong-mei2,ZHOU Jia-hong3
(1.Lianyungang Teachers College,Lianyungang 222006,Jiangsu,China;2.School of Chemical Engineering,Huaihai Institute of Technology,Lianyungang 222005,Jiangsu,China;3.College of Life Sciences,Nanjing Normal University,Nanjing 210023,Jiangsu,China)
A new fading spectrophotometric method for determination of chromium content was developed.Cr(VI)reacted with potassium iodide and janus green B in H3PO4medium,leading to the fading of janus green B after microwave digestion sample and oxidation of Cr(III)to Cr(VI)with potassium permanganate under alkaline conditions.The results showed that the maximum fading wavelength locates at 618 nm,reducing absorbance value was linear with the concentration of Cr(VI)in the range of 0-0.24 μg/mL,and the limit of detection was 2.95 μg/L.The method had been applied to the determination of Cr(Ⅲ)in beer yeast.The results obtained by this method agree well with those obtained by atomic absorption spectrometry.RSD was in the range of 0.86%-1.29%(n=5),and recovery was in the range of 98.7%-101.0%.
fading spectrophotometry;chromium;janus green B;beer yeast
10.3969/j.issn.1005-6521.2017.23.025
2015年度国家自然科学基金面上项目(21571105);2014年江苏省高校“青蓝工程”资助项目;2015年度连云港市第五期“521工程”科研项目(201529);2015年江苏省高等学校大学生创新创业训练计划项目(201511585003Y)
李人宇(1972—),男(汉),教授,博士,主要从事应用化学研究。
2017-04-20
