离子色谱法测定钙镁片中钙、镁离子的含量
2017-11-24朱荣菊
朱荣菊,王 鹏
(延安大学 西安创新学院 陕西 西安 710100)
离子色谱法测定钙镁片中钙、镁离子的含量
朱荣菊,王 鹏
(延安大学 西安创新学院 陕西 西安 710100)
采用离子色谱法进行了钙镁片中Ca2+和Mg2+的含量测定,过程为:先采用盐酸将样品溶解之后,采用阳离子交换色谱柱分离,用阳离子抑制器,分别进行精密度试验,重复性试验,加样回收率试验,系统适用性试验,最后结果检测。实验结果表明Ca2+和Mg2+的质量浓度处于2~18mg·L-1和0.4~9mg·L-1之间时,具有标准的线性关系,其相关系数都接近于1;Ca2+和Mg2+的检出浓度为 0.003mg·L-1和 0.015mg·L-1,其定量浓度为 0.004mg·L-1和 0.002mg·L-1,回收率也均接近 100%;实验测的 5批样品中Ca2+的含量分别为13.5%、14.8%、15.0%、16.3%、10.6%,Mg2+的含量分别为 5.2%、3.8%、4.5%、6.0%、3.9%。
离子色谱法;钙离子;镁离子
前 言
我们平时所服用的营养品钙镁片中既含有Ca2+也含有Mg2+,这是基于在我们的身体中钙镁元素能够参与肌肉的收放活动以及参与神经元的传输。最近的研究结果如果只补充钙镁中的一种元素,导致其中一种元素摄入超标,那么这种元素就会抵制另一种元素的吸收,这样身体吸收的元素就会失衡[1]。所以钙镁片这种营养品以2∶1的比例提供两元素,使得我们身体能够均衡吸收。之前,我们在实验室中分析Ca2+和Mg2+时通常采用火焰原子吸收法。这种方法虽说比较普遍,但是过程复杂,而且在试验过程中会产生大量的有害物质,随着实验员接触时间长之后会危害身体健康[2]。比较之下,我们采用的离子色谱法就比较安全。离子色谱法[3~5]在实验过程中与火焰原子法[6~8]有很大的不同,它主要是利用具有相同电荷的离子能够进行可逆交换,根据与其他交换剂亲和力的不同来进行分离。离子色谱法能够测定的范围很广,例如平常我们所食用的、饮用的药物检测[9],生物体液中的离子分析,工厂排出废水水质检测等等。本实验采用阳离子交换色谱柱分离,来对杂质比较复杂的保健品钙镁片样品中Ca2+和Mg2+含量的测定。实验结果表明,离子色谱法比火焰原子吸收法要好,并且能够准确的测定钙镁片中Ca2+和Mg2+的含量。
1 实验仪器与样品
1.1 实验仪器
DionexICS-5000离子色谱仪(配DionexAS自动进样器、四元梯度分析泵、淋洗液发生器、检测器/色谱单元、电导检测器、CSRS 300 4-mm抑制器、Chromeleon 6.80 SR9色谱工作站);Ion Pac CS12A阳离子交换色谱柱(4 mm×250 mm;填料:乙基乙烯基苯交联55%的二乙烯基苯大孔树脂,键和羧酸-膦酸功能基),Zone Pac CG12保护柱(4mm×50mm;填料:乙基乙烯基苯交联55%的二乙烯基苯大孔树脂,键和羧酸-膦酸功能基);Milli-Q超纯水机;Mettler Toledo MS105DU分析天平(十万分之一);KQ-500DE型数控超声波清洗器。
1.2 实验样品
由中国计量科学研究院提供的钙单元素标准溶液[1000μg·mL-1]、镁单元素标准溶液[1000μg·mL-1]、钾单元素标准溶液[1000μg·mL-1]、钠单元素标准溶液[1000μg·mL-1]、锰单元素标准溶液[1000μg·mL-1]、铵单元素标准溶液 [1000μg·mL-1];碳酸钙(99.99%);碳酸镁(99.99%);甲基磺酸(≥99%);盐酸;N2(99.99%);超纯水(电阻率为18.2MΩ·cm)。样品1-5:五种品牌的钙镁片。
2 实验方法
2.1 实验条件与样品溶液的制备
色谱柱:Ion Pac CS12A阳离子柱(4 mm×250 mm);保护柱:Zone Pac CG12柱(4 mm×50 mm);淋洗液:20mmol·L-1甲基磺酸水溶液:流速 0.8mL·min-1;抑制器:CSRS 300 4-mm;抑制电流:60mA;检测器:电导检测器;氮气流速(压力):35kPa;柱温:30℃;进样量:25μL。之后进行供试品溶液的制备。取20片钙镁片样品,进行研磨成粉末并混合均匀,称取粉末0.3~0.5g,置于250mL容量瓶中,加15mL 0.5mol·L-1盐酸溶液溶解,之后加水稀释至刻度线处并摇匀;然后量取10mL该溶液,放于100mL容量瓶中,加水稀释至刻度并摇匀,通过0.45μm滤膜过滤,取滤液作为供试品溶液。之后制备空白溶液作为对照,研究所用试剂是否对Ca2+和Mg2+的测定产生干扰。
2.2 系列标准溶液配制
用100mL的容量瓶量取钙单元素标准溶液2mL及镁单元素标准溶液1mL,加入水至刻度线并摇匀,得到混合标准溶液;用10mL容量瓶分别量取混合标准溶液 0.5、1、2、4、8、10mL,加水至刻度线并摇匀,制成含 Ca2+分别为 1、2、4、8、16、20mg·L-1及含 Mg2+分别为 0.5、1、2、4、8、10mg·L-1 的一系列混合标准溶液。
3 实验结果与讨论
3.1 线性关系考察
量取上步得到的系列混合标准溶液,并按照色谱条件逐个分析,绘制标准曲线。横坐标为Ca2+和Mg2+的质量浓度,纵坐标为峰面积,得Ca2+和Mg2+的线性方程:
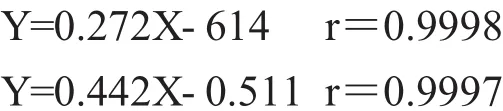
以上方程表明Ca2+和Mg2+质量浓度分别在2~18mg·L-1及 0.4~9mg·L-1范围内线性关系良好。以空白加标样品信噪比等于3(S/N=3)计算Ca2+和Mg2+的检出浓度分别为0.003和0.015mg·L-1;信噪比等于10(S/N=10)计算Ca2+和Mg2+的定量浓度分别为 0.004 和 0.002mg·L-1。
3.2 精密度试验以及重复性试验
按上述方法制备供试品溶液,连续进行6次测定,分别记录各组峰面积,计算Ca2+和Mg2+峰面积的RSD分别为0.71%和0.57%,表明精密度良好。再按上述方法制备供试品溶液6份进行测定,记录各组峰面积,根据当日的随行标准曲线计算Ca2+和Mg2+含量,其RSD分别为1.2%和1.8%,表明该方法的重复性良好。
3.3 加样回收率试验以及系统适用性试验
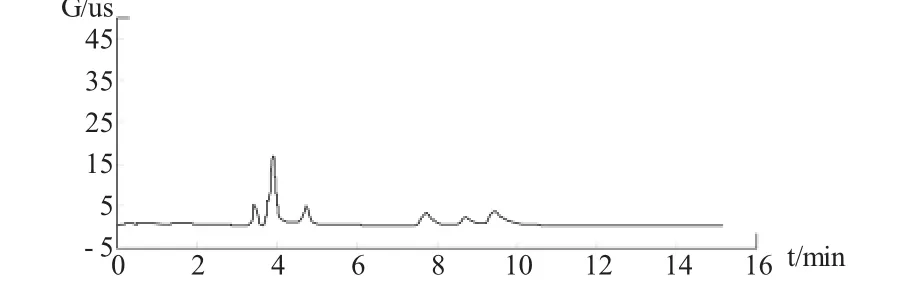
图1 6种阳离子分离情况(从左到右6个高峰依次为钠、铵、钾、镁、锰、钙离子)Fig.1 The separation of 6 kinds of cations ions(from left to right,the 6 peaks are sodium ions,ammonium ions,potassium ions,magnesium ions,manganese ions and calcium ions)
取钙镁片(Ca2+和Mg2+含量分别为12.9%和4.9%)样品0.3g,分别加入碳酸钙0.10g、碳酸镁0.055g,制备6份加标样品,按上述方法制备加标样品待测溶液进行分析,根据当日的标准曲线,分别计算加标样品的浓度,求得钙离子、镁离子的回收率分别为99.1%和99.4%。在本实验色谱条件下,钙、镁离子与钠、钾、铵、锰离子分离情况。量取上述6种离子的标准溶液 1、0.5、0.5、1、2、1mL,分别置于 100mL量瓶中,加水稀释至刻度线并摇匀。测定结果显示,各离子均能达到基线分离,且分离度大于1.5,如图1所示。
3.4 样品测定结果
按上述实验方法对5批钙镁片样品进行测定,记录峰面积,按标准曲线法定量,结果以Ca2+和Mg2+计,同时采用火焰原子吸收法分别测定Ca2+和Mg2+含量,如表1所示。
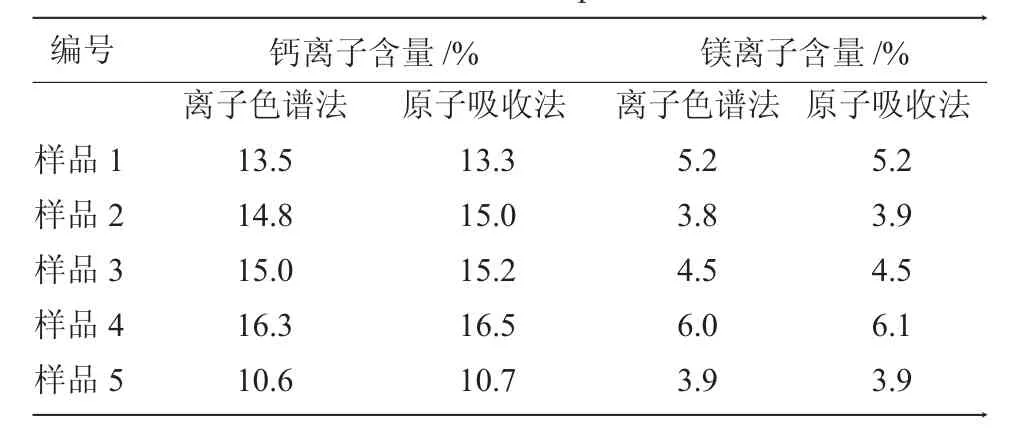
表1 五种样品中的钙镁离子含量检验结果Table 1 Test contents of calcium and magnesium ions in five kinds of samples
3.5 试剂的优化
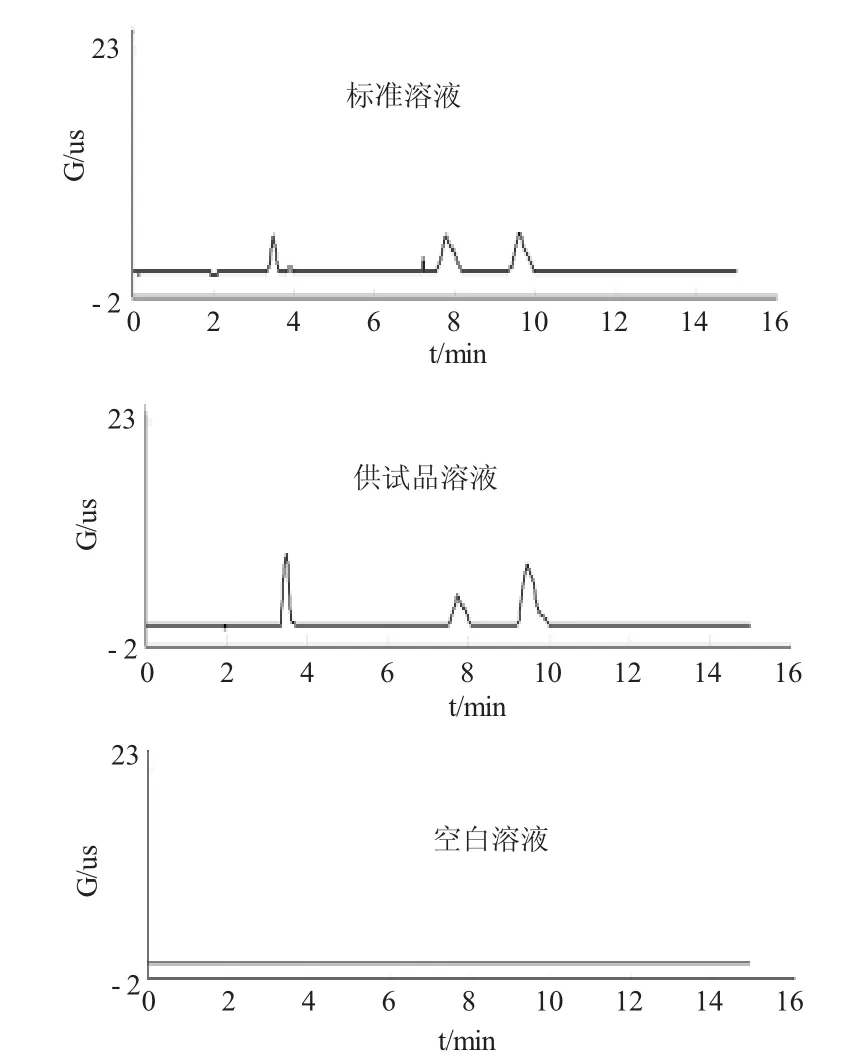
图2 标准溶液、供试品溶液、空白溶液离子色谱图(第二个第三个高峰从左到右为镁离子、钙离子)Fig.2 The ion chromatograms of standard solution,sample solution and blank solution(the second and third peaks from left to right are magnesium ions and calcium ions)
在自然界中存在很多含有Ca2+和Mg2+的物质,所以试剂的选择是十分重要的,尤其是实验用水。因此,本实验研究了实验室条件下所用试剂对Ca2+和Mg2+测定的影响,包括实验用水及盐酸。实验结果得出所用的超纯水及盐酸,在本身的存留时间范围内,均不受影响,对Ca2+和Mg2+的测定没有干扰,如图2所示。
3.6 色谱条件的优化
本实验分别考察了Ion Pac CS12、CS14、CS12A3种阳离子交换色谱柱,填料均为乙基乙烯基苯交联55%的二乙烯基苯大孔树脂,但树脂上的功能基不同,分别为羧酸、羧酸、羧酸-膦酸,三者的柱容量也不同,因此会影响离子在色谱柱上的存活行为。以上述3种色谱柱分别测定钠、铵、钾、镁、钙、锰离子混合溶液,考察系统适用性。采用20mmol·L-1的甲磺酸作为淋洗液,CS14柱存在着Ca2+和Mg2+保留时间短,且与钾离子分不开的现象。CS12与CS12A相比,CS12A是一款高容量阳离子交换色谱柱,更适用于快速等度分离各种样品中锂、钠、铵、钾、镁、钙等离子,且该柱子的离子交换基团除了羧基之外加入了膦酸基,增加了Ca2+和Mg2+的选择性。因此本实验选择Ion Pac CS12A作为分析柱。该色谱柱可以选择甲磺酸作为淋洗液,实验过程中考察了10、15、20、25mmol·L-1甲磺酸对钙、镁离子的分离效果。结果显示,20mmol·L-1的甲磺酸作为淋洗液即可实现钙、镁离子的有效分离,且出峰时间适中。同时考察了该色谱条件下,钙、镁离子与钠、钾、铵、锰离子分离情况。结果显示,各离子均能达到基线分离,且分离度大于1.5。
3.7 样品处理方法的优化
目前人们所食用的保健品钙镁片的主要成分为碳酸钙及碳酸镁,淀粉及硬脂酸镁等为辅料,经过一系列工艺制成的具有补充钙、镁功能的保健食品。本实验所用的材料为以碳酸钙及碳酸镁为原料的样品。经过综合考虑这些材料的化学特性之后,我们采用了一定浓度的稀盐酸为溶剂。Ion Pac CS12A阳离子交换色谱柱可承受高达50mmol·L-1的H+的供试品溶液进样,因此在考虑到使得样品中的Ca2+和Mg2+充分解离的条件下,应使供试品溶液的酸度符合色谱柱的使用要求。本实验采用0.5mol·L-1的稀盐酸作为溶剂,使样品溶解后,用水稀释到刻度线,在这之后还要经10倍稀释,以符合色谱柱的使用要求。样品经盐酸处理后的测定结果与硝酸硝化后的测定结果基本一致。另外,钙镁片中的硬脂酸镁的含量不超过0.08%,其中硬脂酸镁中Mg2+的含量在4.0%~5.0%;因此,在整个实验过程中硬脂酸镁在总镁离子含量小于0.004%,所以可以不考虑对Mg2+含量的影响。
4 结论
目前常用的法定测定方法主要是火焰原子吸收法。火焰原子吸收法测定Ca2+和Mg2+时,曲线浓度较低且范围较窄,较适用于微量样品的测定,而保健食品中Ca2+和Mg2+的含量多在10%左右,需多步稀释才能进入曲线范围,容易引入较大的误差。而采用离子色谱法测定保健食品钙镁片中Ca2+和Mg2+的含量,该处理方法能够有效游离出Ca2+和Mg2+,操作简单、快速,曲线范围宽,测定结果准确,且与火焰原子吸收法分析结果无明显差异,具有一定的使用价值。
[1]王宇昕,于泓离.离子色谱法测定水果和饮料中Na+、NH4+、K+、Mg2+、Ca2+、Zn2+的含量[J].食品科学,2008,29(2):347~349.
[2]赵娅鸿.离子色谱法测定饮料中的钾、钠、钙、镁阳离子[J].大众标准化,2006,(S2):24~25.
[3]牟世芬,刘克纳,丁晓静.离子色谱方法及应用[M].北京:化学工业出版社,2005.
[4]张秀香,王旭珍.原子吸收光谱法测定茶水和茶叶中的微量元素[J].鲁东大学学报:自然科学版,2000,16(3):189~193.
[5]郭岩.乌龙茶中浸出碱金属和碱土金属离子的离子色谱分析[J].现代科学仪器,2002,(6):20~21.
[6]王秀敏,陈彦昌,谷俊涛等.火焰原子发射光谱法测定枣汁饮料中钾和钠[J].分析试验室,2004,23(8):75~77.
[7]郑华宁,刘书君,顾若兰等.电感耦合等离子体质谱法测定尿中钙元素含量[J].药物分析杂志,2009,29(9):1525~1527.
[8]李苗,冯光.离子色谱法测定门冬氨酸钾镁片的含量[J].药物分析杂志,2009,29(10):1738~1740.
[9]张贞丽,袁敏,高燕等.中药紫石英主成分氟化钙含量测定方法的研究[J].药物分析杂志,2010,30(3):495~498.
Determination of the Content of Calcium and Magnesium Ion in Calcium Magnesium Tablets by Ion Chromatography
ZHU Rong-ju and WANG Peng
(Xi'an Innovation College,Yan'an University,Xi'an,710100,China)
In order to determine the content of Ca2+and Mg2+in calcium magnesium tablets,the ion chromatography is used in this experiment.The process is as follows:firstly,the sample dissolves in hydrochloric acid,followed by the separation by cation ions exchange chromatography column,and then the cation suppressor is used for the precision test,repeatability test,recovery test,system suitability test,and the final results test respectively.The experimental results show that when the concentration of Ca2+and Mg2+is between 2~18mg·L-1and 0.4~9mg·L-1respectively,a good linear relationship appeared,and the correlation coefficients are close to 1;the detectable concentration of Ca2+and Mg2+is 0.003 and 0.015mg·L-1respectively,and the quantitative concentration of them is 0.004 and 0.002mg·L-1respectively,and the recovery rate is close to 100%.In these 5 batches of samples,the content of Ca2+are 13.5%,14.8%,15%,16.3%and 10.6%respectively,and the content of Mg2+are 5.2%,3.8%,4.5%,6.0%,3.9%respectively.
Ion chromatography;calcium ions;magnesium ions
TQ460.72
B
1001-0017(2017)05-0389-04
2017-05-22
朱荣菊(1984-)女,陕西镇安人,助教,从事分析化学,药物分析工作。
