小反刍兽疫抗体检测注意事项及结果分析
2017-11-17林小能
林小能
(福建省安溪县动物疫病预防控制中心,福建安溪 362400)
小反刍兽疫抗体检测注意事项及结果分析
林小能
(福建省安溪县动物疫病预防控制中心,福建安溪 362400)
小反刍兽疫(PPR)又称“羊瘟”,是传入我国的外来动物疫病,2007年7月首次在我国西藏阿里地区暴发,至今我国的辽宁、贵州、广西等20多个省份均发生过小反刍兽疫疫情,死亡率最高可达100%,给疫情发生地区的养羊业造成了巨大的经济损失,我国将其列为一类动物疫病。目前,该疫病尚无有效的治疗方法,主要预防措施是做好免疫预防工作,因此如何评价免疫效果在该疫病的防控工作中具有重要的意义。
小反刍兽疫;竞争ELISA;注意事项;结果分析
小反刍兽疫是一种急性、高度接触性传染病,主要感染山羊和绵羊,其中山羊比绵羊的易感性更强,潜伏期一般为3~10d,多数为4~5d,最长也可以达到21d,多数羊发病后10d内死亡;急性暴发期间发病率和死亡率均可达到100%;温和发病期间,发病率仍然较高,但死亡率一般不超过50%。牛多呈亚临床感染,并能产生抗体;猪表现为亚临床感染,无症状,不排毒;野生动物也偶然发生。山羊和绵羊接种小反刍兽疫弱毒疫苗后免疫力可持续36个月以上,为做好小反刍兽疫的免疫效果评价工作,本文主要介绍小反刍兽疫竞争ELISA抗体检测试剂盒的实验步骤和注意事项,并对安溪县山羊养殖场(户)的免疫抗体水平进行分析,旨在为做好小反刍兽疫抗体监测工作提供几点意见。
1 样品来源
安溪县以饲养山羊为主,本次实验共随机采集来自于全县不同地理位置的小反刍兽疫免疫场(户)43个(其中50只以上山羊养殖场(户)19个,每场(户)采集血清样品10份;10~50只的山羊养殖散户24个,每户采集血清样品5份;采集时间为2017年5月17日至6月28日),共310份。样品采集使用5ml/次性注射器和离心管,采集后放入便携式冷藏箱中;样品当天室温(20℃)放置1h(依室温而定),待全血凝固并析出血清后,使用台式高速离心机(型号:200TG16~WS)离心(8000转离心4min,血清样品均无溶血、无腐败,符合检测要求),离心后的血清样品放入冰箱冷冻层(-15℃)保存待检。
2 实验仪器
10ml量筒、200ml量筒、250ml烧杯、、96孔离心管架、普力菲尔超纯水机(型号:FST-I-20)、电热恒温鼓风干燥箱(型号:DHG-9070)、快速混匀器(型号:SK-1)、酶标分析仪(型号:RT-6000)、单道移液器(10~100uL)、单道移液器(100~1000ul)、8道移液器(30~300uL)、300ul移液枪头、5ml离心管、一次性洗液皿、一次性吸水纸。
3 实验试剂
小反刍兽疫竞争ELISA抗体检测试剂盒(中国农业科学院兰州兽医研究所生产,批号:20170504118,有效期:2017年11月3日):已包被的ELISA板(96孔/板)、洗涤液(25×PBST)60ml/瓶、血清稀释液50ml/瓶、阴性对照血清400uL/瓶、阳性对照血清400uL/瓶、单克隆抗体150uL/瓶、兔抗鼠IgG-HRP结合物(酶标二抗)150uL/瓶、底物溶液(TMB)15ml/瓶、终止液25ml/瓶。
4 实验步骤
4.1 实验前准备
将小反刍兽疫竞争ELISA抗体检测试剂盒从冷藏冰箱(2~8℃保存)中取出,将待检血清从冰箱冷冻层中取出,按竖排列于96孔离心管架,并做好记录(待检血清设1孔、另设阳性对照血清2孔、阴性对照血清2孔、单克隆抗体对照4孔、空白对照2孔),待试剂和血清样品恢复至室温20~25℃(使用空调调节室温)才可进行实验,实验开始时按需取出包被的ELISA板。
4.2 溶液配置
(1)使用量筒将洗涤液(25×PBST)用超纯水(普力菲尔超纯水机UP出水口收集)做25倍稀释(如10ml洗涤液加240ml超纯水),放入烧杯中混匀待用。
(2)使用单道移液器(100~1000μl)和单道移液器(10~100μl)将单克隆抗体和兔抗鼠IgG-HRP结合物(酶标二抗)分别用血清稀释液进行1:100稀释(如10μl单克隆抗体或10μl兔抗鼠IgG-HRP结合物加990uL血清稀释液),分别放入5ml离心管中混匀,并做好标记待用。
4.3 操作步骤
4.3.1 加样
(1)取出ELISA板用单道移液器(10~100μl)将待检血清(50μl)和阴阳性血清(50μl)加入相应孔中,单克隆抗体孔加入血清稀释液50μl,空白对照孔加入血清稀释液100μl。
(2)除空白对照孔外,其余各孔用8道移液器加1:100稀释混匀后的单克隆抗体50μl,加样完毕后置于快速混匀器中温柔震荡混匀,用封板膜封板后置于电热恒温鼓风干燥箱(温度设置恒温37℃)中孵育60min。
4.3.2 洗液
(1)恒温37℃孵育60min后取出酶标板(ELISA板),将板中的溶液甩干,将稀释后的洗涤液(25倍稀释后)混匀后倒入一次性洗液皿,用8道移液器加洗涤液(25倍稀释后)300μl洗涤3次,并在吸水纸上甩干。
(2)每孔用多道移液器加入1:100稀释后的兔抗鼠IgG-HRP结合物50μl,加样完毕后将酶标板置于快速混匀器中温柔震荡混匀,用封板膜封板后,再次置于电热恒温鼓风干燥箱(恒温37℃)中孵育60min。
(3)恒温37℃孵育60min后取出酶标板,再次将板中的溶液甩干,用8道移液器加混匀后的洗涤液(25倍稀释后)300uL洗涤3次,并在吸水纸上甩干。
4.3.3 检测
(1)最后一次将酶标板洗板并甩干后,每孔用8道移液器加入底物溶液50μl,之后置于电热恒温鼓风干燥箱(恒温37℃)避光静置反应15min,同时将酶标分析仪接通电源预热。
(2)取出静置反应后的酶标板,每孔用8道移液器加入终止液50μl,并立即用酶标分析仪(设置450nm波长)检测实验结果(10min内测定)。
5 结果判定
阴性对照血清OD450nm值<40%,阳性对照血清OD450nm值>60%,空白对照PI值≥5%,试验有效。PI值=[1-(样品孔的OD450nm值/单抗对照孔的OD450nm值)]×100%。待检血清PI≥45%,抗体阳性;PI<40,抗体阴性;40%<PI<45%,则判定可疑,重复检测一次,根据所测PI值进行判定,如果仍为可疑需再次检测,或用其它方法检测。诊断或流行病学调查时,待检血清PI≥50%,阳性;PI<50%,阴性。
6 注意事项
(1)洗涤液稀释时应使用UP出水口收集的超纯水,避免因水质不符合洗涤液要求,影响数据的准确性。
(2)实验前应注意让试剂和血清样品均恢复至室温时才能开始。
(3)实验时如96孔ELISA板全部使用,单克隆抗体的稀释液(1:100)应比实际需要量多配备10份以上,建议配置5200μl以上(50uL*104,空白对照2孔无需添加);兔抗鼠IgG-HRP结合物应比单克隆抗体多配置2份,建议配置5300μl以上(50μl*106,96孔均需添加);洗涤液(1:25)应比实际需要量多配备一些,需配置172.8ml以上(300μl*96*6,96孔均需添加,共洗涤6次),建议配置250ml;避免因试剂在离心管、一次性洗液皿和移液枪头中的残留而导致的试剂量不足,需临时配置现象,致使反应时间不同步,影响实验结果。
(4)酶标板加单克隆抗体的稀释液(1:100)或兔抗鼠IgGHRP结合物的稀释液(1:100),样品数量少时建议使用单道移液器,量多时可倒入一次性洗液皿,再使用8道移液器添加相应试剂,以使反应时间尽量一致。
(5)实验过程中应穿实验服,佩戴手套、口罩,相关试剂使用后均应立即将试剂瓶旋紧,以免造成试剂的污染,影响今后的检测;实验结束后废弃的移液枪头、一次性洗液皿、一次性吸水纸、酶标板和用完的相关试剂瓶等均应交由具备相关资质的医疗废弃物处理机构回收处理,不得随意丢弃,以免造成外界环境的污染。
7 结果及分析
7.1 实验结果
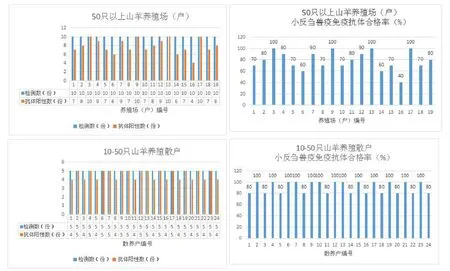
7.2 结果分析
安溪县有24个乡镇437个行政村,有山羊养殖场(户)的行政村204个,50头以上山羊养殖场(户)70个,从实验结果可以看出,安溪县养羊场小反刍兽疫免疫抗体水平总体比较高,共检测50只以上山羊养殖场(户)19个,其中抗体合格率低于70%的有3个,70~90%的有12个,达100%的有4个;共检测10~50只山羊养殖散户24个,其中抗体合格率低于70%的有0个,80%的有11个,达100%的有13个。总体看来安溪县山羊小反刍兽疫的免疫抗体水平较高,免疫屏障稳固,能有效降低感染小反刍兽疫的风险,避免疫情爆发时的急速扩散而导致巨大的经济损失。个别养羊场(户)的免疫抗体水平偏低,可能是免疫注射部位不当(小反刍兽疫应采用颈部皮下注射)或疫苗冷链不完全等因素所致,今后我县将加强小反刍兽疫的免疫预防技术指导和免疫效果监测工作,进一步提高全县的小反刍兽疫免疫抗体水平,巩固免疫屏障,有效地预防小反刍兽疫的发生和流行。
[1]王君玮,王志亮.生物安全实验室兽医病原微生物操作技术规范[M].中国农业出版社,2009.
[2]王志国.羊小反刍兽疫的综合防控措施[J].现代农业,2017,(4):85.
