Fe、Cr共掺杂TiO2纳米球增强光催化制氢
2017-11-02杨定乔吕梅香曾和平
廖 添, 宋 亭, 杨定乔, 吕梅香, 曾和平
(华南师范大学化学与环境学院, 广州 510006)
Fe、Cr共掺杂TiO2纳米球增强光催化制氢
廖 添, 宋 亭, 杨定乔, 吕梅香, 曾和平*
(华南师范大学化学与环境学院, 广州 510006)
以钛酸四丁酯、硝酸铁、硝酸铬为原料,采用改进的溶胶-凝胶法制备铁-铬共掺杂的二氧化钛纳米球. 对该纳米球进行了结晶结构、形貌和光吸收性质方面的表征,测试了该纳米球在紫外-可见光照射下光催化产氢活性. 结果表明,在掺杂总量不变的情况下,铁-铬共掺杂二氧化钛纳米球获得最好的光催化活性(133.6 μmol/(g·h)),并且具有优秀的光催化稳定性.
溶胶-凝胶法; 共掺杂; Fe; Cr; 二氧化钛; 光催化产氢
Keywords: sol-gel method; codoped; Fe; Cr; TiO2; photocatalytic hydrogen evolution
利用太阳能进行光催化产生氢气已经被认为是解决全世界能源与环境问题的有效手段[1-2]. 自从1972年FUJISHIMA和HONDA[3]在二氧化钛(TiO2)电极上发现了水的光电化学分解,TiO2半导体纳米材料在光催化产氢、环境污染修复以及染料敏化太阳能电池方面的应用已经引起了广泛关注[4-6]. 目前TiO2是应用最广泛的一种光催化剂,它具有良好的光催化活性和稳定性、无毒性和廉价等优点. 然而,TiO2具有较宽带隙(锐钛矿为3.2 eV),只能在紫外光照射下产生光催化活性[7-8]. 此外,纯TiO2光生电子空穴对的复合快速也是光催化效率和光催化活性降低的重要原因[9]. 因此,如何改性TiO2使其具有有效电荷分离、优异吸光性能和化学及光化学稳定的光催化剂成为目前的焦点问题.
目前,促进TiO2光催化剂有效电荷分离,同时将其光吸收边缘延伸到可见光区. 主要方法包括:金属或非金属离子掺杂、染料敏化和半导体耦合等[10-12]. 尤其是各种过渡金属离子的掺杂,可以使掺杂离子嵌入TiO2晶格中钛离子的位点,有效减小TiO2半导体的带隙能和阻碍光生电子空穴对的复合[13-14]. 因此,金属离子掺杂是改性TiO2的最有效的方法. 由于铁资源丰富并且环境友好,Fe3+具有半充满d电子构型且Fe3+和Ti4+离子半径大小相近,是理想的掺杂金属离子之一[15]. 最近研究表明,Fe掺杂TiO2在光催化产氢和降解有机物方面被认为是一种非常有前景的催化剂[16]. 除Fe3+外,铬掺杂的TiO2也可以很好地改善催化剂对光的吸收,增强光催化活性[17]. 然而单掺杂光催化剂对带隙的减少有限,同时容易形成杂质态促使光生电子空穴发生复合,因此在修饰光催化剂方面双组份或多组分共掺杂越来越受到人们的关注[18-19]. 研究表明,双组分共掺杂或者多组分共掺杂可产生协同效应,进一步提高光催化效率,获得比任一单组分更好的光催化活性. 例如,BENALIOUA等[20]报道了Bi、Zn 共掺杂TiO2纳米粒子在可见光范围内,对于降解靛胭脂具有明显增强的光催化活性. CHEN等[21]制备了Fe3+和Ti3+共掺杂TiO2纳米结构化合物,进一步减小了带隙能,有效地改善了在可见光照射下的光催化活性. HUO等[22]通过溶胶-凝胶法制备了钇和铝共掺杂氧化锌,具有较高光催化产氢能力以及优异的稳定性. 目前,关于Fe、Cr共掺杂TiO2纳米球的光催化产氢活性还鲜有研究. 本文采用改进的溶胶-凝胶法制备了Fe、Cr共掺杂TiO2纳米球,并以光催化产氢性能来评价其光催化活性,研究了Fe、Cr共掺杂TiO2纳米球的物理化学性质变化,分析了共掺杂对光催化活性的影响.
1 实验
1.1 实验试剂及仪器
原料:钛酸四丁酯(≥99.0%)、硝酸铁(99.0%)、硝酸铬(AR)、冰醋酸(99.5%)、商业TiO2(P25).
仪器:X射线衍射仪(Bruker D8,X射线衍射源为铜靶,狭缝为0.3 nm,工作管电压40 kV,工作管电流100 mA,扫描速率为8°/min,扫描范围2θ为10°~80°)、拉曼谱仪(Renishaw InVia)、扫描电子显微镜(SEM, JSM-6510A)、透射电子显微镜(TEM, JEM-2100HR)、X射线光电子能谱(XPS)、紫外-可见光谱(Hitachi U-3010)、荧光光谱仪(F-4500,Hitachi)、BET比表面积测试仪(Quantochrome NOVA 1200e,氮气吸附).
1.2 光催化剂的制备
采用溶胶-凝胶法制备Fe、Cr共掺杂TiO2纳米球[23]. 首先,3 mL钛酸四丁酯加入到5 mL冰醋酸中(溶液a),然后溶液a在冰浴下充分搅拌0.5 h,以形成溶胶. 然后取适量的硝酸铁和硝酸铬溶解在55 mL去离子水中(溶液b). 随后,在充分搅拌下将溶液b缓慢加入到溶液a中. 将所得混合溶液超声0.5 h,然后继续搅拌2 h,放置在阴凉处静置1 d. 再放入80 ℃烘箱中12 h形成胶体,然后120 ℃完全干燥成干凝胶. 将干凝胶研磨成粉,并在550 ℃下煅烧3 h,取出后研磨即得所需样品. 样品表示为x%M-TiO2,其中x代表掺杂金属M与Ti的摩尔比,因此制得样品分别表示为12%Fe-TiO2,8%Fe-4%Cr-TiO2和12%Cr-TiO2. 同时,纯的TiO2用同样的方法制备作为比较.
1.3 光催化活性的测试
光催化氢气产生实验在300 W Xe 灯照射下于100 mL密闭的Pyrex反应器中进行. 在具体光催化测试中,5 mg光催化剂加入到60 mL含有5%(体积分数,全文同)的三乙醇胺水溶液中. 在光照下样品用磁力搅拌器充分搅拌,溶液的温度通过循环冷却水控制在室温. 氢气产量通过装配0.5 nm分子筛柱热导检测仪的气相色谱仪在线分析检测.
2 结果与讨论
2.1 结晶结构
采用XRD谱和拉曼光谱来表征纯TiO2、12%Fe-TiO2、8%Fe-4%Cr-TiO2和 12%Cr-TiO2的晶型及结构特征. 由样品的XRD谱(图1)可知,所有峰归属于结晶锐钛矿相,与标准卡片(JCPDS NO.73-1764)一致. 峰位置在25.3°、37.8°、48.0°、53.9°、55.1°、62.7°、68.8°、70.4°、75.1°分别归属于锐钛矿相的(101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)、(215)晶面. 与纯TiO2纳米粒子相比,样品8%Fe-4%Cr-TiO2的结晶度稍微降低,并且衍射峰稍微移向较大的布拉格角. 但是没有观察到明显的Fe或Cr物质的相关峰,这表明Fe3+和Cr3+可能成功嵌入TiO2晶格中. 因为Fe3+半径(0.064 5 nm)和Cr3+半径(0.053 0 nm)和Ti4+半径(0.060 5 nm)相似,容易取代TiO2晶格中Ti4+[24]. 对于Fe或Cr单掺杂TiO2纳米粒子,XRD峰出现了少许杂峰,分别归属于Fe3Ti3O10和Cr2O3. 因为单一元素掺杂量较大,掺杂TiO2晶格出现过饱和,因此形成杂峰. 采用Debye-Scherrer方程计算所有样品的结晶尺寸D=0.9/(βcosθ),其中,D为晶粒垂直于晶面方向的平均厚度(nm),是入射波长(nm),θ是衍射的布拉格角(°),β为实测样品衍射峰半高宽度(必须进行双线校正和仪器因子校正). 基于各样品X衍射最强峰的半宽高,带入公式可得TiO2、12%Cr-TiO2、8%Fe-4%Cr-TiO2和12%Fe-TiO2的D分别为18.6、17.1、13.6、9.9 nm.
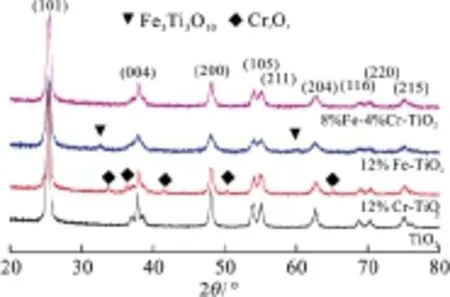
图1 不同样品的 XRD谱
为了进一步了解TiO2和8%Fe-4%Cr-TiO2的结构性质,对样品进行了拉曼光谱测试(图2),TiO2和8%Fe-4%Cr-TiO2的拉曼光谱展示了6个拉曼活性模,即3Eg、2B1g、A1g,这表明其主相属于锐钛矿相[21]. 并且没有观察到Fe或Cr相关化合物的拉曼峰,该结果与XRD分析结果一致. 同时,与纯TiO2相比,8%Fe-4%Cr-TiO2的最强峰从141.8 cm-1到146.4 cm-1发生蓝移,并且峰宽变宽,这进一步印证了Fe或Cr已经嵌入TiO2晶格中.

图2 TiO2 和 8%Fe-4%Cr-TiO2的拉曼光谱
2.2 形貌分析
采用扫描电镜(SEM)和透射电镜(TEM)研究了样品8%Fe-4%Cr-TiO2(光催化产氢活性最好)纳米粒子的形貌及粒子大小(图3A),材料主要呈球形纳米粒子,有轻微的团聚. 同时8%Fe-4%Cr-TiO2的能谱分析(EDS)(图3B)表明,样品包含4种元素(图中Pt峰存在是由于样品在扫描电镜制样过程中喷金处理引入的Pt元素),分别为Ti、O、Fe和Cr,且其中n(Fe)∶n(Ti)和n(Cr)∶n(Ti)的分别为0.088 3和0.043 8. 这一结果与制备8%Fe-4%Cr-TiO2样品时Fe和Cr理论值基本保持一致. 8%Fe-4%Cr-TiO2的TEM图(图3C)中可清晰地观察到8%Fe-4%Cr-TiO2纳米粒子为不规则的球形粒子,与SEM得出结论一致. 同时通过TEM可以得知粒子大小范围为10~15 nm,该结果与采用Debye-Scherrer方程计算结晶大小基本吻合. 采用高分辨透射电镜(HRTEM)进一步去理解纳米粒子的结晶微结构(图3D). 图中0.355 nm的条纹间隔归属于锐钛矿相的[011]晶面,除此之外,还存在晶格条纹为0.238 nm的[004]晶面. 该结果表明,8%Fe-4%Cr-TiO2纳米粒子可能沿着[101]和[004]方向生长. 同时,没有发现Fe或Cr的化合物相关晶格条纹,这再次确认了Fe和Cr已被掺入到TiO2晶格中.

图3 8%Fe-4%Cr-TiO2的SEM图、EDS谱、TEM图和HRTEM图
Figure 3 SEM image, EDS spectrum, TEM and HRTEM images of 8%Fe-4%Cr-TiO2
2.3 XPS分析
采用XPS技术研究8%Fe-4%Cr-TiO2表面元素的氧化态(图4). 以峰位置为284.8 eV的C 1s去校正结合能. Ti 2p结合能区在458.7 eV和464.4 eV出现2个特征峰,分别归属于2p3/2和2p1/2态光电子的自旋轨道裂分[25]. 然而,与Ti4+(TiO22p3/2结合能为458.9 eV, 2p1/2结合能为464.6 eV)相比[26],8%Fe-4%Cr-TiO2的Ti 2p3/2和Ti 2p1/2态的结合能稍微移向较低处,这是由于Fe和Cr共掺杂进入TiO2晶格形成的氧空位造成的[24]. O 1s区拟合为在530.0 eV和531.2 eV的2个组成峰,分别对应于TiO2晶格中的氧和表面羟基自由基中的氧[15]. Fe 2p的XPS谱在711.3 eV和725.4 eV有2个峰(图4C),分别归属于Fe 2p3/2和Fe 2p1/2的结合能. 除此之外,在Fe 2p区观察到1个明显峰,峰位置为719.7 eV,归属于Fe 2p3/2的卫星震动峰,该卫星震动峰是Fe3+的特征[27]. 并且图中Fe3+的Fe 2p3/2卫星震动峰是1个独立明显的峰,而非肩峰. 由此进一步确认了掺杂在TiO2中的Fe化学态为Fe3+[28]. 其余峰位于713.5 eV和727.4 eV可能由Fe3+盐(来源于合成过程中的前驱体)形成[29]. Cr 2p的XPS谱(图4D)中,572.0 eV和587.1 eV处的2个峰归属于Cr3+2p3/2和 Cr3+2p1/2. 此外,位于579.7 eV和589.2 eV处的2个峰归属于Cr6+2p3/2和Cr6+2p1/2[30]. 因此,当Fe和Cr掺杂进入TiO2晶格时,部分Cr原子形成了Cr6+,作为电子给体可以给出比Ti原子多2个电子. 同时,其他Fe和Cr原子作为电子受体,提供比Ti原子少1个电子. 这促使TiO2从n-型向p-型转变,有助于形成电荷补偿促使TiO2纳米粒子在光催化过程中更加有效地进行电荷转移[31-32]. 除此之外,与Fe2O3(Fe 2p3/2710.8 eV、Fe 2p1/2724.0 eV[33]和Cr2O3(Cr 2p3/2576.1 eV、Cr 2p1/2586.0 eV)[32]相比,样品的Fe3+(Fe 2p3/2711.3 eV 和Fe 2p1/2725.4 eV)和Cr3+(Cr 2p3/2577.2 eV和 Cr 2p1/2587.1 eV)的主峰位置明显移向高结合能,这是由于形成Fe—O—Ti和Cr—O—Ti键的原因[33].
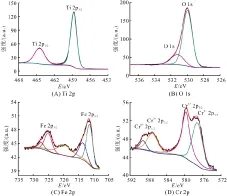
图4 8%Fe-4%Cr-TiO2中 Ti 2p、O 1s、Fe 2p和Cr 2p的XPS谱
Figure 4 XPS spectra for Ti 2p, O 1s, Fe 2p and Cr 2p regions of 8%Fe-4%Cr-TiO2
2.4 光催化产氢活性
在紫外-可见光照射下,所有制备样品在三乙醇胺水溶液中进行光催化活性测试. 实验设计了无光源或者无催化剂的空白试验,结果表明没有无氢气(H2)产生. 商业TiO2(P25)、纯TiO2、12%Fe-TiO2、8%Fe-4%Cr-TiO2和12%Cr-TiO2分别取0.005 0 g光照3 h的产氢速率v(表1)可知,对于P25和纯TiO2,其产氢速率分别为59.3 μmol/(g·h)和68.4 μmol/(g·h),产氢速率远远低于其他样品,这可能是由于较差的光吸收能力以及光催化过程中光生电子空穴对快速复合. 然而,单掺杂12%Fe-TiO2和12%Cr-TiO2的光催化活性明显改善,分别为106.3 μmol/(g·h)和90.4 μmol/(g·h). 值得注意的是,共掺杂8%Fe-4%Cr-TiO2展示了最高光催化氢气产生速率(133.6 μmol/(g·h)),这是纯TiO2(68.4 μmol/(g·h))产氢速率的1.95倍,分别是单掺杂12%Fe-TiO2、12%Cr-TiO2产氢速率的1.26、1.48倍. 这表明共掺杂进一步提高了光催化剂的光催化活性. 此外,较大比表面积也是增加光催化氢气产生速率的另一个重要原因. 因此我们研究了样品的比表面积(SBET). 与未掺杂的TiO2(42.15 m2/g)相比,单掺杂或者共掺杂均明显增加了催化剂的比表面积,其中是8%Fe-4%Cr-TiO2(57.03 m2/g)比单掺杂12%Cr-TiO2(53.83 m2/g)有更大的比表面积,这有助于增加光反应过程中的活性位点,提高光催化产氢活性. 然而单掺杂12%Fe-TiO2(60.72 m2/g)获得最大的比表面积,这可能是由于Fe掺杂比Cr掺杂更易于使纳米二氧化钛形成结晶缺陷,使得样品晶粒尺寸小,有利于提高比表面积.

表1 制备样的BET比表面积、结晶尺寸和产氢速率Table 1 BET surface areas, crystallite sizes and hydrogen evolution rates of the as-prepared photo-catalysts
为了进一步研究8%Fe-4%Cr-TiO2纳米粒子的光稳定性,取样品0.050 0 g,在相同条件下进行累计照射15 h的5次连续循环(图5),5次循环后并未发现样品光催化性能有明显的下降. 这表明8%Fe-4%Cr-TiO2纳米粒子具有很好的光催化活性. 反应前后8%Fe-4%Cr-TiO2纳米粒子的结晶结构通过XRD进行表征(图6). 结果表明8%Fe-4%Cr-TiO2纳米粒子反应前后结晶结构未发生明显改变. 综合以上结果进一步表明8%Fe-4%Cr-TiO2纳米粒子是一种稳定有效的催化剂.

图5 8%Fe-4%Cr-TiO2纳米粒子的长时间循环产氢活性
Figure 5 Long-term hydrogen production activity of 8%Fe-4%Cr-TiO2NPs

图6 15 h光催化测试前后8%Fe-4%Cr-TiO2的XRD谱
Figure 6 XRD patterns of 8%Fe-4%Cr-TiO2before and after 15 h of photocatalytic test
2.5 紫外可见漫反射和光致发光测试
为了进一步研究纯TiO2、12%Fe-TiO2、8%Fe-4%Cr-TiO2和12%Cr-TiO2的光学性质对光催化活性的影响,对样品进行了紫外可见漫反射(图7)和光致发光测试(图8). 纯TiO2的光吸收边约为400 nm,这表明它只对紫外光部分有响应. 对比之下,单掺杂12%Fe-TiO2和12%Cr-TiO2的光吸收边明显红移到可见光区. 并且,12%Fe-TiO2的紫外漫反射图谱中在450~600 nm处出现1个吸收峰,可以用来解释其增强的光催化活性. 而12%Cr-TiO2也在可见光区(550~800 nm)出现明显的吸收峰,这是由于Cr3+的占据d轨道向TiO2导带发生的跃迁以及Cr3+自身的d-d跃迁产生的[32]. 值得注意的是,由于Fe和Cr共掺杂TiO2产生协同效应,8%Fe-4%Cr-TiO2在可见光区获得最好光吸收,增加光催化过程对光能的利用率. 同时,通过Tauc方程计算样品纯TiO2、12%Fe-TiO2、8%Fe-4%Cr-TiO2和12%Cr-TiO2的带隙能分别为3.10、1.62、1.47、1.86 eV. 由计算结果可知,共掺杂8%Fe-4%Cr-TiO2纳米粒子的带隙能进一步减小,使光生电子空穴对更容易、有效地分离,从而改善纳米粒子的光催化活性.

图7 不同样品的紫外-可见漫反射光谱

图8 不同样品的荧光发射谱
除了优异的光吸收,光生电子空穴对有效的分离也是获得良好光催化活性的重要因素. 采用荧光光谱研究了样品的光生电子空穴分离性质. 荧光发射光谱技术是一种无损高敏的方法,人们广泛使用它去表征半导体材料的电荷分离效率,光致发光的峰越强说明电荷复合越快. 使用波长为322 nm的光作为激发光,制备样品表现出了明显差别的荧光发射强度(图8). 其中,纯TiO2展示了最强的荧光发射峰,表明其电子最容易发生复合,这可用来解释纯TiO2具有很差的光催化活性. 然而, Fe或Cr掺杂TiO2后其发射峰的强度大幅度降低,这表明由于Fe或Cr掺杂有效地抑制了光催化反应中光生电子空穴对的复合,有利于提高光催化反应效率.
2.6 光电流测试
为了进一步研究光生电子空穴对分离和理解共掺杂协同效应,在间歇紫外-可见光照射下测试了样品的光电流瞬变响应(图9). 停止光照,光电流密度立刻降为零;开始光照,光电流密度又立刻恢复,这表明了光生电子的迁移. 值得注意的是,8%Fe-4%Cr-TiO2的光电流密度比纯TiO2以及单掺杂样品都明显增强,这表明由Fe和Cr共掺杂的协同效应有效地提高了光生电荷的分离效率.

图9 在1 mol/L Na2SO4水溶液中采用300 W氙灯作为光源时不同样品的瞬变光电流响应
Figure 9 Transient photocurrent responses of different samples 1 mol/L Na2SO4aqueous solution under a 300 W Xe lamp as light source
3 结论
采用改进溶胶-凝胶法成功制备了Fe和Cr共掺杂二氧化钛纳米球,并且表征了其结晶结构、形貌,研究其光学性质和产氢活性. 在所有制备样品中,8%Fe-4%Cr-TiO2获得了最好的光催化产氢活性(133.6 μmol/(g·h)),并且也展示了在光催化反应过程中的可循环性. 结果表明,光吸收和电荷分离是影响光催化产氢活性的关键因素. 由于在Fe和Cr共掺杂二氧化钛中存在协同效应,不仅增强了对光的吸收,还明显改善了光生电子空穴对的分离,所以 8%Fe-4%Cr-TiO2可以获得增强的光催化产氢活性. 总之,采用共掺杂这种方法有效地提高了TiO2的光催化产氢活性,这为修饰宽带隙半导体材料提供了一种可行、简便的策略.
[1] COLMENARES J C,LUQUE R. Heterogeneous photocatalytic nanomaterials:prospects and challenges in selective transformations of biomass-derived compounds[J]. Chemical Society Reviews,2014,43(3):765-778.
[2] REZA G M,DINH C T,BELAND F,et al. Nanocomposite heterojunctions as sunlight-driven photocatalysts for hydrogen production from water splitting[J]. Nanoscale,2015,7(18):8187-8208.
[3] FUJISHIMA A,HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature,1972,238(5358):37-38.
[4] MA Y,WANG X,JIA Y,et al. Titanium dioxide-based nanomaterials for photocatalytic fuel generations[J]. Chemical Reviews,2014,114(19):9987-10043.
[5] WANG M,IOCCOZIA J,SUN L,et al. Inorganic-modified semiconductor TiO2nanotube arrays for photocatalysis[J]. Energy & Environmental Science,2014,7(7):2182-2202.
[6] ETGAR L,GAO P,XUE Z,et al. Mesoscopic CH3NH3PbI3/TiO2heterojunction solar cells[J]. Journal of the American Chemical Society,2012,134(42):17396-17399.
[7] SCHNEIDER J,MATSUOKA M,TAKEUCHI M,et al. Understanding TiO2photocatalysis:mechanisms and materials[J]. Chemical Reviews,2014,114(19):9919-9986.
[8] KAMEGAWA T,MATSUURA S,SETO H,et al. A visible-light-harvesting assembly with a sulfocalixarene linker between dyes and a Pt-TiO2photocatalyst[J]. Angewandte Chemie International Edition,2013,52(3):916-919.
[9] MONIZ S J A,SHEVLIN S A,AN X,et al. Fe2O3-TiO2nanocomposites for enhanced charge separation and photocatalytic activity[J]. Chemical-A European Journal,2014,20(47):15571-15579.
[10] JING L,ZHOU W,TIAN G,et al. Surface tuning for oxide-based nanomaterials as efficient photocatalysts[J]. Chemical Society Reviews,2013,42(24):9509-9549.
[11] LIU B,CHEN H M,LIU C,et al. Large-scale synthesis of transition-metal-doped TiO2nanowires with controllable overpotential[J]. Journal of the American Chemical Socie-ty,2013,135(27):9995-9998.
[12] WANG Z,LIU Y,HUANG B,et al. Progress on extending the light absorption spectra of photocatalysts[J]. Physical Chemisty Chemical Physical,2014,16(7):2758-2774.
[13] INTURI S N R,BONINGARI T,SUIDAN M,et al. Visible-light-induced photodegradation of gas phase acetonitrile using aerosol-made transition metal (V,Cr,Fe,Co,Mn,Mo,Ni,Cu,Y,Ce,and Zr) doped TiO2[J]. Applied Catalysis B:Environmental,2014,144:333-342.
[14] WANG C,CHEN Z,JIN H,et al. Enhancing visible-light photoelectrochemical water splitting through transition-metal doped TiO2nanorod arrays[J]. Journal of Materials Chemistry A,2014,2(42):17820-17827.
[15] FAN X,FAN J,HU X,et al. Preparation and characterization of Ag deposited and Fe doped TiO2nanotube arrays for photocatalytic hydrogen production by water splitting[J]. Ceramics International,2014,40(10):15907-15917.
[16] XU Z,YU J. Visible-light-induced photoelectrochemical behaviors of Fe-modified TiO2nanotube arrays[J]. Nanoscale,2011,3(8):3138-3144.
[17] LI X,GUO Z,HE T. The doping mechanism of Cr into TiO2and its influence on the photocatalytic performance[J]. Physical Chemisty Chemical Physical,2013,15(46):20037-20045.
[18] 张延霖,吴宏海,蔡文娟. 高活性碳氮共掺杂二氧化钦纳米线的制备与应用[J]. 华南师范大学学报(自然科学版),2015,47(3):39-44.
ZHANG Y L,WU H H,CAI W J. Preparation and application of carbon,nitrogen-codoped nanowire with high reactivity[J]. Journal of South China Normal University(Natural Science Edition),2015,47(3):39-44.
[19] LIU H,ZHAO K,WANG T,et al. Facile preparation of cerium (Ce) and antimony (Sb) codoped SnO2for hydrogen production in lactic acid solution[J]. Material Science in Semiconductor Processing,2015,40:670-675.
[20] BENALIOUA B,MANSOUR M,BENTOUAMI A,et al. The layered double hydroxide route to Bi-Zn co-doped TiO2with high photocatalytic activity under visible light[J]. Journal of Hazardous Materials,2015,288:158-167.
[21] CHEN B,HARING A J,BEACH J A,et al. Visible light induced photocatalytic activity of Fe3+/Ti3+co-doped TiO2nanostructures[J]. RSC Advance,2014,4(35):18033-18037.
[22] HUO J,FANG L,LEI Y,et al. Facile preparation of yttrium and aluminum co-doped ZnO via a sol-gel route for photocatalytic hydrogen production[J]. Journal of Materials Chemisty A,2014,2(29):11040-11044.
[23] FEILIZADEH M,MUL G,VOSSOUGHI M E. coli inactivation by visible light irradiation using a Fe-Cd/TiO2photocatalyst:statistical analysis and optimization of operating parameters[J]. Applied Catalysis B:Environmental,2015,168/169:441-447.
[24] HU S,JIA L,CHI B,et al. Visible light driven (Fe,Cr)-codoped La2Ti2O7photocatalyst for efficient photocatalytic hydrogen production[J]. Journal of Power Sources,2014,266(10):304-312.
[25] LIU S,GUO E,YIN L. Tailored visible-light driven anatase TiO2photocatalysts based on controllable metal ion doping and ordered mesoporous structure[J]. Journal of Materials Chemisty,2012,22(11):5031-5041.
[26] BESSERGENEV V G,PEREIRA R J F,MATEUS M C,et al. Study of physical and photocatalytic properties of titanium dioxide thin films prepared from complex precursors by chemical vapour deposition[J]. Thin Solid Films,2006,503(1/2):29-39.
[27] YAMASHITA T,HAYES P. Analysis of XPS spectra of Fe2+and Fe3+ions in oxide materials[J]. Applied Surface Science,2008,254(8):2441-2449.
[28] GRAAT P C J,SOMERS M A J. Simultaneous determination of composition and thickness of thin iron-oxide films from XPS Fe 2p spectra[J]. Applied Surface Science,1996,100/101:36-40.
[29] COLMENARES J C,MAGDZIARZ A,CHERNYAYEVA O,et al. Sonication-assisted low-temperature routes for the synthesis of supported Fe-TiO2econanomaterials: partial photooxidation of glucose and phenol aqueous degradation[J]. Chemcatchem,2013,5(8):2270-2277.
[30] CHENG X,FENG Z,LI C,et al. Investigation of oxide film formation on 316L stainless steel in high-temperature aqueous environments[J]. Electrochim Acta,2011,56(17):5860-5865.
[31] XU H,OUYANG S,LIU L,et al. Recent advances in TiO2-based photocatalysis[J]. Journal of Materials Chemisty A,2014,2(32):12642-12661.
[32] IKEDA T,NOMOTO T,EDA K,et al. Photoinduced dynamics of TiO2doped with Cr and Sb[J]. Journal of Physical Chemisty C,2008,112(4):1167-1173.
[33] WANG C,SHI H,LI Y. Synthesis and characteristics of natural zeolite supported Fe3+-TiO2photocatalysts[J]. Applied Surface Science,2011,257(15):6873-6877.
Fe,Cr Codoped TiO2Nanosphere with Enhanced Photocatalytic Hydrogen Evolution
LIAO Tian, SONG Ting, YANG Dingqiao, LÜ Meixiang, ZENG Heping*
(School of Chemistry and Environment,South China Normal University,Guangzhou 510006,China)
The Fe-Cr codoped TiO2nanosphere was synthesized with titanium butoxide, Fe(Ⅲ) nitrate nonahydrate, Cr(Ⅲ) nitrate nonahydrate by a modified sol-gel method. The crystal structure, morphology and optical absorption property of as-prepared nanosphere were characterized. And the photocatalytic hydrogen evolution was performed under UV-visible light illumination. The results indicated that the Fe-Cr codoped TiO2nanosphere has the best photocatalytic hydrogen evolution activity (133.6 μmol/(g·h)) and also exhibits high reusability for photocatalytic reaction.
2015-11-04 《华南师范大学学报(自然科学版)》网址:http://journal.scnu.edu.cn/n
国家自然科学基金项目(21571064,21371060);广东省自然科学基金项目(S201302001391)
*通讯作者:曾和平,教授,Email:zenghp@scnu.edu.cn.
O649.4
A
1000-5463(2017)05-0031-07
【中文责编:谭春林 英文审校:李海航】
