荧光石墨烯量子点的制备及应用
2017-11-02朱效华南俊民
梁 勇, 朱效华, 南俊民
(华南师范大学化学与环境学院, 广州 510006)
荧光石墨烯量子点的制备及应用
梁 勇*, 朱效华, 南俊民*
(华南师范大学化学与环境学院, 广州 510006)
由于具有独特的量子限域和边界效应,石墨烯量子点(GQDs)碳基纳米材料表现出特殊的性质和诸多潜在应用. 文中概括了近年来在GQDs制备方面的研究进展,包括“自上而下”方法利用水热、电化学和化学氧化等把大片石墨变为GQDs的方法,以及“自下而上方法”利用含碳有机小分子为前驱体,通过溶液化学、超声波和微波等方法实现碳原子重组制得GQDs的方法. 同时,介绍了GQDs在成像技术、生物传感和电化学分析等领域的应用情况. 最后指出,由于GQDs的发光机理还是一个开放性的课题,因此结合GQDs制备方法来研究其发光性质,将是未来该领域的研究重点.
石墨烯; 量子点; 制备; 荧光; 分析应用
Keywords: graphene; quantum dots; synthesis; fluorescence; application
荧光碳纳米材料包括纳米金刚石、碳纳米管、富勒烯、碳纳米颗粒和石墨烯量子点(Graphene Quantum Dots,GQDs)等[1-2]. 其中,当粒径在10 nm以下,具有独特结构的零维GQDs可表现出优异的量子限域效应和边界效应,这使其在诸多领域表现出诱人的潜在应用前景. GQDs与氧化石墨烯的吸收光谱类似,一般在紫外光谱区有较强的吸收,在可见区有一定的吸收. 因具有良好的化学惰性、生物相容性、低毒性和光致发光等特性,GQDs在生物成像、疾病检测、药物运输、光电器件、拉曼增强、催化剂、传感器等各领域的应用已逐渐成为研究热点[3]. 首先,GQDs因具有强度可调的光致发光性质、低毒、生物相容性好,可应用在生物成像和医药方面;其次,GQDs兼具优异的宽吸收窄发射特性、光电转换能力和电子迁移率,又使其在光电器件(如太阳能电池,有机发光二极管)中具有很大的应用潜力[4]. 此外,从GQDs良好的稳定性、生物相容性、环境友好性以及价格等方面考虑,它也有望代替传统贵金属和过渡金属,用作表面增强拉曼散射的基底材料. 因此,围绕GQDs的制备与应用开展研究工作,具有重要意义.
本文对近几年来GQDs的制备方法及其研究进展进行了综述. 同时介绍了GQDs在成像技术、生物传感和电化学分析等领域的应用.
1 石墨烯量子点的制备方法
目前,制备GQDs可分为两大途径,即自上而下和自下而上2种方式. 其中,自上而下方式是利用外力将大片的石墨前驱物变小,主要有水热法、电化学方法和化学氧化法等;自下而上方法则主要利用含碳有机小分子为前驱体,通过溶液化学法、超声波和微波法等促使碳原子重组而制得GQDs.
1.1 自上而下方法
1.1.1 水热法 水热法又称热液法,是在密闭的高温高压容器中,以水为溶剂,使石墨材料发生化学反应. 依据反应类型的不同,水热反应可分为水热氧化、水热还原、水热沉淀、水热水解和水热结晶等. 水热法现已成为制备碳纳米材料的常用方法. 例如,利用水热法处理不同浓度的葡萄糖,可得到不同粒径的碳纳米颗粒,甚至碳量子点. CUI等[5]通过微波辅助-水热处理葡萄糖水溶液,制备出平均粒径200 nm的碳球,在碳球表面固定纳米金后,研究了其电化学发光性能,并用于肿瘤标志物的检测;DONG等[6]采用同样的方法,制备碳纳米颗粒,然后在碳纳米颗粒表面生长CdS量子点,用于肿瘤标志物的标记和电化学检测;我们利用固相法处理海藻酸钠和色氨酸,制备出了氮掺杂的荧光碳纳米颗粒,用于抗坏血酸[7]和组氨酸[8]的高灵敏检测. 另外,PAN等[9]通过硫酸预处理石墨烯纳米片,可称是最早利用水热法直接制备GQDs的研究. 在碱性条件和水热环境中,利用化学切割方法来制备GQDs,最初获得的GQDs直径分布为5~13 nm,具有水溶性,发蓝色荧光,但排列较无序. 以高温热处理后的氧化石墨烯片作前驱体,制得粒径更小(1.5~5 nm)、结晶度更好且发绿色荧光的GQDs[10]. 2种方法所制备GQDs的荧光性质均表现出pH依赖性(碱性环境中发光,酸性环境下猝灭),量子产率均不高(7%左右). 最近,本课题组[11]以加入H2O2的氧化石墨烯为前驱物,采用水热处理制备出发射波长固定(不依赖激发波长)的GQDs,这可能是由于H2O2的引入,可以使GQDs的表面态更统一,从而表现出发射波长固定的行为. 此外,我们在水热处理石墨烯的过程中,同时加入H2O2和氨水,通过简单的透析处理,可以得到不同粒径分布的GQDs[12],并且2种量子点在紫外光激发下,分别发射绿色和黄色荧光.
在水热法制备GQDs机理的认识上,一般认为是基于拉链效应[13],这借鉴了氧化碳纳米管制备石墨烯纳米带的理论. 首先,利用强酸预处理石墨烯,生成链状的环氧键,环氧键链将周围sp2团簇围住,容易引起该区C—C的断裂. 随后,在水热去氧化的反应中,这些环氧键链像拉链一样被打开,氧原子被移除,相对稳定的羧基被保留下来,最终生成水溶性的GQDs,制备机理如图1[11]所示.

图1 水热法制备GQDs的机理[11]
Figure 1 Mechanism for the hydrothermal cutting GO into GQDs[11]
作为水热法的改进,ZHU等[14]通过处理分散在氮-氮-二甲基甲酰胺(DMF)溶剂中的氧化石墨烯,制备了高量子产率的GQDs. 该方法的一个显著优点是产物GQDs可溶解在水和大部分有机溶剂中,且在不同的溶剂中发射不同颜色的荧光. 同时,该GQDs用于人体骨肉瘤细胞的荧光标记时,也得到了很好的效果. LIU等[15]利用类似的方法制备了具有上转换性能的GQDs,利用双光子显微镜,可用于细胞的深层次(1 800 μm)成像. 水热法(包括溶剂热法)与其他方法相比,产物的量子产率较高. 但是,由于材料制备是基于原材料氧化石墨烯及其还原产物,因此,大多数还需进行透析纯化处理,这造成了制备过程比较耗时.
1.1.2 电化学法 电化学方法由于制备条件比较温和且容易调控,已成为制备碳纳米材料的一种较为常用方法. 例如,BAO等[16]采用三电极体系电解碳纤维,通过改变电解电位,制备出粒径可控的碳纳米颗粒. LI等[17]以等离子体预处理的石墨烯薄膜为工作电极,铂丝为对电极,在0.1 mol/L磷酸盐缓冲溶液(pH 6.86)中进行循环伏安扫描,然后进行离心和透析纯化处理,得到了具有绿色荧光的GQDs. 值得注意的是,他们用类似的方法[18],在0.1 mol/L四丁基高氯酸铵的乙腈溶液中进行电解,得到了具有蓝色荧光的氮掺杂GQDs. 在±3 V的扫描过程中,四丁基高氯酸铵可插入到石墨烯片层中,并在石墨烯边缘或缺陷位置使其分裂成小片,同时达到氮掺杂的目的,得到氮掺杂GQDs. SHINDE等[19]在非水盐酸丙烯脂溶剂中电解碳纳米管,制备出了绿色荧光发光特性的GQDs,通过调整反应温度,可制备出粒径和光学性能不同的GQDs,并指出这主要是由于表面不同的氧化程度所致. 最近,ZHANG等[20]以石墨棒为阳极,Pt作对电极,在0.1 mol/L NaOH电解液中制备出可发射特殊黄色荧光的GQDs,与前几种方法不同,该方法的电解产物在室温下经水合肼还原改性,对纯化和筛选GQDs起关键作用. 此外,在离子液体中采用5 V恒电位电解三维石墨烯,可以制备出高质量的GQDs[21].
关于电化学法制备GQDs的主要机理[21],一般认为是基于水的阳极氧化以及离子液体的阴离子插层二者间的相互作用(图2). 通过研究共存离子种类和电解电压大小对产物的影响,可进一步证实该机理. 在所述反应过程中,加入的阴离子由于具有比水更强的氧化性,因此水在阳极被首先氧化,而阴离子则在石墨层上起着嵌入剂的作用. 水被阳极氧化生成的羟基和氧自由基起着电化学“剪刀”的作用,即切割碳纳米晶体并形成含氧官能团. 在切割过程中,涉及“解开机理”,含氧基团链状结构的形成能产生的张力有利于石墨进一步氧化和裂解.
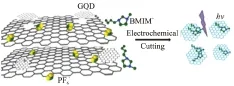
图2 电化学制备GQDs的反应机理[21]
Figure 2 Schematic illustration of the electrochemical generation process of GQDs solution[21]
化学氧化法主要以具有完美晶型的碳(碳纤维、石墨、石墨烯)为前驱物,利用氧化剂的氧化作用将碳源层层剥离制得GQDs. 例如,PENG等[22]以碳纤维为碳源,通过酸处理将纤维中堆垛的石墨剥离,仅一步就能制得大量不同粒径分布的GQDs. 通过改变反应温度,可调节GQDs产物的带隙和尺寸,从而改变其荧光颜色,在120、100、80 ℃的反应温度下,分别获得发射蓝色、绿色和黄色荧光的量子点. DONG等[23]通过在硝酸中回流商业碳黑CX-72,然后通过透析分离方法,一步制备了单层和多层的GQDs,其中,单层GQDs在365 nm激发下可以发出蓝绿荧光,而多层GQDs则发射黄色荧光,通过对制得的GQDs进行了系统表征,在GQDs中观察到了石墨的(002)晶相,通过透射电镜验证出其层间距大约为0.3 nm. 最近,SUN等[24]利用改进的Hummers法,发展了一种大量制备GQDs的方法,他们通过增加制备过程中NaNO3的比例,同时把高温阶段的温度提高到120 ℃,产物的产率达到63%±7%. 此外,以双壁碳纳米管为碳源,SWAIN等[25]利用预处理石墨烯为前驱体,对其连续紫外照射24 h,可以得到具有铁磁性的GQDs.
1.4.2 粪污处理设施 可根据养殖规模配套建设干粪处理房和堆积发酵池,或使用干粪处理机加工生产有机肥料,同时还应配备沼气等粪污处理设施。
化学氧化法的机理(图 3)与氧化法制备石墨烯法机理相类似[24]:环氧基在C-C晶格上排列成链状结构,使所在的石墨域沿着环氧基方向有断裂倾向,引发石墨结构的裂解,从而形成 GQDs. 化学氧化法优势在于步骤简单,仅一步反应能得到大量的GQDs,但是,这种方法用到了强氧化剂,后续处理也较复杂,限制了该方法的进一步推广.

图3 化学氧化法制备GQDs的反应机理[24]
Figure 3 Synthesis of GQDs from graphite via an improved Hummers’ method[24]
1.2 自下而上方法
在自上而下方法中,最常用的是溶液化学法. LI等[26]将增溶基团2′,4′,6′-三烷基取代苯环共价连接到石墨烯基边缘,以此来制备GQDs. 其中,用小分子(如3-碘-4-溴苯胺或其他苯衍生物)逐步反应制得聚苯树突状前驱体,再经氧化反应得石墨烯基,最后制得具有三维笼状构型的GQDs. 但需要注意的是,所有中间体都要用硅凝胶色谱法纯化,还要用标准表征法确认. 为保证最终产量,前驱体上苯基间的连通性要预先设计好,以避免氧化时苯基重排,同时,为防止产物形成时发生聚集,增溶基团要在氧化之前连接上. 与其他方法相比,该方法所得GQDs的尺寸较大、分布均匀且可调. DONG等[27]利用柠檬酸为前驱体,通过电热套加热柠檬酸至熔融态,加热30 min可制得GQDs,加热至2 h得到大片的氧化石墨烯. 利用这种方法得到GQDs的粒径大约为15 nm,厚度分布为0.5~2.0 nm(图4). 该方法所得产物有一个显著特点,即GQDs的荧光最大发射波长不随着激发波长的改变而改变,认为这与GQDs的粒径和表面态比较一致有关.
在溶液化学方法基础上,外加微波或超声波辅助进行材料制备,已被证明是可高效合成碳纳米材料的方法.近期,TANG等[28]以葡萄糖为碳源,将水热和微波结合制备GQDs,该方法制得的GQDs荧光性质无尺寸依赖性,最重要的是产物可发出以前未曾报道过的深紫外光. GOKHALE等[29]通过紫外光诱导有机小分子(邻二氯代苯),将邻二氯代苯直接暴露在紫外光下,通过“缝合”的方法制备了GQDs. 这种方法制备的GQDs粒径不够均匀,有较宽的粒径分布(5~30 nm),同时也有较高的细胞毒性,还存在“光漂白”现象.
微波法采用的碳源多为还原性糖类(如葡萄糖和果糖等),糖类脱水形成CC以此构成GQDs的基本骨架单元. TANG等[28]推测,还原性糖类中的羟基、羧基和羰基中的H及O会在水热环境中脱水除去,残余官能团连接在GQDs表面作为“钝化层”,使GQDs具有良好的水溶性和荧光性质. 一般认为,微波为溶液中葡萄糖和水同时提供快速、均匀的加热条件,使量子点均匀成核生长,最终形成尺寸分布良好的GQDs. 在反应过程中微波强度、加热时间、溶液体积和糖类浓度等均对GQDs的生长产生直接影响,因此可通过控制这些条件制备不同颜色荧光的GQDs. 引入超声波反应条件后,超声在反应溶液中传播产生交替的低压和高压波,这会导致液体内部微小气泡核急速形成、震荡、生长并收缩至崩溃,气泡崩溃时,会使液体微粒之间发生猛烈撞击,在周围极小空间中产生瞬间的高温高压,并伴随着强烈的冲击波和强液体剪切力.

图4 直接加热法制备GQDs和氧化石墨烯[27]
自下而上法虽然操作简单,原料便宜,反应时间短,不需要特殊设备和苛刻的条件,但是这种方法产率较低,产物边缘不光滑,并且所制备的GQDs结晶度普遍不高,大多为无定型结构的碳,在光学中有广泛的应用,但是其电子性能普遍较差.
2 应用
随着对GQDs 研究的深入,其潜在应用范围也在不断扩大. 目前,GQDs在成像技术、分析检测和光催化剂等方面表现出很好的应用前景.
2.1 细胞成像

图5 GQDs用于HeLa细胞在明场和405 nm激发下的成像[11]
Figure 5 Two-photo imaging for HeLa cells using GQDs under bright field and 405 nm excitation[11]
2.2 石墨烯量子点在分析化学中的应用
2.2.1 荧光淬灭法离子检测 由于GQDs具有优异的光学性能(高荧光强度、抗光漂白性、发光颜色可调等)受到了广泛关注,并被广泛应用于金属离子检测、阴离子检测、有机小分子检测及生物分子检测等方面的研究. 与半导体量子点和碳点一样,GQDs通过与待测物的作用,改变表面电子空穴对之间的复合效率,通过电子转移或能量转移,使GQDs本身的荧光增强或猝灭,实现对待测物的定性或定量分析,在荧光光谱分析应用中也表现出良好的前景. 例如,DONG等[30]利用GQDs构建了一种绿色、灵巧的荧光传感器,用于检测饮用水中的氯离子含量,其中,GQDs的制备方法为热解柠檬酸,产物中不完全碳化的柠檬酸可对氯离子有很好的选择性响应,一些常见的金属离子对测定结果无干扰. 另外,采用同样方法合成的GQDs却对Hg2+有很好的响应[31],并建立了一种测定水中Hg2+的方法. 同时,利用类似的方法制备的GQDs还有用于检测Fe3+,所不同的是,对该GQDs进行了氮掺杂处理[32-33]. HUANG等[34]利用混酸n(H2SO4):n(HNO3) =1∶3)对碳纤维超声处理2 h,然后在150 ℃下回流24 h制备的GQDs对过渡金属离子有响应. 但是,这种方法只可检测大部分过渡金属离子,很难选择性检测某种特定的金属离子. WANG等[35]利用水热法处理氧化石墨烯制备了GQDs,实现了对水样中Cu2+的特异性检测,检测线性范围为0~15 mmol/L,检出限为0.226 mmol/L. 此外,利用不同方法制备的GQDs研究Ag+和Eu3+的响应[36-37]. 可以看出,通过不同方法合成的GQDs,对不同分析物有不同的响应,这可能与其表面的功能基团或基团排序有关,深层机理讨论还需要更深入的研究.
以上测定离子的方法中,多数基于离子和GQDs之间的电子转移,从而使荧光猝灭,基于能量转移的方法,大多是用于检测具有共轭结构的有机小分子. 其中,FAN等[38]利用荧光能量共振转移猝灭来测定溶液中2,4,6-三硝基甲苯(TNT). 检测机理为,TNT通过π-π堆叠吸附在未修饰的GQDs表面,TNT可抑制未修饰GQDs的荧光发射,加入TNT的质量浓度(4.95×10-4~ 1.82×10-1g/L)和GQDs的荧光猝灭强度呈线性关系,检出限可达到4.95×10-4g/L. 基于类似的原理,LI等[39]将GQDs用于检测苦味酸,其线性范围为0.1~15 μmol/L,检出限达到0.091 μmol/L.
2.2.2 荧光恢复法传感器 荧光猝灭法的选择性一般不高,研究人员利用GQDs发展了荧光恢复法. 其中,BAI等[37]通过水热法制备了GQDs,设计了一种巧妙的荧光恢复传感器,首先,用Eu3+将GQDs的荧光猝灭(可能是由于Eu3+可使GQDs发生团聚),然后通过Eu3+和磷酸盐的特异性结合,构建了一种选择性好、响应时间短和灵敏度高的荧光传感器. 该传感器对磷酸盐的线性响应范围为(0.5~190 μmol/L),检出限为0.1 μmol/L. 随后,他们又以GQDs为基础构建了一种免标记的葡萄糖传感器[40]. 将硼酸取代双吡啶盐加入GQDs体系中,这时GQDs的荧光强度发生猝灭,再加入葡萄糖置换出硼酸取代双吡啶盐,使GQDs的荧光强度得以恢复,然后根据葡萄糖的浓度和荧光恢复的强度呈线性关系,建立一种新颖的葡萄糖测定方法. 基于相同的原理,他们还将配体换成蛋白、将结合物换成了Zr4+,实现了GQDs对蛋白质的检测[41].
2.2.3 电化学传感器 碳纳米材料具有较好的导电性、大的比表面积和宽的电位窗口,同时碳纳米材料还对许多氧化还原反应具有较高的电催化活性,目前已经被广泛用于修饰电极的制备. 本课题组利用石墨烯基修饰电极分别测试了核酸碱基(腺嘌呤和鸟嘌呤)[42]、神经递质(多巴胺和尿酸)[43]、中草药的有效成分(靛玉红和芦丁)[44-45]以及葡萄糖[46]. GQDs在电化学方面也有较多的应用,例如:RAZMI等[47]利用水热法制备GQDs,并用于在玻碳电极上固定葡萄糖氧化酶,从而得到了葡萄糖氧化酶的直接电化学信号,进而对人体血清中葡萄糖浓度进行了测定,其线性范围为5~1 270 μmol/L,检出限为1.73 μmol/L. WANG等[48]利用微波辅助回流制备GQDs,通过酰胺化固定在预处理的四氧化三铁纳米颗粒上,用于固定抗体和Cu-去铁蛋白,构建“夹心式”的鸟类白血病病毒的免疫传感器. 在这里,GQDs主要起到信号放大的作用,通过在Fe3O4表面固定GQDs,进而可以固定更多的抗体和Cu-去铁蛋白,从而提高了检测的灵敏度. 另外,他们还将同样方法制备的GQDs滴涂在玻碳电极表面[49],进而电沉积纳米金,构建了GQDs和纳米金修饰玻碳电极,用于鱼样中孔雀石绿的检测,线性范围为4.0×10-7~1.0×10-5μmol/L,检出限为1.0×10-7mol/L. 由于GQDs可以很好地和单链DNA相互作用,ZHAO等[50]将GQDs与特定序列的DNA共同修饰到热解石墨电极表面,以铁氰化钾为电化学探针,构建了一种可用于检测目标DNA和目标蛋白质的电化学传感器. 另外,ZHANG[51]等发现,GQDs还具有过氧化物酶的活性,通过共价交联方法可将其固定到电极表面,并用于H2O2的检测.
2.2.4 电化学发光性能 研究表明,GQDs还具有电化学发光性能[52],其电化学发光机理和半导体量子点(如CdSe等)的发光机理相似,在过硫酸根存在的条件下,通过电化学激发产生自由基,从而使GQDs产生激发态,达到电化学发光的目的. 通过加入半胱氨酸作为掩蔽剂的方法,该电化学发光还可以被Cd2+选择性猝灭,基于此可以构建一种电化学发光检测Cd2+的方法,其检出限为13 nmol/L. LU等[53]通过水热法合成GQDs,并用单链DNA固定在SiO2表面,发现在H2O2存在下GQDs的阳极电致发光现象,并用于三磷酸腺苷的电致发光检测,检出限为5 pmol/L.
2.2.5 其他传感器 作为一种新型碳基纳米材料,GQDs还在其他领域有着广泛的应用. 其中,ZHOU等[54]基于GQDs表面丰富的功能基团构建了一种新颖的分子印迹荧光传感器. TIAN等[55]制备了GQDs/硅纳米线复合物,用于构建微囊藻毒素的光电转换传感器,将GQDs引入到硅纳米线表面,可以明显提高传感器的光电响应,在检测水样中微囊藻毒素的含量时,线性范围为0.1~10 μg/L,检出限为0.055 μg/L.
3 结论与展望
目前,GQDs的发光机理还是一个开放性的课题,尽管现在有电子复合辐射、碳烯结构等理论的提出,但是不同条件下制备的GQDs其发光性质也不同. 另外,GQDs有一个重要性质是其最大发射波长会随着激发波长的改变而改变,提出的理论主要是基于GQDs粒径分布和表面态不同所导致的结果. 但是,研究也证明了有一些不同的现象发生. 例如,不同粒径GQDs的最大发射波长并不随着激发波长的改变而改变,这是值得深入探讨的课题,这可为解释量子点的发光机理提供参考.
[1] JEONG J,JUNG J,CHIO M,et al. Color-tunable photoluminescent fullerene nanoparticles[J]. Advanced Matererials,2012,24(15):1999-2003.
[2] LI L,WU G,YANG G,et al. Focusing on luminescent graphene quantum dots:current status and future perspectives[J]. Nanoscale,2013,5(10):4015-4039.
[3] LIN L,RONG M,LUO F,et al. Luminescent graphene quantum dots as new fluorescent materials for environmental and biological applications[J]. Trends in Analytical Chemistry,2014,54:83-102.
[4] 王娇娇,冯苗,詹红兵. 石墨烯量子点的制备[J]. 化学进展,2013,25(1):86-94.
WANG J J,FENG M,ZHAN H B. Advances in preparation of graphene quantum dos[J]. Progress in Chemistry,2013,25(1):86-94.
[5] CUI R,LIU C,SHEN J,et al. Gold nanoparticle-colloidal carbon nanosphere hybrid material:preparation,characterization,and application for an amplified electrochemical immunoassay[J]. Advanced Functional Materials,2008,18(15):2197-2204.
[6] DONG X,MI X,ZHAO W,et al. CdS nanoparticles functionalized colloidal carbon particles:preparation,characterization and application for electrochemical detection of thrombin[J]. Biosensors and Bioelectronics,2011,26(8):3654-3659.
[7] ZHU X,ZHAO T,NIE Z,et al. Non-redox modulated fluorescence strategy for sensitive and selective ascorbic acid detection with highly photoluminescent nitrogen-doped carbon nanoparticles via solid-state synthesis[J]. Analy-tical Chemistry,2015,87(16):8524-8530.
[8] ZHU X,ZHAO T,NIE Z,et al. Nitrogen-doped carbon nanoparticle modulated turn-on fluorescent probes for histidine detection and its imaging in living cells[J]. Nanoscale,2016,8(4):2205-2211.
[9] PAN D,ZHANG J,LI Z,et al. Hydrothermal route for cutting graphene sheets into blue-luminescent graphene quantum dots[J]. Advanced Materials,2010,22(6):734-738.
[10] PAN D,GUO L,ZHANG J,et al. Cutting sp2clusters in graphene sheets into colloidal graphene quantum dots with strong green fluorescence[J]. Journal of Materials Chemi-stry,2012,22(8):3314-3318.
[11] ZHU X,XIAO X,ZUO X,et al. Hydrothermal preparation of photoluminescent graphene quantum dots characterized excitation-independent emission and its application as a bioimaging reagent[J]. Particle & Particle Systems Cha-racterization,2014,31(7):801-809.
[12] ZHU X,ZUO X,HU R,et al. Hydrothermal synthesis of two photoluminescent nitrogen-doped graphene quantum dots emitted green and khaki luminescence[J]. Materials Chemistry and Physics,2014,147(3):963-967.
[13] KOSYNKIN D,HIGGINBOTHAM A,SINITSKII A,et al. Longitudinal unzipping of carbon nanotubes to form graphene nanoribbons[J]. Nature,2009,458(7240):872-876.
[14] ZHU S,ZHANG J,QIAO C,et al. Strongly green-photoluminescent graphene quantum dots for bioimaging applications[J]. Chemical Communications,2011,47(24):6858-6860.
[15] LIU Q,GUO B,RAO Z,et al. Strong two-photon-induced fluorescence from photostable,biocompatible nitrogen-doped graphene quantum dots for cellular and deep-tissue imaging[J]. Nano Letters,2013,13(6):2436-2441.
[16] BAO L,ZHANG Z,TIAN Z,et al. Electrochemical tuning of luminescent carbon nanodots:from preparation to luminescence mechanism[J]. Advanced Materials,2011,23(48):5801-5806.
[17] LI Y,HU Y,ZHAO Y,et al. An electrochemical avenue to green-luminescent graphene quantum dots as potential electron-acceptors for photovoltaics[J]. Advanced Materials,2011,23(6):776-780.
[18] LI Y,ZHAO Y,CHENG H,et al. Nitrogen-doped graphene quantum dots with oxygen-rich functional groups[J]. Journal of the American Chemical Society,2011,134(1):15-18.
[19] SHINDE D,PILLAI V. Electrochemical preparation of luminescent graphene quantum dots from multiwalled carbon nanotubes[J]. Chemistry-A European Journal,2012,18(39):12522-12528.
[20] ZHANG M,BAI L,SHANG W,et al. Facile synthesis of water-soluble,highly fluorescent graphene quantum dots as a robust biological label for stem cells[J]. Journal of Materials Chemistry,2012,22(15):7461-7467.
[21] ANANTHANARAYANAN A,WANG X,ROUTH P,et al. Facile synthesis of graphene quantum dots from 3D graphene and their application for Fe3+sensing[J]. Advanced Functional Materials,2014,24(20):3021-3026.
[22] PENG J,GAO W,GUPTA B K,et al. Graphene quantum dots derived from carbon fibers[J]. Nano Letters,2012,12(2):844-849.
[23] DONG Y,CHEN C,ZHENG X,et al. One-step and high yield simultaneous preparation of single-and multi-layer graphene quantum dots from CX-72 carbon black[J]. Journal of Materials Chemistry,2012,22(18):8764-8766.
[24] SUN Y,WANG S,LI C,et al. Large scale preparation of graphene quantum dots from graphite with tunable fluore-scence properties[J]. Physical Chemistry Chemical Phy-sics,2013,15(24):9907-9913.
[25] SWAIN A,LI D,BAHADUR D. UV-assisted production of ferromagnetic graphitic quantum dots from graphite[J]. Carbon,2013,57:346-356.
[26] LI L,YAN X. Colloidal graphene quantum dots[J]. The Journal of Physical Chemistry Letters,2010,1(17):2572-2576.
[27] DONG Y,SHAO J,CHEN C,et al. Blue luminescent graphene quantum dots and graphene oxide prepared by tuning the carbonization degree of citric acid[J]. Carbon,2012,50(12):4738-4743.
[28] TANG L,JI R,CAO X,et al. Deep ultraviolet photoluminescence of water-soluble self-passivated graphene quantum dots[J]. ACS Nano,2012,6(6):5102-5110.
[29] GOKHALE R,SINGH P. Blue luminescent graphene quantum dots by photochemical stitching of small aromatic molecules:fluorescent nanoprobes in cellular imaging[J]. Particle & Particle Systems Characterization,2014,31(4):433-438.
[30] DONG Y,LI G,ZHOU N,et al. Graphene quantum dot as a green and facile sensor for free chlorine in drinking water[J]. Analytical Chemistry,2012,84(19):8378-8382.
[31] CHAKRABORTI H,SINHA S,GHOSH S,et al. Interfacing water soluble nanomaterials with fluorescence chemosensing:graphene quantum dot to detect Hg2+in 100% aqueous solution[J]. Materials Letters,2013,97:78-80.
[32] JU J,CHEN W. Synthesis of highly fluorescent nitrogen-doped graphene quantum dots for sensitive,label-free detection of Fe(III) in aqueous media[J]. Biosensors and Bioelectronics,2014,58:219-225.
[33] VAN TAM T,TRUNG B,KIM H,et al. One-pot synthesis of N-doped graphene quantum dots as a fluorescent sensing platform for Fe3+ions detection[J]. Sensors and Actuators B:Chemical,2014,202:568-573.
[34] HUANG H,LIAO L,XU X,et al. The electron-transfer based interaction between transition metal ions and photoluminescent graphene quantum dots (GQDs):a platform for metal ion sensing[J]. Talanta,2013,117:152-157.
[35] WANG F,GU Z,LEI W,et al. Graphene quantum dots as a fluorescent sensing platform for highly efficient detection of copper (II) ions[J]. Sensors and Actuators B:Chemical,2014,190:516-522.
[36] RAN X,SUN H,PU F,et al. Ag Nanoparticle-decorated graphene quantum dots for label-free,rapid and sensitive detection of Ag+and biothiols[J]. Chemical Communications,2013,49(11):1079-1081.
[37] BAI J,ZHANG L,LIANG R,et al. Graphene quantum dots combined with europium ions as photoluminescent probes for phosphate sensing[J]. Chemistry-A European Journal,2013,19(12):3822-3826.
[38] FAN L,HU Y,WANG X,et al. Fluorescence resonance energy transfer quenching at the surface of graphene quantum dots for ultrasensitive detection of TNT[J]. Talanta,2012,101:192-197.
[39] LI Z,WANG Y,NI Y,et al. A sensor based on blue luminescent graphene quantum dots for analysis of a common explosive substance and an industrial intermediate,2,4,6-trinitrophenol[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2015,137:1213-1221.
[40] LI Y,ZHANG L,HUANG J,et al. Fluorescent graphene quantum dots with a boronic acid appended bipyridinium salt to sense monosaccharides in aqueous solution[J]. Chemical Communications,2013,49(45):5180-5182.
[41] WANG Y,ZHANG L,LIANG R,et al. Using graphene quantum dots as photoluminescent probes for protein kinase sensing[J]. Analytical Chemistry,2013,85(19):9148-9155.
[42] ZHU X,ZENG L,XU M,et al. A glassy carbon electrode modified with electrochemically reduced graphene for simultaneous determination of guanine and adenine[J]. Analytical Methods,2012,4(9):2935-2939.
[43] ZHU X,LIANG Y,ZUO X,et al. Novel water-soluble multi-nanopore graphene modified glassy carbon electrode for simultaneous determination of dopamine and uric acid in the presence of ascorbic acid[J]. Electrochimica Acta,2014,143:366-373.
[44] ZHU X,JIAO Q,ZHANG C,et al. Electropolymerization of graphene and 5-[o-(4-bromine amyloxy) phenyl]-10,15,20-triphenylporphrin (o-BrPETPP) composite film electrode for the electrocatalytic oxidation of indirubin[J]. Journal of Electroanalytical Chemistry,2012,681:133-138.
[45] ZHU X,JIAO Q,ZUO X,et al. An electrochemical sensor based on carbon nano-fragments and β-cyclodextrin composite-modified glassy carbon electrode for the determination of Rutin[J]. Journal of the Electrochemical Society,2013,160(10):H699-H703.
[46] ZHU X,JIAO Q,ZHANG C,et al. Amperometric nonenzymatic determination of glucose based on a glassy carbon electrode modified with nickel (II) oxides and graphene[J]. Microchimica Acta,2013,180(5/6):477-483.
[47] RAZMI H,MOHAMMADREZAEI R. Graphene quantum dots as a new substrate for immobilization and direct electrochemistry of glucose oxidase:application to sensitive glucose determination[J]. Biosensors and Bioelectronics,2013,41:498-504.
[48] WANG X,CHEN L,SU X,et al. Electrochemical immunosensor with graphene quantum dots and apoferritin-encapsulated Cu nanoparticles double-assisted signal amplification for detection of avian leukosis virus subgroup J[J]. Biosensors and Bioelectronics,2013,47:171-177.
[49] HOU J,BEI F,WANG M,et al. Electrochemical determination of malachite green at graphene quantum dots-gold nanoparticles multilayers-modified glassy carbon electrode[J]. Journal of Applied Electrochemistry,2013,43(7):689-696.
[50] ZHAO J,CHEN G,ZHU L,et al. Graphene quantum dots-based platform for the fabrication of electrochemical biosensors[J]. Electrochemistry Communications,2011,13(1):31-33.
[51] ZHANG Y,WU C,ZHOU X,et al. Graphene quantum dots/gold electrode and its application in living cell H2O2detection[J]. Nanoscale,2013,5(5):1816-1819.
[52] LI L,JI J,FEI R,et al. A facile microwave avenue to electrochemiluminescent two-color Graphene quantum dots[J]. Advanced Functional Materials,2012,22(14):2971-2979..
[53] LU J,YAN M,GE L,et al. Electrochemiluminescence of blue-luminescent graphene quantum dots and its application in ultrasensitive aptasensor for adenosine triphosphate detection[J]. Biosensors and Bioelectronics,2013,47:271-277.
[54] ZHOU Y,QU Z,ZENG Y,et al. A novel composite of graphene quantum dots and molecularly imprinted polymer for fluorescent detection of paranitrophenol[J]. Biosensors and Bioelectronics,2014,52:317-323.
[55] TIAN J,ZHAO H,QUAN X,et al. Fabrication of graphene quantum dots/silicon nanowires nanohybrids for photoelectrochemical detection of microcystin-LR[J]. Sensors and Actuators B:Chemical,2014,196:532-538.
Synthesis and Applications of Fluorescent Graphene Quantum Dots
LIANG Yong*, ZHU Xiaohua, NAN Junmin*
(School of Chemistry and Environment, South China Normal University, Guangzhou 510006, China)
Due to the unique quantum connement and edge effects, graphene quantum dots (GQDs) have exhibited extraordinary properties and potential applications. Herein, the advances on the preparation of GQDs in recent years are summarized, including the “top to down” routine from the graphite sheets through hydrothermal, electrochemical, and chemical oxidation methods, and the “down to up” routine from the carbon-contained organic molecules through solvochemical, sonochemical, and microwave methods. In addition, the applications of the GQDs in optical imaging, biosensor, and electrochemistry analytical fields are introduced. And based on the investigation status of the fluorescent mechanism of GQDs, it is pointed out that combining with the preparation of GQDs, the optical properties of GQDs should be especially studied in the future.
2016-03-15 《华南师范大学学报(自然科学版)》网址:http://journal.scnu.edu.cn/n
国家自然科学基金项目(21645004)
*通讯作者:梁勇,教授,Email:liangy@scnu.edu.cn;南俊民,教授,Email:jmnan@scnu.edu.cn.
O613.71
A
1000-5463(2017)05-0001-08
【中文责编:谭春林 英文审校:李海航】
