胎鼠皮肤无瘢痕愈合培养液优化及皮肤细胞增殖活跃区研究
2017-11-02王海涛姜仁军李树伟
王海涛 姜仁军 李树伟
843300新疆阿拉尔,塔里木盆地生物资源保护利用兵团重点实验室 塔里木大学生命科学学院
·论著·
胎鼠皮肤无瘢痕愈合培养液优化及皮肤细胞增殖活跃区研究
王海涛 姜仁军 李树伟
843300新疆阿拉尔,塔里木盆地生物资源保护利用兵团重点实验室 塔里木大学生命科学学院
目的 优化昆明远交系(KM)胎鼠皮肤无瘢痕愈合模型的培养液,定位并分析皮肤创伤愈合中细胞增殖活跃区。方法 取60只胎龄15 d小鼠背部皮片180块,用无菌微创器在皮片上统一造创,随机等分到6组培养液中培养3 d,包括高糖改良Eagle培养基(DMEM)组、DMEM+5%胎牛血清(FBS)组、DMEM+10%FBS组、低糖Eagle培养基(MEM)组、MEM+5%FBS组、MEM+10%FBS组。HE染色后观察各组皮肤创口愈合情况,筛选最适培养条件。在最适培养条件下采用EdU细胞标记物定位皮肤创口愈合处细胞增殖活跃区,并用免疫荧光检测其中AP⁃1蛋白表达。结果 胎鼠微创皮片培养3 d后,DMEM组、DMEM+5%FBS组、DMEM+10%FBS组、MEM组、MEM+5%FBS组、MEM+10%FBS组皮片愈合率分别为0、3.33%、6.67%、3.33%、46.67%、26.67%,6组皮片愈合率差异有统计学意义(χ2=41.39,P<0.05)。两两比较显示,MEM+5%FBS组皮片愈合率显著高于除MEM+ 10%FBS组外的其他4组(均P<0.01)。logistic回归分析显示,MEM(OR=11.717,95%CI 3.274~41.934,P<0.001)及FBS浓度(5%FBS:OR=24.625,95%CI 3.027~200.299,P=0.003;10%FBS:OR=13.449,95%CI 1.618~111.813,P=0.016)均是促进胎鼠微创皮片愈合的因素。在MEM+5% FBS培养条件下,真皮和表皮愈合形态最好,且创面处表皮无增厚现象。EdU细胞增殖标记分析显示,胎鼠皮肤的真皮乳头层和表皮基底层是创面愈合过程中两个主要的细胞增殖活跃区,同时AP⁃1蛋白在这两个细胞增殖活跃区也有大量表达。结论 MEM+5%FBS为体外培养胎鼠皮肤创伤愈合的最适培养液。胎鼠皮肤的真皮乳头层和表皮基底层是皮肤创伤愈合中两个主要的细胞增殖活跃区,在创面愈合过程中起到重要作用。
伤口愈合;瘢痕;转录因子AP⁃1;无瘢痕愈合;胎鼠
无瘢痕愈合作为机体创伤后最理想的愈合方式,其发生机制一直未阐明。到目前为止,关于胚胎皮肤无瘢痕愈合机制的研究主要以体内为主,并未成功建立体外无瘢痕愈合模型来进行该机制的研究。激活蛋白1(activator protein⁃1,AP⁃1)作为细胞核中一个重要的转录因子,不仅参与细胞凋亡,也参与介导干细胞的增殖和分化[1]。AP⁃1蛋白的激活受很多因素调控,针对不同的组织细胞,AP⁃1蛋白可以激活相应的基因表达,参与介导该组织细胞的增殖和分化等细胞生理功能[2⁃3]。但在胎鼠创面愈合过程中,AP⁃1蛋白是否表达,同时胚胎皮肤创面无瘢痕愈合机制是否与AP⁃1的表达有关尚不清楚。本研究利用不同类型的基础培养液和不同浓度的胎牛血清进行配比,筛选优化胎鼠皮肤无瘢痕愈合模型的体外培养液,并使用细胞增殖标记物5⁃乙炔基⁃2′⁃脱氧尿苷(EdU)荧光定位皮肤生长代谢活跃区,对AP⁃1蛋白的表达进行鉴定,为后期建立胎鼠皮肤人工微创体外愈合模型奠定基础,同时为研究胚胎皮肤无瘢痕愈合机制提供新的思路。
材料与方法
一、主要试剂与仪器
兔抗小鼠AP⁃1一抗(美国Amresco公司),异硫氰酸荧光素(FITC)标记的二抗、基础培养液DMEM(高糖改良Eagle培养基)和MEM(低糖Eagle培养基)(美国Gibco公司),青∕链霉素浓缩液(重庆西南药业股份有限公司),胎牛血清(FBS,美国Sigma公司),EdU keyFluor488荧光检测试剂盒(武汉三鹰生物技术有限公司),其他常规试剂山羊封闭血清、4′,6⁃二脒基⁃2⁃苯基吲哚(DAPI)染液、杜氏磷酸缓冲液(DPBS)、Triton X⁃100原液等(杭州四季青生物工程材料有限公司)。倒置荧光可视化显微镜(德国Zeiss公司)。
二、方法
1.胎鼠皮肤微创后培养:7周龄SPF级健康昆明(KM)远交系小鼠(SCXK 2012⁃0007)由第四军医大学实验动物中心提供,雌雄各10只,体重40~60 g(批号0014379)。塔里木大学实验动物中心定期对小鼠进行致病原检测以确保孕鼠符合本试验要求,试验小鼠饲养在通风洁净区,均采用SPF级洁净鼠粮饲养。小鼠采用断颈法处死,并严格遵守中国实验动物伦理保护法。实验中同一天受孕的母鼠6只,取孕龄为15 d的6只KM母鼠并处死,浸泡于75%乙醇10 min,超净工作台内将子宫取出,共取出63只胎鼠。随机取60只胎鼠(另3只胎鼠取其皮肤直接包埋制冰冻切片,观察胎鼠皮肤正常结构),用眼科微型手术器械小心剥离胎鼠背部皮肤,每只胎鼠于解剖显微镜下分成等面积的3块皮片,共获得180块皮片。用无菌微创器在皮片上统一造创,微创口直径统一为2 mm。用显微外科镊把人工微创胎鼠皮片随机转移到6组培养液中,分别为DMEM组、DMEM+5%FBS组、DMEM+10%FBS组、MEM组、MEM+5%FBS组、MEM+10%FBS组,此外各组培养液中再加入10%青∕链霉素稀释液100 μl。每组有3个相同培养皿,每个培养皿培养10块皮片,其中随机选取1个培养皿加入20 μmol∕L EdU干细胞标记物100 μl,最终每个培养皿中2 ml,在37℃、5%CO2培养箱中培养3 d。皮片OCT包埋后制作冰冻切片,厚度6 μm,-20℃冰箱保存备用。
2.胎鼠皮肤切片的HE染色:从-20℃冰箱中取出胎鼠皮肤冰冻切片,HE染色,中性树胶封片,显微镜下拍照观察。
3.胎鼠皮肤干细胞增殖标记染色:皮片培养3 d后,显微镜下观察皮肤愈合情况,选出愈合最好的标记组,其中每张EdU标记培养的胎鼠皮肤组织切片滴加1 ml 4%甲醛室温固定30 min,3%牛血清蛋白(BSA)漂洗2次,每次5 min,加入1 ml 0.5% Triton X⁃100透膜20 min后,再使用3%BSA漂洗2次,每次5 min,去除渗透剂。每张玻片上加入0.5 ml Key Fluor488 Click⁃iT反应混合物(根据说明书现用现配),室温避光孵育30 min。弃去Click⁃iT反应混合物,使用3%BSA漂洗2次,每次5 min,去除反应混合物,滴加抗荧光猝灭剂,盖玻片封片,倒置荧光显微镜暗房拍照。其中增殖细胞的细胞核可被EdU标记,形成绿色荧光,而未增殖细胞的细胞核,可被Hoechst标记,发出红色荧光。
4.胎鼠皮肤切片的免疫荧光检测:冰冻切片4%甲醛固定30 min,PBS(pH 7.2~7.4)清洗3次,1%Triton X⁃100透膜20 min,3%BSA和10%山羊血清各250 μl混合滴入冰冻切片,放入湿盒4℃避光孵育1 h。倒去孵育液,滴加兔抗小鼠AP⁃1一抗(1∶150稀释)100 μl,以PBS代替一抗做阴性对照,4℃湿盒孵育过夜,PBS清洗3次,滴加山羊抗兔FITC荧光二抗(1∶200稀释)200 μl及DAPI,4℃湿盒避光孵育1 h,PBS冲洗3次,抗荧光猝灭剂封片,倒置荧光显微镜下拍照并分析数据。
5.统计分析方法:利用图像分析软件Motic统计胎鼠微创皮片愈合数目,采用SPSS16.0软件进行统计分析,χ2检验分析各组愈合率差异,logistic回归模型分析胎鼠微创皮片愈合的影响因素,P<0.05为差异有统计学意义。
结果
一、正常胎鼠皮肤结构观察
KM胎鼠皮肤组织切片HE染色显示(图1),胎鼠皮肤由表皮和真皮构成,其中真皮紧贴表皮的基底层,并由乳头层和网状层两部分构成,真皮层中含有大量成纤维细胞和少量淋巴细胞及巨噬细胞(图1A)。在无激发光通道条件下,细胞核DAPI荧光染色显示,胎鼠表皮由颗粒层、棘层和基底层构成(图1B)。
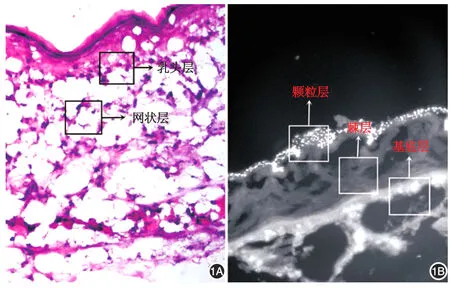
图1 新鲜分离的胎鼠皮肤结构 1A:胎鼠真皮结构,包括乳头层和网状层,含有大量成纤维细胞和少量淋巴细胞及巨噬细胞(HE×100);1B:细胞核DAPI荧光染色显示,胎鼠表皮由颗粒层、棘层和基底层构成(×400)
二、胎鼠皮片人工微创口愈合形态学观察
胎鼠微创皮片培养3 d时,对比相同FBS浓度下不同基础培养液组胎鼠背部皮片创口愈合情况发现,DMEM组的胎鼠皮肤创口总体愈合不好(图2A~2C),创口几乎无愈合迹象。添加FBS后,真皮网状层有不同程度延长,但表皮一直未愈合。MEM组胎鼠皮肤创口同样没有愈合迹象(图2D),添加FBS后,胎鼠皮肤表皮层发生交互融合。5%FBS+MEM组创面愈合处真皮和表皮贴合紧密,真皮部位无缺损(图2E e区),10%FBS+ MEM组创面愈合处表皮愈合无增厚现象,真皮层延伸并紧密相连,但愈合薄弱,与表皮之间的空隙较大(图2F f区)。
三、胎鼠微创皮片愈合最佳培养条件的筛选
以表皮和真皮同时愈合记为愈合,计算各组皮片愈合率。DMEM组、DMEM+5%FBS组、DMEM+ 10%FBS组、MEM组、MEM+5%FBS组、MEM+ 10%FBS组皮片愈合率分别为0、3.33%、6.67%、3.33%、46.67%、26.67%,6组间差异有统计学意义(χ2=41.39,P<0.05)。调整检验水准α=0.01并进行两两比较显示,MEM+5%FBS组皮片愈合率显著高于除MEM+10%FBS组外的其他4组(均P<0.01),且MEM+10%FBS组皮片愈合率亦显著高于DMEM组(均P<0.01)。采用logistic回归模型分析基础培养基的类型(DMEM或MEM)及FBS浓度对胎鼠微创皮片愈合的影响,结果显示,MEM(以DMEM为对照,OR=11.717,95%CI 3.274~41.934,P<0.001)及FBS浓度(以不添加FBS为对照,5% FBS:OR=24.625,95%CI 3.027~200.299,P= 0.003;10%FBS:OR=13.449,95%CI 1.618~111.813,P=0.016),均是促进胎鼠微创皮片愈合的因素。

图2 微创胎鼠皮肤在6种不同条件下培养3 d愈合形态学观察(HE×100) DMEM:高糖改良Eagle培养基,MEM:低糖Eagle培养基;De:真皮,Ep:表皮;e、f框内分别是图2E、2F创面愈合处;2A、2D:分别为DMEM组和MEM组,胎鼠皮肤人工微创口几乎无愈合迹象;2B、2C:分别为DMEM+5%胎牛血清(FBS)组和DMEM+10%FBS组,真皮网状层有不同程度的延长,但表皮一直未愈合;2E:MEM+5%FBS组,胎鼠皮肤创面愈合处(e区)真皮和表皮贴合紧密,真皮部位无缺损;2F:MEM+10%FBS组,胎鼠创面愈合处(f区)表皮愈合无增厚现象,真皮层延伸并紧密相连,但真皮部位愈合薄弱,且与表皮之间的空隙较大
四、胎鼠皮肤干细胞再生标记
选择MEM+5%FBS组行皮肤干细胞增殖标记染色。倒置荧光显微镜下观察,发现增殖细胞主要位于表皮基底层;创面左右两侧的真皮乳头层干细胞也大量增殖(图3A,白色箭头所指处绿色荧光区域),真皮乳头层中细胞大量增殖(图3B);皮片无创伤处乳头层细胞增殖活性强于基底层(图3C)。

图3 MEM+5%FBS组胎鼠皮肤创面愈合过程中EdU标记皮肤干细胞分裂增殖情况 De:真皮,Ep:表皮;白色虚线是胎鼠真皮和表皮的分界线,白色箭头为皮肤干细胞增殖活跃区。3A:胎鼠皮肤创面愈合处,干细胞增殖主要位于表皮基底层和真皮乳头层;3B:胎鼠皮肤外缘游离端,干细胞增殖亦主要位于真皮乳头层;3C:皮片无创伤处,乳头层细胞增殖活性强于基底层;3D:正常未人工造创皮片行Hoechst染色作为对照组,红色荧光为未增殖细胞的细胞核
五、AP⁃1在胎鼠皮肤无瘢痕愈合中的表达
MEM+5%FBS组胎鼠人工微创皮片中AP⁃1抗体免疫荧光染色结果见图4A~4C。胎鼠皮肤创口愈合处真皮细胞核(图4D)和表皮细胞核(图4E)中均见AP⁃1蛋白大量表达,同时创面愈合处表皮增厚,细胞增多,基底层细胞出现不对称分裂,并向真皮部突起,新分裂的细胞核形态和基底层细胞核形态不同,但同样都表达AP⁃1蛋白。阴性对照真皮层细胞中未出现AP⁃1蛋白的绿色荧光,只有细胞核被DAPI染成蓝色荧光(图4F)。
讨论
皮肤的瘢痕愈合一直是临床创面治疗中的主要问题,在目前物理和药物治疗手段下,皮肤创面愈合后的瘢痕可以缩小,但不能完全消除。研究显示[4⁃5],皮肤创面瘢痕的形成与巨噬细胞的炎症反应有密切关系,而胚胎时期机体免疫系统不完整,免疫力相对薄弱,受到创伤后不会发生急性炎症反应,不会形成肉芽组织,因此不会导致瘢痕增生。研究者检测不同胚胎时期和成体小鼠皮肤基因表达差异发现,胚胎晚期及胎鼠出生后一些促进创面愈合的基因表达下调,导致创面愈合达不到无瘢痕,而在胚胎时期一些具有调控干细胞增殖和分化的基因表达是上调的[6⁃7],因此调控干细胞增殖分化的基因表达差异可能是创面瘢痕形成的一个重要因素。
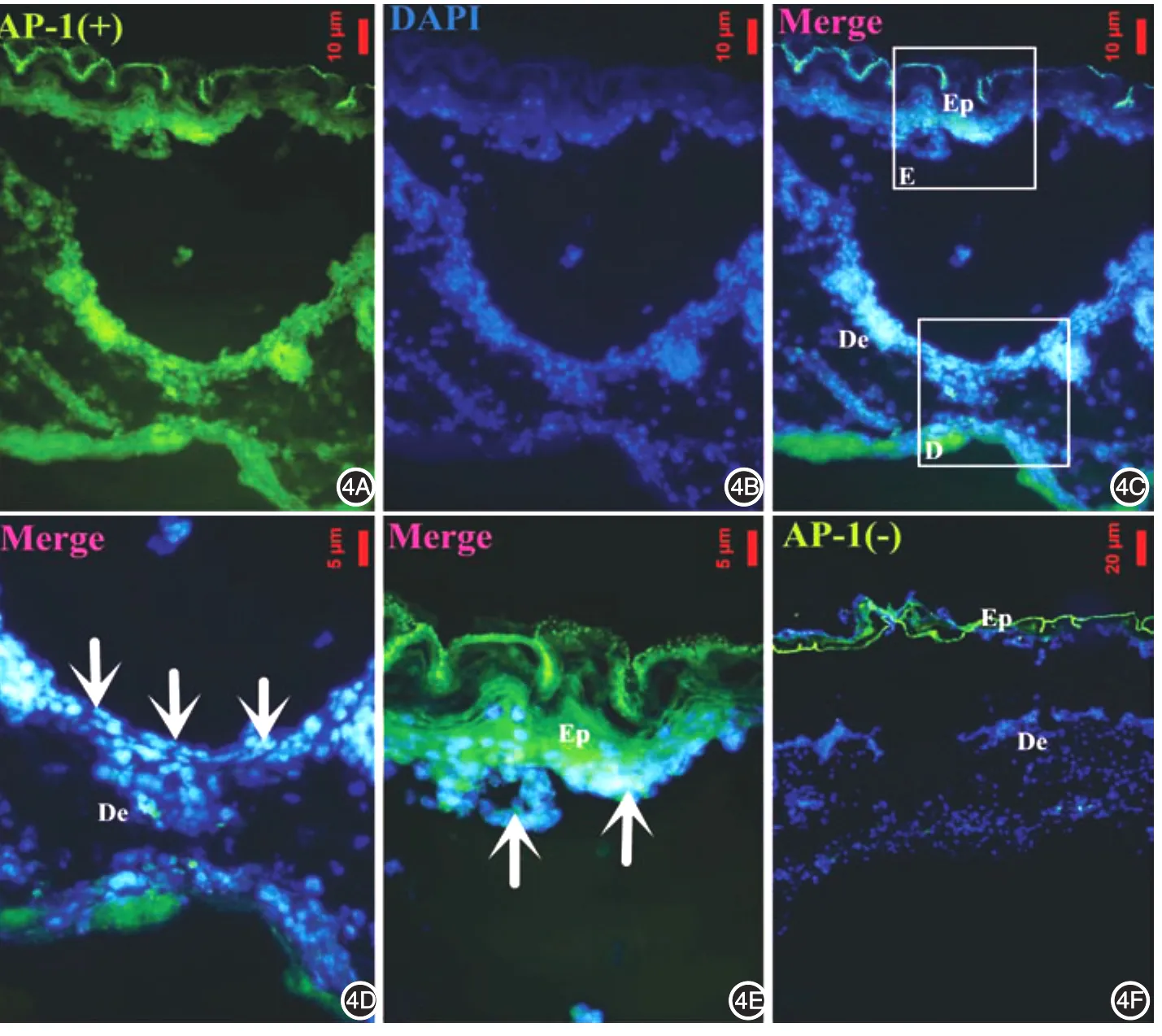
图4 MEM+5%FBS组胎鼠人工微创皮肤愈合过程中AP⁃1蛋白表达的鉴定 4A:胎鼠皮肤创口愈合处AP⁃1蛋白呈绿色荧光;4B:胎鼠皮肤创口愈合处细胞核经DAPI染色呈蓝色荧光;4C:AP⁃1蛋白绿色荧光与细胞核蓝色荧光叠加;4D、4E:分别为图4C中标记区域的局部放大,白色箭头所指处分别显示真皮和表皮部位均有AP⁃1蛋白的大量表达;4F:阴性对照
我们用显微外科解剖技术获取无菌且不含皮下组织的胎鼠皮肤,未经胰酶和胶原酶的消化处理,可较好地保留胎鼠皮片活性及修复功能。培养过程中游离的胎鼠皮片可以自我释放一些细胞生长因子,参与伤口修复[8⁃9],同时皮肤内部少量淋巴细胞也参与轻微炎症反应,它们之间进行一系列复杂的相互作用共同参与创面修复。我们观察正常胎鼠皮肤结构时,发现表皮仅由颗粒层、棘层和基底层构成。可能是因为胎鼠皮肤处于羊水环境中,角质层细胞脱落于羊水中而未被观察到,而透明层主要出现在四肢掌部,一般不出现在背部皮肤。
本研究分别采用MEM(低糖)与DMEM(高糖)2种培养液作为胎鼠皮肤创口愈合的外环境,以优化选择最适用于皮肤创口愈合的培养液。结果显示,DMEM组胎鼠皮片创口总体愈合不如MEM组,可能是高糖因素导致皮肤细胞代谢紊乱,降低细胞运输氧的能力,使创口不易愈合且易被细菌污染。此外,FBS中各种充足的营养成分及生长因子也可促进创面修复。本研究采用logistic回归模型分析显示,MEM及FBS浓度均是促进胎鼠微创皮片愈合的因素,同时结合倒置显微镜观察各组皮片愈合形态,认为MEM+5%FBS为胎鼠微创皮片愈合的最佳培养条件。
本研究中EdU标记荧光强信号区为胎鼠皮肤创面愈合处的真皮乳头层和表皮基底层,是表皮干细胞的存在区域,同时说明胎鼠皮肤的真皮乳头层也含有皮肤源干细胞,在皮肤创面愈合过程中可以进行创面的填充。AP⁃1蛋白作为细胞内一种重要的转录因子,在细胞增殖、分化、凋亡、炎症反应和胚胎发育等病理生理过程中起重要作用[10⁃11]。我们检测MEM+5%FBS组胎鼠皮片时发现,皮肤创面愈合中两个主要增殖活跃区,即真皮乳头层和表皮基底层均有AP⁃1蛋白的大量表达,说明这两个区域在胚胎皮肤损伤愈合过程中发挥重要作用。阴性对照组真皮层细胞中未出现AP⁃1蛋白的绿色荧光,可排除实验中的非特异性染色。其中表皮颗粒层出现绿色荧光,可能是因为表皮颗粒层由富含组氨酸的强嗜碱性蛋白颗粒组成,易与二抗荧光色素结合而引起非特异性着色。
综上所述,胎龄15 d的KM胎鼠皮肤创面最佳愈合培养液条件为MEM+5%FBS,而胎鼠皮肤的真皮乳头层和表皮基底层是创面愈合过程中两个主要的细胞增殖活跃区,其中的细胞可大量表达AP⁃1蛋白。本研究为建立体外胚胎皮肤创伤无瘢痕愈合模型奠定基础,为胚胎皮肤细胞增殖活跃区的定位及胚胎创伤无瘢痕愈合机制研究提供新的思路。
志谢塔里木大学生命科学学院、塔里木盆地生物资源保护利用兵团重点实验室提供实验平台,李树伟教授对本研究提供的支持
[1]Hess J,Angel P,Schorpp⁃Kistner M.AP⁃1 subunits:quarrel and harmony among siblings[J].J Cell Sci,2004,117(1):5965⁃5973.
[2]Ko WC,Chen BC,Hsu MJ,et al.Thrombin induced connective tissue growth factor expression in rat vascular smooth muscle cell via the PAR⁃1∕JNK∕AP⁃1 pathway[J].Acta Pharmacol Sin,2012, 33(1):49⁃56.
[3]Song MO,Lee CH,Yang HO,et al.Endosulfan upregulates AP⁃1 binding and ARE⁃mediated transcription via ERK1∕2 and p38 activation in HepG2 cells[J].Toxicology,2012,292(1):23⁃32.
[4]Das A,Sinha M,Datta S,et al.Monocyte and macrophage plasticity in tissue repair and regeneration[J].Am J Pathol, 2015,23(6):235⁃243.
[5]Biswas SK,Chittezhath M,Shalova IN,et al.Macrophage polarization and plasticity in health and disease[J].Immunol Res,2012,53(1∕2∕3):11⁃24.
[6]Lo DD,Zimmermann AS,Nauta A,et al.Scarless fetal skin wound healing update[J].Birth Defects Res C Embryo Today,2012,96(30):237⁃247.
[7]吴志远,郭晓瑞,黄海华,等.胎儿和成人皮肤相关基因的差异表达[J].中国组织工程研究与临床康复,2011,15(2):286⁃289.
[8]Bock O,Yu H,Zitron S,et al.Studies of transforming growth factors beta 1⁃3 and their receptorsⅠ andⅡ in fibroblast of keloids and hypertrophic scars[J].Acta Derm Venereol,2005,85(3):216⁃220.
[9]Akita S,Akino K,Hirano A.Basic fibroblast growth factor in scarless wound healing[J].Adv Wound Care(New Rochelle), 2013,2(2):44⁃49.
[10]Fisher GJ,Voorhees JJ.Molecular mechanisms of photoaging and its prevention by retinoic acid:ultraviolet irradiation induces MAP kinase signal transduction cascades that induce Ap⁃1⁃regulated matrix metalloproteinases that degrade human skin in vivo[J].J Investig Dermatol Symp Proc,1998,3(1):61⁃68.
[11]Takeuchi K,Motoda Y,Ito F.Role of transcription factor activator protein 1(AP1)in epidermal growth factor⁃mediated protection against apoptosis induced by a DNA⁃damaging agent[J].FEBS J, 2006,273(16):3743⁃3755.
中国麻风史料陈列馆、中国医学科学院皮肤病研究所史料陈列馆征集文物和史料启事
为真实记载中国麻风防治的发展历程,全方位展现中国医学科学院皮肤病医院、研究所(简称院所)60余载的历史变革和文化积淀,传承和发扬老一辈无私奉献的精神,院所决定筹建中国麻风史料陈列馆、院所史料陈列馆。即日起,面向社会各界广泛征集具有历史价值的文物和史料。
一、征集范围
1.反映院所各历史时期发展沿革、重大活动、科研成就、领导关怀及院所职工参加国内外重大活动等方面的重要文献、题词、图片、新闻报道、手稿、徽标、纪念册、音像制品、奖状、证书等。
2.国家领导人、社会知名贤达及重要外宾、杰出校友来院所参观、考察、访问或演讲时的题词、图片、新闻报道、音像制品等。
3.各类皮肤性病、麻风防治的图片、图表及文字说明,医、教、研、防、管等领域工作中使用过的办公用品、仪器设备、书籍教案、教学工具等实物。
4.反映中国麻风防治历程及成就,麻风受累者的医疗及生活状况等有历史价值的文物和史料。
二、征集方式及要求
1.文物和史料的征集采用捐赠、代管、借用等方式。
2.所有文物和史料请提供文字说明,含来源、史料载体、形成时间及其所涉及的人物、事件等要素。
3.文物和史料的征集欢迎直接送达;亦可通过电子传送、信函邮寄、预约拜访、登门征集等途径进行。
4.征集的文物和史料,均登记入册;一经采用,除在史馆陈列时标注捐赠者的姓名外,将授赠荣誉证书。
5.征集时间:长期征集。
三、联系方式
联系人:210042,南京玄武区蒋王庙街12号,中国医学科学院皮肤病研究所中心办公室(科研楼415室)诸萍,电话:025-85478032,传真:025⁃85424903,Email:zhup@ncstdlc.org。
Optimization of culture medium for scarless healing of fetal mouse wounds and analysis of regions with active cell proliferation
Wang Haitao,Jiang Renjun,Li Shuwei
Xinjiang Production&Construction Corps Key Laboratory of Protection and Utilization of Biological Resources in Tarim Basin,College of Life Sciences,Tarim University,Alaer 843300,Xinjiang,China
Li Shuwei,Email:xj_lsw@126.com
Objective To optimize the culture medium for scarless wound healing in outbred fetal Kunming(KM)mice,and to locate and preliminarily analyze the region with active cell proliferation. Methods After 6 pregnant mice were sacrificed at the gestational age of 15 days,a total of 180 skin grafts were obtained from the back of 60 fetal mice,and wounds on the skin grafts were made uniformly with minimally invasive sterile device.Then,these skin grafts with wounds were randomly and equally divided into 6 groups to be treated with high⁃glucose Dulbecco′s modified Eagle′s medium(DMEM),DMEM+5% fetal bovine serum(FBS),DMEM+10%FBS,low⁃glucose Eagle′s minimum essential medium(MEM), MEM+5%FBS,and MEM+10%FBS for 3 days,respectively.Then,these skin grafts were embedded in optimal cutting temperature(OCT)compound,and subjected to hematoxylin and eosin(HE)staining to select the optimal culture condition for wound healing.Under the optimal culture condition,the region with active cell proliferation was located by labeling and tracking cutaneous stem cells with 5⁃ethynyl⁃2⁃deoxyuridine(EdU),and activator protein⁃1(AP⁃1)expression was detected by immunofluorescent staining.Results After 3⁃day cultivation,wound healing rates significantly differed among the DMEM group,DMEM+5%FBS group,DMEM+10%FBS group,MEM group,MEM+5%FBS group and MEM+ 10%FBS group(0,3.33%,6.67%,3.33%,46.67%and 26.67%,respectively,χ2=41.39,P<0.05). Additionally,the MEM+5%FBS group showed a significantly higher wound healing rate than the other groups except the MEM+10%FBS group(all P<0.01).Logistic regression analysis showed that the type of basal medium(MEM:OR=11.717,95%CI:3.274-41.934,P<0.001)and FBS concentrations(5% FBS:OR=24.625,95%CI:3.027-200.299,P=0.003;10%FBS:OR=13.449,95%CI:1.618-111.813,P=0.016)were factors influencing fetal wound healing.Under the culture condition of 5%FBS+ MEM,the dermis and epidermis healed well without epidermal thickening.The cutaneous stem cell labeling technique showed that the papillary dermis and basal layer of the epidermis were the two major regions with active cell proliferation in the wound of fetal mouse skin.Moreover,AP⁃1 was expressed abundantly in these two regions as well.Conclusions The culture condition of 5%FBS+MEM is considered to be optimal for in vitro wound healing in fetal mice.The papillary dermis and basal layer of the epidermis are two major regions with active cell proliferation during wound healing in fetal mouse skin,and play important roles in wound healing process.
Wound healing;Cicatrix;Transcription factor AP⁃1;Scarless wound healing;Fetal mice
李树伟,Email:xj_lsw@126.com
10.3760∕cma.j.issn.0412⁃4030.2017.02.007
国家自然科学基金(31560685);塔里木大学研究生科研创新项目(TDGRI201521)
Fund programs:National Natural Science Foundation of China(31560685);Master Creation Project of Tarim University(TDGRI201521)
2016⁃05⁃13)
(本文编辑:周良佳 颜艳)
