两种化学预处理方法对小麦秸秆纤维素的影响
2017-11-01李春露崔志芳
杨 阳,李春露,崔志芳
(山东科技大学化学与环境工程学院,山东 青岛 266590)
两种化学预处理方法对小麦秸秆纤维素的影响
杨 阳,李春露,崔志芳*
(山东科技大学化学与环境工程学院,山东 青岛 266590)
纤维素在小麦秸秆中含量丰富,但因其结晶度高而不易改性。以小麦秸秆为原料,采用NaOH/硫脲/尿素水溶液法和乙二胺法分别对小麦秸秆纤维素进行预处理,采用正交实验对2种化学预处理方法进行优化,通过FTIR、XRD对红外光谱、结晶度、晶型的测定,比较了2种化学预处理方法对小麦秸秆纤维素的影响。结果表明,采用优化的NaOH/硫脲/尿素水溶液法(NaOH、硫脲、尿素的质量分数分别为8%、7%、6%),能使纤维素结晶度降低51%,晶型由纤维素Ⅰ变为纤维素Ⅱ;而采用优化的乙二胺法[乙二胺质量分数70%、液固比16∶1(mL∶g)、处理温度40 ℃、处理时间4 h],纤维素结晶度仅降低36%,且晶型未变,仍为纤维素Ⅰ。
纤维素;小麦秸秆;NaOH/硫脲/尿素水溶液法;乙二胺法;结晶度;晶型
随着石油资源的日益枯竭,研发以纤维素为原料的新精细化工产品将是21世纪化学工程研究领域的重要课题之一[1-3]。纤维素经过改性可得到更多具有优良性能的新材料,广泛应用于医药、服装、日用化工、吸附剂等各个领域[4-5]。目前,纤维素多从棉花中提取,因棉花应用广泛、需求量大,故原料成本较高。中国作为一个农业大国,农作物秸秆年产量近7亿t,且70%被焚烧得不到充分利用,而纤维素在秸秆中的含量高达40%~50%[6]。因此,从农作物秸秆中提取纤维素意义重大。
纤维素是结构非常致密、复杂的生物大分子,含有大量羟基,易形成致密氢键,结晶度高,这些都不利于其改性[1]。另外,纤维素具有不同晶型,以纤维素Ⅰ及Ⅱ最为常见:纤维素Ⅰ是天然存在的纤维素;纤维素Ⅱ是溶液中再生或者丝光化得到的结晶变体[7],是最稳定的多晶型纤维素[8],这些也影响了其进一步利用[9-10]。近年来,研究者通过各种预处理方法来改变纤维素结构(结晶度或晶型),如:物理方法(机械活化法、微波处理法、超声波处理法等[11-14])、化学方法(碱性氢氧化物水体系、氨类化合物体系、脂肪胺体系等[15-19])等。传统的氢氧化钠/水(NaOH/H2O)体系是化学法预处理纤维素最常用的体系,但它对分子质量较大的纤维素的溶解力较弱,且所需时间较长。陈明凤[20]研究了NaOH/H2O体系降低纤维素结晶度的能力,发现在最适条件下,30 min左右纤维素的结晶度几乎没有变化,25 h结晶度仅降低56%。
鉴于不同原料中纤维素经预处理后的结晶度不同,且有关预处理方法对小麦秸秆纤维素结晶度及晶型改变的报道也不够全面,作者以小麦秸秆为原料提取得到纤维素,利用NaOH/硫脲/尿素水溶液法和乙二胺法分别对其进行预处理,采用XRD测定其结晶度及晶型,采用FTIR测定其红外光谱,在优化2种化学预处理工艺的基础上,对2种预处理方法进行了比较,以期更有效地利用小麦秸秆纤维素资源。
1 实验
1.1 原料、试剂与仪器
小麦秸秆,山东诸城农村。采用碱抽提法[6]对小麦秸秆化学成分进行分析,其化学组成为:47%纤维素、22%半纤维素、24%木质素、7%杂质。
实验所用试剂均为国产分析纯。
DMAXRB-Ⅱ型X-射线衍射仪,日本理学;Nicolet 380型傅立叶变换红外光谱仪,美国Thermo electro;TGL-16C型台式离心机,中国湘仪;ZK-82B型真空干燥烘箱,中国实验仪器厂。
1.2 纤维素的提取
将小麦秸秆剪成3~5 cm的小段,用粉碎机粉碎,过60目筛,80 ℃烘干后用硝酸-乙醇法[21]提取,于80 ℃真空烘箱中干燥24 h,得到纤维素含量为78%的白色粉末状纤维素样品,保存,备用。
1.3 纤维素的预处理
1.3.1 NaOH/硫脲/尿素水溶液法
(1)实验步骤:取2 g提取到的纤维素放入-10 ℃的50 mL NaOH/硫脲/尿素水溶液中,磁力搅拌器上快速搅拌5 min,冰浴中搅拌溶解7~10 min后取出过滤。将得到的滤渣再用50 mL NaOH/硫脲/尿素水溶液溶解30 min后过滤。将两部分滤液合并在大烧杯中,加入大量稀盐酸,室温静置过夜后有白色絮状沉淀出现。10 000 r·min-1离心20 min,弃上清,沉淀用无水乙醇洗至中性,80 ℃烘干得到处理过的纤维素。
(2)正交实验:结合已有文献[22],以纤维素结晶度(CrI)为指标,设计3因素4水平正交实验对各溶质的质量分数(溶液体系中溶质的质量占溶液总质量的百分比)进行优化。CrI用Segal经验法[23]计算:
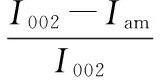
式中:I002为(002)面的最大衍射强度;Iam为无定形区的衍射强度。
1.3.2 乙二胺法
(1)实验步骤:将提取到的纤维素浸泡在一定温度、一定质量分数的乙二胺溶液中,一段时间后用玻璃砂芯过滤器过滤,滤渣用适量蒸馏水洗涤,用热水慢慢冲洗3次,于80 ℃烘干得到处理过的纤维素。
(2)正交实验:为确定乙二胺法的最佳条件,以纤维素结晶度为指标,设计4因素3水平正交实验考察处理时间、液固比、处理温度、乙二胺质量分数对纤维素预处理的影响。
1.4 纤维素的表征
FTIR表征:将一定量样品和KBr充分混合,研磨,压制成薄片进行红外光谱测试,以KBr空白片作为扫描背景。分辨率为4 cm-1,扫描次数为16次·s-1,测量范围为4 000~800 cm-1。
XRD表征:Cu靶;镍单色滤光片;管电压为40 kV;管电流为40 mA;扫描范围2θ为0°~45°;步长为0.1°。
2 结果与讨论
2.1 NaOH/硫脲/尿素水溶液法条件优化(表1)
由表1可知,各因素对NaOH/硫脲/尿素水溶液法预处理纤维素的影响大小依次为:NaOH质量分数>尿素质量分数>硫脲质量分数,最优方案为:8%NaOH、7%硫脲、6%尿素。在最优方案下进行验证实验,纤维素的结晶度由原来的0.7893降低到0.3861,降低了51%。
表1NaOH/硫脲/尿素水溶液法预处理纤维素的正交实验结果与分析

Tab.1Results and analysis of orthogonal experiment for
2.2 乙二胺法条件优化(表2)
表2乙二胺法预处理纤维素的正交实验结果与分析
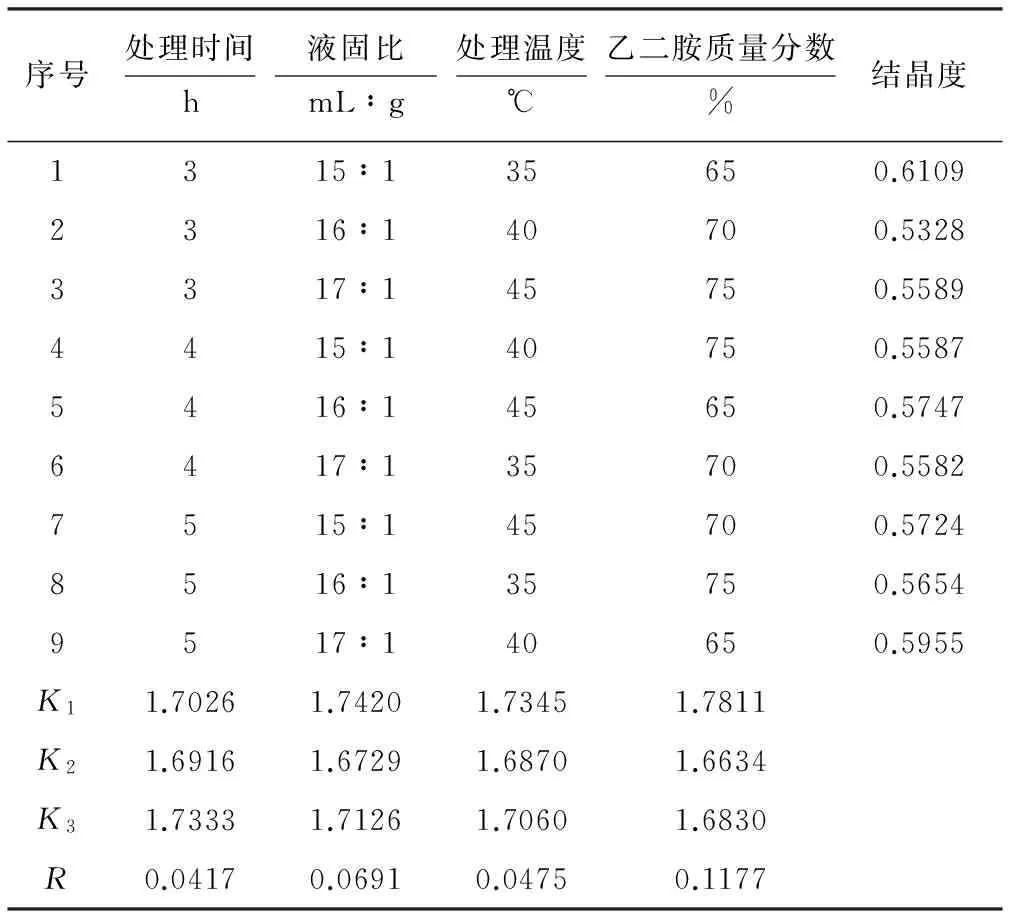
Tab.2Results and analysis of orthogonal experiment for
由表2可知,各因素对乙二胺法预处理纤维素的影响大小依次为:乙二胺质量分数>液固比>处理温度>处理时间,最优方案为:乙二胺质量分数70%、液固比16∶1、处理温度40 ℃、处理时间4 h。在最优方案下进行验证实验,纤维素的结晶度由原来的0.7893降低到0.5036,降低了36%。
2.3 FTIR表征
对小麦秸秆、提取得到的纤维素、NaOH/硫脲/尿素水溶液法预处理纤维素、乙二胺法预处理纤维素分别进行FTIR测试,所得红外光谱如图1所示,红外光谱数据见表3。

a.小麦秸秆 b.提取得到的纤维素 c.NaOH/硫脲/尿素水溶
表3红外光谱数据
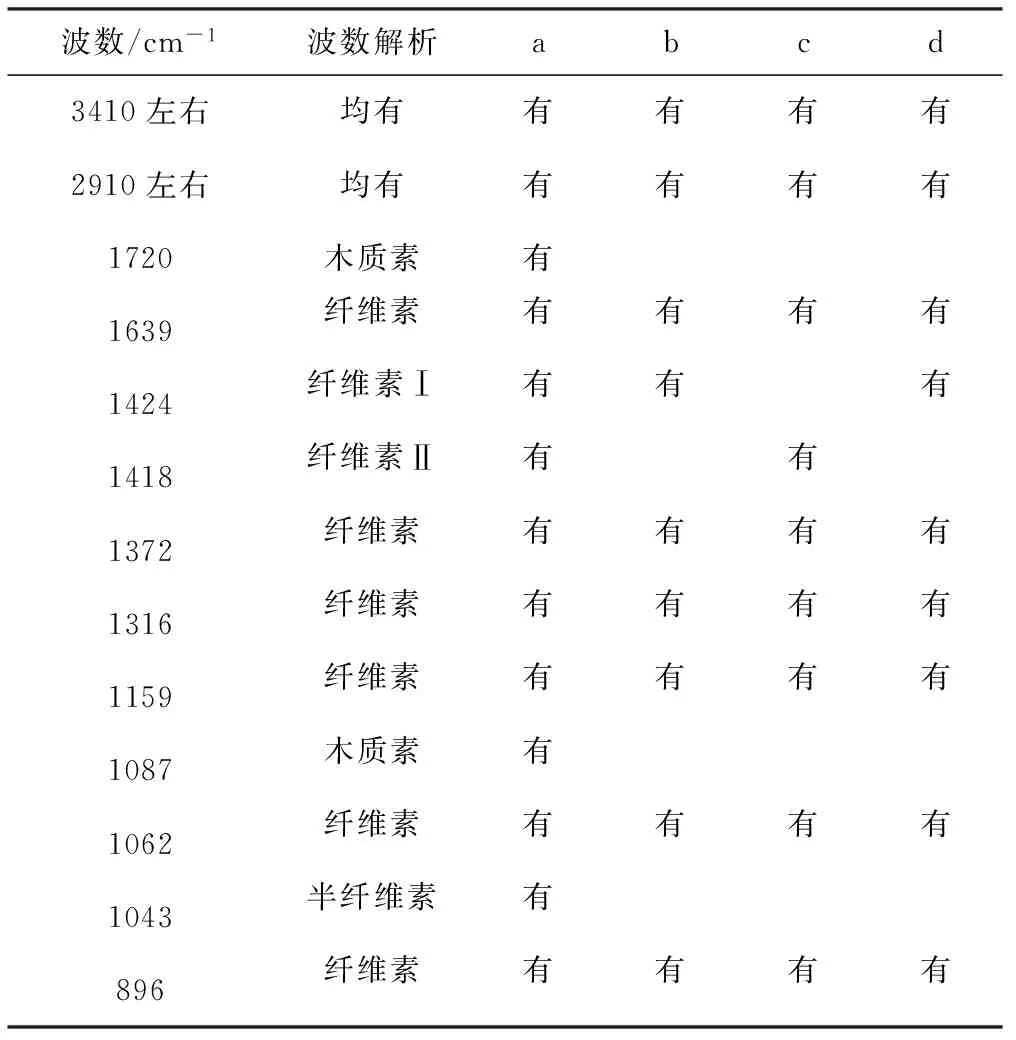
Tab.3Data of FTIR spectra
注:a为小麦秸秆,b为提取得到的纤维素,c为NaOH/硫脲/尿素水溶液法预处理纤维素,d为乙二胺法预处理纤维素。
由图1、表3可知,小麦秸秆、提取得到的纤维素以及用2种预处理方法所得纤维素的红外光谱均在3 410 cm-1左右和2 910 cm-1左右有明显吸收峰,分别对应于碳水化合物-OH和C-H的伸缩振动。对比曲线a和b可以看出:曲线b中,1 720 cm-1处对应的木质素中非共轭羰基的伸缩振动峰消失,1 087 cm-1处对应的木质素的特征吸收峰也消失,1 043 cm-1处对应的半纤维素的C-C、C-O的伸缩振动峰和C-OH的弯曲振动峰的强度明显减弱;而2条曲线的纤维素特征吸收峰(1 639 cm-1、1 424 cm-1、1 372 cm-1、1 316 cm-1、1 159 cm-1、1 062 cm-1及896 cm-1)均存在,以上数据表明在纤维素的提取过程中,绝大多数的木质素和半纤维素被去除,所得纤维素样品较纯。对比曲线b和c、d可以看出:经过不同预处理方法得到的纤维素的红外特征峰的波数没有明显变化,表明2种预处理方法没有在纤维素大分子上引入新的基团,只是对原有基团的振动强度产生影响。对比曲线b和c可以看出,曲线b在1 424 cm-1(纤维素Ⅰ的特征吸收峰)处的吸收峰在曲线c中移至1 418 cm-1(纤维素Ⅱ的特征吸收峰)处,表明在NaOH/硫脲/尿素水溶液预处理过程中,纤维素Ⅰ的分子内氢键被破坏,晶型发生了改变。
2.4 XRD表征(图2)
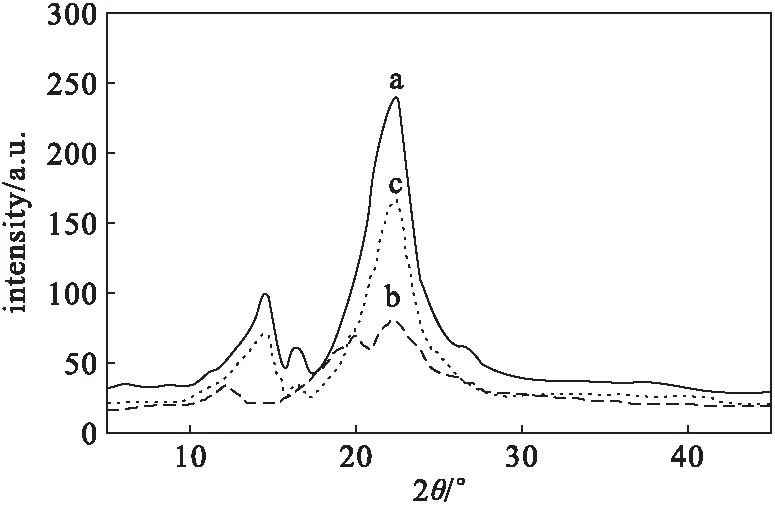
a.提取得到的纤维素 b.NaOH/硫脲/尿素水溶液法
由图2可知:(1)提取得到的纤维素的结晶度为0.7893,晶型为纤维素Ⅰ;(2)乙二胺法预处理纤维素的结晶度下降到0.5036,晶型没有改变,仍是纤维素Ⅰ,这与FTIR图谱结果相吻合,同时与Wada等[25]的结论相符合;(3)NaOH/硫脲/尿素水溶液法预处理纤维素的结晶度大幅下降到0.3861,晶型也发生了改变,由纤维素Ⅰ变为纤维素Ⅱ。Bochek等[24]研究表明,纤维素经NaOH/硫脲/尿素水溶液法预处理后,结晶度降低,纤维素晶型由纤维素Ⅰ变为纤维素Ⅱ,但未给出结晶度降低的具体数值。另一方面,相比传统的NaOH/H2O体系预处理纤维素[20],30 min左右纤维素的结晶度几乎没有变化,25 h结晶度仅降低56%。本研究采用优化的NaOH/硫脲/尿素水溶液法预处理纤维素,仅需1 h即可使结晶度降低51%,在降低结晶度、缩短处理时间等方面具有较大优势。
3 结论
采用NaOH/硫脲/尿素水溶液法和乙二胺法分别对小麦秸秆纤维素进行预处理,采用FTIR、XRD对其红外光谱、结晶度及晶型进行测定。结果表明:采用优化的 NaOH/硫脲/尿素水溶液法(8%NaOH、7%硫脲、6%尿素)预处理纤维素,不仅结晶度降低51%,而且还能得到纤维素Ⅱ,更利于纤维素进一步改性;而采用优化的乙二胺法(乙二胺质量分数70%、液固比16∶1、处理温度40 ℃、处理时间4 h)预处理纤维素,结晶度仅降低36%。
[1] IGARASHI K,UCHIHASHI T,KOIVULA A,et al.Traffic jams reduce hydrolytic efficiency of cellulase on cellulose surface[J].Science,2011,333(6047):1279-1282.
[2] LIU Y S,BAKER J O,ZENG Y N,et al.Cellobiohydrolase hydrolyzes crystalline cellulose on hydrophobic faces[J].Journal of Biological Chemistry,2011,286(13):11195-11201.
[3] KLEMM D,KRAMER F,MORITZ S,et al.Nanocelluloses:a new family of nature-based materials[J].Angewandte Chemie International Edition,2011,50(24):5438-5466.
[4] 罗成成,王晖,陈勇.纤维素的改性及应用研究进展[J].化工进展,2015,34(3):767-773.
[5] 王钰,刘志明.纳米纤丝纤维素制备及硅烷化改性[J].生物质化学工程,2015,49(2):17-20.
[6] 赵蒙蒙,姜曼,周祚万.几种农作物秸秆的成分分析[J].材料导报B:研究篇,2011,25(8):122-125.
[7] LANGAN P,SUKUMAR N,NISHIYAMA Y,et al.Synchrotron X-ray structures of cellulose Iβand regenerated cellulose Ⅱ at ambient temperature and 100 K [J].Cellulose,2005,12(6):551-562.
[8] 蔡杰,吕昂,周金平,等.纤维素科学与材料[M].北京:化学工业出版社,2015:83.
[9] ZUGENMAIER P.Crystalline Cellulose and Derivatives:Characterization and Structures[M].Berlin Heidelbery:Springer,2008:71.
[10] STERNBERG U,KOCH F T,PRIEB W,et al.Crystal structure refinements of cellulose polymorphs using solid state13C chemical shifts[J].Cellulose,2003,10(3):189-199.
[11] 张景强,林鹿,孙勇,等.纤维素结构与解结晶的研究进展[J].林产化学与工业,2008,28(6):109-114.
[12] AGO M,ENDO T,HIROTSU T.Crystalline transformation of native cellulose from cellulose Ⅰ to cellulose ID polymorph by a ball-milling method with a specific amount of water[J].Cellulose,2004,11(2):163-167.
[13] 邱盼盼,任天宝,王风芹,等.木质纤维原料蒸汽爆破-生物联合预处理及其生物脱毒研究进展[J].生物质化学工程,2013,47(2):23-28.
[14] ZHAO H B,KWAK J H,WANG Y,et al.Effects of crystallinity on dilute acid hydrolysis of cellulose by cellulose ball-milling study[J].Energy & Fuels,2006,20(2):807-811.
[15] LEE D M,BURNFIELD K E,BLACKWELL J.Structure of a cellulose Ⅰ-ethylenediamine complex[J].Biopolymers,1984,23(1):111-126.
[16] JIANG Z W,FANG Y,XIANG J F,et al.Intermolecular interactions and 3D structure in cellulose-NaOH-urea aqueous system[J].Journal of Physical Chemistry B,2014,118(34):10250-10257.
[17] OGAWA Y,HIDAKA H,KIMURA S,et al.Formation and stability of cellulose-copper-NaOH crysalline complex[J].Cellulose,2014,21(2):999-1006.
[18] WANG Y,DENG Y L.The kinetics of cellulose dissolution in sodium hydroxide solution at low temperatures[J].Biotechnology and Bioengineering,2009,102(5):1398-1405.
[19] JIN H J,ZHA C X,GU L X.Direct dissolution of cellulose in NaOH/thiourea/urea aqueous solution[J].Carbohydrate Research,2007,342(6):851-858.
[20] 陈明凤.纤维素的去结晶[D].广州:华南理工大学,2011.
[21] 王林风,程远超.硝酸乙醇法测定纤维素含量[J].化学研究,2011,22(4):52-55.
[22] 查纯喜.纤维素在氢氧化钠/硫脲/尿素水溶液中的溶解及溶液性质的研究[D].苏州:东华大学,2007.
[23] 马晓娟,黄六莲,陈礼辉,等.纤维素结晶度的测定方法[J].造纸科学与技术,2012,31(2):75-78.
[24] BOCHEK A M,SEROV I V,NOVOSELOV N P,et al.Dissolution of cellulose aqueous alkaline solutions with added urea and thiourea[J].Fibre Chemistry,2015,47(3):166-170.
[25] WADA M,KWON G J,NISHIYAMA Y.Structure and thermal behavior of a cellulose Ⅰ-ethylenediamine complex[J].Biomacromolecules,2008,9(10):2898-2904.
EffectsofTwoChemicalPretreatmentMethodsonCellulosefromWheatStraw
YANG Yang,LI Chun-lu,CUI Zhi-fang*
(CollegeofChemicalandEnviromentalEngineering,ShandongUniversityofScienceandTechnology,Qingdao266590,China)
Cellulose is rich in wheat straw,but it is hard to be modified because of its high crystallinity.Using wheat straw as a raw material,we pretreated cellulose from wheat straw by NaOH/thiourea/urea aqueous solution method and ethylenediamine method,respectively.Moreover,we optimized two chemical pretreatment methods by orthogonal experiment,and compared their effects on cellulose from wheat straw by determination of FTIR spectrum,crystallinity,and crystal form with FTIR and XRD.Results indicated that,for optimized NaOH/thiourea/urea aqueous solution method,mass fraction of NaOH,thiourea,and urea were 8%,7%,and 6%,respectively,the crystallinity of cellulose decreased 51%,meanwhile the crystal form turned from cellulose Ⅰto cellulose Ⅱ;for optimized ethylenediamine method,mass fraction of ethylenediamine was 70%,liquid-solid ratio was 16∶1(mL∶g),treatment temperature was 40 ℃,treatment time was 4 h,the crystallinity of cellulose only decreased 36%,the crystal form was still remained cellulose Ⅰ.
cellulose;wheat straw;NaOH/thiourea/urea aqueous solution method;ethylenediamine method;crystallinity;crystal form
TQ352
A
1672-5425(2017)10-0061-04
中国科学院生物基材料重点实验室开放基金项目(KLBM2016003)
2017-06-06
杨阳(1992-),女,山东潍坊人,硕士研究生,研究方向:生物质资源利用;通讯作者:崔志芳,副教授,E-mail:zhifangcui@126.com。
10.3969/j.issn.1672-5425.2017.10.014
杨阳,李春露,崔志芳.两种化学预处理方法对小麦秸秆纤维素的影响[J].化学与生物工程,2017,34(10):61-64,69.
