MRI评价子宫肌瘤高强度聚焦超声消融术后盆底筋膜改变
2017-11-01张学花翟昭华董国礼陈建业吴晓莉
张学花,翟昭华,董国礼,陈建业,吴晓莉,刘 颖
(1.重庆市巴南区人民医院放射科,重庆 401320;2.川北医学院附属医院放射科,四川 南充 637000)
MRI评价子宫肌瘤高强度聚焦超声消融术后盆底筋膜改变
张学花1,翟昭华2*,董国礼2,陈建业2,吴晓莉1,刘 颖1
(1.重庆市巴南区人民医院放射科,重庆 401320;2.川北医学院附属医院放射科,四川 南充 637000)
目的探讨MRI评价子宫肌瘤高强度聚焦超声消融术(HIFU)后盆底筋膜改变的价值。方法回顾性分析初次行HIFU治疗的283例子宫肌瘤患者的盆腔MRI及临床资料,观察盆腔筋膜水肿情况,记录HIFU治疗总能量、辐照时间。分析患者年龄、肌瘤情况(位置、类型、数量、体积)及HIFU治疗总能量、辐照时间与盆底筋膜改变的相关性。结果共201例(201/283,71.02%)患者HIFU后盆腔筋膜出现水肿,59.71%(169/283)为1度和2度。不同肌瘤位置患者术后盆底筋膜水肿程度差异有统计学意义(χ2=27.50,P=0.007)。患者年龄、肌瘤情况(数目、体积)与盆腔筋膜水肿程度无相关性(P均>0.05);HIFU治疗总能量、辐照时间与盆腔筋膜水肿程度呈正相关(rs=0.288、0.317,P均<0.001)。结论采用MRI可评价HIFU治疗子宫肌瘤引起的盆腔筋膜水肿,HIFU辐照时间、治疗总能量、子宫肌瘤位置是引起盆底筋膜水肿的主要影响因素。
高强度聚焦超声消融;磁共振成像;平滑肌瘤;筋膜
近年来,高强度聚焦超声(high intensity focused ultrasound, HIFU)消融术作为一种安全、有效的子宫肌瘤治疗手段被广大患者及妇科医师重视,其疗效及应用前景已被临床实践证实。但超声波的复杂生物效应及物理效应可能对靶区周围正常组织产生损伤,从而造成术后骶尾部疼痛、阴道出血、盆腔炎(盆腔筋膜水肿、盆腔积液)等。目前对HIFU治疗后不良反应的研究较少[1-2]。MRI可清晰显示盆底筋膜情况,为后续治疗及HIFU治疗总能量、辐照时间的调整提供参考,尽可能减小靶区外组织的受损程度及范围。本研究采用MRI观察子宫肌瘤患者经HIFU治疗后盆底筋膜水肿情况,旨在为临床治疗提供参考依据,尽可能减少对患者的损伤。
1 资料与方法
1.1 一般资料 回顾性分析2014年1月—2015年6月在我院初次接受HIFU治疗的子宫肌瘤283例患者的临床及MRI资料,年龄15~54岁,平均(40.9±0.2)岁。纳入标准:①经临床或影像检查诊断除子宫肌瘤外无其他盆腔疾病;②初次接受超声消融,未经接受他手术治疗;③膀胱、直肠充盈良好,直肠周围脂肪清晰;④HIFU治疗前后均有完整的MRI及临床资料;⑤HIFU术前MRI显示盆底筋膜无水肿。所有患者均于HIFU治疗前后3天内接受MR检查。单发肌瘤者166例,多发者117例,多发肌瘤者以体积最大肌瘤入组。
1.2 仪器与方法
1.2.1 HIFU治疗 采用HIFU JC200型聚焦超声肿瘤治疗系统(重庆海扶技术有限公司)。术中通过脱气水囊压迫、推挤子宫前方的肠道,使声通道避开肠道。超声逐层定位肌瘤,设定声发射初始功率为400 W,强度1 s∶3 s,并将焦点置于病灶中央层面,采用点照射方式逐层扫描治疗,至靶区出现明显灰度增加时即可换下一个点进行治疗,至整个计划治疗区完全覆盖为止。辐照时间及治疗能量依肿瘤的不同而调整。手术全过程镇静、镇痛,使患者处于安静清醒状态,术后进行抗感染、对症处理,并监测不良反应。
1.2.2 MR检查 采用GE Discovery MR750 3.0T扫描仪,32通道体部阵列线圈。行轴位及矢状位扫描,T2WI和脂肪抑制T2WI采用FRFSE序列,TE 119 ms,TR 5 000 ms,矩阵384×256;T1WI采用3D-LAVA-Flex序列水像,TE 1.7 ms,TR 4.1 ms,激励次数0.75,矩阵384×256。以上序列扫描层厚均为5 mm,层间隔5 mm。患者HIFU治疗前后MR扫描序列和参数一致。
1.3 图像分析 由2名影像诊断医师采用盲法分析所有MR资料,意见有分歧时经协商达成共识。观察肌瘤数目、体积、类型、位置。盆底筋膜水肿的观察以脂肪抑制T2WI为主。将盆底筋膜划分区域,分别为盆腔4个侧壁(后壁筋膜即为骶前筋膜)、直肠周围。根据水肿累及范围对盆底筋膜水肿程度进行分度,子宫周围、膀胱周围,无水肿为0度,1个区域筋膜水肿为1度,2个区域筋膜水肿则为2度,以此类推分为3度、4度、5度等。
在脂肪抑制T2WI图像所示最大病变层面测量肌瘤径线,前后径平行子宫内膜方向,左右径平行子宫内膜方向,上下径垂直于前后径,计算肌瘤体积:肌瘤体积(cm3)=左右径×前后径×上下径×0.523[3]。
1.4 统计学分析 采用SPSS 17.0统计分析软件。计量资料以±s表示,不同肌瘤类型、位置中盆底筋膜水肿情况比较采用χ2检验。患者年龄、肌瘤情况(大小、数目)、HIFU治疗总能量及辐照时间与盆底筋膜水肿程度的相关性采用Spearman秩相关分析。P<0.05为差异有统计学意义。
2 结果
283例患者中,位于前壁156例、后壁106例、侧壁21例;肌壁间肌瘤210例、浆膜下肌瘤54例、黏膜下肌瘤19例。肌瘤体积为0.75~555.43 cm3,平均(60.29±0.60)cm3。HIFU投放能量7.2~800.0 kJ,平均(232.30±3.32)kJ;辐照时间18~2 600 s,平均(602.07±5.01)s。
2.1 HIFU治疗后盆底筋膜改变情况 盆腔筋膜水肿MRI表现为条片状、网状的长T1长T2信号,脂肪抑制T2WI呈明显高信号,见图1、2。
HIFU术后盆底筋膜水肿分度见表1。82例(82/283,28.98%)盆底筋膜无水肿,201例(201/283,71.02%)出现不同程度的盆底筋膜水肿,1、2度水肿169例(169/283,59.71%),3度水肿24例(24/283,8.48%),4~6度水肿8例(8/283,2.83%)。在盆腔筋膜各部位中,骶前筋膜水肿163例,盆腔前侧壁水肿116例,子宫周围41例,膀胱周围27例,直肠周围18例,盆腔右侧壁8例,盆腔左侧壁6例。
2.2 不同肌瘤位置和类型与盆底筋膜水肿的关系 不同肌瘤位置患者术后盆底筋膜水肿程度不同,差异有统计学意义(χ2=27.50,P=0.007);不同肌瘤类型患者术后盆底筋膜水肿程度差异无统计学意义(χ2=15.79,P=0.201);见表2。
2.3 肌瘤与盆底筋膜水肿的相关性 HIFU治疗总能量、辐照时间与盆底筋膜水肿程度呈正相关(rs=0.288、0.317,P均<0.001);患者年龄、肌瘤数目、体积与盆底筋膜水肿程度均无相关性(rs=-0.046、-0.117、0.050、0.080,P均>0.05)。
3 讨论
HIFU治疗子宫肌瘤主要通过热效应使靶组织迅速升温(>80℃)后,发生凝固性坏死而达到治疗目的,而靶区外组织温度较低(<50℃)不至于遭受热损伤[4]。但一定程度上,超声波的复杂物理特性(反射、折射等)及空化效应可引起部分不良反应,如腹痛、阴道内膜损伤[5]、前腹壁组织损伤[6]、骶骨异常等,HIFU治疗子宫肌瘤的安全性仍然是目前国内外研究的热点。
盆筋膜分为壁筋膜、脏筋膜及膈筋膜,位于骶骨前方壁筋膜为骶前筋膜(Waldeyer筋膜),包裹膀胱的脏筋膜为膀胱筋膜,包裹直肠的为直肠深筋膜。MRI可显示95%以上盆腔筋膜[7],盆腔筋膜正常时呈线样低信号,不易观察,水肿时则呈条、片状的长T1长T2信号。王世栋[8]通过MRI的多方位成像研究显示,直肠筋膜呈细线状低信号,其后侧与骶前筋膜水平走行呈“双轨样”低信号。
超声消融损伤组织的机制除热效应、空化效应外,还有机械效应、弥散效应等。HIFU消融子宫肌瘤时靶组织温度瞬时升高、热量沉积,随着辐照时间的延长,局部热量扩散,并开始热传导,当生物学焦域形成后,凝固性坏死组织对声能的吸收即会减低,同时空化效应使组织产生声束屏障,生物学焦域随机向近场方向推移且呈三角形发展,靶区邻近组织将会沉积热量致热损伤。辐照时间越长、辐照能量越大,组织焦点温升越高、组织内产生的相对累积热剂量越大[9-10],组织损伤概率随即增加,损伤程度也越重,与本研究中盆底筋膜水肿程度与HIFU投放能量、辐照时间呈正相关的结果相符。此外,HIFU辐照时,声道上的组织(包括膀胱、筋膜等)也会吸收声能产生温升效应,且超声波在各生物组织界面产生物理效应(如反射、折射等),反射界面可能有能量沉积或存在异位小聚焦点,使超声发生二次聚焦而对靶区外组织产生热损伤[11-12],也是HIFU治疗子宫肌瘤后盆底筋膜产生水肿的原因。而空化效应可增加组织对热的敏感性,使聚焦外的组织受到损伤[10]。有研究[5]发现聚焦超声可刺激机体释放一定的炎性介质,局部组织受炎性介质的作用而出现充血水肿。以上因素均可使盆底筋膜发生水肿。本研究发现骶前及盆腔前侧壁筋膜出现水肿的比例最高,其原因为:①发生水肿的筋膜多位于声道上,如盆腔前侧壁筋膜、膀胱周围筋膜;②骶尾部能反射超声波并沉积超声热量,故骶前筋膜水肿的概率(57.60%)相对较高。
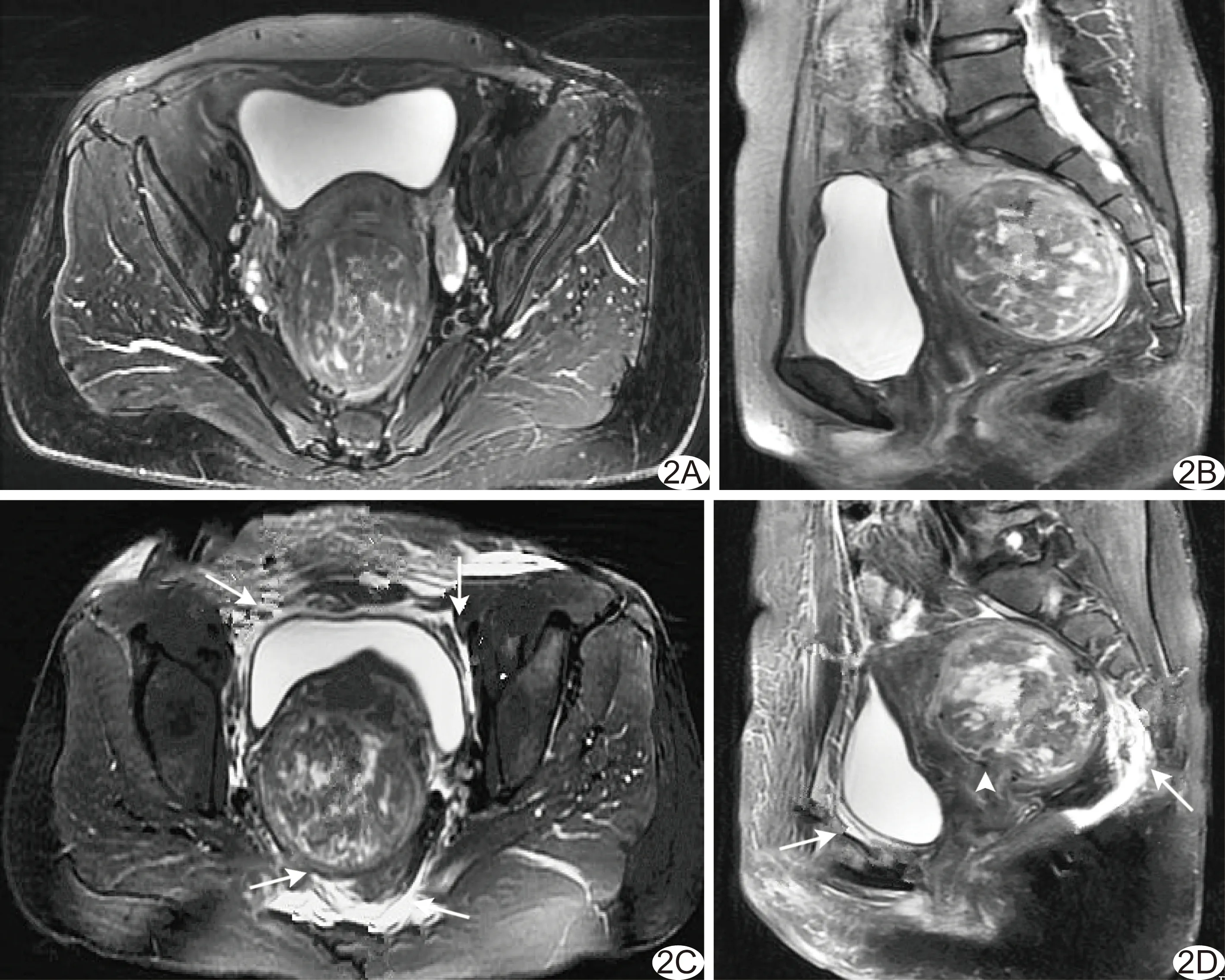
图2 患者42岁,子宫肌瘤HIFU后盆底筋膜4度水肿 A、B.分别为子宫肌瘤HIFU术前轴位、矢状位脂肪抑制T2WI,子宫后壁肌瘤呈高、低混杂信号; C、D.分别为HIFU术后轴位、矢状位脂肪抑制T2WI,肌瘤信号增高(箭头),骶前筋膜、直肠筋膜、膀胱周围筋膜及盆腔前壁筋膜水肿,呈条片状高信号(箭)
本研究还发现子宫后壁肌瘤引起盆底筋膜水肿的比例较高(87/106,82.08%),差异有统计学意义。超声波能量的衰减随传播距离的增加而增大,到达靶组织的能量也会相应减低,故目前多采用增大辐照能量及辐照时间的方法达到治疗目的,一定程度上也加大了周围组织能量沉积[13],从而增加了热损伤的概率及程度。子宫前壁肌瘤距前腹壁近,所需能量小、传导衰减也相对较少,相对较安全,故HIFU后治疗前壁肌瘤造成筋膜水肿的病例相对较少且程度较轻,多局限于盆腔前侧壁;而后壁肌瘤在HIFU治疗时需用脱气水囊压迫子宫前方的肠道推挤出声通道,后壁肌瘤距皮肤表面较远,水囊又能增加反射界面,故治疗所需超声波能量较大,且传导中易衰减,所需时间较长,因此后壁肌瘤治疗后筋膜出现水肿比例高于其他部位。
HIFU治疗时严格控制并适时调整治疗时间及剂量尤为重要。鄢利梅等[14]认为只要在治疗过程中根据患者反应实时调整HIFU辐照能量及时间,并控制好治疗节奏,则可较好地完成HIFU治疗。
总之,盆底筋膜水肿在MRI上的表现具有一定的特征性,MRI可有效观察并评价HIFU治疗子宫肌瘤对盆底筋膜的影响,并可指导HIFU治疗能量、辐照时间的选择及调整。
[1] 邓凤莲,邹建中,李锐,等.高强度聚焦超声治疗子宫肌瘤对骶骨影响因素探讨.中国介入影像与治疗学,2009,6(5):457-460.
[2] Ritchie RW, Leslie T, Phillips R, et al. Extracorporeal high intensity focused ultrasound for renaltumours: A 3-year follow-up. BJU Int, 2010,106(7):1004-1009.
[3] Wang W, Wang Y, Wang T, et al. Safety and efficacy of US-guided high-intensity focused ultrasound for treatment of submucosal fibroids. Eur Radiol, 2012,22(11):2553-2558.
[4] Jung SE, Cho SH, Jang JH, et al. High-intensity focused ultrasound ablation in hepatic and pancreatic cancer: Complications. Abdom Imaging, 2011,36(2):185-195.
[5] 李权.超声消融子宫肌瘤时对子宫内膜影响的形态学研究.重庆:重庆医科大学,2013:106.
[6] 肖雅楠,许永华,杨利霞,等.高强度聚焦超声消融子宫肌瘤患者腹壁损伤的影响因素研究.临床超声医学杂志,2015,17(5),297-300.
[7] 孙秋德.直肠区域影像解剖与直肠癌局部浸润的术前MRI研究.重庆:第三军医大学,2005:83.
[8] 王世栋.直肠固有筋膜的解剖与MRI对比研究.合肥:安徽医科大学,2011:45.
[9] 李发琪,张樯,杜永洪,等.高强度聚焦超声治疗剂量对组织温升影响的研究.生物医学工程学杂志,2003,20(3):466-471.
[10] Yu T, Luo J. Adverse events of extracorporeal ultrasound-guided high intensity focused ultrasound therapy.PLoS One, 2011,6(12):e26110.
[11] 李发琪.高强度聚焦超声(HIFU)肿瘤热消融技术的关键问题简析.中华肝胆外科杂志,2011,17(2):175-176.
[12] Yu T, Fu X. Extracorporeal ultrasound-guided high intensity focused ultrasound: Implications from the present clinical trials. Scientific World Journal, 2014,2014:537260.
[13] 黎建军,徐国良,罗广裕,等.原发性肝癌经高强度聚焦超声治疗后并发症分析.中华超声影像学杂志,2006,15(9):668-670.
[14] 鄢利梅,何佳,黄国华,等.高强度聚焦超声消融治疗子宫后位肌瘤的临床研究.中国超声医学杂志,2012,28(1):72-74.
MRIevaluatingchangesofpelvicfasciaafterhighintensityfocusedultrasoundablationofuterinefibroids
ZHANGXuehua1,ZHAIZhaohua2*,DONGGuoli2,CHENJianye2,WUXiaoli1,LIUYing1
(1.DepartmentofRadiology,Ba'nanPeople'sHospitalofChongqing,Chongqing401320,China; 2.DepartmentofRadiology,AffiliatedHospitalofNorthSichuanMedicalUniversity,Nanchong637000,China)
ObjectiveTo explore the value of pelvic fascia changes after high intensity focused ultrasound (HIFU) ablation of uterine fibroids patients with MRI.MethodsThe pelvic MRI and clinical data of 283 patients with uterine fibroids after treatment of HIFU were analyzed retrospectively. Thetotal power and irradiation time of HIFU, and the degree of pelvic fascia edema changes were observed. The correlation between age, fibroids location, type, number, volume, total energy, irradiation time of HIFU and the degree of pelvic fascia edema were analyzed.ResultsTotally 201 patients (201/283, 71.02%) had pelvic fascia edema and 59.71% (169/283) were degree 1 and 2. There was significant difference in the degree of pelvic fascia edema in patients with different fibroids (χ2=27.50,P=0.007). There was no correlation between patients age, number, volume, type of fibroids, nor pelvic fascia edema (allP>0.05). HIFU energy and irradiation time were positively correlated with the degree of pelvic fascia edema (rs=0.288, 0.317, bothP<0.001).ConclusionMRI can observe pelvic fascia edema caused by HIFU treatment of uterine fibroids. HIFU irradiation time, total energy, and location of uterine fibroids location are the main influencing factors.
High intensity focused ultrasound ablation; Magnetic resonance imaging; Leiomyoma; Fascia
10.13929/j.1003-3289.201703126
R737.33; R445.2
A
1003-3289(2017)10-1540-05
张学花(1988—),女,贵州六盘水人,硕士,医师。研究方向:中枢神经系统影像诊断。E-mail: 1041169807@qq.com
翟昭华,川北医学院附属医院放射科,637000。E-mail: zhaizhaohuada@163.com
2017-03-23
2017-08-21
