新型热电厂烟气脱硫剂的制备及中试试验
2017-10-31张兆云吕晓英
张兆云,刘 超,吕晓英
(唐山三友化工股份有限公司,河北 唐山 063305)
新型热电厂烟气脱硫剂的制备及中试试验
张兆云,刘 超,吕晓英
(唐山三友化工股份有限公司,河北 唐山 063305)
采用乙醇胺、乳酸及乙醇合成了乙醇胺乳酸盐,并将其与水复配制得含水量为15%的乙醇胺乳酸盐离子液体脱硫剂(ELIL脱硫剂),探讨了中试脱硫试验过程中脱硫剂的SO2吸收性能及重复使用性能。试验结果表明:在长达72 h的吸收过程中,该脱硫剂的硫容(以SO2计)与吸收时间呈一次函数关系;在硫容达到3.0%左右时,ELIL脱硫剂的黏度达到最大值;以w(SO2)为0.69%的模拟烟道气连续中试运转72 h,尾气中的SO2质量浓度远小于50 mg/cm3,达到GB 13271—2014《锅炉大气污染物排放标准》的要求;使用5次后,ELIL脱硫剂的饱和硫容基本稳定在4.6%,重复使用性良好;随着重复使用次数的增加,SO42-积累量逐次增加,可通过加入Ca(OH)2除去SO42-,提高ELIL脱硫剂的脱硫性能。
烟气脱硫;离子液体;乙醇胺乳酸盐;吸收;解吸;中试
1996年至2007年,我国SO2排放量逐年增加,尤其是2006年我国SO2排放量高达2.54×107t,跃居世界第一位[1]。每年因SO2排放导致我国经济损失高达5 000亿元。而热电厂因化石燃料燃烧排放的废气是SO2排放的主要来源之一。因此,加强热电厂烟道气脱硫十分必要且迫切。传统的热电厂烟道气脱硫方法根据脱硫过程是否有水参与及脱硫产物的干湿状态可以分为干法和湿法[2-5]。干法脱硫是气固反应,效率不高、反应速率低、设备庞大;湿法脱硫是气液接触,效率较高、设备小,但工艺复杂、设备多、占地面积大、投资费用高、能耗大、存在二次污染。因此迫切需要找到一种新的脱硫方法或脱硫剂。
利用离子液体(IL)脱除烟气中的SO2,是继传统干、湿法脱硫等常用技术的一次创新。脱硫功能化离子液体新材料的研究主要集中于含有氨基功能基团的胍类、咪唑类、醇胺类等[6-7]。但是它们普遍存在成本高、黏度大等问题。杜红彩等[8-10]详细研究了胺类离子液体的脱硫性能,发现乙醇胺乳酸盐离子液体在脱硫量、稳定性和选择性上表现优异,而且成本低。目前该技术国内外大多停留在小试阶段。因此,研究离子液体在中试脱硫试验中的性能尤为重要。
本工作将乙醇胺、乳酸与乙醇反应并与水复配,制备乙醇胺乳酸盐(EL)离子液体脱硫剂(ELIL脱硫剂),并进行中试放大试验,研究其在放大化过程中的脱硫性能及重复使用性能,为工业化应用提供数据支持。
1 试验部分
1.1 试剂和仪器
乙醇胺:w=99%,乳酸:w=88%,乙醇:w=99.9%,SO2:w=99.99%。
模拟烟道气:w(SO2)为0.69 %,其余为空气。
尾气吸收剂:w(NH3)为10%的氨水。
KM-940型烟气分析仪:英国凯恩国际有限公司;AVANCE500MHz型核磁共振仪:德国布鲁克公司;BSA124S型电子分析天平:德国赛多利斯集团;RE-3000A型旋转蒸发器:上海亚容生化仪器厂;石油毛细管黏度计:浙江椒江玻璃仪器厂;PHS-3E实验室酸度计:上海雷磁仪器厂。
1.2 ELIL脱硫剂的制备
乙醇胺、乳酸与乙醇按1∶1∶4的摩尔比加入至50 L反应釜中,在45 ℃、常压、机械搅拌条件下反应24 h。将釜液于95 ℃真空旋转蒸发,除去溶剂乙醇,得到目标产物乙醇胺乳酸盐离子液体。由于乙醇胺乳酸盐离子液体黏度较大,加入一定量的水,配成含水量15%左右的混合液,即为ELIL脱硫剂。
1.3 中试流程和装置
中试试验流程见图1。由图1可见:空气经风机压缩进入分级缓冲罐,经流量计稳定控制流量进入混合气缓冲罐;SO2气体经质量流量计控制流量进入混合气缓冲罐;混合气从填料塔下部进入填料塔,储液罐中的ELIL脱硫剂通过装了变频器的齿轮泵以一定流量进入塔顶,气液逆流接触,吸收尾气进入碱液槽,吸收完SO2的ELIL脱硫剂从塔底再回到储液罐。当ELIL脱硫剂吸收SO2达到饱和后,通过加热储液罐进行解吸,并用空气吹扫,解吸气通入碱液槽,其中的SO2以氨水吸收制成化肥。

图1 中试试验流程
填料塔[11-14]:高1.00 m,半径0.10 m,填料层:厚度0 .75 m,填料为瓷拉西环;空塔气速0.174 m/s,泛点气速0.29 m/s,空气流量 3.8 m3/h,SO2流量 0.334 L/min;ELIL脱硫剂流量 2.1 L/min,最小喷淋密度 20 m3/(m2·h),最小喷淋量 2.03 L/min;压降 228 Pa/m,气液体积比30。
缓冲罐:高1.00 m,半径0.81m;储液罐:容积50 L。
1.4 分析方法
采用核磁共振氢谱(1H-NMR)对脱硫剂进行表征。
2-):以酚酞为指示剂、0.05 mol/L氢氧化钠溶液为标准溶液进行滴定,加入双氧水将SO氧化成SO,m(积累SO)=m(SO)- m(SO);采用石油毛细管黏度计测定ELIL的黏度;采用酸度计测定ELIL的pH;采用烟气分析仪测定尾气中的SO2质量浓度;采用电子天平测定m(ELIL);m(H2O)=15%m(EL)×100%。
2 结果与讨论
2.1 ELIL脱硫剂的表征
新鲜ELIL脱硫剂、脱硫后ELIL脱硫剂、解吸后ELIL脱硫剂的1H-NMR谱图见图2。

图2 脱硫剂的1H-NMR谱图
由图2a谱线可见,位移Δ为1.102×10-6,3.696×10-6,2.756×10-6,3.512×10-6处的吸收峰分别归属于(d,3H,CHCH3),(m,1H,CHCH3),(t,2H,CH2CH2),(t,2H,CH2CH2),证明了合成的EL的离子液体结构准确性,且与文献[10]报道相符。对比图2a,2b谱线可见,吸收SO2后的ELIL脱硫剂在5.155×10-6处多了一个归属于S—O—H键的吸收峰,证明ELIL具有化学吸收作用,与文献[8]报道相一致。对比图2b,2c谱线可见,解吸后S—O—H键已经断裂,证明了EL吸收SO2后形成的是较弱的化学键,解吸容易。对比图2a,2c谱线可见,ELIL脱硫剂结构也没有发生变化,循环使用性能良好。
2.2 中试试验中ELIL脱硫剂对SO2的吸收效果
ELIL脱硫剂的硫容(以SO2计)与吸收时间的关系见图3。由图3可见,在长达72 h的吸收过程中,硫容与吸收时间呈一次函数关系,函数关系式为y=0.412+0.106x,表明随着ELIL中SO2的积累,ELIL脱硫剂仍能保持较好的SO2吸收效果。

图3 ELIL脱硫剂的硫容与吸收时间的关系
2.3 中试试验中ELIL脱硫剂黏度的变化
适宜的离子液体黏度对保证填料塔正常运行十分重要。ELIL脱硫剂的黏度与硫容的关系见图4。
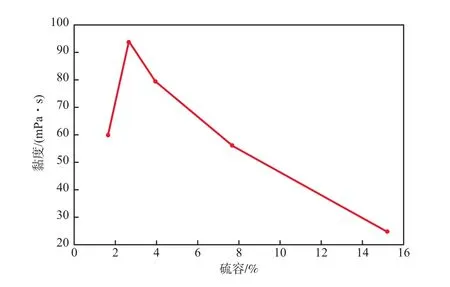
图4 ELIL脱硫剂的黏度与硫容的关系
由图4可见,随着硫容的增加,ELIL脱硫剂的黏度先增大后减小,在硫容达到3.0%左右时黏度达到最大值,这与文献[10]的报道相一致。这是由于离子液体刚开始的吸收以化学吸收为主,随着SO2吸收量的增加,水含量逐渐减少,而且新生物质的黏度也较大,导致整个体系黏度增大,当化学吸收达到平衡后,随后的吸收为物理吸收,黏度也随之下降。
2.4 中试试验尾气排放情况
中试装置连续运转72 h,尾气中SO2质量浓度的变化见图5。由图5可见,在72 h的吸收过程中,尾气中SO2的质量浓度均远小于50 mg/cm3,能达到GB 13271—2014《锅炉大气污染物排放标准》[16]的要求。
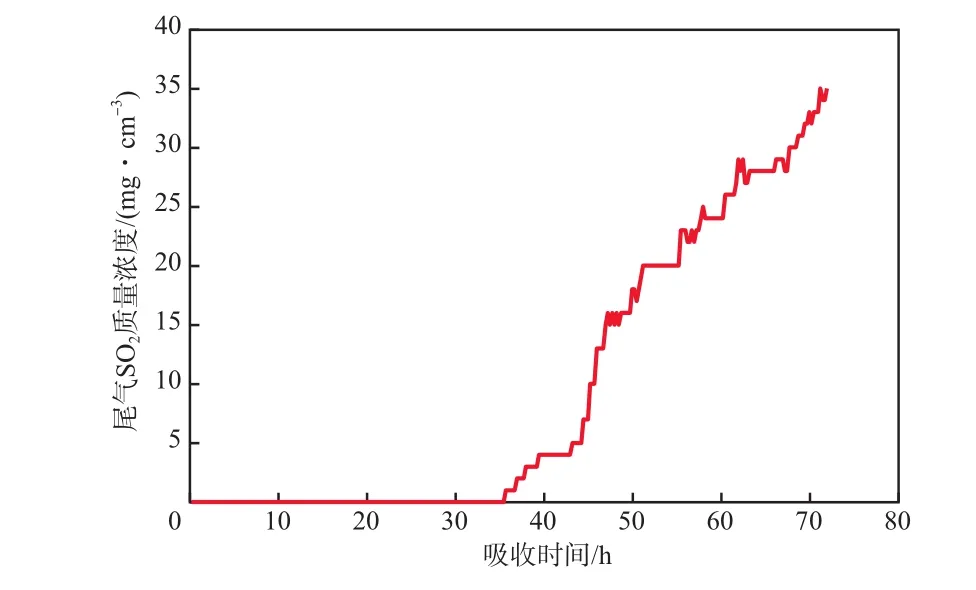
图5 尾气中SO2质量浓度的变化
2.5 中试试验中ELIL脱硫剂的重复使用性能
2.5.1 ELIL脱硫剂的重复使用效果
重复使用性是离子液体脱硫剂最重要的工业化指标之一。在空气解吸下采用ELIL脱硫剂重复进行5次脱硫试验,ELIL脱硫剂饱和硫容的变化见图6。

图6 ELIL脱硫剂饱和硫容的变化
由图6可见,ELIL脱硫剂使用5次以后饱和硫容基本稳定在4.6%,证明EL在中试试验中的重复使用性良好。之所以第1次使用时的饱和硫容与最后的稳定值差异大,是因为合成时过量的乙醇胺对SO2有吸收作用,使第1次使用时的饱和硫容高于其他各次;解吸时有可能局部温度过高,造成少量离子液体炭化;另外,空气中的氧气促使吸收液中SO氧化成SO较多,不易解吸完全。
2.5.2 ELIL脱硫剂重复使用过程中酸的积累
离子液体中酸含量的变化极大地影响着其脱硫性能。饱和吸收液中各形态S的含量(各形态S基团与EL的质量比)及pH的变化见图7。由图7可见,随着使用次数的增加,吸收液中SO的积累量会逐次增加,SO的含量逐渐减少,氧化后总SO的含量从使用第2次开始变化很小,pH逐渐降低。SO的含量随着SO积累量的增多而逐渐减少,说明ELIL脱硫剂的脱硫性能在逐渐下降。这可能有3个原因:1)吸收过程中,模拟烟道气中过多的O2在溶液环境下参与反应,促进了氧化反应,使SO转化为SO;2)解吸过程中,高温环境下SO被加速氧化;3)硫酸根不能被解吸出来,逐次的累积造成pH降低,进而降低了ELIL脱硫剂对SO2的吸收能力。因此,实际应用中需抑制氧化反应,或者不时加入Ca(OH)2除去SO,提高离子液体的脱硫性能。

图7 饱和吸收液中各形态S的含量及pH的变化■ SO;■ 积累SO;■ 氧化后总SO;■ pH
解吸后ELIL脱硫剂中各形态S的含量及pH的变化见图8。

图8 解吸后ELIL脱硫剂中各形态S的含量及pH的变化■ SO;■ 积累SO;■ pH
3 结论
a)采用乙醇胺、乳酸及乙醇合成了乙醇胺乳酸盐,且经1H-NMR表征确认了其结构的准确性。
b)以含水率15%的乙醇胺乳酸盐为ELIL脱硫剂,考察了其在中试脱硫试验中的吸收性能。试验结果表明:在长达72 h的吸收过程中,该脱硫剂的硫容与吸收时间呈一次函数关系,函数关系式为y=0.412+0.106x;随着硫容的增加,ELIL脱硫剂的黏度先增大后减小,在硫容达到3.0%左右时黏度达到最大值;以w(SO2)为0.69%的模拟烟道气连续中试运转72 h,尾气中的SO2的质量浓度远小于50 mg/cm3,达到GB 13271—2014《锅炉大气污染物排放标准》排放标准。
c)ELIL脱硫剂的重复使用性较好,使用5次后饱和硫容基本稳定在4.6%。随着ELIL脱硫剂重复使用次数的增加,吸收液中SO42-的积累、pH的降低阻碍了离子液体对SO2的吸收,ELIL脱硫剂的脱硫性能在缓慢下降。因此,实际应用中可不时加入Ca(OH)2除去SO42-,以提高ELIL脱硫剂的脱硫性能。
d)乙醇胺乳酸盐离子液体价格便宜、脱硫性能良好、重复使用性强,而且经过了中试放大试验的考验,具有极大的工业应用价值,为新型热电厂烟道气脱硫剂的研制迈出了坚实的一步。
[1] 蒋文举. 烟气脱硫脱硝技术手册[M]. 2版. 北京:化学工业出版社,2012:10 - 45.
[2] 李长海,汪颖军,孙丽丽. 烟道气脱硫技术研究进展[J]. 西部煤化工,2007(2):63 - 68.
[3] 李肇全. 工业脱硫脱硝技术[M]. 北京:化学工业出版社,2014:15 - 55.
[4] 张星辰. 离子液体:从理论基础到研究进展[M]. 北京:化学工业出版社,2009:45 - 65.
[5] 汪多仁. 绿色增塑剂[M]. 北京:科技文献出版社,2011:112 - 119.
[6] 张英锋,李长江,包富山,等. 离子液体的分类、合成与应用[J]. 化学教育,2005(2):7 - 12.
[7] 姜海超. 离子液体性质及其与SO2相互作用机理研究[D]. 北京:北京化工大学,2012.
[8] 杜红彩. 醇胺类离子液体的合成及其在烟气脱硫中的性能研究[D]. 南京:南京理工大学,2008.
[9] 刘超,王建英,程刘备,等. 丙胺类离子液体的合成及其脱硫性能[J]. 化工环保,2016,36(1):78 - 83.
[10] 王晨星,任树行,侯玉翠,等. 乙醇胺乳酸盐离子液体吸收SO2过程中的物理化学性质[J]. 化工学报,2015,66(S1):17 - 24.
[11] 中国石化集团上海工程有限公司. 化工工艺设计手册:上册[M]. 4版,北京:化学工业出版社,2010:466 - 500.
[12] 中国石化集团上海工程有限公司. 油化工设备设计选用手册:塔器[M]. 北京:化学工业出版社,2010:215 - 400.
[13] 徐宝东. 化工管路设计手册[M]. 北京:化学工业出版社,2011:150 - 189.
[14] 杜军驻. 散装填料塔设计及核算软件开发[D]. 青岛:青岛科技大学,2013.
[15] 北京博奇电力科技有限公司企业技术标准化委员会.BQ XXXX-2007 湿法烟气脱硫化学分析方法 亚硫酸盐的测定 碘量法[S/OL]. 北京:北京博奇电力科技有限公司,2007[2017-01-03]. http://www.docin.com/p-1546637578.html.
[16] 环境保护部. GB 13271—2014 锅炉大气污染物排放标准[S]. 北京:中国环境科学出版社,2014.
Preparation and pilot test of new type adsorbent for flue gas desulfurization in thermoelectric plant
Zhang Zhaoyun,Liu Chao,Lü Xiaoying
(Tangshan Sanyou Chemical Industries Co. Ltd,Tangshan Hebei 063305,China)
Ethanolamine lactate was synthesized using ethanolamine,lactic acid and ethanol,and then was compounded with water to prepare the ethanolamine lactate ionic liquid desulfurization adsorbent(ELIL adsorbent)with 15% of water content. The SO2absorption performance and reusability of ELIL adsorbent were studied in a pilot desulfurization test. The test results showed that:The relationship between sulfur capacity(based on SO2calculation)and absorption time was a linear function in the process of absorption for 72 h;The viscosity of ELIL adsorbent reached maximum when the sulfur capacity was about 3.0%;When the pilot test was carried out using the simulated fl ue gas with 0.69% of w(SO2)for 72 h,the SO2mass concentration in the exhaust gas was much less than 50 mg/cm3,which met the emission standard of GB13271-2014;After used for 5 times,the saturated sulfur capacity of the ELIL adsorbent was basically stable at 4.6% which indicated that the reusability of the ELIL adsorbent was good;With the increase of reuse time,the SO42-accumulation increased gradually and the desulfurization capability of ELIL adsorbent could be improved by adding Ca(OH)2to remove SO42-.
flue gas desulfurization;ionic liquid;ethanolamine lactate;absorption;desorption;pilot test
X511
A
1006-1878(2017)05-0557-05
10.3969/j.issn.1006-1878.2017.05.012
2017 - 01 - 19;
2017 - 06 - 14。
张兆云(1971—),男,河北省唐山市人,学士,高级工程师,电话 13483539428,电邮 zhang924001@126.com。联系人:刘超,电话 18730516939,电邮 1004503081@qq.com。
(编辑 叶晶菁)
