Ni2P/SBA-15耦合[Bmim]BF4催化加氢脱氮的新过程
2017-10-16陈能王红岩张香平李春山高金森
陈能,王红岩,张香平,李春山,高金森
(1中国石油大学(北京)重质油国家重点实验室,北京 102249;2中国科学院过程工程研究所多相复杂系统国家重点实验室,离子液体清洁过程北京市重点实验室,北京 100190)
Ni2P/SBA-15耦合[Bmim]BF4催化加氢脱氮的新过程
陈能1,2,王红岩2,张香平2,李春山2,高金森1
(1中国石油大学(北京)重质油国家重点实验室,北京 102249;2中国科学院过程工程研究所多相复杂系统国家重点实验室,离子液体清洁过程北京市重点实验室,北京 100190)
通过改性固体催化剂,耦合离子液体进行催化反应,实现了在温和条件下催化加氢脱氮性能的提高。采用助剂Mo对Ni2P/SBA-15催化剂进行改性,并用XRD、BET、XPS对催化剂结构进行表征。以吡啶为含氮模型化合物,将固体催化剂耦合[Bmim]BF4在温和的条件下进行加氢脱氮活性评价。结果表明,低温时的脱氮过程主要以离子液体萃取为主;随着温度的升高,耦合加氢脱氮效果表现显著,且改性后的5% Mo-25% Ni2P/SBA-15催化剂耦合离子液体在150℃、3 MPa的条件下评价脱氮率最高,达到了80.1%。离子液体4次加氢循环之后,其加氢性能没有明显的下降。离子液体的参与使得催化加氢脱氮反应在温和的条件下得以实现,这为催化加氢在低温低压条件下提供了新的理论和工艺。
离子液体;耦合;催化剂;加氢;萃取;脱氮;温和
Abstract:Catalytic hydrodenitrogenation under mild conditions was improved by using modified solid catalyst coupled with [Bmim]BF4ionic liquid.Ni2P/SBA-15 catalyst was modified with different Mo loadings and structures of Mo-Ni2P/SBA-15 modified catalysts were characterized by N2adsorption-desorption,X-ray diffraction,and X-ray photoelectron spectroscopy.These catalysts coupled with [Bmim]BF4were evaluated for denitrification of pyrrolidine model compound in batch reactor at mild pressure and temperature.The results showed that Mo addition improved catalytic hydrodenitrogenation activity.At low temperature,the denitrification process was dominated by ionic liquid extraction.As temperature was increased,coupling hydrodenitrogenation was more obvious.5%Mo-25%Ni2P/SBA-15 catalyst coupled with [Bmim]BF4exhibited the best hydrodenitrogenation efficiency up to 80.1% at 150℃ and 3 MPa.Furthermore,the ionic liquid did not show significant decrease in hydrogenation efficiency after four cycles.The presence of ionic liquids achieved good catalytic hydrodenitrogenation under mild conditions,which could be a new process for catalytic hydrogenationunder low temperature and pressure conditions.
Key words:ionic liquid; coupling; catalyst; hydrogenation; extraction; denitrification; mild
引 言
页岩油为油母页岩的有机质热裂解后的产物[1]。统计表明:世界油页岩的储量相当于4000亿吨的页岩油,远远超过天然原油的储量,是一种理想的石油代替能源。我国页岩油年产量为80×104t,这对缓解我国石油对外依存具有深远的意义[2-4]。然而页岩油中含有大量的不饱和烃和氧、硫、氮等杂原子有机物,尤其是含氮有机物含量高[5-7]。这些含氮有机物不仅影响油品的安定性,而且会产生大量的氮氧化物,对大气和环境造成污染。因此,页岩油的深度脱氮对清洁燃料的生产具有十分重要的意义。
常见的脱氮技术有溶剂萃取法、吸附法等[8],其中最为普遍和有效的方法是催化加氢技术。但加氢反应在高温高压的条件下能耗高,设备投入成本大,还容易导致催化剂积炭和结焦。因此,需要探究一种在温和条件下催化加氢的新途径。
离子液体作为阳离子和阴离子构成的一类特殊物质,具备挥发性极低、特殊氢键和极性可调及可设计性的独特性能,在众多领域都有着广泛的应用。特别是作为新型溶剂/催化剂,离子液体不但可以改变固体催化剂与油品之间的界面张力,使得氢分子的转移更加自由,而且可有效抑制氢气的析出,增加液相中的氢含量,提高加氢效率[9-10]。近年来,离子液体在加氢饱和、脱硫、脱氮方面[11-14]的研究逐渐成为热点,也有文献报道耦合催化剂离子液体在温和条件下促进加氢反应的研究成果。如Dai等[15]将固体催化剂耦合离子液体在低温低压下进行了加氢脱硫实验,发现离子液体提高了催化剂的加氢脱硫性能,Yao等[16]在温和条件下进行了催化剂耦合离子液体加氢脱氮实验,研究结果表明氢气溶于离子液体有利于氢气在固体催化剂内表面的扩散,从而提高了催化剂的脱氮性能,且对离子液体进行了筛选发现[Bmim]BF4耦合催化剂脱氮效果最佳。
本文将实验室中最常见的Ni2P/SBA-15催化剂进行优化,并以吡啶为模型化合物,在温和条件下评价不同催化剂耦合[Bmim]BF4离子液体的加氢脱氮性能,并探究了助金属催化剂Mo对Ni2P/SBA-15催化剂结构的影响以及对催化剂耦合离子液体加氢脱氮性能的影响。
1 实验部分
1.1 试剂材料与仪器
硝 酸 镍 [Ni(NO3)2·6H2O]、 磷 酸 氢 二 铵[(NH4)2HPO4]、六水合硝酸钴[Co(NO3)2·6H2O]、偏钨酸铵[(NH4)6W7O24·6H2O]、偏钒酸铵(NH4VO3)、九水硝酸铬[Cr(NO3)3·9H2O]、四水合钼酸铵[(NH4)6Mo7O24·4H2O]、吡啶、硝酸、正己烷均为分析纯,购于西陇化工股份有限公司;1-丁基-3-甲基咪唑四氟硼酸盐购于林州市科能材料科技有限公司;SBA-15分子筛购于南京先丰纳米材料科技有限公司。
1.2 催化剂的制备
催化剂的制备采用等体积浸渍法。将Ni/P摩尔比为2的(NH4)2HPO4和Ni(NO3)2·6H2O分别配成溶液,采用二次浸渍法将SBA-15加入溶液中,室温浸渍12 h,再以120℃干燥12 h,空气气氛中550℃焙烧4 h,得到Ni2P/SBA-15催化剂的前体,然后80 ml·min−1的 H2气氛中升温还原活化。升温程序为:从室温以 10℃·min−1升到 300℃,然后以 1℃·min−1的升温速率至650℃且保持温度2 h,自然冷却至室温。最后通入 80 ml·min−11%O2-99%Ar气氛中钝化2 h,从而得到Ni2P/SBA-15催化剂。同样的方法分别与 Mo、W、Co、Cr、V的盐溶液进行二次浸渍,制得负载不同助剂的X-Ni2P/SBA-15催化剂(X为Mo、W、Co、Cr、V)。
1.3 催化剂的性能评价
加氢脱氮催化剂的评价在微型间歇浆态床反应器上进行。模型油为含氮量为100 mg·m−3的吡啶-正己烷溶液。将固体催化剂均匀地分布在离子液体中,并与模型油搅拌均匀。在一定压力的H2和温度下进行充分反应。
采用硫氮分析仪测定模型油加氢反应前后的含氮量,通过式(1)得出催化剂的脱氮率。
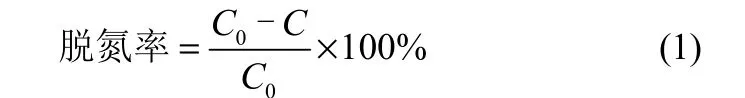
式中,C0为反应前的模型油的含氮浓度,C为模型油反应后的含氮浓度。
1.4 催化剂的表征
1.4.1 X射线粉末衍射分析 采用 X'Pert PROMPD的XRD射线衍射仪对催化剂样品进行检测表征,光源为CuKα射线(λ=0.154187 nm),管电压40 kV,电流为 30 mA,扫描速率为 10 (°)·min−1,扫描角度 2θ为 5°~90°。
1.4.2 物理吸附-脱附等温线测试 采用Autosorb-1型BET技术测定催化剂的比表面积、孔容和孔径。以氮气为介质,300℃下脱气6 h,液氮温度下吸附和脱附。
1.4.3 X射线光电子能谱 采用ESXALab220I-XL型X射线光电子能谱仪(VG Scientific公司)进行分析。激发源为AlKα,其功率为300 W,其测试的真空度为3×10−7Pa,且C l s峰以284.5 eV较正。
2 实验结果与讨论
2.1 催化剂表征
2.1.1 催化剂的物相分析图1是不同助剂7%X-25%Ni2P/SBA-15 (X为Mo、Co、W、Cr、V)的 XRD谱图。不同助剂的加入,7%X-25%Ni2P/SBA-15 在 2θ为 40.8°、44.7°、47.5°、54.3°和55.1°均出现了主要物相为Ni2P的特征峰,即P/Ni摩尔比为0.5的情况下,Mo、Co、W、Cr、V等金属助剂的加入,所得到的7%X-25%Ni2P/SBA-15催化剂主要物相依然是Ni2P,表明这些助剂的加入对Ni2P物相成分几乎不产生影响。但有些助剂的加入会产生新的物相,如Mo-Ni2P/SBA-15催化剂在2θ为 31.0°和 45.1°处呈现了 MoNiP2物相的特征峰。W-Ni2P/SBA-15催化剂在2θ=48.8°处出现了WP4物相的衍射峰。有些助剂的加入有助于Ni2P更加均匀地分散在载体的孔道中,如Cr的加入,Ni2P的衍射峰强度有所下降,表明Cr有助于Ni2P在载体孔道中均匀分散。

图1 wX-Ni2P/SBA-15催化剂的XRD谱图Fig.1 XRD patterns ofwX-Ni2P/SBA-15 catalysts1—Ni2P/SBA-15; 2—Mo-Ni2P/SBA-15; 3—Co-Ni2P/SBA-15;4—W-Ni2P/SBA-15; 5—Cr-Ni2P/SBA-15; 6—V-Ni2P/SBA-15
图2为不同Mo负载量的Mo-Ni2P/SBA-15催化剂的XRD谱图。由图可知,4种催化剂的2θ为40.8°、44.7°、47.5°、54.3°和 55.1°均出现了主要物相为 Ni2P的特征峰,且随着 Mo负载量的增加,Ni2P衍射峰的位置不变,这与Korányi等[17]的研究结果及标准衍射峰(PDF03-0953)相一致。当 Mo负载含量为1%、5%时,基本没有明显Mo的衍射峰,说明低负载量的Mo较好地分散在载体的孔道中,但促使Ni2P物相的晶型增强。
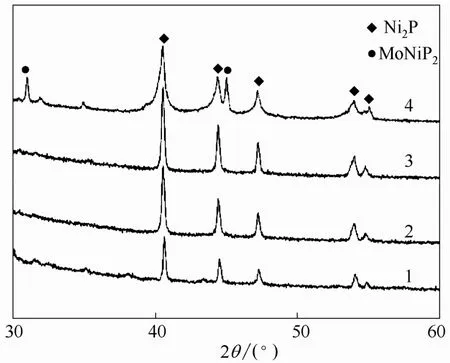
图2 不同Mo负载量的Mo-Ni2P/SBA-15催化剂的XRD谱图Fig.2 XRD patterns of Mo-Ni2P/SBA-15 catalysts with different Mo loadings 1—25%Ni2P/SBA-15; 2—1% Mo-25%Ni2P/SBA-15;3—5% Mo-25%Ni2P/SBA-15; 4—9% Mo-25%Ni2P/SBA-15
当Mo负载量为9%时,催化剂在2θ为31.0°和45.1°处出现了MoNiP2的特征峰,且发现此时的Ni2P的特征峰强度稍有减弱,这也说明了一定量Mo有助于Ni2P的分散并与之形成了晶相MoNiP2。2.1.2 催化剂的BET表征 由表1中不同Mo负载量的 Mo-Ni2P/SBA-15催化剂的孔结构性质参数可以得知,随Mo负载量的增加,其比表面积存在略减少的趋势,说明Mo负载量的增大会堵塞催化剂的孔道,从而会降低催化剂的比表面积。

表1 不同Mo负载量的Mo-25%Ni2P/SBA-15催化剂的孔结构理化性质Table 1 Pore structure parameters of Mo-25%Ni2P/SBA-15 catalyst with different Mo loadings
2.1.3 催化剂表面的元素价态(XPS) 图 3是不同Mo负载量的Mo-Ni2P/SBA-15催化剂的XPS谱图。不同价态的Ni、Mo、P的峰面积分析所得的Niδ+、Pδ−、Moδ+相对含量见表2。图3(a)中 Ni 2p3/2结合能的峰值在853.4~853.7 eV,归属于Ni2P和MoNiP2物相中的 Niδ+(0<δ<2),而 857.6~857.8 eV 归属于Ni3(PO4)2中的 Ni2+[18],当 Mo 的负载量增加时,Niδ+的相对含量随之增加,这说明 Mo的加入有助于MoNiP2新相的形成。图3(b)表示的是P 2p2/3的结合能位于129.3~129.5 eV归属于Ni2P、MoNiP2的Pδ−[19],而134~134.2 eV归属于P2O5或者Ni3(PO4)2的P5+[20],其相对含量较大,是因为少量的P参与形成金属磷化物,大部分P以催化剂表面钝化的氧化物而存在。图3(c)中Mo的结合能为228.1和231.1 eV的特征峰属于金属磷化物中的 Mo 3d5/2和 Mo 3d3/2的 Moδ+(0<δ<4),位于 233.1 和 236.0 eV 的特征峰则属于Mo 3d5/2和Mo 3d3/2的Mo6+[21],即在各个催化剂中,Moδ+的相对含量变化不大。

图3 不同Mo负载量的Mo-Ni2P/SBA-15催化剂的XPS 谱图Fig.3 X-ray photoelectron spectra of Mo-Ni2P/SBA-15 catalysts with different Mo loadings 1—Ni2P/SBA-15; 2—1% Mo-Ni2P/SBA-15; 3—5% Mo-Ni2P/SBA-15;4—9% Mo-Ni2P/SBA-15
2.2 催化剂的脱氮性能评价
2.2.1 不同Ni负载量的Ni2P/SBA-15脱氮性能的比较 图4是不同Ni负载量下的Ni2P/SBA-15催化剂的脱氮性能。可知,当Ni负载量为25%时,其脱氮率达到了 55.1%,这与 Ni负载量为 35%的Ni2P/SBA-15脱氮率达到的 56.2%基本持平,因此进一步把25%Ni负载量的Ni2P/SBA-15催化剂进行优化。
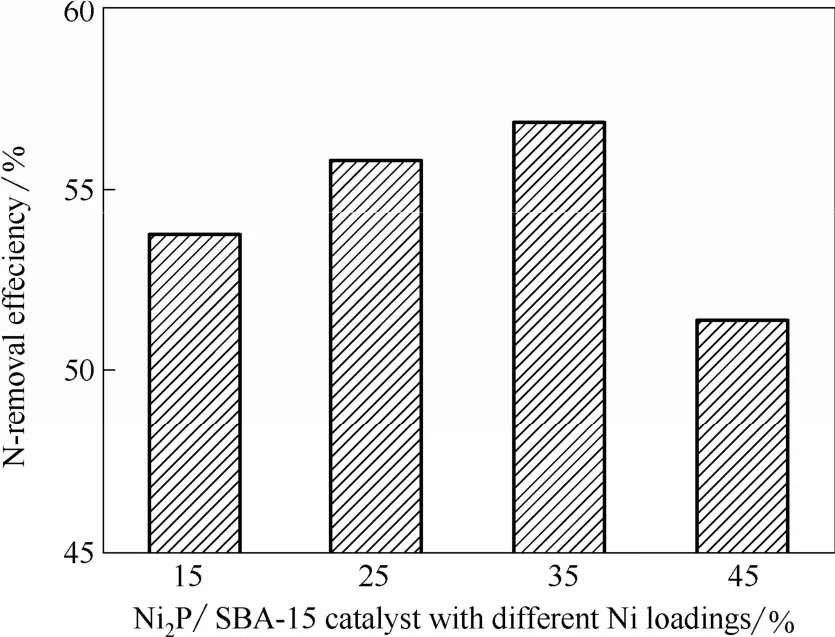
图4 不同Ni负载量的Ni2P/SBA-15催化剂对脱氮性能的影响Fig.4 Effect of Ni2P/SBA-15 catalysts with different Ni-loadings on N-removal efficiency
2.2.2 负载不同助催化剂的Ni2P/SBA-15对脱氮性能的影响 采用二次浸渍法将 25%的 Ni含量和Mo、W、Co、Cr、V的7%含量负载于SBA-15介孔分子筛上的催化剂探究其耦合离子液体加氢脱氮性能。图5是这6种催化剂耦合离子液体进行加氢脱氮反应时的脱氮效果,结果发现催化剂的脱氮效果依次为:Mo-Ni2P/SBA-15>W-Ni2P/SBA-15> Ni2P/SBA-15>Cr-Ni2P/SBA-15>Co-Ni2P/SBA-15>V-Ni2P/SBA-15。这表明二元组分的催化剂中,Mo、W分别和 Ni互相配合形成的催化剂表现出较高的脱氮性能,从而提高了催化剂耦合离子液体加氢反应的脱氮率。

表2 不同Mo负载量的Mo-Ni2P/SBA-15催化剂的XPS结果Table 2 XPS results of Ni2P/SBA-15 catalysts with different Mo loadings
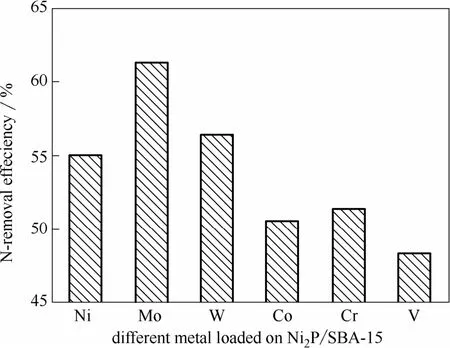
图5 不同助剂对Ni2P/SBA-15催化剂脱氮性能的影响Fig.5 Effect of Ni2P/SBA-15 catalysts with different kinds of additives on N-removal efficiency
2.2.3 不同催化剂的温度-脱氮率曲线 图 6是5%~25%Ni2P/SBA-15耦合4 g [Bmim]BF4离子液体在模型油为20 g、压力为3 MPa的条件下考察温度对催化剂耦合离子液体的加氢脱氮性能的影响。当温度为60~90℃时,曲线5中,催化剂加氢脱氮的效果只有11.3%和13.8%,曲线6中可知随着温度的变化,离子液体萃取脱氮变化不大,60℃时的脱氮率为18.7%,而60℃条件下的催化剂耦合离子液体脱氮率为23%,仅比萃取高4.3%,即催化剂加氢脱氮效果忽略不计;在低温的情况下,不同 Mo负载量的催化剂耦合离子液体催化加氢的脱氮效果相差不明显,因此低温条件下,催化剂加氢效果不显著,催化剂耦合离子液体主要是萃取为主导的脱氮过程。当温度达到90℃以上,甚至达到150℃的条件下,最佳的5% Mo-25%Ni2P/SBA-15耦合达到了 81.3%,其加氢性能要高于催化剂加氢脱氮和萃取脱氮的加和,这也说明在较高的温度条件下,离子液体对加氢催化具有促进作用。
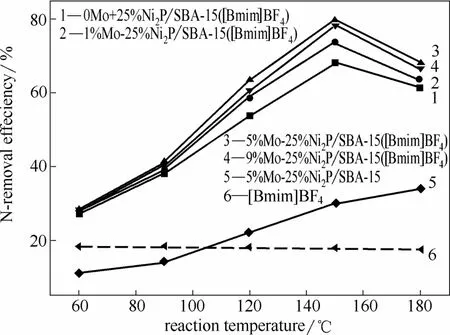
图6 不同温度和不同Mo负载量的Mo-Ni2P/SBA-15催化剂对脱氮性能的影响Fig.6 Effect of Ni2P/SBA-15 catalysts with different Mo loadings and reaction temperature on N-removal efficiency
通过GC-MS检测分析,较高温反应中检测发现模型油中含有2-丁烯、丁烷、戊烷和四氢吡啶,说明了耦合的加氢反应;低温条件下,这些物质几乎没有,所以进一步验证了低温条件下为萃取主导的脱氮过程。
当温度超过 180℃,催化性能出现了下降的趋势。Liang等[22]采用非等温热重分析法 TG对[Bmim]BF4分解温度进行研究,表明较长时间的实验会导致其分解,且长时间实验后的离子液体所耐用的最高温度低于其初始实验时所耐用的最高温度。因此高于 180℃加氢脱氮活性的下降是由于离子液体的分解,失去了耦合催化剂的作用。纵向来看,5% Mo-Ni2P/SBA-15时催化性能最佳,脱氮率达到了80.1%。
2.2.4 压力对脱氮性能的影响 图 7是 5%~25%Ni2P/SBA-15耦合4 g [Bmim]BF4离子液体在模型油为20 g,温度为150℃的条件下考察催化剂耦合离子液体的加氢脱氮性能。研究表明,当系统的压力小于3 MPa时,压力的增大有利于溶于离子液体中,并与催化剂充分接触,进而脱氮率呈上升的趋势。当达到3 MPa时,脱氮率达到最大,随压力的进一步增大,脱氮率呈现略微下降的趋势,这是由于系统气氛中NH3的增加和加氢之后的含氮化合物的累积抑制了催化剂的催化性能[23-24]。

图7 加氢压力对催化剂脱氮性能的影响Fig.7 Effect of hydrogen pressure on N-removal efficiency
2.3 离子液体的循环使用过程
在加氢体系中,离子液体能否再生或者重复使用也是考察其耦合加氢脱氮性能的重要指标[25]。通过抽滤、分液、烘干、再循环使用,结果如图8所示,参与加氢反应前后的[Bmim]BF4的化学结构没有发生变化。[Bmim]BF4首次加氢反应脱氮率为80.1%,经过 4次循环使用后,发现加氢脱氮性能没有明显的下降,这表明了离子液体循环使用性能良好(表3)。

图8 参与反应前后的[Bmim]BF4的FT-IR谱图Fig.8 FT-IR spectra of [Bmim]BF4before and after reaction
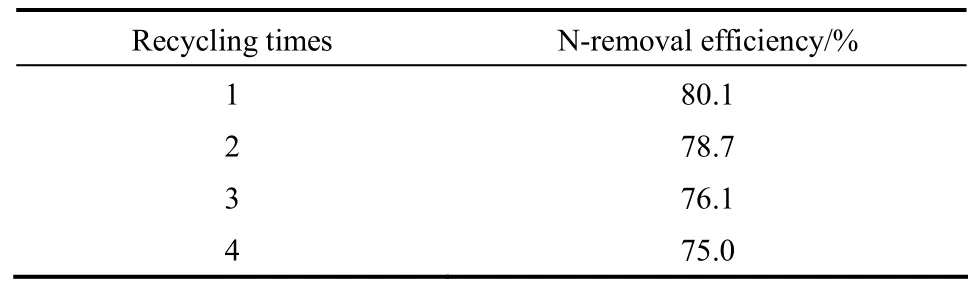
表3 离子液体的循环使用对脱氮性能的影响Table 3 Effect of regeneration of ILs on N-removal efficiency
2.4 固体催化剂耦合离子液体加氢脱氮机理
固体催化剂耦合离子液体加氢脱氮的过程如图8所示。在加热搅拌的条件下,氢气充分扩散到模型油、离子液体耦合的固体催化剂表面,离子液体由于氢键作用在固体催化剂表面形成油膜,促进氢气的传递,加快了催化剂表面的扩散速率,进而将影响到加氢催化反应的效率。从文献[16]中通过模拟计算得知,氢气与离子液体之间的作用键能(例如氢气与[Bmim]BF4的作用键能为 2.5405 kJ·mol−1)远远大于氢气与正己烷之间的作用键能(0.0029 kJ·mol−1),表明了离子液体本身与 H2有较强的作用力,比模型油的溶剂具有较高的溶氢效率。更重要的是,反应底物在离子液体中的溶解度对催化加氢具有重要作用[26-27],实验表明,反应底物吡啶在离子液体中有一定的溶解度,即离子液体萃取反应底物吡啶,且同时将氢气与吡啶更好地扩散在催化剂的表面,从而提高了加氢催化反应的效率。
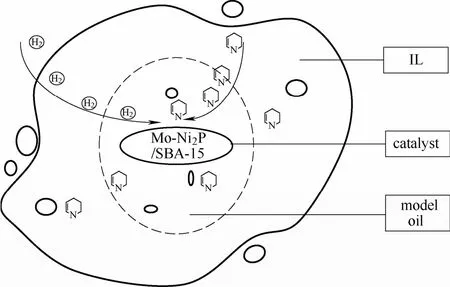
图9 固体催化剂耦合离子液体催化加氢的过程Fig.9 Process of catalytic hydrodenitrogenation by solid catalyst coupled with ionic liquids
3 结 论
本研究采用固体催化剂耦合离子液体实现了在温和条件下的加氢脱氮过程。结果表明,5%Mo-25%Ni2P/SBA-15催化剂耦合[Bmim]BF4离子液体表现较高的脱氮性能,这是因为Mo促进了催化活性,这在耦合离子液体加氢脱氮的过程中起到了关键性的作用。
催化剂耦合离子液体加氢反应的过程中,当温度低于90℃,系统的脱氮过程主要表现为离子液体的萃取脱氮作用,当温度不断升高,催化加氢脱氮表现明显,且催化剂耦合离子液体加氢脱氮效率随之提高,在温度为150℃、压力为3 MPa的反应条件下加氢脱氮活性最佳,脱氮率高达 80.1%。离子液体的氢键作用在固体催化剂表面形成了液膜,同时将氢气与吡啶更好地扩散在催化剂的表面,从而提高了加氢催化反应的效率,这相对于固体催化剂加氢和离子液体萃取而言,脱氮性能有了较大改善。将离子液体耦合催化剂循环反应4次之后,脱氮活性未见明显降低,表明了离子液体表现出良好的重复再生能力。
[1]侯祥麟.中国页岩油工业[M].北京: 石油工业出版社,1984: 153.HOU X L.China Shale Oil Industry [M].Beijing: Petroleum Industry Press,1984: 153.
[2]钱家麟,伊亮.油页岩——石油的补充能源[M].北京: 中国石化出版社,2008.QIAN J L,YI L.Oil Shale—Oil Supplementary Energy [M].Beijing:China Petrochemical Press,2008.
[3]王清强,马跃,李术元,等.世界油页岩资源研究开发利用近况——并记 2016 年国外两次油页岩国际会议[J].中外能源,2017,22(1): 23-29.WANG Q Q,MA Y,LI S Y,et al.International oil shale resources research and development status — and in 2016 foreign oil shale two international conference [J].Chinese and Foreign Energy,2017,22(1): 23-29.
[4]ZHAO C,CHEN B.China's oil security from the supply chain perspective:a review[J].Applied Energy,2014,136(31): 269-279.
[5]徐明,陈登峰,肖双全,等.大庆页岩油脱氮工艺实验研究[J].石油学报 (石油加工),2012,28(1): 55-59.XU M,CHEN D F,XIAO S Q,et al.Experimental study on denitrification process of Daqing shale oil [J].Journal of Petroleum Science(Petroleum Processing),2012,28(1): 55-59.
[6]DIJKMANS T,DJOKIC M R,VAN GEEM K M,et al.Comprehensive compositional analysis of sulfur and nitrogen containing compounds in shale oil using GC×GC-FID/SCD/NCD/TOF-MS[J].Fuel,2015,140(15): 398-406.
[7]李楠,王斌,杨朝合,等.页岩油窄馏分性质表征及其催化裂化性能研究[J].石油炼制与化工,2016,47(2): 16-20.LI N,WANG B,YANG C H,et al.Studies on characterization and catalytic cracking performance of shale oil narrow fraction [J].Petroleum Processing and Chemical Industry,2016,47(2): 16-20.
[8]栾业志.抚顺页岩油组分分析和喹啉在 NiW/γ-Al2O3催化剂上的加氢脱氮研究 [D].大连: 大连理工大学,2009.LUAN Y Z.Fractional shale oil composition analysis and quinoline hydrogenation on NiW/γ-Al2O3catalyst [D].Dalian: Dalian University of Technology,2009.
[9]张锁江,刘晓敏,姚晓倩,等.离子液体的前沿、进展及应用[J].中国科学 (B辑: 化学),2009,39(10): 1134-1144.ZHANG S J,LIU X M,YAO X Q,et al.Forefront,development and application of ionic liquid [J].Science in China,Series B: Chemistry,2009,39(10): 1134-1144.
[10]MEYER C,HAGER V,SCHWIEGER W,et al.Enhanced activity and selectivity inn-octane isomerization using a bifunctional SCILL catalyst[J].Journal of Catalysis,2012,292(8): 157-165.
[11]DUPONT J,FONSECA G S,UMPIERRE A P,et al.Transition-metal nanoparticles in imidazolium ionic liquids: recyclable catalysts for biphasic hydrogenation reactions[J].Journal of the American Chemical Society,2002,124(16): 4228-4229.
[12]DYSON P J,ELLIS D J,WELTON T,et al.Arene hydrogenation in a room-temperature ionic liquid using a ruthenium cluster catalyst[J].Chemical Communications,1999,(1): 25-26.
[13]STANISLAUS A,MARAFI A,RANA M S.Recent advances in the science and technology of ultra low sulfur diesel (ULSD)production[J].Catalysis Today,2010,153(1): 1-68.
[14]ZHANG S,ZHANG Q,ZHANG Z C.Extractive desulfurization and denitrogenation of fuels using ionic liquids[J].Industrial &Engineering Chemistry Research,2004,43(2): 614-622.
[15]DAI F,MUHAMMAD Y,GONG X,et al.Low-temperature and low-pressure fuel hydrodesulfurization by solid catalyst coupling with ionic liquids[J].Fuel,2014,134(15): 74-80.
[16]YAO H,WANG G,ZUO C,et al.Deep hydrodenitrification of pyridine by solid catalyst coupling with ionic liquids under mild conditions[J].Green Chemistry,2017,19(7): 1692-1700.
[17]KORÁNYI T I,PFEIFER É,MIHÁLY J,et al.Infrared spectroscopic investigation of CO adsorption on SBA-15and KIT-6-supported nickel phosphide hydrotreating catalysts[J].The Journal of Physical Chemistry A,2008,112(23): 5126-5130.
[18]WANG Z J,WU P Y,LAN L,et al.Preparation,characterization and hydrodesulfurization catalytic performances of Mo-Ni2P/SBA-15 catalysts[J].Acta Physico-Chimica Sinica,2015,31(3): 533-539.
[19]BUI P,CECILIA J A,OYAMA S T,et al.Studies of the synthesis of transition metal phosphides and their activity in the hydrodeoxygenation of a biofuel model compound[J].Journal of Catalysis,2012,294(10): 184-198.
[20]CECILIA J A,JIMÉNEZ-MORALES I,INFANTES-MOLINA A,et al.Influence of the silica support on the activity of Ni and Ni2P based catalysts in the hydrodechlorination of chlorobenzene.Study of factors governing catalyst deactivation[J].Journal of Molecular Catalysis A: Chemical,2013,368(3): 78-87.
[21]郭亚男,曾鹏晖,季生福,等.Mo 助剂含量对 Mo-Ni2P/SBA-15/堇青石整体式催化剂加氢脱硫性能的影响[J].催化学报,2010,31(3): 239-334.GUO Y N,ZENG P H,JI S F,et al.Effect of Mo promoter on hydrodesulfurization performance of Mo-Ni2P / SBA-15 / cordierite monolithic catalyst[J].Chinese Journal of Catalysis,2010,31(3):239-334.
[22]LIANG R,YANG M R,ZHOU Q X.Thermal stability,equilibrium vapor pressure and standard enthalpy of vaporization of 1-butyl-3-methylimidazolium tetrafluoroborate[J].Acta Physico-Chimica Sinica,2010,26(6): 1468-1472.
[23]RANA M S,NAVARRO R,LEGLISE J.Competitive effects of nitrogen and sulfur content on activity of hydrotreating CoMo/Al2O3catalysts: a batch reactor study[J].Catalysis Today,2004,98(1): 67-74.
[24]GUELTEKIN S,ALI S A,SATTERFIELD C N.Effects of hydrogen sulfide and ammonia on catalytic hydrogenation of propylbenzene[J].Ind.Eng.Chem.,Prod.Res.Dev.,1984,23(1): 179-18.
[25]WANG J,LUO J,FENG S,et al.Recent development of ionic liquid membranes[J].Green Energy & Environment,2016,1(1): 43-61.
[26]DYSON P J,LAURENCZY G,OHLIN C A,et al.Determination of hydrogen concentration in ionic liquids and the effect (or lack of) on rates of hydrogenation[J].Chemical Communications,2003,(19):2418-2419.
[27]HALLETT J P,WELTON T.Room-temperature ionic liquids:solvents for synthesis and catalysis.[J].Chemical Reviews,2011,111(5): 3508-3576.
New catalytic hydrodenitrogenation process by Ni2P / SBA-15 coupled with[Bmim]BF4
CHEN Neng1,2,WANG Hongyan2,ZHANG Xiangping2,LI Chunshan2,GAO Jinsen1
(1State Key Laboratory of Heavy Oil Processing,China University of Petroleum,Beijing102249,China;2Beijing Key Laboratory of
Ionic Liquids Clean Process,State Key Laboratory of Multiphase Complex Systems,Institute of Process Engineering,Chinese Academy of Sciences,Beijing100190,China)
O 643.3
A
0438—1157(2017)10—3755—07
10.11949/j.issn.0438-1157.20170535
2017-05-02收到初稿,2017-08-01收到修改稿。
联系人:王红岩。
陈能(1992—),男,硕士研究生。
国家重点基础研究发展计划项目(2014CB744306);国家自然科学基金项目(21576261)。
Received date:2017-05-02.
Corresponding author:WANG Hongyan,hywang@ipe.ac.cn
Foundation item:supported by the National Basic Research Program of China (2014CB744306) and the National Natural Science Foundation of China (21576261).
