活性二氧化氯降解硫代硫酸钠动力学
2017-10-16兰益周唐晓璐诸爱士
兰益周,唐晓璐,诸爱士
(1.浙江东天虹环保工程有限公司,浙江 杭州 310012;2.浙江科技学院生物与化学工程学院,浙江 杭州 310023)
活性二氧化氯降解硫代硫酸钠动力学
兰益周1,唐晓璐1,诸爱士2
(1.浙江东天虹环保工程有限公司,浙江 杭州 310012;2.浙江科技学院生物与化学工程学院,浙江 杭州 310023)
为研究活性ClO2降解Na2S2O3,考察了ClO2与 Na2S2O3摩尔比、反应温度对降解效果的影响,建立了动力学方程,得到了动力学参数。实验结果表明:ClO2降解Na2S2O3时,反应摩尔比是0.64∶1,反应温度对降解有明显影响;降解反应对ClO2和Na2S2O3均为1/2级,总级数为一级;反应速率常数,活化能 Ea=82.60 kJ/mol。
活性 ClO2;Na2S2O3;降解;动力学
硫化染料生产中用Na2S作硫化剂,多余的Na2S一部分以S2-形式随废水排放,另一部分转化为S2O32-形式存在于废水中[1-2]。直接排放,不仅浪费资源,而且对环境造成极大的污染,因此必须加以妥善处理。处理高浓度含S2O32-废水,一般先经浓缩结晶或加试剂生产工业Na2S2O3产品降低浓度[2],而后再采用降解等方法加以处理[3-4]。二氧化氯(ClO2)具有强降解性,在废水处理领域有着广泛的应用[5-9]。虽文献[10-11]报道了活性ClO2氧化Na2S2O3动力学研究,但它们测定和描述的均是反应5 s内甚至2 s内的数据和动力学行为,其工程应用性不强;同时文献[11]报道ClO2氧化过量Na2S2O3的反应进行得很快,认为反应时间约10 min体系应已达到稳态,而本研究发现反应20min后仍能测出ClO2降解过量Na2S2O3反应的进行及S2O32-浓度的变化。为了能给工程实际应用提供理论参考,试验研究了活性ClO2降解Na2S2O3,考察了摩尔比(ClO2mol数:Na2S2O3mol数,全文同)、反应温度对降解效果的影响,建立了整个降解过程的动力学方程,得到了动力学参数。
1 材料与方法
1.1 主要试验材料
活性 ClO2溶液,自制;硫代硫酸钠,Na2S2O3·5H2O,AR,杭州萧山化学试剂厂;N,N—二甲基苯二胺盐酸盐,AR,天津市化学试剂研究所。
1.2 主要试验仪器
752型紫外分光光度仪 (上海菁华科技仪器有限公司);DK-S24型恒温水浴缸 (上海精密实验设备有限公司),S212-40型恒速搅拌器 (上海申胜生物技术有限公司)。
1.3 实验步骤
用亚氯酸钠与盐酸制备活性ClO2溶液;用Na2S2O3·5H2O配制一定浓度的溶液;控制降解反应条件,在密闭500 mL圆底三口烧瓶中进行反应,采用锚式搅拌桨搅拌;在设定的时间下取样,采用降温法使反应淬灭[12],即迅速将样品瓶浸入盛有冰水的烧杯中并快速吹除可能未反应完的ClO2,快速终止反应,直接用分光光度法测定溶液中的残余S2O32-浓度。
1.4 浓度分析方法与结果表达
活性ClO2溶液浓度用分光光度法在430 nm波长下用5mm玻璃比色皿测定[13];S2O32-浓度用紫外分光光度法在220 nm下用1 cm石英比色皿直接测定[14]。
降解效果用溶液中的残余S2O32-浓度(mol/L)表达。
2 结果与讨论
2.1 S2O32-浓度与吸光度的关系曲线
取不同体积的浓度为 3.48×10-3mol/L的Na2S2O3溶液各加去离子水定容、显色,并以去离子水做空白,测量其吸光度,得到S2O32-浓度(mol/L)与吸光度的关系,见图1。
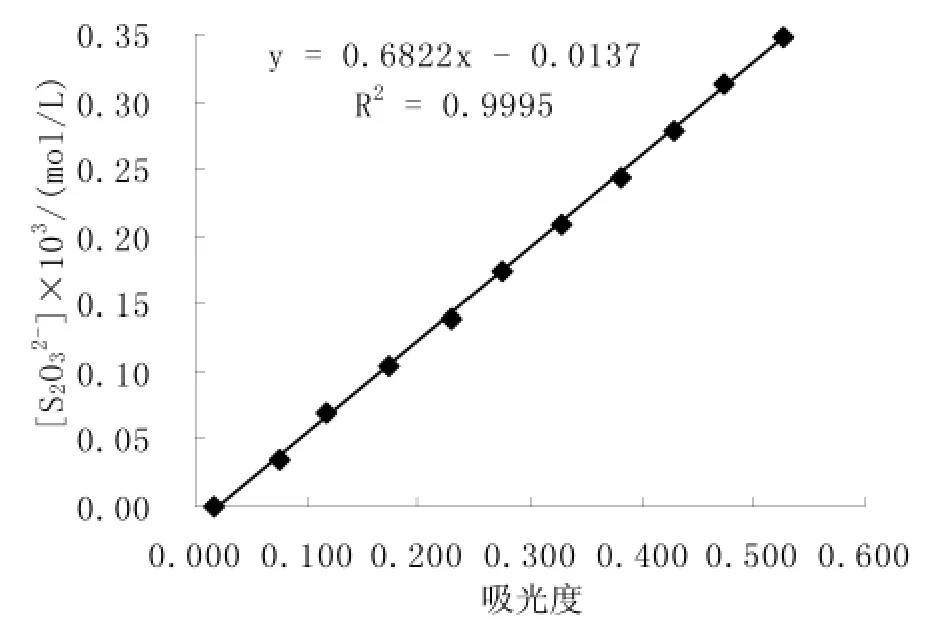
图1 S2O32-的关系曲线Fig.1 The relationship curve of S2O32-
实验中,经测定溶液吸光度后计算出溶液中Na2S2O3的摩尔浓度。
2.2 因素考察
2.2.1 投料摩尔比对降解的影响
为确定ClO2降解完Na2S2O3的真实摩尔比,考察了投料摩尔比与反应液中Na2S2O3浓度的关系。选取Na2S2O3溶液初始浓度3.43×10-3mol/L、搅拌速度50 r/min,在反应温度45℃下反应1 500 s(25 min)取样,考察投料摩尔比对降解效果的影响,进而确定实际的反应摩尔比,结果见图2。
图2表明,在投料摩尔比低于0.57时,ClO2全部被反应掉,并呈线性。当摩尔比达到0.64∶1时溶液中已经几乎测不出S2O32-,表明S2O32-已经完全被降解。因此降解时,ClO2投料时只要达到摩尔比0.64即可。
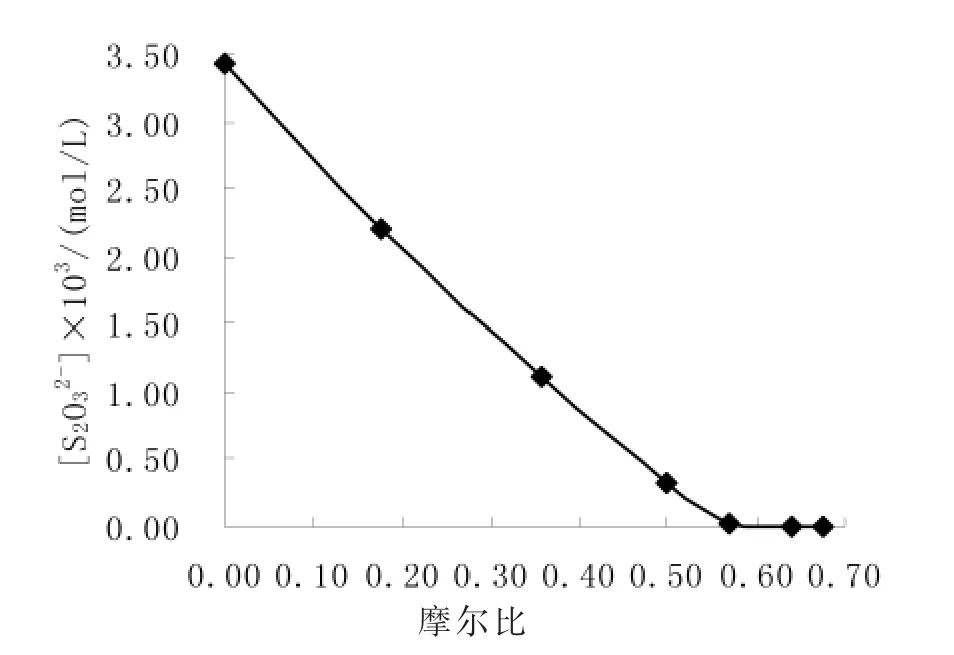
图2 摩尔比对降解S2O32-的影响Fig.2 The effects ofmolar ratio on degradation of S2O32-
2.2.2 反应温度对降解的影响
Na2S2O3溶液初始浓度3.43×10-3mol/L,摩尔比 0.64∶1,50 r/min 搅拌,测定了反应温度、反应时间与 S2O32-浓度的关系,结果见图3。
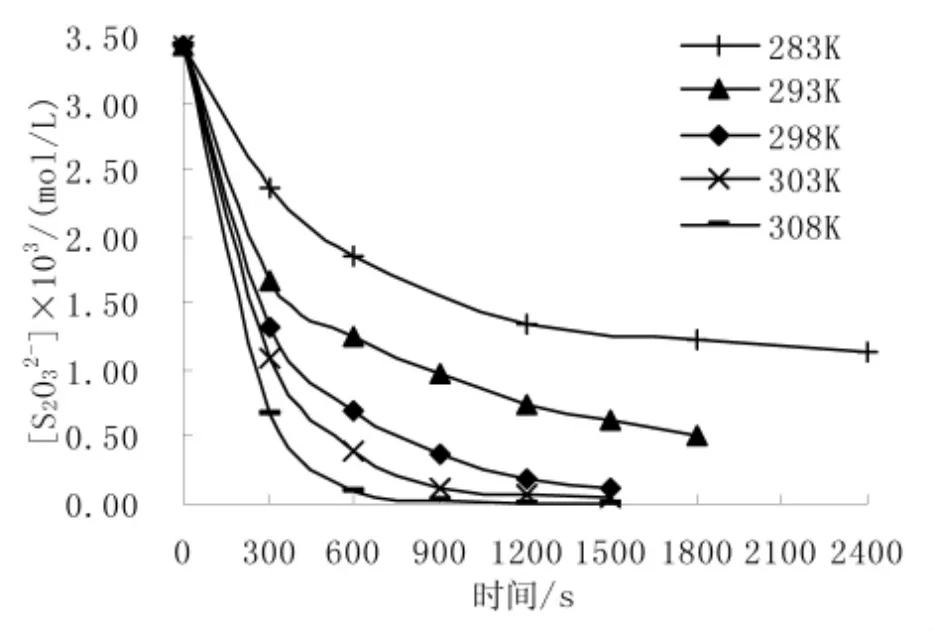
图3 反应温度、时间对S2O32-浓度的影响Fig.3 The influence of reaction temperature and time on concentration of S2O32-
从图3可以看出,相同反应时间下随反应温度的升高S2O32-浓度快速下降,即升温加快了反应速度;在低温下,反应进行2 400 s,溶液中S2O32-浓度仍很高;25℃时反应1500 s后,溶液中S2O32-浓度几乎恒定;25℃以上时,溶液中S2O32-浓度几乎为零,说明反应在1500 s内已经完成,故实际降解时温度宜控制在25℃以上。
2.3 动力学研究
2.3.1 反应级数计算
ClO2降解Na2S2O3的过程,有两个反应物参与,一般情况下该过程的反应动力学方程模型可表示为:
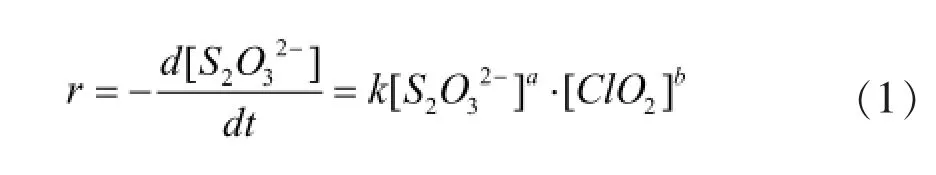
式中:r—反应速率,mol/(L·s);t—反应时间,s;k—反应速率常数,(mol/L)[(a+b)-1]/s;a、b—反应级数。
反应级数可以体现反应速率对各个组份浓度的敏感程度,a、b值越大,则S2O32-和ClO2的浓度对反应速率的影响也越大,其值对反应过程的操作设计和分析具有重要意义。
由于已经测定了两者实际反应摩尔比为0.64∶1,又每次反应开始时控制了投料比为0.64∶1,并经测定验证ClO2浓度的变化趋势与S2O32-浓度变化相同,且两者变化幅度基本符合投料比,故式(1)可写成下式(2):
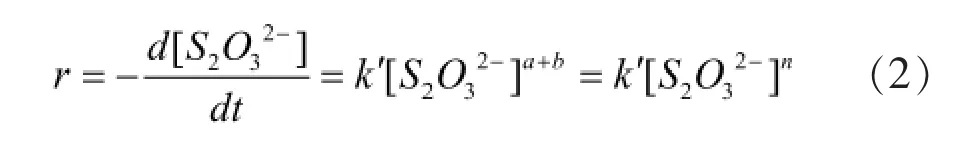
采用尝试法[12],分别作各温度的ln[S2O32-]~t图(n=1)及图(n≠1),呈现出线性关系的图对应于正确的速率方程。结果发现,各温度下的ln[S2O32-]~t图均呈现出良好的线性关系,各温度下的决定系数R2见表1,故可以确定反应的总级数为 1级,即 n=(a+b)=1。

表1 不同温度下ln[S2O32-]~t的决定系数Table 1 The determ ination coefficient of ln[S2O32-]~t at different temperatures
再确定对S2O32-和ClO2各自的级数。先对图3中5个温度的浓度与时间的关系进行多项式拟合曲线方程,要求方程的决定系数R2大于0.990以上(由于图的幅面小,这5个温度下的趋势线、方程和R2没有在图中显示),分别得到 [S2O32-]~t方程;然后对方程进行求导,得出d[S2O32-]/dt~t的关系,分别计算出测定时间下对应的r值;再根据测定的[S2O32-]~t和 [ClO2]~t关系,在(a+b)=1 的前提下,根据“对于非基元反应,反应分级数(级数)一般为零、整数或半整数(正或负)”的原理[12],对a、b的值进行组合尝试计算,计算出相应时间下的 [S2O32-]a·[ClO2]b值;最后对各温度下的r与[S2O32-]a·[ClO2]b进行拟合,如两者具有良好的线性关系,则a、b假设正确。结果表明a、b均为1/2时各温度的r与[S2O32-]a·[ClO2]b线性关系最好,各温度下的决定系数见表2。

表2 不同温度下r~[S2O32-]0.5[ClO2]0.5的决定系数Table 2 The determ ination coefficient of r~[S2O32-]0.5[ClO2]0.5at different temperatures
2.3.2 速率常数计算
拟合了各温度下的r~[S2O32-]0.5·[ClO2]0.5后,得到的各直线之斜率即为该温度下的反应速率常数k,结果见表3。
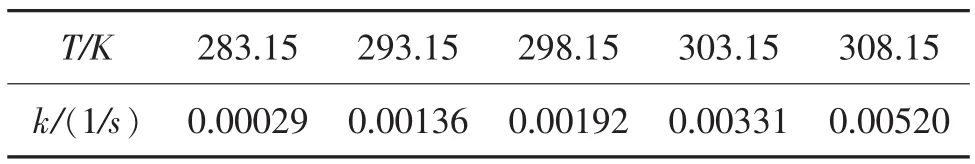
表3 不同温度下的反应速率常数Table 3 The reaction rate constant at different temperatures
2.3.3 反应活化能计算
活化能Ea体现了把反应分子“激发”到可进行反应的“活化状态”时所需的能量。所以,其值的大小直接反映了反应的难易程度,还表明了反应速率对温度的敏感度。Ea越大,所需的反应温度就越高,反应速率对温度就越敏感。
根据阿伦尼乌斯方程:
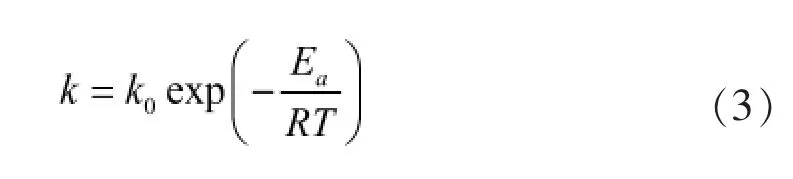
式中:k0—频率因子,1/s;Ea—反应活化能,J/mol;R—通用气体常数,8.314 J/(mol·K);T—反应温度,K。
用表3数据对该式进行拟合,先对方程(4)线性化:
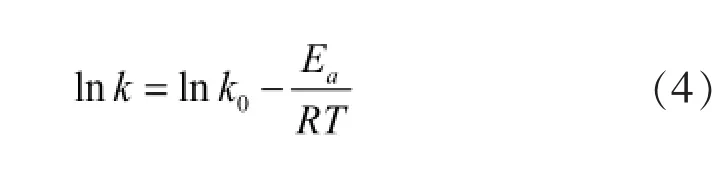
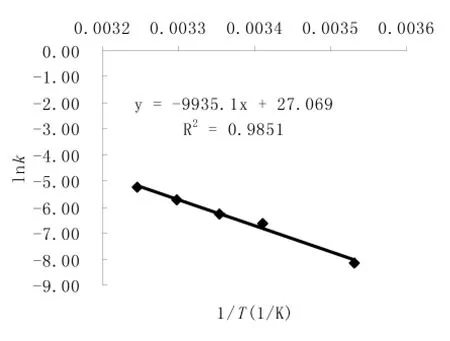
图4 lnk~1/T的关系Fig.4 The relationship of lnk and 1/T
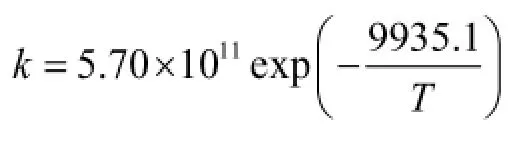
由此得出活性ClO2降解Na2S2O3总的反应速率方程:
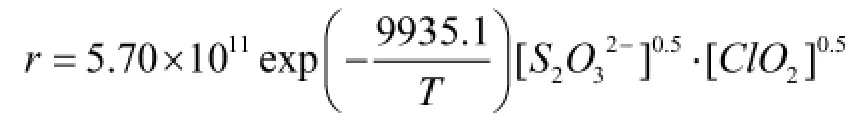
3 结语
经考察,得到用活性ClO2降解Na2S2O3的实际反应摩尔比是0.64∶1,反应温度宜控制在25℃以上。在Na2S2O3溶液初始浓度3.43×10-3mol/L,摩尔比 0.64∶1,50 r/min搅拌的条件下,活性ClO2降解Na2S2O3的反应对 Na2S2O3和ClO2均为1/2级,总级数为一级,反应速率常数k=5.70×,活化能 Ea=82.60 kJ/mol,反应速率方程是:
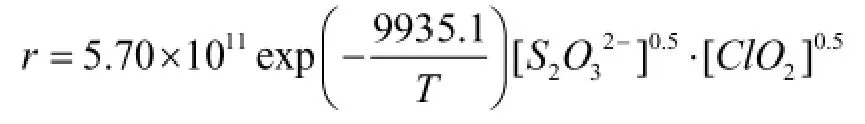
活性ClO2降解Na2S2O3速度较快、用量少,有良好的工程应用前景。
[1] 蔡瑞琳,邱勇,胡溪明,等.化工废水循环利用工艺[J].化工进展,2009,28(增刊):75-78.
[2] 毛自举,曾英杰,谷永庄.从甲萘胺生产废水中回收硫代硫酸钠[J].河南化工,1997,(7):25-26.
[3] 晋日亚,胡双启,朱智钊.硫化黑工艺母液—大苏打废水的处理研究[J].华北工学院学报,2005,26(1):38-41.
[4] 周爱民.负载型二降解钛的制备、表征及降解硫代硫酸钠生产废水的实验研究[J].河北化工,2009,32(10):12-13,45.
[5] 诸爱士,蒋家新.二降解氯杀菌剂的研究、生产及应用[J].浙江科技学院学报,2005,17(2):118-121.
[6] Loginova IV,Chukicheva IY,Kuchin A V.Oxidation of substituted phenolswith chlorine dioxide[J].Russian Journal of Organic Chemistry, 2011, 47(10):1501-1503.
[7] 李伟然,胡国勤,韩绿霞,等.稳定性二降解氯处理含硫化物和氰化物废水[J].辽宁化工,2006,35(2):81-84.
[8] Kuroshima K N ,Barreiros M A B,Lacava L A,et al.The influence of dioxide chloride on water quality of Balneário Camboriúbeach, Brazil[J].Environmental Monitoring and Assessment, 2007, 129 (1~3): 179-187.
[9] 何会玉.二降解氯高级降解技术及其在废水处理中的应用[J].科技资讯,2010,(24):128.
[10]Horváth A K, Nagypál I.Kinetics and mechanism of the reaction between thiosulfate and chlorine dioxide[J].The Journal of Physical Chemistry A, 1998, 102 (37):7267-7272.
[11]曹向禹,崔崇威,黄君礼,等.二降解氯对过量硫代硫酸钠降解的动力学[J].哈尔滨工业大学学报,2008,40(12):1923-1926,1936.
[12]天津大学物理化学教研室.物理化学(下册)[M].第5版.北京:高等教育出版社,2009:520-525.
[13]诸爱士.稳定性二降解氯活化研究[J].实验室研究与探索,2007,26(6):16-18,82.
[14]刘晓健,朱兴年.紫外分光光度法测定硫代硫酸钠溶液的含量[J].中南药学,2009,7(7):559-560.
Abstract:To research the degradation of sodium thiosulfatewith active chlorine dioxide, the influences of themolar ratio of ClO2to Na2S2O3and reaction temperature on the treatment effectwere investigated,the reaction kinetic equation was established and the kinetics parameterswere obtained.The experimental results showed that: when sodium thiosulfate was degradated by active chlorine dioxide, the reaction molar ratio was 0.64∶1, the reaction temperature had obvious influence to the degradation, the reaction of chlorine dioxide and sodium thiosulfate was 0.5-order with respect to both chlorine dioxide and sodium thiosulfate,and the overall reaction was first-order.The reaction rate constant k was 5.70×1011exp,the reaction activation energy was 82.60 kJ/mol.
Keywords:active chlorine dioxide; sodium thiosulfate; degradation; kinetics
K inetics of Sodium Thiosulfate Oxidation w ith Active Chlorine Dioxide
LAN Yi-zhou TANG Xiao-lu ZHU Ai-shi
(1.Zhejiang Dongtianhong Environmental Protection Engineering Co.,Ltd.,Hangzhou,Zhejiang310012,China;2.School of Biological and Chemical Engineering,Zhejiang University of Science and Technology,Hangzhou, Zhejiang 310023,China)
1006-4184(2017)9-0024-04
2017-05-02
兰益周(1990-),男,浙江温州人,助理工程师,主要从事环境工程项目设计工作。E-mail:810556004@qq.com。
