废旧电池黑粉中锰的回收利用方法探究
2017-10-14王焕英王晓鹏李晨雪
王焕英,王晓鹏,李晨雪
废旧电池黑粉中锰的回收利用方法探究
王焕英,王晓鹏,李晨雪
(衡水学院 化工学院,河北 衡水 053000)
以铁粉、过氧化氢等为原料,采用还原法进行废旧电池中锰的回收利用实验,探究实验室回收锰元素并合成碳酸锰的最佳条件,结果显示:在硫酸介质中使用30 %过氧化氢为还原剂,饱和碳酸氢铵为沉淀剂,可以制得较纯的碳酸锰.
废旧电池;锰;过氧化氢
我国是干电池的生产与消费大国,据统计,全国目前每年约需电池220多亿支,并且绝大多数为一次性电池,随着通信技术的迅速发展,手机的更换频率也越来越快,造成大量的废弃电池,使用后废弃的旧电池如果得不到及时处理会严重污染生活环境.同时由于目前我国在生活垃圾分类、收集、处理方面手段还不够完善,产生的大量废旧电池常常与普通生活垃圾一起混放、填埋,其中的重金属锰、汞等泄漏,会造成土壤以及地下水的污染,由此带来的环境污染与资源浪费问题日益突出.所以对废旧电池黑粉中重金属的回收和利用已成为目前需要解决的现实问题,也成为学术界目前研究热点之一.人们日常生活中用的干电池主要是无汞锰锌干电池,如果将干电池黑粉中的锌和锰进行回收利用,既可达到废旧电池的无害化,又可实现资源的再利用.
二氧化锰是锰锌干电池的正极活性物质,含量约占33 %[1],故锰的回收是目前废旧锰锌干电池回收利用的热点研究内容之一[2].碳酸锰是一种非常重要的工业原料,可用于制造电信器材软磁铁氧体,用作脱硫的催化剂、瓷釉、涂料和清漆的颜料,还可用于生产电解金属锰的原料等[3-6].因此本文对废旧无汞锰锌电池中锰的实验室回收再生方法进行了探究,采用过氧化氢还原法将锰再生为碳酸锰.
1 实验
1.1 实验流程
废旧电池黑粉中锰的回收及碳酸锰制备流程如下:
拆开电池,取粉末,称质量→加水溶解,过滤后酸浸→加热,再过滤.粉末强热,冷却→称5g粉末,加硫酸,加过氧化氢,加热溶液→冷却过滤,加氨水调节pH 5 ~ 6,以除去铁,加少量活性炭,过滤→取适量滤液,加几滴硫酸,几滴KSCN,检验铁是否除尽→配碳酸氢铵饱和溶液,加到滤液中,直至不产生沉淀为止→过滤,洗涤沉淀,烘干,称量→用配位滴定法分析Mn2+含量.
1.2 主要仪器与试剂
电磁加热搅拌器,电热炉,坩埚,酸、碱式滴定管一套,镊子,剪子,电子天平,pH试纸,表面皿,减压抽滤泵,布氏漏斗,抽滤瓶.
浓H2SO4,活性炭,碳酸氢氨固体,6 mol/L的盐酸溶液,0.05 mol/mL的EDTA标准液,氨-氯化铵(pH = 10),5 %的铬黑T指示剂,KSCN溶液.
1.3 实验步骤
1.3.1 废电池的预处理
将电池用小刀剖切,取出黑色粉末,称量,溶解(用以除去KOH,NH4Cl等),搅拌,过滤,得到黑色粉末.水洗,加硫酸浸泡,调节溶液pH值为2(用以除去铁,锌等杂质).加热约20 min,冷却后抽滤,再次水洗,得黑色粉末,主要成分为MnO2.
将黑色粉末放置在蒸发皿内,用煤气灯加强热,并不断搅拌至无红点出现.冷却,得到粉末.
1.3.2 碳酸锰的合成
称取所得粉末,用稀硫酸溶解至呈酸性,滴加30 %双氧水溶液,同时进行搅拌.当反应不再特别剧烈后,用小火加热直至样品完全溶解.再继续加热至过量的过氧化氢完全分解掉,冷却、过滤.
主要反应方程式为:MnO2+ H2O2+ H2SO4=MnSO4+ 2O2+ H2O
1) 除铁:向得到的滤液中加入1︰1 NH3·H2O,调节溶液pH值为5 ~ 6,此时可得氢氧化铁沉淀,加少量活性炭,过滤.
2) 检测铁:取上面所得滤液少许,加入硫酸和硫氰化钾,观察现象,若有血红色出现,则重复第一步;否则进行下一步.
3) 制备碳酸锰:称取一定量的NH4HCO3,放水浴锅内加热,配制成饱和溶液,将此饱和溶液缓慢加到2)所得滤液中,充分反应至不再产生白色沉淀.
主要反应方程式为:MnSO4+ 2NH4HCO3=MnCO3+ CO2+ H2O + 2(NH4)2SO4
1.3.3 碳酸锰纯度分析
称取0.18 g左右样品,加20 mL水,加6 mol/L盐酸溶液,水浴加热至样品溶解.必要时加1 ~ 2滴过氧化氢溶液至暗色褪去,再加100 mL水,2 mL10 %盐酸羟胺溶液,用0.05 mol/L EDTA标准液滴定,近终点时,加10 mL氨—氯化铵溶液(pH=10),5滴5 %铬黑T指示剂.继续滴定溶液由紫红色变为纯蓝色.
涉及的反应方程式:Mn2++H2Y2-=MnY2-+2H+,Mn %按下式计算:
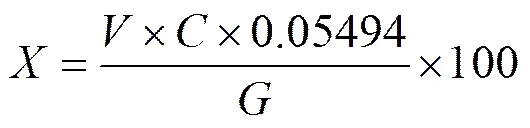
式中:—EDTA的体积;—EDTA的浓度;—样品质量;0.054 94—每毫摩尔Mn之克数.

表1 碳酸锰合成过程数据记录
1.3.4 实验现象与实验结果的记录
1.3.4.1 过程中的有关数据记录
“点破朦胧,笔画朱砂”,随着音乐响起,李校长和嘉宾以及班主任老师端起朱砂,手执毛笔,在同学们额头正中点上红痣,祝福学生们从此眼亮心明。
碳酸锰合成过程中的数据记录如表1所示.
1.3.4.2 二价锰含量的分析结果记录
碳酸锰含量测定数据及结果如表2所示.
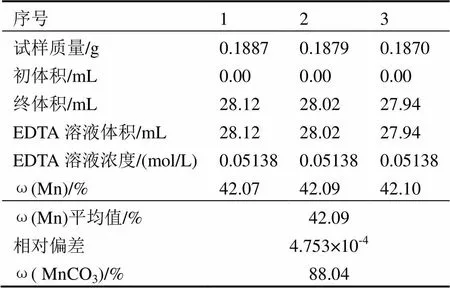
表2 碳酸锰含量测定数据记录
从表2可以看出,合成碳酸锰的纯度大于88 %,远远超过了国标工业级碳酸锰44 %的标准(国标号:CAS#:598-62-9),可用作工业生产原料.
2 结果与讨论
2.1 还原剂种类对碳酸锰产率的影响
实验过程中分别用锌粉、过氧化氢、铁粉、硫化亚铁为还原剂,反应起始物的质量为5 g,判别还原剂对碳酸锰产量的影响,结果如表3所示.
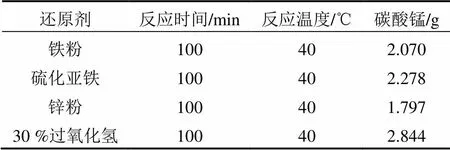
表3 还原剂对碳酸锰产量的影响
从表3可以看出,使用硫化亚铁、过氧化氢做还原剂比锌粉、铁粉生成碳酸锰的量要多,但是使用硫化亚铁容易引进硫、铁等杂质,是后续过程不好处理,而且对环境造成二次污染,所以后续过程都使用过氧化氢做还原剂.
2.2 过氧化氢用量对碳酸锰产率的影响
固定反应时间和反应温度,改变H2O2用量,结果如表4所示.

表4 还原剂用量对碳酸锰产量的影响
从表4可以看出,还原剂H2O2用量增加,MnCO3生成量也随着增加,但是当H2O2用量增大到某一程度,MnCO3生成量又逐渐减小.这是因为过氧化氢用量过低,不能将二氧化锰中的四价锰完全转化为二价锰,所以碳酸锰的生成量较少,随着过氧化氢用量的增加MnCO3的产量有明显提高,但当H2O2增加到一定程度碳酸锰的产量反而下降,这可能是因为过量的H2O2反而将生成的Mn2+氧化导致碳酸锰产量下降.
3 结论
本论文采用了人工分选与湿法相结合技术,回收废旧锌锰电池中的锰,采用条件为:用30 %过氧化氢为还原剂,硫酸介质,以饱和碳酸氢铵溶液为沉淀剂,结果得到了纯度较高的碳酸锰,回收率也比较高.而且该实验室回收方法简便易行,值得推广到实际工艺生产过程中.
[1] 李月红,王晓,赵联朝,等.由废旧锌锰电池回收氯化锰和锌的一种工艺[J].河南科技大学学报(自然科学版),2004(5):93-95.
[2] 江忠远,林永,金茜,等.还原法回收废旧锌锰电池中锰的研究[J].科技通报,2013,29(6):47-49.
[3] 陈为亮,戴永年.废旧干电池的综合回收与利用[J].再生资源研究,1999(1):30-35.
[4] 蒋玉萍,张建强,李杏兰,等.废旧锌锰干电池回收利用的探讨[J].实验技术与管理,2002(6):68-70.
[5] 胡修权,韩军,高山.高视密度碳酸锰的制备工艺[J].化工技术与开发,2004(6):50-51.
[6] 赵东江,李秋生,白晓波,等.酸浸法由废旧锌锰电池制取碳酸锰的研究[J].环境科学与技术,2009(5):158-160.
Waste Battery Recycling and Utilization of Manganese
WANG Huanying, WANG Xiaopeng, LI Chenxue
(College of Chemical Engineering, Hengshui University, Hengshui, Hebei 053000, China)
With iron powder, hydrogen peroxide as raw materials, a reduction method is adopted to improve the recycling of waste battery manganese in the experiment, to explore the optimum condition for laboratory manganese recycling and synthesis of manganese carbonate. The result shows that in sulfuric acid medium, with 30% hydrogen peroxide as the reducing agent and saturated ammonium bicarbonate as precipitant, a pure manganese carbonate can be produced.
waste battery; manganese; hydrogen peroxide
(责任编校:李建明 英文校对:李玉玲)
10.3969/j.issn.1673-2065.2017.04.003
O614.7+1
A
1673-2065(2017)04-0011-03
2017-04-05
衡水学院校级课题(2016L052)
王焕英(1967-),女,河北武邑人,衡水学院化工学院教授,理学硕士; 王晓鹏(1995-),男,河北沧州人,衡水学院化工学院2014级应用化学专业本科生.
