渗透汽化-结晶耦合分离稀溶液中的香兰素
2017-10-14王倩张新儒王永洪侯蒙杰张桃李龙刘成岑
王倩,张新儒,王永洪,侯蒙杰,张桃,李龙,刘成岑
渗透汽化-结晶耦合分离稀溶液中的香兰素
王倩,张新儒,王永洪,侯蒙杰,张桃,李龙,刘成岑
(太原理工大学化学化工学院,山西太原030024)
以聚醚嵌段共聚酰胺(PEBA2533)为膜材料,采用干法相转化法制备性能优异的高分子膜,用于渗透汽化-结晶耦合(PVCC)分离系统中回收稀水溶液中的香兰素。采用扫描电子显微镜(SEM)对PEBA2533膜的形貌进行表征。考察原料液浓度、温度对膜渗透汽化性能的影响。结果表明:随着溶液浓度的增加,PEBA2533膜溶胀性能增加,说明PEBA2533能够优先吸附香兰素;随原料液浓度增加,香兰素渗透通量增加,分离因子略微下降;原料液温度增加,香兰素渗透通量和分离因子都增加;并通过Arrhenius方程计算得到香兰素比水对温度更加敏感。PVCC系统中控制一级冷凝器温度为2℃时,一级冷凝器中结晶态香兰素通量为39.52 g·m−2·h−1,纯度在99%以上。
香兰素;渗透汽化;渗透汽化-结晶耦合;聚醚嵌段共聚酰胺
引 言
香兰素是日常生活中应用最为广泛、需求量最大的香料之一[1-2]。然而,传统化学法[3-5]制备的香兰素“三废”污染严重且产品质量等级低,不能满足人们的需求。天然香兰素主要是从香草兰豆荚中提取获得,环保健康,但是香草兰不易种植并且其中香兰素的含量低。近年来,新型的生物合成法能够快速、高效、低成本、低污染地合成天然香兰素[6-8]。面对天然香兰素的产量不到整体香兰素需求量1%的情况下[9],从生物合成的发酵液中高效环保的分离出香兰素意义重大。
传统分离提取香兰素的方法主要有吸附、溶剂抽提、超临界CO2萃取等,这些方法能耗大、易造成环境污染,同时会引入其他化学试剂污染菌种[10-13]。渗透汽化膜分离是一种低能耗、不添加化学试剂、无二次污染的新型分离技术[14],利用渗透汽化膜分离法回收香兰素秉持了可持续发展原则[7]。而选择性能良好的膜材料并优化渗透汽化分离工艺是高效分离香兰素的关键科学问题。
Böddeker等[15]利用PEBA40渗透汽化回收二元水溶液中的香兰素,研究原料液浓度、温度及PEBA40膜厚对渗透性能的影响。当原料液中香兰素质量分数为0.5%,温度为45℃时,香兰素渗透通量为2.1 g·m−2·h−1,水的渗透通量为32 g·m−2·h−1。Brazinha等[7]为了提高香兰素的通量制备了致密层厚度为10 μm的POMS-PEI复合膜分离回收香兰素,结果显示:当原料液质量分数为0.5%,温度为30℃时,操作4 h后,香兰素的渗透通量最高能够达到0.5 g·m−2·h−1左右,水的渗透通量达到200 g·m−2·h−1左右。此外,他们设计了两个冷凝器,控制第一个冷凝器温度为0℃收集香兰素晶体,研究了时间对渗透管路中各部分收集情况的影响,表明时间越长,影响越小。Camera-Roda等[16]光催化合成香兰素并耦合渗透汽化技术利用PEBAX®2533膜分离回收香兰素,在浓度为0.1 mmol·L−1的原料液中收集到总渗透液390 g·m−2·h−1,其中香兰素为0.025 g·m−2·h−1。
一般,单级冷凝回收得到的产品纯度低。为了能够收集到高纯度的产品,Zhang等[17-18]设计渗透汽化-结晶耦合系统(PVCC)回收到质量分数99.8%的高纯度苯酚,并进一步研究了PVCC回收苯酚晶体的热力学性质。他们设计的PVCC系统是将传统的单级冷凝装置改变为两级冷凝,通过操控第1个冷凝器的温度回收得到结晶态的高纯度苯酚,而第2个冷凝器收集到低浓度的产品可循环进入原料液中进行再回收。PVCC工艺可节省后续提纯过程中产生的大量能耗,符合当今绿色节能的主题。
基于以上,本文选择对有机物有良好亲和性的PEBA2533膜[19-22]回收水溶液中高沸点的香兰素。考察原料液浓度和温度对膜渗透性能的影响,设计PVCC系统回收香兰素工艺中一级冷凝器的温度,计算一级冷凝器中香兰素的回收率。
1 实验材料与方法
1.1 材料与试剂
PEBA2533购于Arkema公司。香兰素,分析纯,购于西陇化学试剂厂。,-二甲基乙酰胺,分析纯,购于天津市光复精细化工研究所。所有分析纯试剂没有进一步纯化,去离子水实验室自制。
1.2 膜的制备
将15 g的PEBA2533加入85 g的,二甲基乙酰胺溶液中,配成15%(质量分数,下同)的铸膜液。将铸膜液在65℃的条件下磁力搅拌3 h,恒温(65℃)静置脱泡24 h后制膜。制膜过程如下:将铸膜液平铺在65℃水平放置的干净玻璃板上,用刮膜机调控湿膜厚度在450 µm。室温通风干燥24 h后放置在65℃烘箱内继续干燥24 h。随后,在40℃真空干燥箱内放置24 h去除剩余溶剂。
1.3 膜的表征
采用日本Hitachi SU8010型扫描电镜表征PEBA2533均质膜表面和断面的形貌。将样品固定在样品台上,离子溅射喷金,在1 kV电压下进行测试。
1.4 溶胀实验
将PEBA2533膜置于真空烘箱内干燥至膜的质量保持不变,准备若干3 cm×3 cm的膜样待用。称重标记干膜的质量为d(g)。将膜样分别置于不同质量分数(0%、0.1%、0.2%、0.4%、0.6%、0.8%、1.0%)的香兰素水溶液中,其中0%的香兰素水溶液为纯水溶液。保持温度在70℃,经过24 h浸泡后取出膜,擦干表面溶液快速称重,重复上述操作直至恒重,记为湿膜质量s(g)。膜的溶胀度(DS)用式(1)进行描述
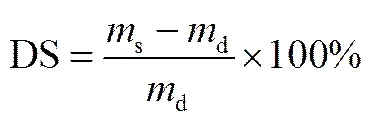
1.5 渗透汽化实验
图1包含了渗透汽化-单级冷凝、PVCC系统实验装置。PVCC系统比单级冷凝系统多一个冷凝器,其中第1个冷凝器的温度控制在2℃,其余冷凝器都以液氮控温。根据发酵液中香兰素浓度一般在2~10 g·L−1,选择实验操作浓度在0.2%~0.8%,温度范围在55~85℃。膜有效面积为18.09 cm2,下游侧压力通过真空泵维持在150 Pa。每次实验前,至少经过2 h循环以保证系统稳定。渗透汽化长时间稳定性实验,持续操作72 h,且每2 h换一次原料液,以保证原料液中香兰素的浓度。紫外可见光分光光度计(美国Varian公司Cary50型)在波长280 nm时,测试所有溶液的浓度。一级冷凝器中的结晶态香兰素纯度由卡氏微量水分仪(ZDJ-1S型)测定。用渗透通量()和分离因子()评价膜的渗透汽化性能,见式(2)和式(3)。
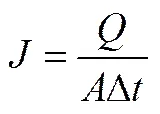
(3)
在PVCC系统中,以1,V/T,V表示一级冷凝中结晶态香兰素与总香兰素的值。
2 实验结果与讨论
2.1 膜的表征
图2(a)为PEBA2533膜表面的扫描电镜图,从图中可看出,PEBA2533膜表面形貌平整、致密,没有孔和裂缝出现在膜的表面。图2(b)为PEBA2533膜断面的扫描电镜图,由图中可看出PEBA2533膜厚度为55 μm。
2.2 溶胀实验
膜材料的溶胀度可以预测与某些特定化合物结合力的大小[23]。图3是70℃时,不同浓度香兰素水溶液下PEBA2533膜的溶胀度。由图可知,纯水中PEBA2533膜基本没有溶胀,然而随着香兰素在溶液中浓度的不断增加,PEBA2533膜的溶胀度也不断增加。当香兰素质量分数在1.0%时,溶胀度达到了15.63%。
根据溶解度参数理论,若某物质与膜之间的溶解度参数越接近,则越易溶于膜中[24]。PEBA2533膜的溶解度参数是19.42 J1/2·cm−3/2 [25],香兰素和水的溶解度参数分别为24.45、48.08 J1/2·cm−3/2[26]。可见PEBA2533膜和香兰素的溶解度参数相近,而和水的相差较大,说明PEBA2533膜能够优先溶解香兰素,这为后续渗透汽化膜分离香兰素提供了基础。随着香兰素浓度的增加,香兰素和PEBA2533膜中的聚醚段相互作用更加强烈,使得香兰素在PEBA2533膜中的吸附量增加。综上,PEBA2533膜对香兰素有优先吸附的能力。
2.3 原料液浓度对渗透汽化性能的影响
原料液温度85℃,考察不同原料液浓度下PEBA2533膜的渗透汽化性能,见图4。图4(a)为香兰素和水的渗透通量随原料液浓度的变化曲线,由图可知随着香兰素质量分数的增加,香兰素渗透通量呈现不断增加的趋势,而水的通量则基本保持不变。当质量分数在0.6%时,香兰素渗透通量为30 g·m−2∙h−1,分离因子为4.6,高于其他的同类工作[7, 15-16]。图4(b)显示的分离因子随着香兰素浓度的增加有轻微的下降,当香兰素的质量分数从0.2%上升到0.8%时,分离因子从5减小到4.39。
香兰素渗透通量的增加一方面是由于香兰素质量分数的增加,膜中会吸附更多的香兰素,导致溶胀度增加,膜结构变得更疏松,链段运动加剧,自由体积分数也随之增加,有利于香兰素通过PEBA2533膜。另一方面原料液中香兰素质量分数整体较低,因此增加香兰素的质量分数,膜上下游两侧的渗透推动力增加,香兰素更易通过膜。
随着香兰素质量分数增加,水分子浓度减小,膜两侧推动力较小,但由于香兰素中羟基等极性基团和水分子之间存在氢键耦合作用[27],香兰素携带一部分水进入膜中,导致水的通量增加。因此,水渗透通量基本保持不变。
2.4 温度对渗透汽化性能的影响
原料液质量分数为0.8%,温度对渗透性能的影响见图5。从图5(a)中可看出,随着温度的增加香兰素和水的通量都随之增加。图5(b)中分离因子也呈现出增加的趋势。温度升高,香兰素和水的渗透通量都增加的原因主要有:①原料液侧香兰素、水分子的饱和蒸气压增加,分子通过膜两侧的渗透推动力增加,促使渗透组分易于渗透。②香兰素、水分子的吸脱附速率增强,加速香兰素和水的渗透。③香兰素、水及PEBA2533链段的热运动加强,使小分子在膜内的扩散速率增加。因此,香兰素和水的渗透速率同时随着温度的增加而增加。
通量和温度的关系可以用Arrhenius方程进行描述,见式(4)

对式(4)两边取对数
图5 温度对渗透通量和分离因子的影响
Fig.5 Effect of operating temperature on flux and separation factor of PEBA2533 membrane
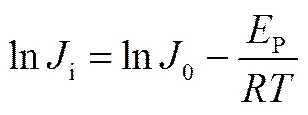
从式(5)可知,ln和1/呈线性关系,图6为ln和1/的线性关系,根据斜率可以计算得各组分的渗透活化能。当渗透活化能为正值时,渗透通量随温度的增加而增加,渗透活化能越大,该组分对温度越敏感[28]。通过计算,香兰素的渗透活化能(P,V=86.1 kJ·mol−1)大于水的活化能(P,W=40.5 kJ·mol−1),说明通过膜时香兰素对温度变化更加敏感,因而温度升高分离因子逐渐升高。
2.5 二级冷凝回收香兰素
通过上述实验可知,只通过渗透汽化-单级冷凝工艺回收香兰素,产品质量分数虽能从0.8%富集到3.4%,但仍然需要对香兰素进一步富集。为了能够直接在实验过程中收集到高纯度香兰素,结合其高沸点、低饱和蒸气压(22℃,香兰素:v=80.3 Pa[29],水:v=2644 Pa[30])、易结晶的物理性质,设计了PVCC工艺来分离稀水溶液中的香兰素。
PVCC系统中,渗透汽化膜的下游侧保持抽真空状态,气态的香兰素和水到达第1个冷凝器,通过控制第1个冷凝器的温度,使水蒸气的饱和蒸气压大于渗透侧水蒸气的分压;而香兰素蒸气的饱和蒸气压仍然小于其在渗透侧的分压,因而香兰素蒸气优先冷凝结晶在第1个冷凝器中,剩余的水蒸气和香兰素蒸气在第2个冷凝器中收集。据此,PVCC一级冷凝器中可收集到高纯度的香兰素。
在一定原料液浓度、温度、操作压力的条件下,膜下游侧香兰素和水的渗透通量和渗透浓度保持不变。原料液温度为85℃,一级冷凝器温度为2℃,不同原料液浓度下,PVCC一级冷凝器中收集到的结晶态香兰素和总香兰素的关系见表1。由表1可知1,VT,V均在0.98以上,并且纯度也均在99%以上,印证了上述的理论推测。
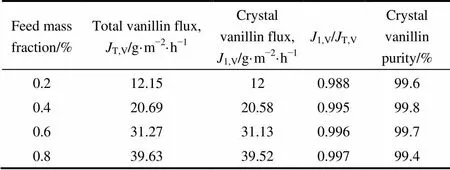
表1 PVCC系统一级冷凝器中收集的结晶态香兰素
图7为原料液温度为85℃,香兰素质量分数为0.8%,PEBA2533膜在PVCC系统中回收结晶态香兰素的稳定性测试,测试时间为72 h。由图可知,PEBA2533膜长时间操作下结晶态香兰素的渗透通量在误差范围内,随着操作时间的增加,香兰素的渗透通量有轻微上升的趋势,说明随着操作时间的增加PEBA2533膜溶胀。操作到75 h后,膜有轻微破损。
3 结 论
(1)纯水中PEBA2533膜几乎不溶胀,随着原料液中香兰素浓度的增加膜溶胀度逐渐增加,在质量分数为1%的原料液中溶胀度达到15.63%,说明PEBA2533膜能够优先吸附香兰素,为后续实验提供可操作性。
(2)考察原料液浓度和温度对PEBA2533膜渗透性能的影响,结果表明:原料液浓度增加,水的渗透通量基本保持不变,香兰素渗透通量增加明显,分离因子呈现逐渐减小的趋势。温度增加,香兰素和水的渗透通量都增加,由于香兰素对温度变化更加敏感所以增幅更大,因此,分离因子随温度的增加而增加。
(3)设计PVCC装置回收香兰素,一级冷凝器温度控制在2℃时,结晶态香兰素通量为39.52 g·m−2·h−1,占总香兰素0.98以上,纯度在99%以上。采用该工艺可省去后续的提纯步骤,提高其经济效应。在提倡绿色节能、经济环保的时代背景下,PVCC工艺的研究意义重大。
符 号 说 明

A——膜有效面积,m2 EP——渗透活化能,kJ·mol−1 EP,V,EP,W——分别为香兰素、水的渗透活化能,kJ·mol−1 J——膜渗透通量,g·m−2·h−1 J1,V, JT,V——分别为一级冷凝管中香兰素渗透通量、香兰素总渗透通量,g·m−2·h−1 md, ms——分别为干膜、湿膜质量,g pv——饱和蒸气压,Pa Q——渗透物质量,g R——气体常数,J·mol−1·K−1 T——操作温度,K t——渗透物收集时间,h XV, XW——分别为原料液中香兰素和水的质量分数 YV, YW——分别为渗透侧香兰素和水的质量分数 α——分离因子 下角标 V——香兰素 W——水
References
[1] ALBUQUERQUE I D, MAZZOTTI M. Crystallization process design using thermodynamics to avoid oiling out in a mixture of vanillin and water[J]. Crystal Growth & Design, 2014, 14(11): 5617-5625.
[2] SON G E, SUGARTSEREN N, YOON W B,. Phase behavior of ternary mixtures of water-vanillin-ethanol for vanillin extractiondissipative particle dynamics[J]. Journal of Chemical & Engineering Data, 2014, 59(10): 3036-3040.
[3] PLAGGENBORG R, OVERHAGE J, LOOS A,. Potential of rhodococcus strains for biotechnological vanillin production from ferulic acid and eugenol[J]. Applied Microbiology and Biotechnology, 2006, 72(4): 745.
[4] FARGUES C, MATHIAS Á, RODRIGUES A. Kinetics of vanillin production from kraft lignin oxidation[J]. Industrial & Engineering Chemistry Research, 1996, 35(1): 28-36.
[5] 杨晓慧, 周永红, 胡丽红, 等. 木质素制备香草醛的研究进展[J]. 纤维素科学与技术, 2010, 18(4): 49-54. YANG X H, ZHOU Y H, HU L H,. Research advances in preparation of vanillin from lignin[J]. Journal of Cellulose Science and Technology, 2010, 18(4): 49-54.
[6] DI GIOIA D, SCIUBBA L, SETTI L,. Production of biovanillin from wheat bran[J]. Enzyme and Microbial Technology, 2007, 41(4): 498-505.
[7] BRAZINHA C, BARBOSA D S, CRESPO J G. Sustainable recovery of pure natural vanillin from fermentation media in a single pervaporation step[J]. Green Chemistry, 2011, 13(8): 2197.
[8] DONG Z Z, GU F L, XU F,. Comparison of four kinds of extraction techniques and kinetics of microwave-assisted extraction of vanillin from vanilla planifolia andrews[J]. Food Chemistry, 2014, 149: 54-61.
[9] MOTA M I F, RODRIGUES PINTO P C, LOUREIRO J M,. Recovery of vanillin and syringaldehyde from lignin oxidation: a review of separation and purification processes[J]. Separation & Purification Reviews, 2015, 45(3): 227-259.
[10] 葛业超. 香兰素的合成与分离的研究现状及发展趋势[J]. 当代经理人, 2006: 127-128. GE Y C. Study on the synthesis and separation of vanillin and development trend[J]. Contemporary Managers, 2006: 127-128.
[11] 刘礼旺. 香兰素的合成与分离提取研究进展[J]. 农技服务, 2010, 27(8): 1038-1039. LIU L W. Research advances in synthesis and separation of vanillin[J]. Agricultural Technology Service, 2010, 27(8): 1038-1039.
[12] MOTA M I F, PINTO P C R, LOUREIRO J M,. Successful recovery and concentration of vanillin and syringaldehyde onto a polymeric adsorbent with ethanol/ water solution[J]. Chemical Engineering Journal, 2016, 294: 73-82.
[13] MOTA M I F, PINTO P C R, LOUREIRO J M,. Adsorption of vanillin and syringaldehyde onto a macroporous polymeric resin[J]. Chemical Engineering Journal, 2016, 288: 869-879.
[14] LIU F F, LIU L, FENG X S. Separation of acetone-butanol-ethanol (ABE) from dilute aqueous solutions by pervaporation[J]. Separation and Purification Technology, 2005, 42(3): 273-282.
[15] BÖDDEKER K W, GATFIELD I L, JÄHNIG J,. Pervaporation at the vapor pressure limit: vanillin[J]. Journal of Membrane Science, 1997, 137(1): 155-158.
[16] CAMERA-RODA G, AUGUGLIARO V, CARDILLO A,. A pervaporation photocatalytic reactor for the green synthesis of vanillin[J]. Chemical Engineering Journal, 2013, 224: 136-143.
[17] ZHANG X R, LI C C, HAO X G,. Recovering phenol as high purity crystals from dilute aqueous solutions by pervaporation[J]. Chemical Engineering Science, 2014, 108: 183-187.
[18] LI C C, ZHANG X R, HAO X G,. Thermodynamic and mechanistic studies on recovering phenol crystals from dilute aqueous solutions using pervaporation-crystallization coupling (PVCC) system[J]. Chemical Engineering Science, 2015, 127: 106-114.
[19] HAO X, PRITZKER M, FENG X. Use of pervaporation for the separation of phenol from dilute aqueous solutions[J]. Journal of Membrane Science, 2009, 335(1/2): 96-102.
[20] DING C, ZHANG X R, LI C C,. ZIF-8 incorporated polyether--amide membrane for phenol permselective pervaporation with high efficiency[J]. Separation and Purification Technology, 2016, 166: 252-261.
[21] LI C C, ZHANG X R, HAO X G,. Efficient recovery of high-purity aniline from aqueous solutions using pervaporation-fractional condensation system[J]. AIChE Journal, 2015, 61(12): 4445-4455.
[22] HAYAHA G O. Separation of phenol from aqueous streams by a composite hollow fiber based pervaporation process using polydimethyl siloxane (PDMS) polyether--amide (PEBA) as two-layer membranes[J]. Journal of Separation Science and Technology, 2009, 44(12): 2894-2914.
[23] MINHAS B S, CHUBA M R, SAXTON R J. Membrane process for separating sulfur compounds from FCC light naphtha: WO2002053253A1[P]. 2003.
[24] HASANOĞLU A, SALT Y, KELEŞER S,. Pervaporation separation of organics from multicomponent aqueous mixtures[J]. Chemical Engineering and Processing: Process Intensification, 2007, 46(4): 300-306.
[25] 杨超. 聚醚共聚乙酰胺膜的溶胀及渗透汽化性能研究[D]. 广西: 广西大学, 2008. YANG C. Swelling of poly-etheramide membrane and its pervaporation[D]. Guangxi: Guangxi University, 2008.
[26] HANSEN C M. Hansen Solubility Parameters: A User’s Handbook[M]. CRC Press, 2007.
[27] MANDAL M K, BHATTACHARYA P. Poly (ether--amide) membrane for pervaporative separation of pyridine present in low concentration in aqueous solution[J]. Journal of Membrane Science, 2006, 286(1): 115-124.
[28] GARCÍA V, PONGRÁCZ E, MUURINEN E,. Pervaporation of dichloromethane from multicomponent aqueous systems containing-butanol and sodium chloride[J]. Journal of Membrane Science, 2009, 326(1): 92-102.
[29] JANG M, KAMENS R M, LEACH K B,. A thermodynamic approach using group contribution methods to model the partitioning of semivolatile organic compounds on atmospheric particulate matter[J]. Environmental Science & Technology, 1997, 31(10): 2805-2811.
[30] 范仲元. 水和水蒸气热力性质图表[M]. 北京: 中国电力出版社, 1996: 118. FAN Z Y. The Thermodynamic Properties of Water and Steam[M]. Beijing: China Electric Power Press, 1996: 118.
Separationof vanillin from dilute aqueous solutions by pervaporation-crystallization coupling
WANG Qian, ZHANG Xinru, WANG Yonghong, HOU Mengjie, ZHANG Tao, LI Long, LIU Chengcen
(College of Chemistry and Chemical Engineering, Taiyuan University of Technology, Taiyuan 030024, Shanxi, China)
The high performance poly(ether--amide) (PEBA2533) membrane was prepared by dry phase inversion method, and then used for separation of vanillin from dilute aqueous solutions in the pervaporation-crystallization coupling (PVCC) system. The structural morphology of PEBA2533 membranes were characterized by SEM. The effects of feed concentration and operating temperature on the pervaporation performances of membrane were investigated. The results showed that the swelling degree of PEBA2533 membrane increased with the increase of concentration. This indicated that PEBA2533 could preferentially adsorb vanillin. With the increase of the feed concentration, the flux of vanillin increased while the separation factor decreased slightly. The vanillin permeation flux and separation factor both increased as the operating temperature increased. The equation of Arrhenius indicated that vanillin was more sensitive to temperature than water. When the temperature of first condenser was controlled at 2℃in the PVCC system, the flux of crystal vanillin in the first condenser was 39.52 g·m−2·h−1and the purity was more than 99%.
vanillin; pervaporation; pervaporation-crystallization coupling; poly(ether--amide)
10.11949/j.issn.0438-1157.20161828
TQ 028.8
A
0438—1157(2017)08—3126—07
张新儒。第一作者:王倩(1990—),女,硕士研究生。
国家自然科学基金青年基金项目(21506140);山西省高等学校科技创新项目(2015114)。
2016-12-29收到初稿,2017-05-03收到修改稿。
2016-12-29.
ZHANG Xinru, zhangxinru@tyut.edu.cn
supported by the National Natural Science Foundation of China (21506140) and the Scientific and Technological Innovation Programs of Higher Education Institutions in Shanxi (2015114).
