Ni2P/SiO2催化剂制备及其乙酸加氢制乙醇催化性能评价
2017-10-14任杰胡望伟袁海宽慎炼
任杰,胡望伟,袁海宽,慎炼
Ni2P/SiO2催化剂制备及其乙酸加氢制乙醇催化性能评价
任杰,胡望伟,袁海宽,慎炼
(浙江工业大学化工学院,浙江杭州 310014)
通过等体积浸渍和N2气流中热处理过程制备了系列氧化硅负载过渡金属磷化物催化剂,经乙酸加氢制乙醇反应实验和动力学分析评价催化剂性能。研究结果表明,随着反应温度从280℃升高到340℃,乙酸转化率和乙醇选择性均逐渐提高。随着催化剂制备的P/Ni摩尔比从2:1增大到4:1,催化剂活性和乙醇选择性均先增大后减小,P/Ni摩尔比为3:1催化剂性能较佳。250℃热处理制备催化剂的催化性能优于200℃及300℃。Ni2P/SiO2催化剂活性和乙醇选择性均高于Co2P/SiO2催化剂。用次磷酸钠作为磷补充源制备催化剂的性能优于次磷酸钾。采用较佳条件下制备的Ni2P/SiO2催化剂,在温度340℃、压力2.0 MPa、氢酸进料量比10:1、质量空速0.4 h-1条件下进行乙酸加氢反应,乙酸转化率为100%,乙醇选择性达到74.56%,并且适当升高反应温度会进一步提高乙醇选择性。
乙酸;加氢;乙醇;磷化镍;催化剂;制备;反应动力学
引 言
由于乙醇作为汽油调和组分,能够改善汽油的使用性能,世界各国都在发展乙醇汽油。以农作物秸秆和林业加工废料为原料生产乙醇,生产成本较高,产能偏低,而以煤基乙酸为原料通过催化加氢反应生产乙醇是一条可行的路径。开展乙酸加氢制乙醇催化剂制备及反应过程研究具有重要的现实意义。
乙酸加氢制乙醇的方法包括乙酸先酯化后加氢的间接法和乙酸加氢制乙醇的直接法,催化剂包括铂、钯等贵金属催化剂和非贵金属催化剂[1-4]。铜基催化剂较早用于甲酸甲酯的催化加氢反应,具有较高的催化活性,但易发生热失活[5-6]。以Fe2O3作为前体,石墨烯氧化物为载体可制备活性较高的铁基加氢催化剂[7]。加入第2活性组分制备负载型镍基催化剂,可提高活性成分Ni的分散性,并且降低Ni基催化剂的还原温度[8-10]。经过还原处理制备Mo-Ni/γ-Al2O3催化剂,其乙醇选择性为23.80%[11]。
过渡金属磷化物是一种新型加氢催化剂,受到人们的极大关注[12]。MoP/SiO2催化剂的加氢脱硫(HDS)活性是MoS2/SiO2的4倍[13],MoP/Al2O3催化剂的加氢脱氮(HDN)活性比MoS2/Al2O3高6倍[14]。Ni2P/SiO2催化剂的加氢精制活性和活性稳定性均好于Fe2P/SiO2和Co2P/SiO2[15]。Ni2P/SiO2的加氢脱氧(HDO)催化性能优于Co2P/SiO2,并且当P/N摩尔比为3时,催化活性较高[16]。当P/Ni=3时,Ni2P/Al2O3催化剂的二苯并噻吩加氢脱硫活性较高[17]。在制备负载型Ni2P/MCM-41催化剂过程中,随着P/Ni增大,Ni2P晶粒分散度提高[18]。在300℃温度下,Ni2P/MCM-41催化剂的苯酚HDO转化率达到100%[19]。随着Mo基催化剂的MoO3、MoO2、MoS2和MoP中Mo的电子密度递增,催化剂的HDO性能逐渐提高,MoP的催化活性最高[20]。磷化物催化剂的愈创木酚HDO活性稳定性好于CoMoS/Al2O3催化剂[21]。在负载型Ni2P催化剂制备过程,Ni(H2PO2)2和NH4H2PO2热分解生成Ni2P、P2O3、PH3、H2、NH3和水[22-23]。次磷酸盐的次磷酸根自身发生歧化反应,生成PH3气体,PH3将金属离子还原,最终使其完全磷化[24-25]。采用热分解方法制备磷化镍调变的MoS2/γ-Al2O3,增加了MoS2晶簇的平均堆积层数,提高了催化剂的加氢催化性能[26]。以过渡金属化合物和磷酸氢二铵为原料,经溶解、干燥、焙烧,通入氢气还原,以及O2/N2气氛下钝化处理,制备过渡金属磷化物催化剂粉末,其具有较高的乙酸加氢催化活性和乙醇选择性[27]。只是固定床反应器应装填一定粒度和机械强度的颗粒催化剂,降低床层压降;随着催化剂粒径增大其外表面积减小,活性组分利用率降低,催化性能会显著降低。制备催化剂活性组分利用率高、机械强度大的负载型催化剂是发展方向。目前,负载型过渡金属磷化物催化剂用于乙酸加氢制乙醇反应研究少见报道。
本文通过等体积浸渍、N2气流中热处理过程制备氧化硅负载过渡金属磷化物催化剂,通过乙酸加氢反应及反应动力学分析评价催化剂性能,考察P/Ni用量配比、热处理温度、活性组分种类、碱金属次磷酸盐种类对催化剂性能的影响。
1 实验方法
1.1 化学试剂与反应原料
乙酸,分析纯,杭州化学试剂公司;高纯氢气和高纯氮气,杭州今工特种气体公司;次磷酸镍 [Ni (H2PO2)2·6H2O]和次磷酸钠(NaH2PO2·H2O),分析纯,上海笛柏化学品技术公司;次磷酸钾 (K H2PO2·H2O),分析纯,阿拉丁试剂公司;硝酸钴[Co(NO3)2·6H2O],化学纯,国药集团化学试剂公司;活化硅胶,分析纯,青岛海洋化工分厂。
1.2 催化剂制备
首先,对比表面积350 m2·g-1、孔容0.5 ml·g-1、粒度0.425~0.850 mm的活化硅胶进行30%稀硝酸溶液浸泡、水洗、焙烧预处理,得到催化剂载体。测定载体的饱和吸水率为1.65 ml·g-1。
在确定过渡金属占过渡金属、磷和载体总质量分数为7.0%的情况下,利用等体积浸渍法制备过渡金属磷化物负载型催化剂。某种Ni2P/SiO2催化剂的制备过程:①将4.3350 g的Ni(H2PO2)2·6H2O溶解于适量的蒸馏水中,再加入1.5588 g的 NaH2PO2·H2O,补加蒸馏水并搅拌,得到16.7 ml的浸渍溶液;②对10.1005 g处理的活化硅胶载体搅拌滴加浸渍溶液,然后静置24 h,在烘箱中60℃真空干燥12 h,得到催化剂前体;③将7.5 g催化剂前体装入反应器中,在氮气流中按2℃·min-1的加热速率,从室温升温至250℃,恒温3 h,热处理过程中氮气压力为1.5 MPa,氮气流量为45 ml·min-1,得到P/Ni摩尔比3:1、N2气流中热处理温度250℃、添加Na盐的Ni2P/SiO2催化剂。
1.3 加氢反应实验及产物分析方法
采用固定床反应装置进行乙酸加氢反应,不锈钢反应器尺寸为内径10 mm、外径14 mm、长100 cm,将催化剂装填在反应器中部,反应器两端填满惰性石英砂。乙酸与氢气从固定床反应器上端注入,反应流体从反应器下端流入储罐,气体从储罐上部排出经过背压阀,经流量测定后排到室外;液体产物储存在储罐中,并定时取出和分析。以催化剂前体填装量(7.5 g)为基准计算乙酸质量空速。在温度280~340℃、压力2.0 MPa、氢气与乙酸进料量摩尔比10:1、质量空速0.4 h-1的反应条件下,进行乙酸加氢反应,评价催化剂性能。
用岛津GC-2014C气相色谱仪分析反应产物组成,色谱检测器为热导检测器,色谱柱为2 m×4 mm的GDX-102填充柱,进样器温度为140℃,柱温为120℃,检测器温度为130℃,色谱数据处理方法为校正面积归一化法。
反应产物混合物中含有未转化乙酸(HAc)、乙醇(EtOH)、乙酸乙酯(EtOAc)、少量丙酮(acetone)及乙醛(acetal),反应产物混合物相对乙酸的总有机物量(0)为

乙酸转化率(A)和乙醇选择性(C)分别为
(2)

式中,A为组分色谱面积分率;M为组分摩尔质量;λ为组分色谱校正因子,其中HAc=1.0208,EtOH=1.3158,EtOAc=2.9321,acetone= 0.9763。
2 实验结果与讨论
2.1 P/Ni摩尔比的影响
确定过渡金属占过渡金属、磷和载体总质量分数为7.0%,改变Ni(H2PO2)2和NaH2PO2的用量,经过浸渍,在250℃氮气流中热处理3 h,制备P/Ni摩尔比为2:1、3:1和4:1的Ni2P/SiO2催化剂。3种催化剂的乙酸加氢反应实验结果如图1所示。
由图1可知,随着反应温度升高,乙酸转化率和乙醇选择性均呈现增大趋势,这是因为乙酸加氢反应主要受反应动力学影响,升高反应温度有利于提高乙酸加氢反应速率,更有利于乙醇生成反应速率,致使乙酸转化率和乙醇选择性提高。P/Ni=2:1与P/Ni=3:1催化剂相比,两者的乙酸转化率相差不大,但后者乙醇选择性明显高于前者,说明当P/Ni=3:1时催化剂的加氢催化活性较高,这与文献[16-17]的结果相似。这可能因为,当P与Ni摩尔比为3:1时,在催化剂加热处理过程生成的活性相Ni2P最多,提高了催化剂的加氢催化活性,致使乙酸转化率和乙醇选择性均较高;由于在催化剂热处理过程中,有部分次磷酸根分解生成的PH3会随N2气流出反应器,当P/Ni=2时,实际参与还原Ni2+的PH3不足,无法将Ni2+完全还原,致使生成的活性相Ni2P较少,催化剂加氢催化活性有限,并且由于未添加次磷酸碱金属盐补充磷源,没有催化剂表面酸性中心的碱金属钝化作用,加速了乙酸与乙醇酯化生成乙酸乙酯的酸催化反应速率,降低了乙醇选择性,较高的加氢和酯化反应速率导致较高的乙酸转化率。当P/Ni=4时,由于P过量较多,不仅生成Ni2P,还生成副产物NiP4O11和Ni5P4,影响催化剂的加氢活性[25],致使乙酸转化率较低;并且催化剂表面上可能存在较多的酸性中心,加速了乙醇与乙酸的酸催化酯化反应速率,致使乙醇选择性很低。
总之,较佳催化剂制备的磷与镍摩尔比为3:1,在340℃加氢反应温度下用所制备催化剂进行乙酸加氢反应,乙酸转化率为100%,乙醇选择性达到74.56%,并且适当升高反应温度,乙醇选择性呈进一步升高的变化趋势。
2.2 热处理温度的影响
确定P/Ni=3:1,用次磷酸钠作为补充磷源,在氮气流中分别进行200、250、300℃温度热处理,制备3种Ni2P/SiO2催化剂,评价催化剂催化性能的实验结果如图2所示。
从图2可以看出,在不同温度下热处理制备的3种催化剂中,250℃处理催化剂的乙酸转化率和乙醇选择性均最高,200℃处理催化剂的乙酸转化率最低,而其乙醇选择性介于中间,300℃处理催化剂的乙酸转化率介于中间,而其乙醇选择性最低。这可能因为,在250℃条件下热处理,催化剂前体能够生成较多活性相Ni2P,使催化剂具有较高的乙酸加氢活性,导致较高的乙酸转化率和乙醇选择性;当热处理温度为200℃时,温度偏低导致H2PO-2分解和PH3还原Ni2+的速率偏低,生成Ni2P量偏少,使乙酸转化率最低和乙醇选择性较低;当热处理温度为300℃时,温度偏高致使生成PH3的速率大于PH3还原Ni2+的速率,部分PH3未参与还原Ni2+反应就已损失,使Ni2+还原不完全,不能生成较多的Ni2P,同时还生成NiP4O11和Ni5P4,影响催化剂的加氢催化活性[25],并且催化剂表面上存在较多的酸性中心,提高了乙酸和乙醇的酸催化反应速率,致使乙酸转化率较低和乙醇选择性最低。可见,较佳的催化剂制备热处理温度为250℃。
2.3 Ni2P/SiO2与Co2P/SiO2催化剂性能比较
用次磷酸钠作为补充磷源,在P与金属摩尔比为3:1、N2气流中热处理温度为250℃条件下,制备了Ni2P/SiO2和Co2P/SiO2催化剂,两种催化剂催化性能的评价结果见图3。
由图3可知,以Ni2P为活性组分催化剂的乙酸转化率及乙醇选择性均明显高于Co2P催化剂,说明Ni2P/SiO2催化剂的加氢催化活性高于Co2P/SiO2催化剂,这与文献[16]的结果相似。负载型Ni2P/SiO2催化剂是较佳的乙酸加氢制乙醇反应催化剂。
2.4 碱金属盐种类的影响
在催化剂制备过程中,添加碱金属盐有利于钝化催化剂表面酸性,降低乙酸乙酯选择性,并减少催化剂表面积炭,提高催化剂活性稳定性[28]。在P/Ni=3、N2气流中250℃热处理的制备条件下,用Ni(H2PO2)2作为镍源和磷源,分别以NaH2PO2和KH2PO2作为补充磷源,制备两种Ni2P/SiO2催化剂。考察两种催化剂性能差别的实验结果见图4。
从图4可以看出,在340℃加氢温度下,用次磷酸钠制备催化剂的乙酸转化率和乙醇选择性均高于次磷酸钾,次磷酸钠是较佳的催化剂制备补充磷源。
综上所述,P/Ni摩尔比、热处理温度、活性组分种类、碱金属盐种类均影响催化剂性能,提高Ni2P催化活性组分生成量和降低表面酸性是提高乙酸加氢催化活性和乙醇选择性的关键。较佳的催化剂制备条件包括活性组分为Ni2P、P/Ni=3:1、热处理温度为250℃、补充磷源为次磷酸钠。
3 催化剂性能的动力学评价
3.1 反应流体的相态及变化分析
利用Antoine蒸气压方程计算反应流体中各组分的饱和蒸气压,以含量较高、饱和蒸气压较低的乙酸作为模型化合物,在温度范围280~340℃,压力2.0 MPa,氢气与乙酸进料量摩尔比10:1的加氢反应实验条件下,反应流体气相乙酸分压明显小于乙酸的饱和蒸气压,催化剂床层中反应流体处于气相。
反应气体流过催化剂床层,其氢气分率和体积流量均逐渐减小。在加氢反应条件范围内,催化剂床层入口处的氢气分率为H2,0=0.9091,气体流量与乙酸进料量之比为D0=11.0,氢气分率与D0之比为H2,0/D0=0.0826。依据反应实验数据,计算催化剂床层出口处的H2/D数值,比入口数值相对减小0.0319%~2.6918%,平均减小0.6496%。为了简化反应动力学数据处理,假设催化剂床层中的H2/D数值不变,取H2/D=H2,0/D0=0.0826数值。
3.2 反应动力学方程推导
假设乙酸浓度和氢气浓度对乙酸加氢反应的影响均为1级,催化剂床层相对高度为=/,对某催化剂床层高度处的床层体积微元进行乙酸物料衡算,得到式(4)。

考虑反应气体为理想气体,催化剂质量为C=CC,H2=TH2/,对式(4)在=0~1范围内积分,得到乙酸转化率的反应动力学积分式(5)
(5)
由于乙醇收率为乙酸转化率与乙醇选择性之积,假设乙酸加氢反应为生成乙醇等产物的平行反应,经过推导,得到乙醇生成反应动力学积分式(6)
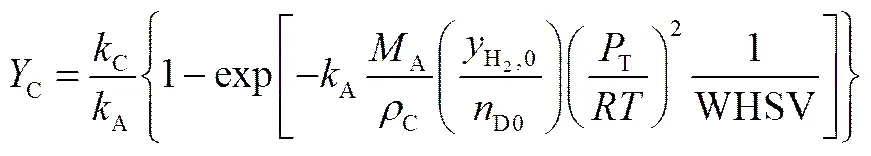
由式(5)和式(6)得到乙醇选择性关系式(7)
(7)
在上述公式中,气体常数=8.314×10-3L·MPa·(K·mol)-1,A=60.05 g·mol-1,C=690.0 g·L-1。将反应温度对反应速率常数的影响表示为Arrhenius关系式。

表1 催化剂制备条件及催化性能动力学评价结果
3.3 动力学参数估值
以乙酸转化率或乙醇选择性实验值与方程计算值的残差平方和作为目标函数,利用图1~图4实验数据进行参数估值,确定340℃的乙酸转化速率常数和表观反应活化能,以及乙醇生成速率常数和表观活化能,结果列于表1。将表1中的动力学参数分别代入式(5)和式(7),计算乙酸转化率和乙醇选择性,乙酸转化率计算值与实验值的相关系数为2XA=0.6717~0.9951,其平均值为0.8972;乙醇选择性计算值与实验值的相关系数为2SC=0.3136~0.8433,其平均值为0.6435。
由表1可知,Cat-2(P/Ni=3:1)Ni2P/SiO2催化剂的A1、C1、C1/A1数值均大于Cat-1和Cat-3,说明Cat-2催化剂的乙酸转化、乙醇生成催化活性、乙醇选择性均最高。另外,不同热处理温度、活性组分和碱金属盐制备催化剂的催化活性和乙醇选择性均不如Cat-2催化剂。这些催化剂动力学评价结果与上述加氢反应实验评价结果相同。
再者,Cat-2催化剂的乙酸转化和乙醇生成表观活化能均大于其他催化剂,并且其乙醇生成表观活化能远大于乙酸转化。这说明,在340℃反应温度基础上适当升高反应温度,Cat-2催化剂乙酸转化和乙醇生成速率的提高幅度均大于其他催化剂;由于Cat-2催化剂乙醇生成速率提高幅度大于乙酸转化速率,该催化剂的乙醇选择性也会进一步增大。
4 结 论
(1)以次磷酸镍(或硝酸钴)、碱金属次磷酸盐为原料,通过等体积浸渍、N2气流中热处理过程,制备了不同P/Ni摩尔比、热处理温度、活性组分种类、碱金属次磷酸盐种类的氧化硅负载过渡金属磷化物催化剂。
(2)在280~340℃条件下进行乙酸加氢反应,乙酸转化率和乙醇选择性均随着反应温度升高而增大。随着催化剂制备的P/Ni摩尔比从2:1增大到4:1,催化剂活性和乙醇选择性均呈现山峰形趋势,P/Ni=3:1催化剂性能较佳;250℃热处理制备催化剂的活性和乙醇选择性均优于200℃及300℃;Ni2P/SiO2催化剂活性和乙醇选择性均优于Co2P/SiO2催化剂;用次磷酸钠作为补充磷源制备催化剂的性能优于次磷酸钾。
(3)在确定乙酸加氢反应流体为气体、分析反应气体变化的基础上,经过推导确定了乙酸转化和乙醇生成动力学方程。利用加氢反应实验数据确定了各催化剂的340℃乙酸转化和乙醇生成速率常数,以及表观活化能。由乙酸转化速率常数,以及乙醇生成和乙酸转化速率常数比值评价催化剂活性与乙醇选择性,定量地比较了各催化剂性能,其结果与加氢实验评价结果相同。
(4)以次磷酸镍作为镍源和磷源、次磷酸钠作为补充磷源,在P/Ni=3:1条件下通过等体积浸渍、N2气流中250℃热处理过程制备Ni2P/SiO2催化剂,在温度340℃、压力2.0 MPa、氢酸进料量比10:1、质量空速0.4 h-1条件下进行乙酸加氢制乙醇反应,乙酸转化率为100%,乙醇选择性达到74.56%,并且适当升高反应温度会进一步提高乙醇选择性。
符 号 说 明

CA,CA0——分别为乙酸浓度、乙酸初始浓度,mol·L-1 CH2——氢气浓度,mol·L-1 EA,EC——分别为乙酸转化表观活化能、乙醇生成表观活化能,J·mol-1 kA——乙酸转化速率常数,L·(mol·h)-1 kA1——340℃乙酸转化速率常数,L·(mol·h)-1 kC——乙醇生成速率常数,L·(mol·h)-1 kCl——340℃乙醇生成速率常数,L·(mol·h)-1 MA——乙酸摩尔质量,g·mol-1 nD——气体流量与乙酸进料量摩尔比 PT——反应压力,MPa T——反应温度,K t——反应温度,℃ tZ——热处理温度,℃ VC——催化剂床层体积,L vT0——反应器入口气体流量,L·h-1 WHSV——质量空速,h-1 YC——乙醇收率 yH2——气体中氢气分率 Z——催化剂床层相对高度 rC——催化剂堆积密度,g·L-1
References
[1] 王彪,王熙庭,徐国辉. 醋酸和醋酸酯加氢制乙醇技术进展[J]. 天然气化工(C1化学与化工),2013, 38(3): 79-83. WANG B, WANG X T, XU G H. Advances in technologies for hydrogenation of acetic acid and acetates to ethanol[J]. Natural Gas Chemical Engineering (C1Chemistry and Chemical Engineering), 2013, 38(3): 79-83.
[2] 刘继业. 我国醋酸乙酯合成技术进展及市场分析[J]. 精细与专用化学品, 2010, 18(8): 5-12.LIU J Y. Production technologies progress and market analysis of ethyl acetate in china[J]. Fine and Specialty Chemicals,2010, 18(8): 5-12.
[3] 王科,陈鹏,胡玉蓉,等. 一种用醋酸酯加氢制备乙醇的方法: 102093162A[P]. 2010-12-13.WANG K, CHEN P, HU Y R,. A method of producing ethanol by hydrogenation of acetate: 102093162A[P]. 2010-12-13.
[4] JOHNSTON V J, CHEN L Y, KIMMICH B F,. Direct and selective production of ethanol from acetic acid utilizing a platinum/tin catalyst: US7863489[P]. 2011-6-4.
[5] 王峰云,陆大勋. 铜基催化剂上甲酸甲酯的分解和加氢动力学[J]. 燃料化学学报, 1988, 16(1): 17-23WANG F Y, LU D X. Kinetics of methyl formate decomposition and hydrogenolysis over copper based catalyst[J]. Journal of Fuel Chemistry and Technology, 1988, 16(1): 17-23.
[6] YU J, MAO D S, HAN L P,. CO hydrogenation over Fe-promoted Rh-Mn-Li/SiO2catalyst: the effect of sequences for introducing the Fe promoter[J]. Fuel Processing Technology, 2013, 112: 100-105.
[7] ZHAO H B, ZHU Q J, GAO Y J,. Iron oxide nanoparticles supported on pyrolytic grapheme oxide as model catalysts for Fischer Tropsch synthesis[J]. Applied Catalysis A: General, 2013, 456: 233-239.
[8] ECHEANDIA S, ARIAS P L, BARRIO V L,. Synergy effect in the HDO of phenol over Ni-W catalysts supported on active carbon: effect of tungsten precursors[J]Applied Catalysis B: Environmental, 2010, 101(1/2): 1-12.
[9] HOFFER B W, CREZEE E, DEVRED F,. The role of the active phase of Raney-type Ni catalysts in the selective hydrogenation of D-glucose to D-sorbitol[J]. Applied Catalysis A: General, 2003, 253(2): 437-452.
[10] 王雪峰,王锋,陈满英,等. Ni基双金属催化剂加氢脱氧性能的研究[J]. 燃料化学学报,2005, 33(5): 612-616. WANG X F,WANG F,CHEN M Y,. Studies on nickel-based bimetallic catalysts for hydrodeoxygenation[J]. Journal of Fuel Chemistry and Technology,2005, 33(5): 612-616.
[11] 吕恩静,张怀科,任杰. 预处理方法对Mo-Ni/γ-Al2O3催化剂加氢脱氧性能的影响[J]. 石油学报(石油加工),2012,28(5): 764-768. LÜ E J, ZHANG H K, REN J. Effect of pretreatment methods of Mo-Ni/γ-Al2O3catalyst on its catalytic performance for hydrodeoxygenation[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2012, 28(5): 764-768.
[12] WU Z L, SUN F X, WU W C,. On the surface sites of MoP/SiO2catalyst under sulfiding conditions: IR spectroscopy and catalytic reactivity studies[J]. Journal of Catalysis, 2004, 222(1): 41-52.
[13] PHILLIPS D C, SAWHILL S J, SELF R,. Synthesis, characterization, and hydrodesulfurization properties of silica-supported molybdenum phosphide catalysts[J]. Journal of Catalysis,2002207(2): 266-273.
[14] STINNER C, PRINS R, WEBER T. Formation, structure, and HDN activity of unsupported molybdenum phosphide[J]. Journal of Catalysis2000, 191(2): 438-444.
[15] WANG X Q, CLARK P, OYAMA S T. Synthesis, characterization, and hydrotreating activity of several iron group transition metal phosphides[J]. Journal of Catalysis, 2002, 208(2): 321-331.
[16] OYAMA S T, WANG X, LEE Y K,. Effect of phosphorus content in nickel phosphide catalysts studied by XAFS and other techniques[J]. Journal of Catalysis, 2002, 210(1): 207-217.
[17] LIU D P, WANG A J, LIU C G,. Bulk and Al2O3-supported Ni2P HDS catalysts prepared by separating the nickel and hypophosphite sources[J]. Catalysis Communications, 2016, 77: 13-17.
[18] 宋华, 宫静, 姜楠, 等. 磷镍物质的量比对溶剂热法制备的磷化镍催化剂加氢脱硫性能的影响[J]. 燃料化学学报, 2016, 44(5): 557-563. SONG H, GONG J, JIANG N,. Effect of P/Ni ratio on the structure and hydrodesulfurization performance of nickel phosphide catalyst prepared by the solvothermal method[J]. Journal of Fuel Chemistry and Technology, 2016, 44(5): 557-563.
[19] DUAN X P, TENG Y, WANG A J,. Role of sufur in hydrotreating catalysis over nickel phosphide[J]. Journal of Catalysis, 2009, 261(2): 232-240.
[20] WHIFFEN V M L, SMITH K J. Hydrodeoxygenation of 4-methyphenol over unsupported MoP, MoS2, and MoOcatalysts[J]. Energy & Fuels2010, 24(9): 4728-4737.
[21] ZHAO H Y, LI D, BUI P,. Hydrodeoxygenation of guaiacol as model compound for pyrolysis oil on transition metal phosphide hydroprocessing catalysts[J]. Applied Catalysis A: General, 2011, 391(1/2): 305-310.
[22] SHI G J, SHEN J Y. Mesoporous carbon supported nickel phosphide catalysts prepared by solid phase reaction[J]. Catalysis Communications, 2009, 10(13): 1693-1696.
[23] SHI G J, SHEN J Y. New synthesis method for nickel phosphide nanoparticles: solid phase reaction of nickel cations with hypophosphites[J]. Journal of Materials Chemistry, 2009, 19: 2295-2297.
[24] 李景锋,李学辉,柴永明,等. 磷化镍的制备、表征及其催化性能研究进展[J]. 化工进展,2013, 32(11): 2621-2630. LI J F,LI X H,CHAI Y M,. Progress in the fabrication, characterization and catalytic reactivity of nickel phosphide[J]. Chemical Industry and Engineering Progress, 2013, 32(11): 2621-2630.
[25] GUAN Q X, LI W, ZHANG M H,. Alternative synthesis of bulk and supported nickel phosphides from the thermal decomposition of hypophosphites[J]. Journal of Catalysis,2009, 263(1): 1-3.
[26] 刘理华,李广慈,刘宾,等. 磷化镍调变MoS2/γ-Al2O3催化剂的加氢脱硫性能[J]. 化工学报,2011,62(5): 1296-1301. LIU L H, LI G C, LIU B,. Hydrosulfurization performance study of Ni2P-modified MoS2/γ-Al2O3catalysts[J]. CIESC Journal, 2011, 62(5): 1296-1301.
[27] 李德宝,肖勇,陈从标. 一种合成乙醇的催化剂及制法和应用: 102631941B[P]. 2012-03-07.LI D B, XIAO Y, CHEN C B. A catalyst for synthesis of ethanol and its preparation and application: 102631941B[P]. 2012-03-07.
[28] PRASERTHDAM P, CHOUNGCHAISUKASAM P, ASSABUMRUNGRAT S,. Role of Sn and K on hydrogen spillover on Pt/γ-Al2O3catalyst[J]. Journal of the Chinese Institute of Chemical Engineers, 2001, 32(2): 143-149.
Preparation and performance evaluation of Ni2P/SiO2catalysts for acetic acid hydrogenation to produce ethanol
REN Jie, HU Wangwei, YUAN Haikuan, SHEN Lian
(College of Chemical Engineering, Zhejiang University of Technology, Hangzhou 310014, Zhejiang, China)
A series of silica supported transition metal phosphide catalysts were prepared through isovolumetric impregnationand heat treatment under N2protection. Their catalytic performances were evaluated by ethanol yield and reaction kinetics of acetic acid hydrogenation. Results showed that both conversion of acetic acid and ethanol selectivity were gradually increased with reaction temperature increasing from 280℃ to 340℃. With P/Ni molar ratio for catalyst preparation was increased from 2:1 to 4:1, the obtained catalysts exhibited first increase and then decrease in activity and selectivity with optimal performance at P/Ni=3:1. The catalyst prepared by heat treatment at 250℃ had better catalytic performances than those at 200℃ and 300℃. The activity and ethanol selectivity of Ni2P/SiO2catalysts were higher than that of Co2P/SiO2catalysts. Catalysts using sodium hypophosphite as phosphorus supplement had better performance than those of potassium hypophosphite. Under temperature at 340℃, pressure at 2.0 MPa, molar ratio of hydrogen to acetic acid at 10:1, and WHSV at 0.4 h-1, acetic acid hydrogenation over Ni2P/SiO2prepared in better conditions showed 100% conversion of acetic acid and 74.56% selectivity of ethanol. In addition, ethanol selectivity could be further improved by appropriate increase of reaction temperature.
acetic acid; hydrogenation; ethanol; nickel phosphide; catalyst; preparation; reaction kinetics
10.11949/j.issn.0438-1157.20170109
TQ 032.41
A
0438—1157(2017)08—3082—07
任杰(1961—),男,教授。
2017-02-06收到初稿,2017-05-26收到修改稿。
2017-02-06.
Prof. REN Jie, Renjie.R@263.net
