骨质疏松性椎体压缩骨折PKP术后近期手术椎体再骨折原因探讨
2017-09-27彭冉东邓强李中锋张彦军韩宪富李军杰
彭冉东,邓强,李中锋,张彦军,韩宪富,李军杰
(1.甘肃中医药大学,甘肃 兰州 730000;2.甘肃省中医院脊柱骨二科,甘肃 兰州 730000)
骨质疏松性椎体压缩骨折PKP术后近期手术椎体再骨折原因探讨
彭冉东1,邓强2*,李中锋2,张彦军2,韩宪富1,李军杰1
(1.甘肃中医药大学,甘肃 兰州 730000;2.甘肃省中医院脊柱骨二科,甘肃 兰州 730000)
目的探讨经皮椎体后凸成形术治疗单椎体骨质疏松性椎体压缩骨折术后近期手术椎体再骨折相关原因,为临床预防提供参考。方法对已行椎体后凸成形术(percutaneous kyphoplasty,PKP)治疗且符合纳入标准的188例患者临床资料进行回顾性分析,根据患者的临床表现及影像学显示,分为手术椎体再骨折组(A组,共24例),无再发椎体骨折组(B组,共164例)。术后随访1年以上,记录所有入选患者的性别、年龄、身高、体重、身体质量指数(body mass index,BMI)、骨密度、手术节段、骨水泥注入量、骨水泥弥散形态、骨水泥与椎体上下终板间距离、术后佩戴支具的时间、术后是否规范化使用抗骨质疏松治疗等相关因素,探讨导致术后手术椎体再骨折的原因。结果性别、年龄、身高、体重、BMI、手术节段、骨水泥注入量、术后佩戴支具时间等因素在A、B两组间差异无统计学意义(P>0.05)。A组患者术后规范抗骨质疏松治疗依从性较B组差,术后6个月A、B两组骨密度T值分别为(-2.46±0.700)、(-2.21±0.715),差异有统计学意义(P<0.05),末次随访时A、B两组分别为(-2.37±0.896)、(-1.92±0.804),差异有统计学意义(P<0.01)。将椎体内骨水泥弥散形态分为团块状与海绵状,其中A、B两组团块状分布分别为15例、58例,海绵状分布分别为9例、106例,差异有统计学意义(χ2=6.490,P<0.05)。术后3 d复查测量A、B两组骨水泥上缘距上终板距离分别为(3.38±0.744)mm、(1.98±0.707)mm,骨水泥下缘距下终板距离分别为(3.13±0.835)mm、(1.82±0.475)mm,差异均有统计学意义(P<0.05)。结论PKP术后近期手术椎体再骨折是多方面综合因素共同引起的,其中骨水泥弥散形态、骨水泥与椎体上下终板间距离以及骨密度是导致手术椎体再骨折的重要危险因素。
经皮椎体后凸成形术;骨质疏松;椎体压缩骨折;再骨折
近年来,经皮球囊扩张椎体后凸成形术(percutaneous kyphoplasty,PKP)广泛用于治疗骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fractures,OVCF),临床疗效显著[1,2]。但椎体强化术后再骨折时有发生,国内外文献[3-6]对术后邻近椎体再骨折相关因素报道较多,有关手术椎体再骨折的发生原因报道较少。本研究将我科近年来行PKP术患者的临床资料进行回顾性分析研究,探寻导致手术椎体再骨折的相关危险因素,为加强预防提供参考。
1 资料与方法
1.1 研究对象 2014年1月至2015年1月甘肃省中医院脊柱骨二科行PKP治疗OVCF患者共253例,其中符合纳入标准并获完整随访者188例,根据是否发生手术椎体再骨折分为手术椎体再骨折组(A组,共24例)和无再发椎体骨折组(B组,共164例)。两组患者一般情况比较见表1。
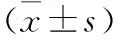
表1 两组患者一般情况比较
1.2 诊断标准 主要通过患者的临床症状、体征及影像学表现确诊。临床表现:患者术后腰背部疼痛基本缓解后再次出现原部位疼痛;原手术椎体棘突叩压痛阳性或该手术节段神经支配区域疼痛。影像学表现:a)部分患者疼痛不明显但通过侧位X线片检查可见原手术椎体高度较术后降低,脊柱后凸角增大[7-9];b)CT检查显示原手术椎体内骨质连续性中断或骨水泥碎裂;c)MRI检查显示椎体内水肿,T1加权像呈低信号,T2加权像呈高信号[10]。
1.3 纳入标准 a)手术方法均为单侧穿刺行PKP术,由同一组手术医师操作;b)骨质疏松引起的胸腰椎单椎体新鲜压缩骨折患者;c)术前影像学显示无椎体裂隙样变及骨坏死;d)术后未发生骨水泥渗漏引起的脊髓、神经损伤及肺栓塞等相关并发症;e)随访时间大于1年;f)临床及影像学资料完整。
1.4 排除标准 a)因肿瘤、感染或长期使用激素等原因导致的病理性骨折(不包括骨质疏松性骨折);b)非手术椎体发生骨折或手术椎体并发其他椎体骨折;c)严重精神障碍患者;d)资料不完善者;e)术前合并其他骨折病史以及术后有明确外伤史所致爆裂性骨折。
1.5 治疗方法
1.5.1 骨水泥品牌及型号 本研究选用低黏度骨水泥。患者俯卧位,在C型臂X线机引导下进行定位,明确责任椎及进针点,消毒、铺巾。使用球囊扩张系统扩张椎体,待椎体恢复一定高度后,将调制好的骨水泥在透视机下缓慢、均匀注入病椎内。记录每例患者骨水泥总量。
术后医嘱:a)术后嘱患者平卧,24~48 h后佩戴支具适度下地活动;b)术后3 d复查以伤椎为中心的正侧位X线片及CT;c)术后3~5 d出院,出院医嘱:(a)出院后继续佩戴支具2~3个月,术后1个月、3个月、6个月、12个月门诊复查;(b)坚持适度、适量行腰背肌功能锻炼:术后腰背痛及活动障碍完全缓解,每日早晚行五点支撑式腰背肌锻炼,每次10~20个;(c)嘱患者均衡膳食营养,多晒太阳(每天30 min~1 h);(d)术后规范化抗骨质疏松治疗:口服活性维生素D+钙剂0.6 g/次,1次/日,长期服用;阿仑膦酸钠70 mg,每周1次;根据骨密度及血钙、尿钙等相关水平调整用药。
1.5.2 观察指标及评定方法 所有患者均记录性别、年龄、身高、体重、BMI、手术节段、骨水泥注入量、术后佩戴支具时间、术后是否规范化抗骨质疏松治疗。采用双能X线骨密度仪测量治疗前后腰椎(L2~4)侧位骨密度T值。术后3 d X线及CT检查观察骨水泥在病椎内的弥散形态、测量骨水泥上下缘距病椎上下终板间的最小距离。相关影像学资料均由我院两名骨科专家分别在PACS图像系统上单独进行测量,测量结果如有不同,则由两名专家重新测定以达到一致。
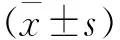
2 结 果
A、B两组患者在年龄、性别、身高、体重、BMI、术前骨密度值、骨水泥用量,支具佩戴时间上差异无统计学意义,具有可比性(P>0.05,见表1)。
A组椎体再骨折主要集中在胸腰结合部位(T12~L1),其中T11共6例,T12共8例,L1共7例,L2共3例。但通过统计分析两组手术节段(胸腰椎结合部:非胸腰结合)分布A组(16例:8例),B组(89例:75例)有一定差异,差异无统计学意义(χ2=1.305,P=0.253)。平均随访(13.35±0.52)个月,再骨折最早发生在术后26 d,最晚发生在术后9个月,平均发生时间为术后(5.82±1.44)个月。
通过对比观察,B组144例患者术后坚持规范化抗骨质疏松治疗,A组仅9例,差异有统计学意义(χ2=10.276,P<0.05);骨密度测定结果表明B组术后6个月、末次随访T值均高于A组(P<0.05),两组术后6个月至末次随访组内BMD比较,B组较A组改善明显,这可能与B组术后规范化使用抗骨质疏松药物有关(见表2)。
A、B两组术后骨水泥弥散情况比较:通过影像学显示,将椎体内骨水泥弥散形态分为团块状与海绵状,其中A、B两组团块状分布分别为15例、58例,海绵状分布分别为9例、106例,差异有统计学意义(χ2=6.490,P<0.05)。A组术后与末次随访骨水泥距上、下终板距离比较,差异均有统计学意义(P<0.01,见表3)。
典型病例为一57岁男性患者,摔伤致腰背部疼痛、活动受限4 d以“L2骨质疏松性椎体压缩骨折”入院。骨密度示T=-2.6,在局麻下行经皮椎体后凸成形术,术后疼痛缓解明显,腰椎活动恢复正常。患者术后未坚持服用抗骨质疏松药物,术后145 d不慎跌倒致腰背部剧烈疼痛, L2椎体PKP术后再骨折。手术前后影像学资料见图1~5。
3 讨 论
经皮球囊扩张椎体后凸成形术作为一种新型微创技术广泛用于治疗骨质疏松性椎体压缩骨折,且取得了良好的疗效,受到了广大骨科医师和患者的青睐,但是椎体强化术后手术椎体再骨折也引起了学者的广泛关注。Kim等[7]报道PKP术后手术椎体再骨折发生率为12.5%,发生时间平均为术后3.4个月,Lavelle等[11]研究发现PKP术后90 d之内同一椎体再骨折发生率为10%。通过1年随访,本研究手术椎体再骨折发生率为12.7%,时间集中在术后(5.82±1.44)个月,与以上报道结果基本相符。
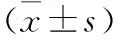
表2 两组术后6个月及末次随访时骨质疏松程度对比
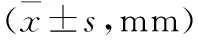
表3 术后及末次随访骨水泥上下缘距椎体终板间距离
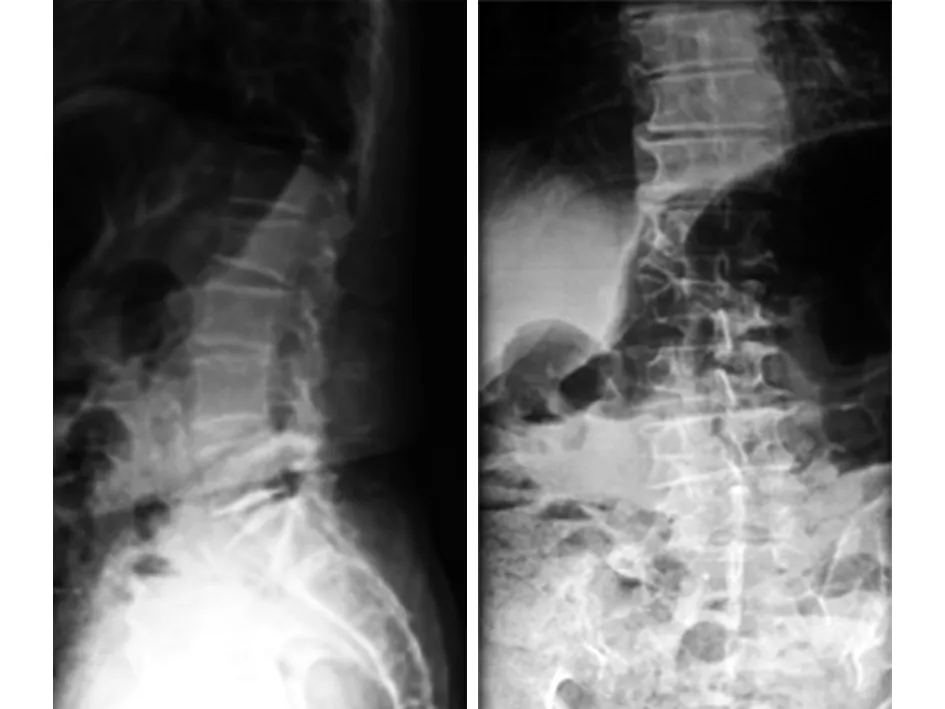
图1 术前正侧位X线片示L2椎体前柱压缩楔形改变
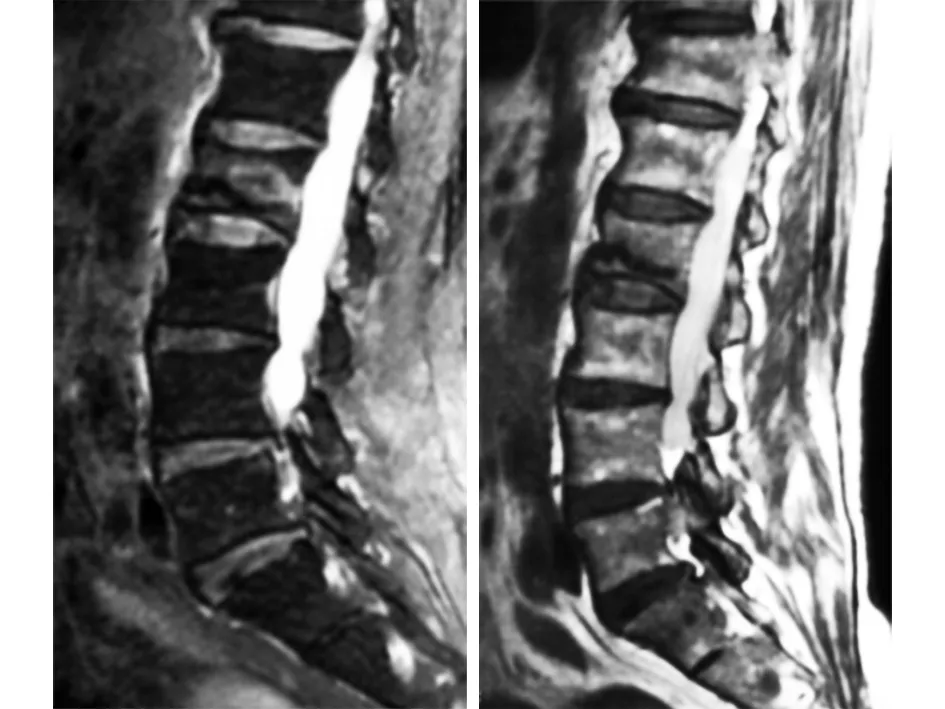
图2 术前MRI示椎体内水肿,T1加权像呈低信号,抑脂像呈高信号
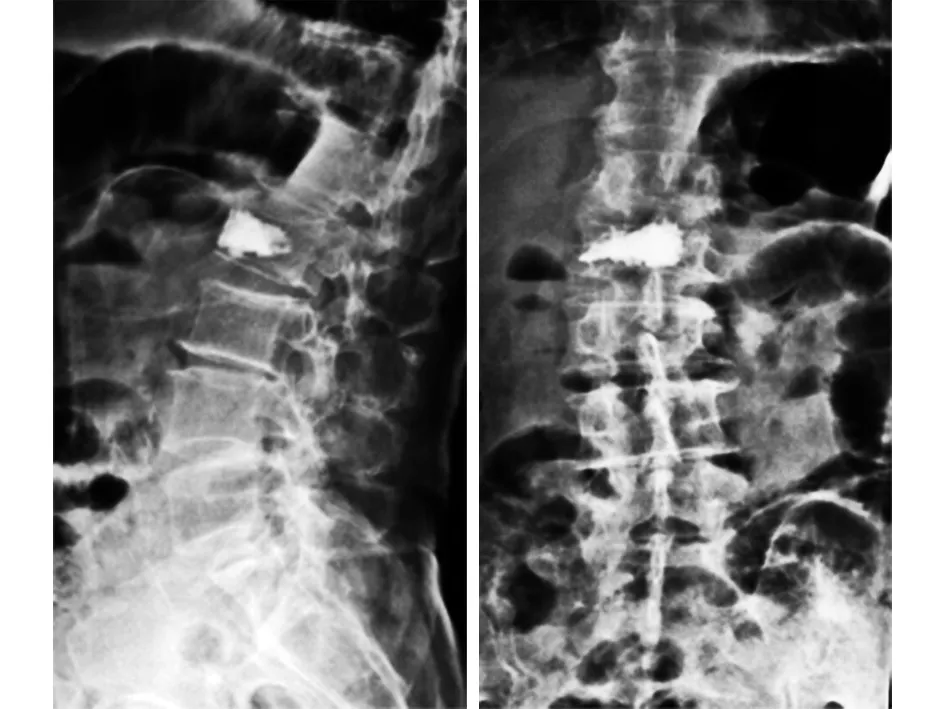
图3 PKP术后3 d正侧位X线片示骨水泥弥散良好
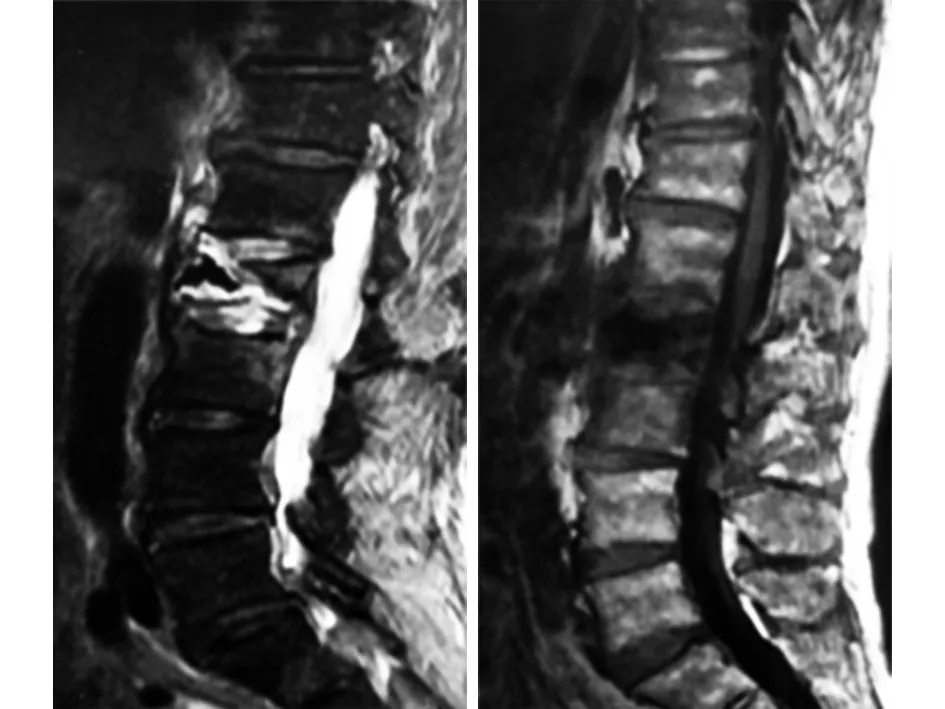
图4 腰椎MRI示L2椎体PKP术后再骨折
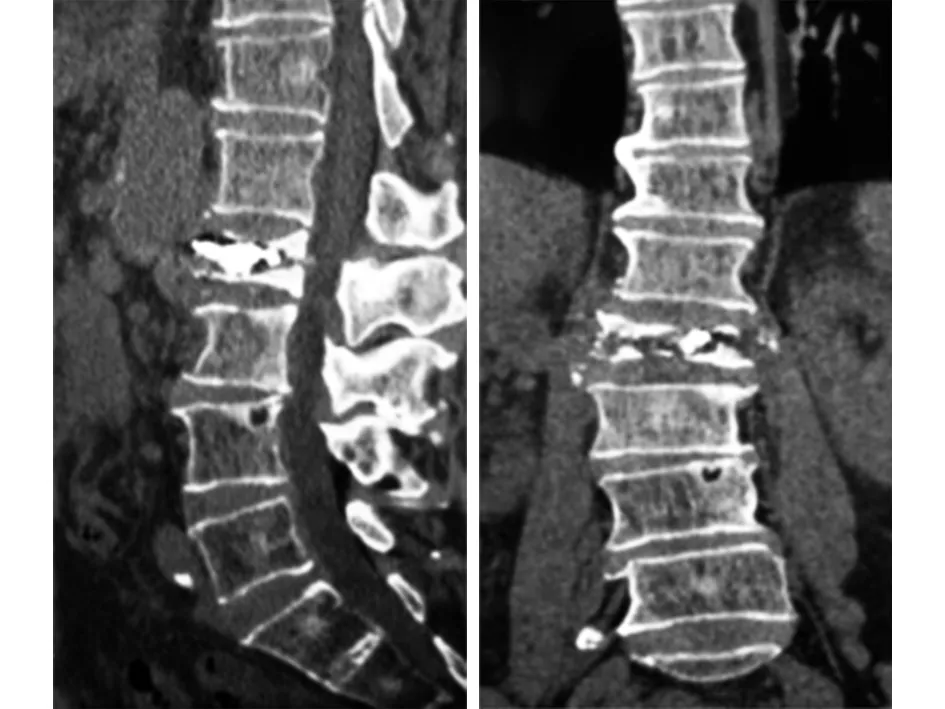
图5 腰椎二维重建CT示L2椎体PKP术后再骨折
3.1 手术节段对手术椎体再骨折的影响 Chen等[10]研究发现术椎再发骨折节段主要在T11~L2。本研究再骨折主要发生T11~L1,笔者认为主要是由于胸腰椎交界处活动度大,椎体承受压力大,极易发生手术椎体再发骨折。但是目前缺乏生物力学研究证实胸腰段是手术椎体再骨折的危险因素。
3.2 病椎骨质情况对手术椎体再骨折的影响 目前普遍认为[12-13]椎体再骨折与骨质疏松程度进展密切相关。本研究中A、B两组患者术后6个月BMD值与末次随访组间比较,差异均有统计学意义(P<0.05),B组组内纵向比较差异有统计学意义(P<0.05)。椎体多为松质骨,伤后骨小梁微细结构发生破坏,新骨生长缓慢,随着骨质疏松的进一步加重,椎体骨强度下降都将影响术后椎体高度的维持,极易发生再骨折。
3.3 病椎术中骨水泥弥散情况对手术椎体再骨折的影响 骨水泥充分填充骨折线,均匀弥散于病椎内,多呈海绵状,若骨水泥在病椎内弥散不佳,多呈团块状。Tanigawa[14]将术后骨水泥在病椎内弥散形态分为团块状和海绵状,术后随访发现团块状分布组患者再骨折发生率较高。本研究中A、B两组骨水泥团块状分布占有比例分别为62.5%、54.7%(P<0.05),但是有关骨水泥椎体内分布形态对手术效果和再骨折的影响,国内外文献报道较少,尚需进一步研究。A组术后测量骨水泥上缘距上终板距离由(3.38±0.744)mm降低到末次随访时的(2.25±0.707)mm,术后测量骨水泥下缘距下终板距离由(3.13±0.835)mm降低到末次随访的(2.00±0.535)mm,两者改变均有统计学意义(P<0.05)。我们认为是由于骨水泥未能同时接触上下终板,没有骨水泥的骨性区域,可能会发生应力遮挡,随着骨量进一步减少并在长期应力作用下易发生骨折。田伟等[15]及Chevalier等[16]均表明骨水泥未同时接触上下终板时,发生再骨折的概率更高。引起术后近期手术椎体再骨折是多方面因素共同作用的结果,其中术中骨水泥弥散不佳以及骨质疏松进一步加重是导致手术椎体再骨折的重要危险因素。术中严格操作,术后坚持规范化抗骨质疏松治疗是预防术后椎体再骨折的重要措施。
[1]唐明.单侧入路经皮椎体后凸成形术治疗骨质疏松性椎体压缩骨折[J].实用骨科杂志,2016,22(6):542-544.
[2]黄卫国,李玉民,海涌.PKP治疗骨质疏松性椎体压缩性骨折的中期临床疗效分析[J].实用骨科杂志,2015,21(2):105-109.
[3]黄江发,桑莉莉,谢雨舟,等.PVP/PKP术后非手术椎体再发骨折的相关因素分析[J].中国中医骨伤科杂志,2016,24(7):40-43.
[4]张斌,尚咏.经皮椎体后凸成形术后继发邻近椎体骨折的危险因素分析[J].临床骨科杂志,2014,17(3):249-252.
[5]李格,梅伟,刘沛霖,等.骨质疏松性椎体压缩骨折经皮椎体成形术后邻近椎体再骨折的危险因素探讨[J].中医正骨,2016,28(6):18-20.
[6]李俊青,刘纪恩,勾瑞恩,等.经皮穿刺椎体后凸成形术后邻近椎体骨折的危险因素[J].河南外科学杂志,2016,22(2):10-12.
[7]Kim YY,Rhyu.KWRe compression of vertebral body after balloon kyphoplasty for osteoporotic vertebral compression fracture[J].Eur Spine J,2010,19(11):1907-1912.
[8]唐政杰,侯宇,张亘瑷,等.椎体后凸成形术后再发骨折的相关危险因素分析[J].中国矫形外科杂志,2015,23(2):124-131.
[9]余博臣,张亮,高梁斌.PVP/PKP术后手术椎体再发骨折的研究进展[J].中国脊柱脊髓杂志,2012,22(2):183-185.
[10]Chen LH,Hsieh MK,Liao JC,et al.Repeated percutaneous vertebroplasty for refracture of cemented vertebrae[J].Arch Orthop Trauma Surg,2011,131(7):927-933.
[11]Lavelle WF,Cheney R.Recurrent fracture after vertebral kypho-plasty[J].Spine J,2006,6(5):488-493.
[12]Klazen CA,Venmans A,de Vries J,et al.Percutaneous vertebroplasty is not a risk factor for new osteoporotie compression fractures:resuhs from VERTOS Ⅱ[J].Am J Neuroradiol,2010,31(8):1447-1450.
[13]Heo DH,Chin DK,Yoon YS,et al.Recollapse of previous vertebral compression fracture after percutaneous vertebroplasty[J].Osteoporos Int,2009,20(3):473-480.
[14]Tanigawa N,Komemushi A,Kariya S,et al.Relationship between cement distribution pattern and new compression fracture after percutaneous vertebroplasty[J].AJR Am J Roentgenol,2007,189(6):348-352.
[15]田伟,韩骁,刘波,等.经皮椎体后凸成形术后骨水泥分布与手术椎体再骨折的关系[J].中华创伤骨科杂志,2012,14(3):211-215.
[16]Chevalier Y,Pahr D,Charlebois M,et al.Cement distribution,volume,and compliance in vertebroplasty:some answers from an anatomy-based nonlinear finite element study[J].Spine,2008,33(16):1722-1730.
OsteoporoticVertebralCompressionFracturesafterPKPHoldstheRecentSurgeryVertebralFractureReasonagainExploretheDelta
Peng Randong1,Deng Qiang2,LI Zhongfeng2,et al
(1.Gansu CollegeTraditonal Chinese Medicine,Lanzhou 730000,China;2.The TCM Hospital of Gansu Province,Lanzhou 730000,China)
ObjectiveTo investigate the cause of vertebral fracture after recent percutaneous kyphoplasty for vertebral osteoporosis vertebral compression fractures.MethodsA retrospective analysis of related clinical data of 188 patients with PKP treatment who meet theinclusion criteria was performed.According to the clinical manifestation and imaging of thepatient,the patients were divided intogroup A(surgicalvertebral fracture,n=24) and group B (Nosurgical vertebral fracture,n=164).Follow-upafter the operationwasone year at lest.The records included the patient's age、gender、 height、weight、body mass index (BMI)、bone mineral density、operation section、 injection amount of bone cement、 bone cement dispersion morphology、the distance that between bone cement and cranial endplates andcaudalendplates、wear the support time after surgery and whether to use a standardized antiosteoporosis treatment and other related factors,to explore the cause of postoperative surgical vertebral fracture.ResultsThere was no significant difference between group A and group B,in terms of age、gender、 height、weight、body mass index (BMI)、operation section、 injection amount of bone cement and wear the support time(P>0.05).For postoperative management of patients with postoperative adherence to the treatment of osteoporosis,group A was not as good asto group B.Six months after surgery,the bone mineral density were(-2.46±0.700)、(-2.21±0.715)respectively.The difference was statistically significant(P<0.05).The final follow-up bone mineral density were (-2.37±0.896) and(-1.92±0.804)respectively.There was a significant difference between group A and group B(P<0.01).The shapes of bone cement in vertebral body were divided into masses and spongy.There were 15 cases and 58 caseswith mass-shapedbonecement,and 9 cases and 106 cases with the spongy-shapedbone cementin group A and group B respectively.The difference was statistically significant(χ2=6.490,P<0.05).3 day safter surgery,we measured the distance that between bone cement and caudal endplates.It were(3.38±0.744)mm in group A and(1.98±0.707)min group B.And the distance between bone cement and cranial endplates were(3.13±0.835)mm in group A and(1.82±0.475)min group B.The differences were statistical significance(P<0.05).ConclusionThe refractures after PKP are caused by multiple factors.The important risk factors include bone cement shape、the distance between bone cement and cranial endplates andcaudalendplates and bone mineral density.
percutaneous kyphoplasty;osteoporotic;vertebral compression fractures;broken again
李嘉坤(1984- ),男,主治医师,玉林市中西医结合骨科医院脊柱科,537000。
1008-5572(2017)09-0781-05
卫生部医药卫生科技发展研究中心科研基金(W2014ZT210);甘肃省中医药管理局科研课题(GZK-2016-49);国家中医药管理局国家中医临床研究基地业务建设科研专项课题(JDZX2015039);*本文通讯作者:邓强
R683.2
:B
2017-03-12
彭冉东,邓强,李中锋,等.骨质疏松性椎体压缩骨折PKP术后近期手术椎体再骨折原因探讨[J].实用骨科杂志,2017,23(9):781-785.
