帕金森病病人的疲劳发生特点及睡眠行为干预对疲劳的影响
2017-09-20,
,
帕金森病病人的疲劳发生特点及睡眠行为干预对疲劳的影响
贾培兰,任金红
[目的]观察帕金森病病人的疲劳发生特点及影响因素,探讨睡眠行为干预对疲劳的影响。[方法]选择2011年7月—2015年12月来我院就诊帕金森病病人55例为研究对象,研究分为2个阶段,第一阶段(2011年7月—2015年12月)为观察性横断面研究,采用统一帕金森病评分表(UPDRS)第3部分评价运动症状,采用修订的Hoehn-Yahr量表评价疾病严重程度,采用非运动症状量表(NMSS)评估非运动症状,采用疲劳严重度量表(FSS)评价病人的疲劳程度。应用Logistic多元回归分析疲劳的独立危险因素。第二阶段(2016年1月—2016年6月)为干预性前瞻性研究。对研究对象行基线FFS评分和帕金森病睡眠量表(PDSS)评分后,给予睡眠行为干预,3个月后再次行FFS评分和PDSS评分。[结果]帕金森病病人首次FSS评分为3.8分±1.8分,25例(45.5%)病人存在疲劳。Logistic多元回归分析显示,睡眠评分、情绪与认知评分是影响疲劳的独立危险因素。睡眠行为干预后FFS评分、疲劳发生率均降低,而PDSS评分升高。[结论]疲劳是帕金森病病人常见非运动症状,睡眠障碍、情绪与认知障碍是其独立的危险因素,睡眠行为干预能够有效地降低疲劳水平。
帕金森病;疲劳;睡眠干预;非运动症状
帕金森病(Parkinson’s disease,PD)是一种以多巴胺能神经元减少或缺失为病理、生理特征的渐进性神经退行性疾病,其典型表现为运动症状,包括运动迟缓、肌强直、静止性震颤,因此,传统上帕金森病一直归属于运动障碍疾病。然而,近年的研究注意到,运动障碍仅为帕金森病复杂症状的冰山一角,非运动症状包括神经精神症状、自主神经症状和感觉症状也十分普遍[1-2]。其中疲劳是帕金森病常见非运动症状之一,发生率波动在37%~56%[3]。疲劳也是最能致残的非运动症状之一。研究表明,在排除年龄、病程和疾病严重程度等因素后,疲劳仍对帕金森病病人的日常生活能力和总体生活质量造成明显的损害[4-5]。然而,由于疲劳缺乏特异性,医务人员和家庭照顾者均对其认识及干预不足[6]。并且,对于这种渐进性神经系统疾病自身所导致的疲劳,其处理也比较棘手。因此,本研究拟观察帕金森病病人的疲劳发生特点及影响因素,并据此选择其中易干预因素进行干预,探讨其对帕金森病病人疲劳的效果。
1 对象与方法
1.1 对象 选择2011年7月—2015年12月来我院就诊的帕金森病病人55例为研究对象,所有病人均符合1992年英国帕金森病脑库制定的原发性帕金森病的诊断标准。排除标准:非典型性帕金森病、继发性帕金森病、严重精神疾病,合并其他神经系统疾病如卒中、癫痫,合并其他可能与疲劳相关的严重疾病如恶性肿瘤、心肺疾病等病人。其中男35例,女20例,年龄49岁~84岁(67.5岁±11.6岁)。研究经院伦理委员会批准,研究对象或其家属均知情同意。
1.2 研究方法 本研究分为两个阶段,第一阶段(2011年7月—2015年12月)为观察性横断面研究,第二阶段(2016年1月—2016年6月)为干预性前瞻研究。
1.2.1 研究第一阶段
1.2.1.1 运动症状评估 ①采用统一帕金森病评分表(Unified Parkinson’s Disease Rating Scale,UPDRS)第3部分(运动功能)评价运动症状,各亚症状得分计算方法如下:震颤20项~21项,肌强直22项,运动迟缓23项~26项,中轴症状27项~30项。分值越高,运动功能越差。评分均在“关”期进行,即评分时间距末次服用左旋多巴制剂时间必须达12 h或以上。②采用修订的Hoehn-Yahr量表评价疾病严重程度(0级~5.0级)。
1.2.1.2 非运动症状评估 应用非运动症状量表(Non-Motor Symptoms Scale,NMSS)评估。该量表是专为评估帕金森病非运动症状而开发的量表,包含心血管系统症状、睡眠与疲劳、情绪与认知、幻觉与妄想、注意力与记忆力、胃肠道症状、泌尿系统症状、性功能症状和其他症状9个维度,共30项,能客观描述非运动症状的进展情况和疗效反应。得分越高表示症状越严重。
1.2.1.3 首次疲劳评估 采用疲劳严重度量表(Fatigue Severity Scale,FSS)评价病人近2周的疲劳程度。FSS是临床应用最广泛的疲劳自评量表,被推荐用于帕金森病病人疲劳的筛选和严重程度评估,由9个条目组成,每个条目评分为1分(非常不同意)到7分(非常同意),FSS得分为总分/9,>4分评定为疲劳,并据此将研究对象分为疲劳组和非疲劳组。
1.2.2 研究第二阶段
1.2.2.1 基线评估 第一阶段结束后,联系所有研究对象和家属,联系方式包括门诊随访联系、电话联系、QQ联系、微信联系,必要时至病人家里联系。所有研究对象再次进行疲劳评估,方法同前。同时采用帕金森病睡眠量表(Parkinson’s Disease Scale,PDSS)评价睡眠状况,此量表由15项组成,每项计0分~10分,得分越高,提示睡眠质量越好。
1.2.2.2 睡眠干预 由研究人员对病人和家庭主要照顾者进行专门的培训。①一般措施:创造良好的睡眠环境和条件,如室温和光线适宜;床褥不宜太软,以免翻身困难等;进行睡眠卫生教育,如指导病人养成良好的睡眠习惯和方式,建立比较规律的活动和休息时间表。②睡眠行为干预:采用刺激控制疗法[7],其是一套帮助病人减少与睡眠无关的行为和建立规律性睡眠-觉醒模式的程序,可减少药物治疗的用量。包括:只在有睡意时才上床;床及卧室只用于睡眠,不能在床上阅读、看电视或工作;若上床15 min~20 min不能入睡,则应考虑换别的房间,仅在又有睡意时才上床(目的是重建卧室与睡眠间的关系);无论夜间睡多久,清晨应准时起床;白天不打瞌睡。每个月电话随访1次,监督病人及其主要照顾者的睡眠干预执行情况,交流在实际操作中的问题,并提出解决方案。睡眠行为干预时间为3个月。
1.2.2.3 干预后评估 睡眠行为干预3个月后,联系病人进行疲劳评估和睡眠评估,方法同前。

2 结果
2.1 帕金森病病人首次疲劳评分和疲劳发生情况 研究对象的FSS评分为3.8分±1.8分,其中25例(45.5%)病人存在疲劳。单因素分析见表1,Logistic多元回归分析显示,睡眠评分、情绪与认知评分是影响疲劳的独立危险因素,见表2。
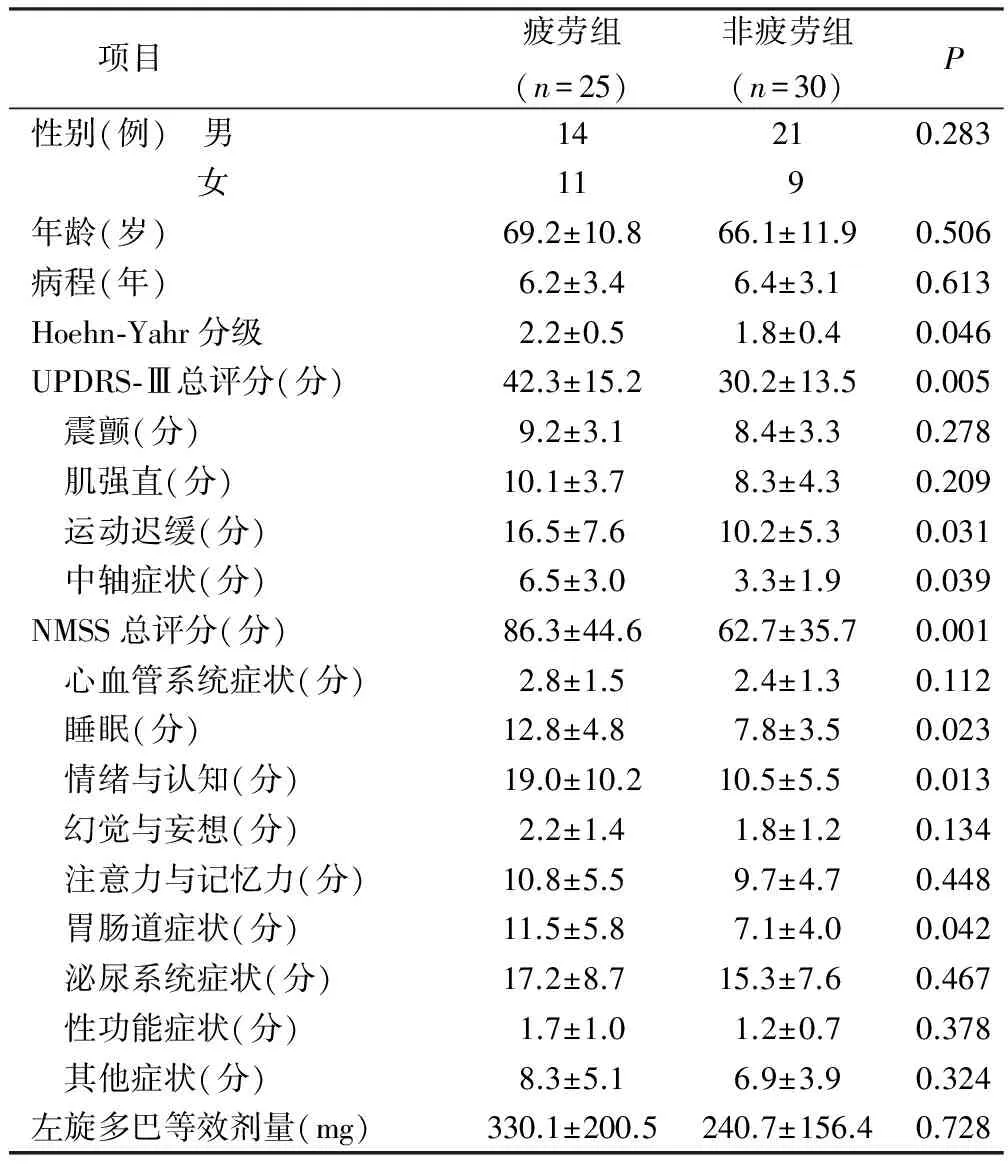
表1 疲劳组和非疲劳组的临床指标比较
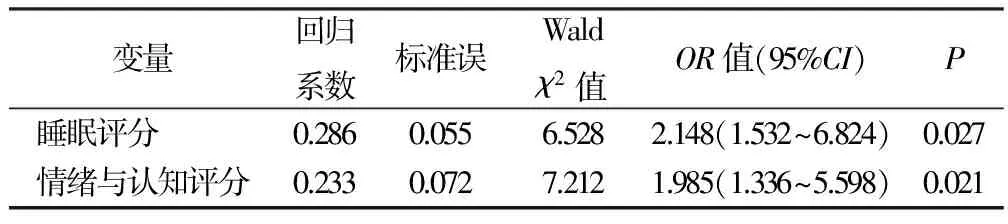
表2 帕金森病病人疲劳得分的Logistic多元回归分析
2.2 睡眠行为干预对帕金森病病人疲劳的影响 研究第一阶段结束后有4例病人失访,因此,研究第二阶段共有51例病人纳入干预性研究。干预后FSS评分、疲劳发生率均降低,而PDSS评分升高,见表3。
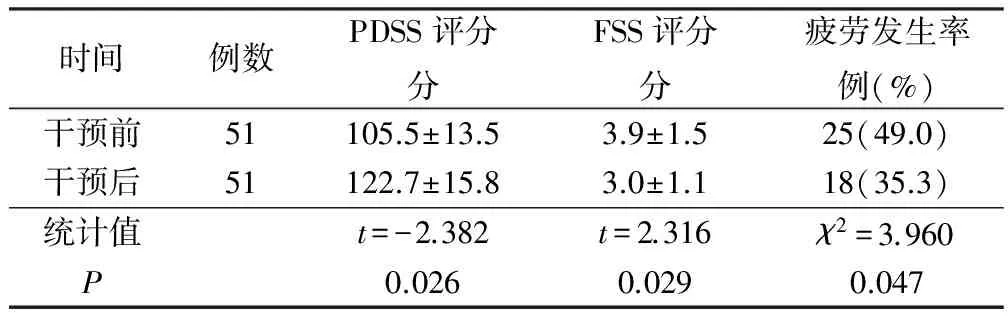
表3 帕金森病病人干预前后疲劳和睡眠情况比较
3 讨论
疲劳是病人个人的一种主观感觉和经验。目前仍无关于帕金森病疲劳的准确而标准的定义,国外有学者将其定义为一种体力缺乏、疲惫的感觉,对躯体功能和社会生活产生干扰,有别于精神上的疲惫、悲伤、失眠,继帕金森病的运动症状(肌强直、震颤)进一步对其运动功能造成损害[8]。有研究对170例帕金森病病人进行研究,结果显示,疲劳的发生率在所有非运动症状中位居第5位[9]。国外研究报道帕金森病病人的疲劳发生率为37%~56%[3],国内研究报道为42.7%~76.7%[10-12],本研究中帕金森病病人疲劳发生率为45.5%,与国内外的研究结果一致。目前,对疲劳的病理生理机制尚不明确。Pavese等[13]应用PET对帕金森病疲劳者和非疲劳者进行了比较,发现帕金森病伴疲劳者的基底节及边缘结构的5-羟色胺转运体结合率低于无疲劳者,而纹状体多巴的摄取则无明显改变,反映非多巴胺能机制可能更多地参与了病理生理进程。有研究应用心肌123I-苄基胍闪烁显像评价帕金森病病人的心交感神经功能,发现123I-苄基胍的心脏/纵隔摄取率与疲劳评分呈负相关,认为帕金森病的疲劳可能与心交感神经变性、心肌收缩力降低有关[14]。总之,帕金森病病人的疲劳可能既涉及中枢性疲劳,又涉及周围性疲劳。
由于纳入标准、病情轻重、研究人种和评价工具的不同,关于帕金森病疲劳的危险因素的研究结果并不一致。Herlfson等[15]认为疲劳属于疾病的独立症状。Karlsen等[16]研究结果表明,抑郁水平是帕金森病疲劳的独立危险因素。楼跃等[12]研究发现,UPDRS第二部分评分及抑郁情绪是疲劳的独立危险因素。本研究经过单因素和多因素分析之后,发现非运动症状与疲劳的关系更为密切,尤其是睡眠障碍、情绪与认知障碍为疲劳的独立危险因素。这与董青等[10]研究结果基本一致,该研究采用17项汉密尔顿抑郁量表评价抑郁状况,采用帕金森病睡眠量表评价睡眠状况,结果显示,汉密尔顿抑郁量表评分和PDSS评分是帕金森病病人疲劳的独立危险因素。意大利的一项研究结果也提示,帕金森病病人的疲劳与睡眠障碍、情感障碍关系密切[17]。
国内的一项调查表明,疲劳严重影响帕金森病病人的生活质量,其中有近25%的病人认为疲劳是最严重的致残症状,50%以上的病人认为疲劳影响工作和日常生活,并且这种疲劳感在性质和程度上与以往不同[12]。因此,采取有效的措施降低疲劳水平具有重要的实用意义。左旋多巴虽然能够有效改善运动症状,但是对疲劳没有明显效果[8]。本研究基于第一阶段的研究结果对病人进行了睡眠干预,结果发现,干预后PDSS评分升高,而疲劳评分和疲劳发生率下降,提示改善睡眠行为能够降低疲劳水平。帕金森病具有一定的异质性,姿势不稳、行走困难型的帕金森病病人较震颤型和中间型病人更易出现疲劳,非震颤为主型帕金森病病人快速眼球运动睡眠期行为障碍发生率高于震颤型[18-20],提示帕金森病病人疲劳和睡眠障碍在病理机制上可能也存在重叠。因此,改善睡眠有助于降低疲劳水平。Alves等[21]对233例帕金森病病人长达8年的随访研究显示,疲劳与昼间睡眠过多呈正相关。本研究采用的睡眠行为干预方法的一个重要原则是减少白天睡眠时间,这可能是病人疲劳水平下降的另一个原因。此外,睡眠作为最有效的休息方式,也必然有利于病人体力和精神的恢复,对于躯体疲劳和精神疲劳均会有一定的缓解作用。本研究针对第一阶段的研究结果进行睡眠行为干预,主要是因为与情绪与认知领域如抑郁、体验困难相比,改善睡眠似乎要相对简单,并且干预措施的专业性较弱,无须专业人员,由家庭主要照顾者即可完成。采用的方法主要是行为干预,无额外费用,无须特殊仪器和药物,非常适合病人在家中长期应用。并且,一旦好的习惯养成,可能会取得事半功倍的效果。
本研究表明疲劳是帕金森病病人常见非运动症状,睡眠障碍、情绪与认知障碍是其独立的危险因素。睡眠行为干预能够有效地降低疲劳水平。
[1] 郑瑾,孙圣刚,乔娴.帕金森病病人非运动症状的发生状况及影响因素[J].中华老年医学杂志,2010,29(10):796-799.
[2] 董宏利,刘春风,胡小伟.帕金森病病人非运动症状对其生活质量的影响[J].中华医学杂志,2014,94(11):813-815.
[3] Beiske AG,Svensson E.Fatigue in Parkinson’s disease:a short update[J].Acta Neurol Scand Suppl,2010,1(190):78-81.
[4] Miwa H,Miwa T.Fatigue in patients with Parkinson’s disease:impact on quality of life[J].Intern Med,2011,50(15):1553-1558.
[5] Elbers RG,van Wegen EE,Verhoef J,etal.Impact of fatigue on health-related quality of life in patients with Parkinson’s disease;a prospective study[J].Clin Rehabil,2014,28(3):300-311.
[6] Chaudhuri KR,Prieto-Jurcynska C,Naidu Y,etal.The nondeclaration of nonmotor symptoms of Parkinson’s disease to health care professionals:an international study using the nonmotor symptoms questionnaire[J].Mov Disord,2010,25(6):704-709.
[7] 杨亚娟,赵金娣.帕金森病病人睡眠障碍的临床护理进展[J].中华护理杂志,2004,39(11):855-856.
[8] 李姗姗,彭国光.帕金森病的非运动症状——疲劳[J].世界科技研究与发展,2012,34(4):677-680.
[9] 高俊华,闫兆芬,孙莉,等.帕金森病病人非运动症状的临床研究[J].中国全科医学,2010,13(23):2576-2580.
[10] 董青,王智樱,沈沸,等.帕金森病病人伴疲劳症状的调查分析[J].上海交通大学学报(医学版),2012,32(7):926-929.
[11] 左丽君,余舒扬,曹辰杰,等.帕金森病病人疲劳及其相关因素的研究[J].中华临床医师杂志(电子版),2012,6(22):7238-7244.
[12] 楼跃,肖勤,陈生弟.帕金森病疲劳的相关因素研究[J].老年医学与保健,2012,18(2):76-78;86.
[13] Pavese N,Metta V,Bose SK,etal.Fatigue in Parkinson’s disease is linked to striatal and limbic serotonergic dysfunction[J].Brain,2010,133(11):3434-3443.
[14] Nakamura T,Hirayama M,Hara T,etal.Does cardiovascular autonomic dysfunction contribute to fatigue in Parkinson’s disease?[J].Mov Disord,2011,26(10):1869-1874.
[15] Herlofson K,Larsen JP.Measuring fatigue in patients with Parkinson’s disease:the fatigue severity seale[J].Eur J Neurol,2002,9(6):595-600.
[16] Karlsen K,Larsen JP,Tandberg E,etal.Fatigue in patients with Parkinson’s disease[J].Mov disord,1999,14(2):237-241.
[17] Solla P,Cannas A,Mulas CS,etal.Association between fatigue and other motor and non-motor symptoms in Parkinson’s disease patients[J].J Neurol,2014,261(2):382-391.
[18] Post B,Speelman JD,de Haan RJ.Clinical heterogeneity in newly diagnosed Parkinson’s disease[J].J Neurol,2008,255:716-722.
[19] Reijnders JS,Ehrt U,Lousberg R,etal.The association between motor subtypes and psychopathology in Parkinson’s disease[J].Parkinsonism Relat Disord,2009,15:379-382.
[20] Chou KL,Persad CC,Patil PG.Change in fatigue after bilateral subthalamic nucleus deep brain stimulation for Parkinson’s disease[J].Parkinsonism Relat Disord.2012,18(5):510-513.
[21] Alves G,Wentzel-Larsen T,Larsen JP.Is fatigue an independent and persistent symptom in patients with Parkinson’s disease?[J].Neurology,2004,63:1908-1911.
(本文编辑苏琳)
CharacteristicsoffatigueinpatientswithParkinson’sdiseaseandinfluenceofsleepbehaviorinterventiononfatigue
JiaPeilan,RenJinhong
(Brain Hospital of Liaocheng City,Shandong 252000 China)
Objective:To observe the characteristics and influencing factors of fatigue in patients with Parkinson’s disease,and to probe into the influence of sleep behavior intervention on fatigue.Methods:A total of 55 cases of Parkinson’s disease in our hospital from July 2011 to December 2015 were selected as the study objects.The study was divided into 2 stages,The first phase(July 2011 - December 2015)was a observational cross-sectional study,Unified Parkinson’s Disease Rating Scale(UPDRS)was used to evaluate the motor symptoms in the third part,Non-Motor Symptoms Scale(NMSS)was used to assess non motor symptoms,Fatigue Severity Scale(FSS)was used to assess the patient’s fatigue.Independent risk factors of fatigue were analyzed by Logistic multiple regression analysis.The second phase(January 2016 - June 2016) was an intervention prospective study.The baseline FFS score and the Parkinson’s Disease Scale(PDSS)were used to score the subjects,and sleep behavioral intervention was given,3 months later,the FFS and PDSS scores were again scored.Results:The first FSS score of Parkinson’s disease was 3.8±1.8,and fatigue occurred in 25 patients(45.5%).Logistic regression analysis showed that sleep scores,emotional and cognitive scores were independent risk factors for fatigue.After sleep behavior intervention,the FFS score and fatigue rate decreased,while the PDSS score increased.Conclusions:Fatigue was a common non motor symptom in patients with Parkinson’s disease.Sleep disturbance,mood and cognitive impariment were independent risk factors.Sleep behavioral intervention could effectively reduce fatigue level.
Parkinson’s disease;fatigue;sleep intervention;non motor symptoms
贾培兰,主管护师,本科,单位:252000,聊城市脑科医院;任金红单位:252000,聊城市脑科医院。
信息贾培兰,任金红.帕金森病病人的疲劳发生特点及睡眠行为干预对疲劳的影响[J].护理研究,2017,31(27):3410-3413.
R473.74
:Adoi:10.3969/j.issn.1009-6493.2017.27.016
:1009-6493(2017)27-3410-04
2016-12-29;
2017-08-21)
