双歧杆菌完整肽聚糖对结肠癌SW480细胞株增殖能力及VEGF、Ki67表达的影响
2017-09-15王伟杰荣诗阔王金凯
王伟杰,荣诗阔,王金凯,李 海
·论 著·
双歧杆菌完整肽聚糖对结肠癌SW480细胞株增殖能力及VEGF、Ki67表达的影响
王伟杰1,荣诗阔2,王金凯2,李 海1
目的探讨双歧杆菌完整肽聚糖(WPG)对结肠癌SW480(原位结肠癌细胞)细胞株增殖能力及VEGF、Ki67表达的影响。方法常规结肠癌SW480细胞株培养后,给予不同浓度的WPG(20、40、80、160、320 μg/mL)共孵育一定时间(24 h、48 h和72 h)后,计算不同浓度WPG对SW480细胞株的抑制率;CCK-8法检测干预后细胞的增殖能力,Western blot(免疫印迹法)检测干预后VEGF、Ki67的表达水平变化。结果CCK-8(Cell Counting Kit-8)法显示不同浓度干预SW480细胞株的抑制率不同,具有浓度依耐性,并显示干预后细胞株增殖能力降低;Western-blot显示干预后SW480细胞株中VEGF(P<0.05)、Ki67(P<0.05) 较对照组蛋白表达水平下降。结论双歧杆菌完整肽聚糖能抑制结肠癌SW480细胞株的增殖能力,并能下调VEGF、Ki67表达水平,从而抑制肿瘤的发展。
双歧杆菌完整肽聚糖;结直肠癌;增殖;VEGF;Ki67
结直肠癌是常见的消化系统恶性肿瘤之一,在男性恶性肿瘤中排第三位、女性恶性肿瘤中排第二位[1],在我国的发病率呈逐年上升趋势,严重影响着人们的生活质量水平[2]。肠道的微生态系统是机体最重要也是最庞大的微生态系统,对宿主的健康与营养都起着非常重要的作用,是激活和维持肠道生理功能的关键因素[3]。本文主要通过CCK-8法检测双歧杆菌完整肽聚糖干预SW480细胞株后细胞增殖能力的变化,并利用Western-blot法检测干预后VEGF、Ki67的表达水平变化,探讨双歧杆菌完整肽聚糖对结肠癌SW480细胞株增殖能力及VEGF、Ki67表达的影响,并探讨其影响肿瘤发展的可能机制。
1 材料与方法
1.1 主要试剂及仪器:结肠癌SW480细胞株(ATCC,CCL-228TM),Leibovitz’s L-15培养基(Thermo Fisher公司,货号11415-064),胰蛋白酶(Thermo Fisher公司,货号12604-021),培养皿(康宁),兔抗人多克隆抗体VEGF(Abcam公司,货号ab9570)、兔抗人多克隆抗体Ki67(Abcam公司,货号ab15580),羊多克隆抗兔二抗(北京中杉金桥,货号ZDR-5306),还有CCK-8(日本同仁)、凯基全蛋白提取试剂盒、凯基蛋白含量检测试剂盒、凝胶成像仪(Bio-Rad)等。
1.2 细胞培养:SW480在含10% FBS的Leibovitz’s L-15培养基中(添加0.1%的青霉素、链霉素)放置于37℃、5% CO2的细胞培养箱中培养,当细胞生长密度达到80%~90%时传代培养。
1.3 双歧杆菌完整肽聚糖干预实验:双歧杆菌完整肽聚糖按梁延春等[4]报道的方法从分叉双歧杆菌中提取而成,并经过鉴定。通过人结肠癌SW480细胞与不同浓度WPG(20、40、80、160、320、100 μg/mL) 共孵育一定时间(24 h、48 h和72 h)后,观察低、中、高浓度WPG对SW480细胞的杀伤作用。
1.4 CCK-8实验检测细胞的抑制率及增殖实验:在96孔板中配制100 μl的细胞悬液,将培养板在37 ℃、CO2的培养箱中预培养24 h,向96孔培养板中加入不同浓度(20、40、80、160、320 μg/mL)的WPG溶液,每个浓度6个重复,并做无WPG培养基及无CCK-8溶液为阴性、空白对照。将培养板在培养箱孵育24 h、48 h和72 h,同时向每孔加入CCK-8溶液至终浓度为10%。将培养板在培养箱内孵育2 h后用酶标仪测定在450 nm处的吸光度,计算WPG对细胞的抑制率,并计算IC50,选取最适宜的干预浓度,选取时间点(0、24、48、72、96 h)检测干预后细胞增殖能力。
1.5 Western-blot检测干预后VEGF、Ki67的蛋白表达:利用凯基全蛋白提取试剂盒提取全蛋白、凯基蛋白含量检测试剂盒检测提取蛋白浓度,配平各蛋白浓度,沸水煮5 min使蛋白变性后-20 ℃保存备用,避免反复冻融。配制4%浓缩胶、10%分离胶,用50 μg蛋白量上样后SDS-PAGE电泳(80 V恒压电泳2 h左右),然后4 ℃恒压150 V湿性电转1 h。用含0.5‰TBST 的5%脱脂牛奶封闭非特异性蛋白1 h。在含0.5‰TBST 的5%脱脂牛奶中加入一抗VEGF(1∶2 000)、Ki67(1∶1 000),4 ℃一抗孵育过夜;次日在含0.5‰TBST 的5%脱脂牛奶中加入二抗(羊抗兔1∶5 000),室温二抗孵育1 h后用1‰TBST水平摇床清洗,化学显影并凝胶图像显影拍照并分析。
1.6 结果判定:CCK-8结果由Bio-Rad酶标仪检测分析结果,抑制率=(OD值对照组-OD值干预组)/OD值对照组。IC50结果由GraphPad Prism 5.0计算得出。
Western-blot利用IPP 6.0软件分析干预组与对照组IOD(灰度值)及Area(面积),以GAPDH为内参统计分析干预组与对照组平均IOD(灰度值)/Area(面积)比值,分析干预后平均灰度值与未干预组平均灰度值及相对倍数关系。
2 结果
2.1 WPG抑制SW480细胞增殖能力随浓度的增加而增强:CCK-8法显示不同浓度(20、40、80、160、320 μg/mL)干预SW480细胞的抑制率不同,且具有浓度依耐性,随浓度的增加抑制能力增强,见表1。当IC50为116.2 μg/mL时细胞抑制能力最强,用WPG 116.2 μg/mL干预后显示细胞增殖能力下降,在48 h(F=0.926,P<0.05)、72 h(F=0.867,P<0.05)、96 h(F=1.603,P<0.05)时差异均有统计学意义,在区间48~72 h差异最为明显。
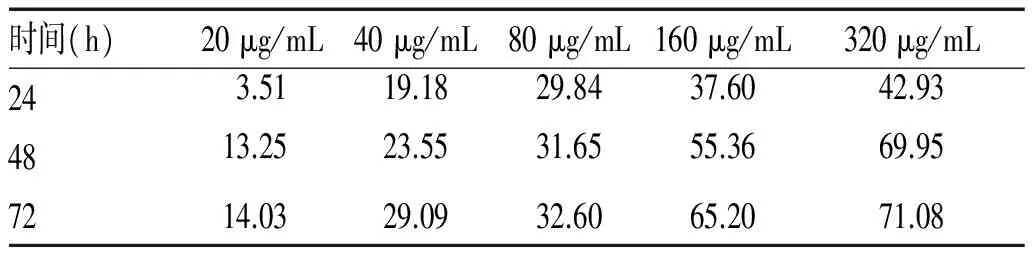
表1 不同浓度双歧杆菌WPG对SW480细胞的抑制率(%)
2.2 WPG能下调SW480细胞株中VEGF、Ki67蛋白的表达:Western-blot显示干预后SW480细胞株中VEGF(P<0.05)、Ki67(P<0.05) 较对照组蛋白表达水平下降,差异有统计学意义。
3 讨论
双歧杆菌是人体肠道中具有营养机体、抑制细菌生长、免疫调节、抗肿瘤等作用的益生菌,其在肠道的数量平衡对维持机体健康至关重要[5-10]。双歧杆菌WPG是一种多糖与肤聚糖聚合而成的袋状结构,它保持了双歧杆菌细胞壁的完整性,在体内外均可保留其多种生物学活性[11]。研究证明,双歧杆菌WPG对多种肿瘤的发生、发展都具有一定的抑制作用[12]。蔡良真等[13]研究证明,双歧杆菌WPG 在体外对人结肠癌细胞株LS-174T具有显著的选择性杀伤作用。Sekine等[14]将双歧杆菌细胞壁中的完整肽聚糖及细胞壁骨架分别和MethA 纤维肉瘤细胞一起混合接种到小鼠皮下,发现都能显著抑制肿瘤细胞的增长。而Sekine等[15]在研究双歧杆菌WPG 对T 细胞介导的免疫反应和绵羊红细胞致敏小鼠的迟发型超敏反应过程中发现双歧杆菌WPG 对小鼠免疫反应具有调节作用,可能在免疫抗肿瘤过程中发挥重要的作用。而彭艳华等[16]在研究双歧杆菌脂磷壁酸对不同大肠癌细胞株LoVo细胞和HT-29细胞转移能力及VEGF表达的影响时发现,双歧杆菌脂磷壁酸能抑制大肠癌细胞黏附、侵袭、迁移的能力,能下调VEGF的mRNA和蛋白质的表达。郑昌京等[17]将双歧杆菌注射到大肠癌裸鼠移植瘤动物模型中,检测发现大肠癌组织中VEGF及其微血管密度(MVD)明显低于对照组,可见双歧杆菌抑制大肠癌的发展可能是通过下调VEGF 达到的。在胃癌、肝癌等其他肿瘤的研究中也有类似报道[18-19]。
在本研究中,给予不同浓度的WPG与结肠癌SW480细胞株共孵育一定时间后发现,不同浓度WPG对SW480细胞的抑制率不同,且具有浓度依耐性,即浓度越高对细胞的抑制能力越强。同时,我们利用CCK-8法计算IC50,选取最适宜浓度干预细胞后检测细胞的增殖能力,发现WPG抑制了SW480细胞株的增殖。同时发现,干预组的VEGF表达水平较未干预组下降,差异有统计学意义,并检测了与增殖相关的Ki67基因,发现干预组的Ki67表达水平呈下降趋势。这些结果证明,双歧杆菌完整肽聚糖能抑制结直肠癌SW480细胞株的增殖,其抑制肿瘤的发展可能是通过下调VEGF蛋白的表达形成的,但就其具体机制还需进一步的研究来证明。
结合大量的文献资料及本实验结果分析,双歧杆菌完整肽聚糖在结直肠肿瘤的发生、发展中发挥了重要作用,能抑制结肠癌细胞的增殖,这可为结直肠癌早期预防及治疗提供一定的指导价值。但就目前而言,双歧杆菌完整肽聚糖作用于结直肠癌发生、发展的具体机制还需要在进一步的研究中去证实。相信在不久的将来,双歧杆菌完整肽聚糖在治疗肿瘤的过程中会发挥越来越重要的作用。
[1] Torre LA,Bray F,Siegel RL,et al.Global cancer statistics,2012[J].CA-A Cancer Journal for Clinicians,2015,65(2):87-108.
[2] 李道娟,李倩,贺宇彤.结直肠癌流行病学趋势[J].肿瘤防治研究,2015,42(3):305-310.
[3] 中华预防医学会微生态学分会.中国消化道微生态调节剂临床应用共识[J].中国微生态学杂志,2016,28(6):621-631.
[4] 梁延春,李荣华,刘宁.双歧杆菌肽聚糖的提取及其白蛋白磁性微球的制备[J].中国医院药学杂志,2008,28(12):957-960.
[5] 吴彬彬,杨莉丽,梁岩.双歧杆菌与肠易激综合征的研究进展[J].世界华人消化杂志,2016,24(2):229-235.
[6] 田颖,戴倩倩,时明慧.双歧杆菌BB12对便秘大鼠的通便作用及对胃肠激素的调节[J].食品科学,2016,37(13):204-208.
[7] 宋娜娜,宋静慧.乳杆菌胞外多糖及肽聚糖抗肿瘤作用研究进展[J].内蒙古医学院学报,2012,34(6):996-999.
[8] 李俊洁,陈庆森.双歧杆菌调理和改善肠道相关疾病作用的研究进展[J].食品科学,2011,32(23):326-332.
[9] 吕锡斌,何腊平,张汝娇,等.双歧杆菌生理功能研究进展[J].食品工业科技,2013,16(1):353-358.
[10] Van Der Werf MJ,Venema K.Bifidobacteria:genetic modification and the study of their role in the colon[J].Journal of Agricultural and Food Chemistry,2001,49(1):378-383.
[11] 张延坤,马燕.双歧杆菌的生物特性及其保健功能[J].解放军预防医学杂志,2005,23(5):386-389.
[12] 朱辉,张德纯.双歧杆菌抗肿瘤机制的研究现状与展望[J].中国微生态学杂志,2011,23(8):764-767.
[13] Cai LZ,Li SJ,Guan CN.In vitro and in vivo antitumor effects of whole peptidoglycan from bifidobacterium on colon carcinoma[J].Journal of Guangdong Medical College,2005,23(5):500-503.
[14] Sekine K,Toida T,Saito M,et al.A new morphologically characterized cell wall preparation (whole peptidoglycan) from Bifidobacterium infantis with a higher efficacy on the regression of an established tumor in mice[J].Cancer Research,1985,45(3):1300-1307.
[15] Sekine K,Watanabe Sekine E,Toida T,et al.Adjuvant activity of the cell wall of Bifidobacterium infantis for in vivo immune responses in mice[J].Immunopharmacology and Immunotoxicology,1994,16(4):589-609.
[16] 彭艳华,刘健龙,王跃,等.双歧杆菌脂磷壁酸对不同大肠癌细胞株转移能力及VEGF表达的影响[J].第三军医大学学报,2008,30(13):1256-1259.
[17] 郑昌京,王立生,李俊达,等.双歧杆菌对实验性大肠癌血管形成的影响[J].海南医学,2004,15(2):15-16.
[18] 粟敏,黄春霞,周建波,等.双歧杆菌WPG对肝癌H22细胞的抑制作用研究[J].实用预防医学,2011,18(9):1617-1619.
[19] Pallini R,Pierconti F,Falchetti ML,et al.Evidence for telomerase involvement in the angiogenesis of astrocytic tumors:expression of human telomerase reverse transcriptase messenger RNA by vascular endothelial cells[J].Journal of Neurosurgery,2001,94(6):961-971.
关于征稿范围的要求
本刊欢迎述评、专题论坛、论著、实验研究、临床研究、调查研究、经验交流、综述、临床护理、病例报告、讲座、技术与方法、中医中药、会议(座谈)纪要、临床病例与病理讨论、国内外有关学术会议征文通知及学会活动等栏目的稿件。欢迎在本刊刊登医疗机构、科室宣传等广告(封面或彩页)。
TheeffectsofbifidobacteriumintactpeptidoglycanonproliferationinSW480celllineandtheexpressionofVEGFandKi67incoloncancer
WANGWeijie1,RONGShikuo2,WANGJinkai2,LIhai1.
1.DepartmentofColorectalSurgery,GeneralHospitalofNingxiaMedicalUniversity,Yinchuan750004,China;2.NingxiaMedicalUniversity,Yinchuan750004,China
Correspondingauthor:LIHai,Email:zhuoran1126@163.com
ObjectiveTo investigate the effects of bifidobacterium intact peptidoglycan (WPG) on the proliferation and expression of VEGF and Ki67 in colon cancer cell line SW480 (colorectal carcinoma cell line).MethodsAfter cultured for 24 hours,48 hours and 72 hours,different concentrations of WPG (20 μg/mL,40 μg/mL,80 μg/mL,160 μg/mL,320 ug/ml),the inhibitory rate of WPG on SW480 cells was detected by CCK-8 method.The expression of VEGF and Ki67 in the SW480 cells was detected by Western-blot.ResultsThe inhibitory rate of SW480 cells treated with different concentrations of CCK-8 (Cell Counting Kit-8) was different,and the cell proliferation was decreased after treated with CCK-8.The expression of VEGF(P<0.05),Ki67(P<0.05) was different compared with that in control group.ConclusionThe complete peptidoglycan of Bifidobacterium can inhibit the proliferation of SW480 cell line and down-regulate the expression of VEGF and Ki67,and inhibit the development of tumor.
WPG;Colorectalcancer;Proliferation;VEGF;Ki67
宁夏医科大学校级科研项目(XM2015066)
1.宁夏医科大学总医院结直肠外科,宁夏 银川 750004 2.宁夏医科大学,宁夏 银川 750004
王伟杰(1981-),男,医学硕士,主治医师,主要从事消化道肿瘤临床与基础研究工作。
李海,Email:zhuoran1126@163.com
http://kns.cnki.net/kcms/detail/64.1008.R.20170713.0845.012.html
10.13621/j.1001-5949.2017.08.0694
R735
A
2017-01-21 [责任编辑]李 洁
