布洛芬异构体在大鼠体内的药代动力学研究
2017-09-13曾文学周春阳
曾文学,周春阳,何 林
(1.川北医学院药学院,四川 南充 637100;2.四川省医学科学院·四川省人民医院,四川 成都 610072)
布洛芬异构体在大鼠体内的药代动力学研究
曾文学1,周春阳1,何 林2
(1.川北医学院药学院,四川 南充 637100;2.四川省医学科学院·四川省人民医院,四川 成都 610072)
目的研究布洛芬异构体在大鼠体内的药代动力学特征。方法将9只SD大鼠简单随机化分为低、中、高剂量3组,每组3只,分别灌胃给予布洛芬消旋液13.6、27.0、54.5 mg/kg。建立高效液相色谱法,分别测定左旋和右旋布洛芬的血药浓度,计算药代动力学参数。结果左旋布洛芬低、中、高剂量组的药代动力学参数峰浓度Cmax分别为(15.75±3.07)、(15.73±4.47)、(53.75±10.83) μg/ml,曲线下表面积AUC0-t分别为(15.23±2.15)、(18.23±2.54)、(57.58±5.94) μg/(ml·h),清除率CLz 分别为(0.86±0.11)、(1.39±0.12)、(0.88±0.10)L/(kg· h);右旋布洛芬低、中、高剂量组的药代动力学参数Cmax分别为(29.69±2.55)、(39.63±2.50)、(83.32±9.27) μg/mL,AUC0-t分别为(96.17±13.42)、(117.90±18.19)、(259.35±52.24) μg/(ml·h)、CLz分别为(0.11±0.03)、(0.19±0.05)、(0.16±0.03)L/(kg· h)。结论布洛芬的左旋体和右旋体都符合线性药代动力学特征。
布洛芬;药代动力学;手性药物
手性药物(chiral drug),是指药物分子结构中引入手性中心后,得到的一对互为实物与镜像的对映异构体。手性药物进入体内后,它的两个对映异构体通常会表现出不同的生物活性,一个异构体可能是有效的,而另一个异构体可能是无效甚至是有害的。手性制药就是利用这种原理,开发出药效高、副作用小的药物。在临床治疗方面,服用对映体纯的手性药物不仅可以排除由于无效(不良)对映体所引起的毒副作用,还能减少药剂量和人体对无效对映体的代谢负担,对药物动力学及剂量有更好的控制,提高药物的专一性。布洛芬是一个选择性抑制环氧化酶-2的非甾体抗炎药[1],在临床上广泛用于解热、镇痛、抗炎。在治疗关节炎方面也有良好的作用[2]。布洛芬具有对映异构体结构,就消旋布洛芬而言,其体内过程呈线性动力学特征[3],但其左旋体和右旋体在体内的药理活性、代谢过程存在显著差异[4]。由于目前对于是否存在开发右旋布洛芬的必要性存在争议,本研究试图从药动学、药效学及不良反应等方面进行探究。因体内的辅酶A硫酯和甲基丙二酰辅酶A的消旋酶可将左旋布洛芬单向转化为右旋布洛芬等因素存在,而且右旋又是优势构型[5],因此有必要研究进入在体内后左旋和右旋布洛芬药代动力学特征。本研究通过大鼠灌胃给予三个剂量的消旋布洛芬,用建立的HPLC法测定体内左旋和右旋布洛芬血药浓度,并在此基础上分别考察左旋与右旋布洛芬的体内药代动力学特征,为手性药物的开发和临床用药提供依据。
1 材料与方法
1.1实验动物健康SD大鼠,体重(180~220)g,购于成都达硕生物科技有限公司。9只SD雄性大鼠简单随机化分为低、中、高剂量3组,每组3只。饲养温度:22~25 ℃,相对湿度:40~70%。
1.2试剂布洛芬(含量:99.9% 批号:11043231,山东新华制药股份有限公司);右旋布洛芬(含量:100.2%,批号:C102-1310023 M,湖北百科亨迪药业有限公司);左旋布洛芬(含量:99.8%,批号:R131108,成都苑东药业有限公司);水杨酸(内标,批号:1503023,华阳市锦前程药业有限公司);布洛芬混悬液(规格:2 g/100 ml,批号:151019140,上海强生制药有限公司);正己烷、异丙醇、三氟乙酸均为色谱纯。盐酸、乙醚均为分析纯。可证号:SCXK(川)2008-24。Waters2690高效液相色谱仪(美国Waters)。
1.2测定条件与样品处理
1.2.1色谱 条件色谱柱为CHIRALCEL OD-H (4.6 mm×250 mm,5 μm) 流动相为正己烷-异丙醇-三氟乙酸=100∶1.8∶0.1;流速为1 ml/min;柱温为30 ℃;进样量为20 μl。
1.2.2血浆样品处理 取血浆样品100 μl加入内标100 μg/ml水杨酸20 μl和甲醇20 μl,涡旋10 s,加入4 mol/ml HCL 100 μl,涡旋30 s。再加入提取剂乙醚3 ml 涡旋2 min,以3500 r/min 离心10 min,取上层有机相,40 ℃水浴空气流吹干后加入流动相100 μl复溶,涡旋1 min,以 3500 r/min离心3 min,取上清液20 μl。
1.3给药方法与样品采集将9只大鼠随机分为3组,每组3只。实验前禁食12 h,不禁水。分别灌胃给予布洛芬混悬剂低、中、高三个剂量组,剂量分别为13.6、27.0、54.5 mg/kg。三组大鼠均于给药前(0 h)和给药后 0.083、0.167、0.333、0.5、0.667、1、2、4、5、6 h颈动脉采血,分离血浆,-20 ℃保存待测。
1.4方法学考察
1.4.1专属性 在上述色谱条件下,血浆内源性物质不干扰左旋布洛芬、右旋布洛芬和内标水杨酸的测定。药物峰与内标峰分离良好,保留时间分别为16.59、18.81和24.05 min,符合生物样品的测定要求,色谱图见图1。
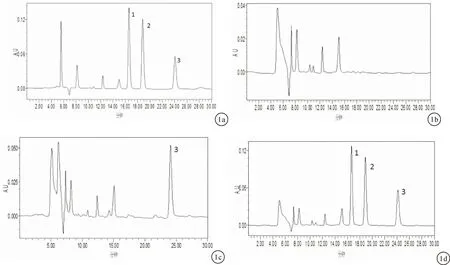
图1 色谱图 a:标准品;b:空白血浆;c:空白加内标;d:样品血浆 1.左旋布洛芬 2.右旋布洛芬 3.内标
1.4.2标准曲线与定量下限 取大鼠空白血浆100 μl加入左旋和右旋布洛芬系列标准溶液20 μl得到左旋布洛芬和右旋布洛芬浓度为0.3125、0.625、1.25、2.5、5、10、20、40、50 μg/ml的血浆样品按“1.2.2”项下处理。分别以左旋布洛芬和右旋布洛芬浓度为横坐标,待测物与内标峰面积比为纵坐标,用加权最小二乘法(W=1/χ2)进行线性回归,得左旋布洛芬标准曲线方程为Y=0.2664X-0.0221(r=0.9996),右旋布洛芬的标准曲线方程为Y=0.2569X-0.0193(r=0.9992),左旋布洛芬和右旋布洛芬分别在0.3125~50 μg/ml内线性良好,定量下限均为0.3125 μg/ml。
1.4.3精密度和准确度 取大鼠空白血浆,精密配制低、中、高浓度分别为0.3125、5、50 μg/ml的质控样品,按“1.2.2”项下操作,每个浓度平行6份样本分析,连续测定3天,计算精密度和准确度,结果见表1。
1.4.4提取回收率 取大鼠空白血浆,精密配制低、中、高浓度分别为0.3125、5、50 μg/ml的质控样品,按“1.2.2”项下操作,另取与质控样品同浓度同体积的标液挥干,加同体积流动相配制相应浓度的标准溶液,进样,记录其峰面积,两者的比值即为提取回收率,见表1。

表1 左旋布洛芬、右旋布洛芬精密度与回收率(n=6)
1.4.5稳定性 取大鼠空白血浆,配制低、中、高浓度分别为0.3125、5、50 μg/ml的质控样品,按“血浆样品处理”项下操作,左旋布洛芬于-20 ℃保存到第14天的测定值与第0天的测定值相比,偏差分别为4.89%、4.28%、2.60%;第14天测定值的相对标准偏差RSD分别为4.27%、2.36%、1.61%;右旋布洛芬于-20 ℃保存到第14天的测定值与第0天的测定值相比,偏差分别为4.83%、4.43%、1.90%;第14天测定值的RSD分别为4.36%、2.25%、1.92%;表明血浆中布洛芬的左旋体和右旋体在上述条件下稳定性良好,满足实验要求。低、中、高三个浓度的左旋血浆样品冻融3次后测定值与未冻融测定值相比,偏差分别为7.30%、1.45%、2.38%;冻融3次后测定值的相对标准偏差RSD分别为4.16%、4.19%、4.52%;右旋布洛芬血浆样品冻融3次后测定值与未冻融测定值相比,偏差分别为2.06%、5.94%、6.58%;冻融3次后测定值的RSD分别为3.80%、2.00%、3.36%;说明血浆样品冻融3次内稳定性良好。
1.4.6稀释可靠性 制备左/右旋布洛芬浓度为80 μg/ml和100 μg/ml的标准血浆样品,用空白血浆稀释1倍后进行测定,考察稀释效应:结果显示,稀释1倍后测定结果乘以稀释倍数所得计算值,与标识浓度相比,左旋布洛芬的精密度相对标准偏差RSD分别为3.15%、2.63%。右旋布洛芬的精密度相对标准偏差RSD分别为3.85%、2.67%。表明对血浆样品进行稀释后分析,校正计算的结果能够准确反映超出曲线范围的药物浓度。
1.5统计学方法采用DAS 2.1.1软件计算药动学参数,采用SPSS 21.0软件进行统计学分析,结果以均值±标准差表示,采用单因素方差分析进行统计。P< 0.05为差异有统计学意义。
2 结果
2.1血药浓度-时间曲线大鼠灌胃分别给予左旋及右旋布洛芬低、中、高三个剂量后体内浓度平均药-时曲线,见图2。

图2 不同剂量布洛芬大鼠体内浓度平均药-时曲线 (n=3) a:左旋布洛芬;b:右旋布洛芬
2.2药代动力学参数大鼠灌胃分别给予左旋及右旋布洛芬13.6、27.0、54.5 mg/kg低、中、高三个剂量后的主要药动学参数见表2。右旋布洛芬的t1/2、Tmax较左旋布洛芬长,其Cmax、AUC均远远大于左旋布洛芬的Cmax和AUC。

表2 左旋布洛芬和右旋布洛芬的主要药动学参数(n = 3)
3 讨论
由于手性化合物理化性质几乎完全相同,所以对其分离难度也较大。但随着现代分析技术的不断进步,已经可以对手性异构体进行分离分析[6]。这使的对手性药物的立体选择性药物代谢动力学的研究成为可能,对深入研究手性药物的药理和毒理作用具有重大意义[7]。之前文献报道过布洛芬异构体分别的体内血药浓度研究[8],但没有对布洛芬的左旋体和右旋体分别进行药代动力学特征的研究。本文首次分别对左旋和右旋布洛芬3个剂量组的主要药动学参数Cmax、AUC0-∞及AUC0-t与剂量进行线性回归,得到左旋布洛芬主要药动学参数的回归方程分别为Cmax= 0.9965X-3.179,R2= 0.8965;AUC0-∞= 1.1919 X-5.2243,R2= 0.9359;AUC0-t= 1.094 X-4.3405,R2=0.9321;右旋布洛芬主要药动学参数的回归方程分别为Cmax= 1.3525 X +8.006,R2= 0.9771;AUC0-∞= 5.9887 X +20.069,R2= 0.9459;AUC0-t= 4.1612 X +25.895,R2= 0.9589;左旋和右旋布洛芬的t1/2在不同剂量组间比较差异无统计学意义(P> 0.05)。综上,左旋和右旋布洛芬大鼠体内过程均具有一定的线性动力学特征。
比较两种异构体三个剂量组在体内的主要药动学参数,可以得到如下结果:右旋布洛芬的达峰时间较左旋布洛芬长,其Cmax、AUC均远远大于左旋布洛芬的Cmax和AUC;同时,右旋布洛芬半衰期较左旋布洛芬长,结果可重复。表明右旋布洛芬在体内的吸收较左旋布洛芬长,消除更慢,说明其被生物体吸收更完全。从临床需要持续发挥降温作用的效果来讲,右旋布洛芬具有开发利用的价值。至于药效学与不良反应的研究结果,将另文讨论。
关于内标的选择,曾先后选择吲哚美辛、酮洛芬[9],但由于吲哚美辛的其出峰时间与右旋布洛芬的出峰时间相重叠,而酮洛芬自身出现双峰现象,分析其原因可能是因为酮洛芬也具有对映体的结构,通过手性柱而得到分离。因此,最后选择的水杨酸为内标,药物峰与内标峰分离良好,符合生物样品的测定要求。
关于血浆样品处理,曾采用环己烷、正己烷与正己烷-异丙醇(95:5)等不同溶剂萃取[10],但因内标水杨酸的萃取回收率不稳定,而改为乙醚,即可满足试验要求。
[1] Xiang J,Yu Qi,Liang MZ,et al.Pharmacokinetic studies of ibuprofen enantiomers in healthy human[J].J Sichuan Univ Med Sci,2010,1: 176-178.
[2] 刘洪彦,郑毅.布洛芬对兔骨关节炎模型Wnt/β-catenin信号通路和软骨细胞基质代谢的影响[J].实用医院临床杂志,2015,12(5):57-61.
[3] 宋敏,谭鸿毅,谭志荣,等.单剂量和多剂量口服布洛芬伪麻那敏干混悬剂在健康人体的药代动力学[J].中国临床药理学杂志,2010,26(123):28-36.
[4] 向瑾,余勤,梁茂植,等.柱切换HPLC法测定人血浆中布洛芬对映体浓度方法研究[J].分析化学,2008,36(3): 311-315.
[5] 赵秀红,夏媛媛,黄玉荣.LC-MS/MS法测定Beagle犬血浆中布洛芬对映体的浓度[J].中国药理学通报,2015,31(4):570-575.
[6] Kim DH.Origin cf chiral pharmacology: stereochenristry in metalloprotesse inhibition[J].Mini RcvMed Chem,2011,1 (2): 155-158.
[7] YinXiang Sun,BiYun Huang,Mu Yuan,et al.Development of a chiral HPLC method for the analysis of YM0302 topidil enantiomers[J].Journal of Chinese pharmaceutical sciences,2009,18(1):61-63
[8] Sharmap,Guttikar S,Solanki G,et al.Determination of (S)-(+)-and (R)-(-)-iburofen enantiomers in human plasma after chiral precolumn derivatization by reversed-phase LC-ESI-MS/MS (S)[J].Bioanalysis,2012,4(24): 2909-2927.
[9] 王红艳,孔爱英,杨波,等.手性 HPLC 方法测定布洛芬对映体及其在比格犬体内的药代动力学[J].药学学报,2015,50(12):1607-1612.
[10]何海云,黄华,王慧,等.消旋体药物生物等效性研究中的立体选择性[J].中国药房,2012,23(2): 162-165.
Pharmacokineticsofchiralibuprofeninrats
ZENGWen-xue1,ZHOUChun-yang1,HELin2
(1.NorthSichuanMedicalCollege,Nanchong637100,Sichuan,China;2.SichuanAcademyofMedicalSciences&SichuanProvincialPeople’sHospital,Chengdu610072,China)
HELin
ObjectiveTo study the pharmacokinetic characteristics of chiral ibuprofen in rats.MethodsNine SD rats were randomly divided into three groups with low,middle and high dose,3 in each group.The animals
gavages of 13.6,27 and 54.5 mg/kg ibuprofen suspension,respectively.The concentrations of S-and R-ibuprofen were determined by an established HPLC method and their pharmacokinetic parameters were calculated.ResultsThe pharmacokinetic parameters of R-ibuprofen in the three groups were as follow: Cmax=(15.23 ± 2.15),(18.23 ± 2.54)and(57.58 ± 5.94) μg/ml,respectively;AUC0-t=(15.23 ± 2.15),(18.23 ± 2.54)and(57.58 ± 5.94)L/(kg·h),respectively and CLz =(0.86 ± 0.11),(1.39 ± 0.12)and(0.88 ± 0.10)L/(kg·h),respectively.The pharmacokinetic parameters of S-ibuprofen were as follow: Cmax=(29.69 ± 2.55),(39.63 ± 2.50)and (83.32 ± 9.27) μg/mL,respectively;AUC0-t=(96.17 ± 13.42),(117.90 ± 18.19)and(259.35±52.24)L/(kg·h),respectively and CLz =(0.11 ± 0.03),(0.19 ± 0.05)and (0.16 ± 0.03)L/(kg· h),respectively.ConclusionThere are somewhat linear characteristics of the pharmacokinetic parameters of Cmax,AUC0-tand AUC0-∞for both R-ibuprofen and S-ibuprofen in rats.
Ibuprofen;Pharmacokinetic;Chiral drug
何 林
R91
A
1672-6170(2017)05-0023-04
2017-01-09;
2017-05-31)
