血清学与核酸检测在无偿献血血液传染性疾病筛查中作用分析
2017-09-08樊新艳
樊新艳
(濮阳市红十字中心血站检验科, 河南 濮阳 457000)
血清学与核酸检测在无偿献血血液传染性疾病筛查中作用分析
樊新艳
(濮阳市红十字中心血站检验科, 河南 濮阳 457000)
目的 分析血清学与核酸检测在献血者血液传染疾病筛查中的作用。方法 21 325份无偿献血者血液标本采用酶联免疫吸附试验(ELISA)检测HBsAg、HCV抗体、HIV抗体,ELISA双试剂检测苍白球螺旋体(TP)抗体,并使用核酸检测技术(NAT)对HBV-DNA、HCV-RNA、HIV-RNA进行联合检测,分析上述检测结果。结果 21 325份血液标本中,血清学检测HBsAg(+)50份,阳性率为0.16%;HCV抗体(+)24份,阳性率0.08%;HIV抗体(+)15份,阳性率0.05%;NAT阳性检测率0.16%(35份)。其中NAT(+)HBsAg(+)检测18份,NAT(+)HCV抗体(+)检测6份,NAT(+)HIV抗体(+)检测4份。结论 在“2遍ELISA+1遍NAT”模式下(除TP抗体),ELISA和NAT检测可以相互补充,不能互相替换单独运用,联合检测可保证血液安全。
血液传染性疾病;血清学检测;核酸检测;血液筛查
输血在临床上应用越来越广泛,临床对血液进行传染疾病筛查尤为重要。多年来,临床血液中心普遍采用血清学检测技术进行疾病筛查,即检测相应病毒的抗体,除乙肝病毒(HBV)可使用乙肝表面抗原(HBsAg)检测,其它病毒检测均可采用血清学检测[1]。随着医学发展,该方法的灵敏度及特异度不断上升,但当献血者处于疾病感染的“窗口期”、病毒变异、免疫沉默及其他相关因素仍可导致输血后发生感染。核酸检测技术(nucleic acid detection technotogy,NAT)可直接检测病原体核酸,大大缩短窗口期,保证血液安全[2]。本研究以21 325份血液标本为研究对象,分析血清学与NAT技术在血液传染疾病筛查的作用,报道如下。
1 材料与方法
1.1 标本来源 选择2016年6月—2016年10月濮阳市血液中心收集的无偿献血者血液标本21 325份。
1.2 试剂与仪器 首先选用酶联免疫吸附试验(ELISA)法进行血清学检测,HBsAg试剂(法国伯乐、厦门英科新创),丙型肝炎病毒(HCV)抗体试剂(珠海丽珠试剂公司、北京万泰),人类免疫缺陷病毒(HIV)抗体试剂(珠海丽珠试剂公司、法国伯乐),TP抗体试剂(北京万泰、厦门英科新创),丙氨酸转氨酶(ALT)试剂(深圳迈瑞),所有试剂均经过批检并在有效期内使用。NAT检测采用EDTA K2抗凝BD管离心,选用乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂进行HBV-DNA、HCV-RNA、HIV-RNA三联8样混合核酸检测,苏州华益美试剂盒及对照试剂盒支持同时混样、拆分检测。仪器包括澳斯邦FAME全自动酶免检测仪、爱康全自动酶免检测仪、迈瑞BS-480全自动生化仪、澳斯邦STAR全自动加样仪、澳斯邦全自动核酸分离纯化提取仪、AB7500扩增检测仪。
1.3 检测方法 HBsAg、HCV抗体、HIV抗体、TP抗体均采用ELISA法,用两种不同厂家生产的试剂先后进行血清学检测,两种试剂均有反应,则报告该样本血清学检测双试剂阳性,任一试剂阳性则用原试剂进行双孔复试,复试结果均为阳性或单孔阳性则报告该样本血清学检测单试剂阳性,双试剂检测均为阴性则报告该样本血清学检测阴性;ALT采用速率法检测,>50 U/L则为不合格;NAT检测三联8样混合检测,混样标本为阳性时则对每份标本进行单检,单检为阳性则判断不合格。
2 结果
2.1 HBV、HCV、HIV血清学及NAT检测结果 21 325份血液标本经血清学检测结果阴性21 173份,HBsAg(+)50份,阳性率为0.16%;HCV抗体(+)24份,阳性率0.08%,HIV抗体(+)15份,阳性率0.05%。除去合并TP阳性或ALT异常未参与检测,49份HBsAg阳性标本中,NAT(+)18份,阳性率36.73%;21份HCV抗体(+)标本中,NAT(+)6份,阳性率28.57%;13份HIV抗体(+)标本中,NAT(+)4份,阳性率30.76%。其中21 173份血清学检测阴性标本行NAT检测,显示35个混合检测模式(minipool)为阳性,拆分检测阳性18个pool,拆分阳性率51.43%。
2.2 血清学检测与NAT检测结果比较 混合样本不同酶联值(S/CO值)分布及NAT阳性数值,见表1-3。

表1 HBsAg S/CO值与NAT结果比较
注:5.01-6.001 1例合并TP抗体阳性未进行NAT比较。
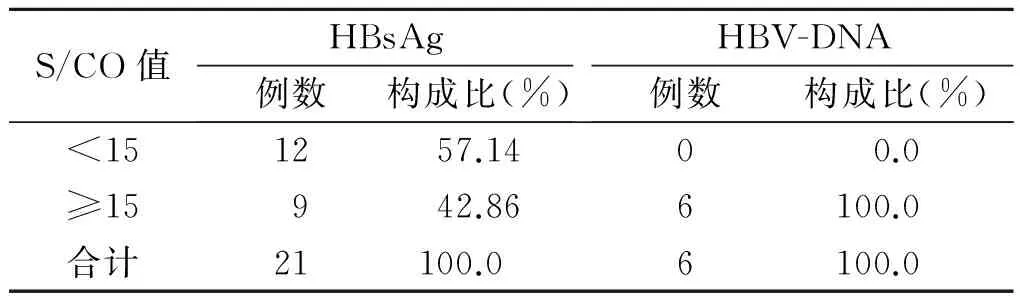
表2 HCV抗体 S/CO值与NAT结果比较
注:0.95-10.002 1例合并TP抗体阳性、>15.001 2例合并ALT异常均未进行NAT。

表3 HIV抗体 S/CO值与NAT结果比较
注:0.95-10.002 1例合并TP抗体阳性、15.01-20.001 1例合并TP抗体阳性未进行NAT检测。
3 讨论
本研究根据2012年出版的《血站技术操作规程》,使用的检测方式是“2遍ELISA+1遍NAT”,不包括TP抗体检测。张峰等[3]通过对33 736人份血液标本进行检测,其中HBsAg(+)NAT(+)符合率60.5%,HCV抗体(+)NAT(+)符合率11.2%,HIV抗体(+)NAT(+)符合率30.3%,该研究依次是42.86%、28.57%、30.3%、30.76%,结果类似,但存在一定的差异,分析原因是该研究在进行ELISA与NAT比较中剔除了不同S/CO值合并TP抗体(+)标本,对实验结果有一定的影响,但整体影响不大,说明该实验具有一定的可信度。 朱绍汶等[4]研究者报道南京地区的无偿献血中,HCV-RNA(+)39.45%,美国[5]报道为73.9%,该研究为28.57%,分析原因有以下几种种,一是区域、环境因素,二是HCV抗体试剂检测灵敏度过高出现假阳性情况,三是献血者感染过HCV,但病毒并不进行复制,患者无症状,此外,还可能与检测技术相关,核酸扩增技术至少扩增两个保守基因才有可能检测出基因突变的病原体[6],血清学检测结果、S/CO值与NAT之间的相关性仍是医学难题。该研究结果还显示,HBsAg(-)、HCV抗体(-)及HIV抗体(-)中,阳性pool 35份,有效拆分率为51.43%,刘胡敏等[7]报道有效拆分率为48.38%,刘丽等[8]报道为73.1%,均证明NAT可有效提高血液安全性。
综上,本研究没有分析因病毒载量低或假阳性的情况,存在一定的误差,但整体研究具有一定的可靠性,充分证实血清学与核酸检查两种技术均具有一定的重要性,其中核酸检查较血清学检测具有更高的灵敏度。
[1] 于志军,邓雪莲,高慧卉,等.血清学检测与核酸检测在献血者血液筛查中的相关性研究[J].实用预防医学,2014,21(5):532-534.
[2] 冯秋霞,许雷,杨忠思,等.青岛地区核酸检测在血液筛查中的应用研究[J].中国输血杂志,2013,26(7):632-634.
[3] 张锋,张琼,林碧,等.血清学联合核酸检测在献血者血液筛查中的互补性[J].中国艾滋病性病,2016,22(3):197-199.
[4] 朱绍汶,陈显,王金花,等.2011—2012年南京地区无偿献血人群丙型肝炎病毒感染情况分析[J].临床血液学杂志:输血与检验,2013,26(10):718-720.
[5] Egli A,Binet I,Binggeli S,et al.Cytomegalovirus-specific T-cell responses and viral replication in kidney transplant recipients[J].Journal of Translational Medicine,2008,6(1):1507.
[6] 蔡丽娜,陈宝安.核酸扩增技术(NAT)在献血者血液初筛中的应用现状[J].中国实验血液学杂志,2014,22(4):1171-1177.
[7] 刘胡敏,陶传敏,高加良,等. ELISA结合核酸检测技术对献血者作血液筛查结果分析[J].中国输血杂志,2013,26(5):456-458.
[8] 刘丽,杨忠思,单玉.血液检测新模式在无偿献血者血液筛查中的应用分析[J].中国输血杂志,2015,28(3):304-306.
[责任编辑:张亚光]
2016-12-23
樊新艳(1985-),女,河南省长垣县人,本科,主管技师,从事检验工作。
R 446.1
B
1008-9276(2017)05-0496-02
